09. tbl. 109. árg. 2023
Fræðigrein
Rannsókn. Umfang undanþágulyfja á Íslandi 2020-2021 – greining og samanburður við Svíþjóð árið 2020
Unlicensed drugs in Iceland in the years 2020 and 2021 with comparison to Sweden in 2020
ÁGRIP
INNGANGUR
Ávísun og umræða um undanþágulyf á Íslandi hefur aukist undanfarin ár. Óljóst hefur verið hverjar eru ástæður fyrir aukningunni.
EFNIVIÐUR OG AÐFERÐIR
Afturskyggn lýsandi rannsókn á undanþágulyfjaumsóknum sem samþykktar voru af Lyfjastofnun árin 2020 og 2021 ásamt undanþágulyfjaumsóknum frá Svíþjóð frá árinu 2020. Teknar voru saman upplýsingar um undanþágulyfjaumsóknir, skráð lyf og biðtíma eftir ATC-númerum (Anatomical Therapeutic Chemical Code). Upplýsingar voru greindar og flokkaðar eftir ástæðum og umfang undanþágulyfja í löndunum tveimur borið saman.
NIÐURSTÖÐUR
Á Íslandi voru samþykktar undanþágulyfjaumsóknir 49.161 árið 2020 og 46.581 árið 2021. Ástæða fyrir ávísun undanþágulyfjanna var í langflestum tilfellum sú að ekkert annað lyf var á markaði með sama ATC-númer og lyfjaform fyrir bæði árin. Lyfjaskortur var aðeins ástæða undanþágulyfja í 8,8% tilvika árið 2020 og 7,6% tilvika árið 2021. Fimmtíu mest ávísuðu undanþágulyfin voru um 70% sömu lyfin og 5 mest ávísuðu undanþágulyfin voru þau sömu bæði árin. Í Svíþjóð voru samþykktar undanþágulyfjaumsóknir 38.458, og 46% af 50 mest ávísuðu lyfjunum, voru samþykkt þar sem ekkert lyf var á markaði með sama ATC-númer og lyfjaform.
ÁLYKTANIR
Mikið af þeim undanþágulyfjum sem ávísað er hér á landi eru þau sömu ár eftir ár. Aðeins lítill hluti var samþykktur vegna skorts. Ávísun undanþágulyfja á Íslandi árið 2020 var meiri samanborið við í Svíþjóð þegar horft er til fólksfjölda og fjölda skráðra lyfja í löndunum. Draga mætti verulega úr heildarfjölda ávísana undanþágulyfja með markaðssetningu á þeim undanþágulyfjum sem er mest ávísað.
Greinin barst til blaðsins 6. febrúar 2023, samþykkt til birtingar 14. júlí 2023.
Inngangur
Í allri heilbrigðisþjónustu eru lyf og aðgengi að lyfjum mikilvægur þáttur. Hins vegar er lyfjaskortur vandamál um allan heim og hefur verið tilkynntur skortur á nær öllum tegundum lyfja á einhverjum tímapunkti. Skilgreiningin á lyfjaskorti er þegar eftirspurn á landsvísu mætir ekki framboði. Ástæðan getur verið margvísleg og má meðal annars nefna framleiðsluvandamál og skort á hráefni1 ásamt dreifingar- og framboðsvandamálum.2 Þetta getur haft mikil áhrif á sjúklinga og þeir þurfa að nota önnur lyf, sem getur reynst óákjósanleg meðferð og jafnvel þurft að borga meira fyrir lyfjameðferðina.1 Til þess að forðast neikvæð áhrif á sjúklinga er mikilvægt að bregðast við lyfjaskorti. Til þess að mæta lyfjaskorti hafa verið flutt inn lyf sem ekki hafa markaðsleyfi í landinu, öðru nafni undanþágulyf.3 Læknar geta því, með samþykki Lyfjastofnunar, ávísað lyfi með undanþágu sem ekki hefur markaðsleyfi í landinu ef lyfið er ekki fáanlegt á markaði.2 Slíkum lyfjum hefur þá verið veitt markaðsleyfi í öðru landi.4 Samþykki fyrir sölu lyfs sem ekki hefur markaðsleyfi í tilteknu landi er háð því að það sé mikilvægt fyrir heilsu þjóðarinnar.5 Læknir ber ábyrgð á að veita sjúklingi nauðsynlegar upplýsingar, tilkynna honum að lyfið hafi ekki markaðsleyfi hér á landi og gera grein fyrir mögulegum aukaverkunum. En læknir ber alfarið ábyrgð á ávísun og verkun lyfsins ef lyfið hefur ekki markaðsleyfi í öðru EES-ríki.6
Þegar læknir ávísar undanþágulyfi í lyfjagátt er það um leið umsókn um heimild hjá Lyfjastofnun fyrir ávísuninni. Starfsmenn stofnunarinnar fá þá umsóknina senda í tölvukerfi stofnunarinnar og meta umsóknina. Ef hún er samþykkt, birtist umrætt lyf í lyfjagátt og er hægt að afgreiða í lyfjabúð.7,8 Þegar markaðssett lyf skortir tímabundið er lyfjafræðingum heimilt, í sérstökum tilvikum þar sem Lyfjastofnun gefur heimild til, að breyta lyfseðli sem er upp á markaðssetta lyfið yfir í undanþágulyfið. Slík heimild er þó aðeins veitt í ákveðinn tíma og Lyfjastofnun hefur þá lagt mat á öryggi breytingarinnar.6 Þegar lyfjafræðingar nýta slíka heimild þurfa þeir að upplýsa lyfjanotendur um að lyfið sé í erlendum pakkningum og að það hafi ekki markaðsleyfi hér á landi og gera grein fyrir mögulegum aukaverkunum ásamt öðrum nauðsynlegum upplýsingum er varða notkun lyfsins.9 Afgreiðslutími undanþágulyfja hér á landi er að öllu jöfnu hraður, eða að jafnaði afgreiðsla samdægurs.10
Í Svíþjóð þarf læknir að hafa rökstudda ástæðu fyrir ávísun á hverju og einu undanþágulyfi líkt og læknar hér á landi. Ólíkt ferlinu hér á landi sækir apótekið um heimildina til lyfjastofnunar í Svíþjóð (Läkemedelsverket, Swedish Medical Products Agency). Afgreiðslutími undanþágulyfja er nokkru lengri en á Íslandi, en 7 virkir dagar er venjulegur afgreiðslutími umsókna.11
Markmið rannsóknarinnar var að greina umfang undanþágulyfja á Íslandi á árunum 2020 til 2021 til að varpa ljósi á stöðu undanþágulyfja á landinu. Greining var gerð á ástæðum fyrir þörf á ávísun undanþágulyfs. Jafnframt var markmiðið að bera stöðuna á Íslandi saman við stöðu undanþágulyfja í Svíþjóð árið 2020.
Efniviður og aðferðir
Rannsóknin fólst í því að leita upplýsinga um undanþágulyfjaumsóknir mannalyfja á Íslandi í IMAMED (gagnagrunnur Lyfjastofnunar). Undanþágulyfjaumsókn er umsókn um ávísun á undanþágulyfi í lyfjagátt einstaklings sem berst Lyfjastofnun frá lækni. Aflað var upplýsinga fyrir hvert vörunúmer sem samþykkt var á undanþágu og meðal annars um afskráningar, lyfjaskort og hvaða lyf eru markaðssett á Íslandi. Aðeins voru skoðuð mannalyf og aðeins þau sem ávísað var úr lyfjagátt Embættis landlæknis. Út frá gögnunum sem safnað var saman var hvert vörunúmer flokkað í viðeigandi flokk eftir því hvort sambærilegt skráð lyf var fáanlegt eða hvort skráða lyfið var í tímabundnum skorti þegar undanþágan var samþykkt. Á mynd 1 má sjá flokkana nánar.
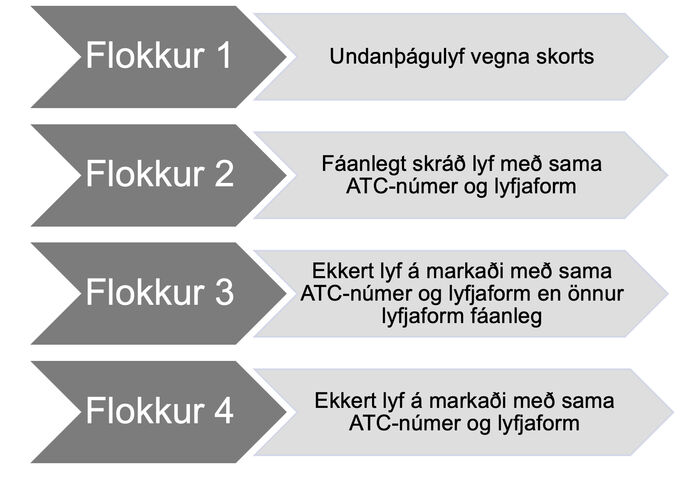 Mynd 1. Gögnin voru sett í fjóra flokka. (ATC - Anatomical Therapeutic Chemical Code).
Mynd 1. Gögnin voru sett í fjóra flokka. (ATC - Anatomical Therapeutic Chemical Code).
Undanþágulyf á Íslandi
Lyfjastofnun heldur úti sérlyfjaskrá þar sem hægt er að leita eftir ATC-númerum (Anatomical Therapeutic Chemical Code) lyfja sem hafa markaðsleyfi á Íslandi og eru markaðssett. ATC-númer segir til um hvaða ATC-flokki viðkomandi lyf tilheyrir, hvaða líffærakerfi lyfinu er ætlað að hafa áhrif á.12 Því var Sérlyfjaskrá notuð til þess að sjá hvort til væri skráð lyf með sama ATC-númer og lyfjaform og undanþágulyfið sem samþykkt var.
Upplýsingar um lyf sem hafa markaðsleyfi á Íslandi var að finna í lista sem ber heitið „Lyf með útgefin markaðsleyfi fyrir menn“. Á þeim lista var einnig tilgreint hvort lyfið væri markaðssett. Lyf sem áður höfðu markaðsleyfi á Íslandi en búið er að afskrá var að finna í lista sem ber heitið „Afskráð lyf og pakkningar 2017-2021“. Á þeim lista var hægt að sjá hvenær lyfið var tekið af markaði og hvenær markaðsleyfið var fellt niður. Listarnir eru aðgengilegir á heimasíðu Lyfjastofnunar.
Upplýsingar um þau lyf sem voru í tímabundnum skorti var að finna undir „Lyfjaskortsfréttir“ á heimasíðu Lyfjastofnunar. Þar var að finna lista yfir tilkynningar um lyfjaskort sem berast stofnuninni. Að auki var biðlisti lyfja hjá Sjúkratryggingum Íslands skoðaður. Horft var til þess hvenær lyfið fór á biðlista og hvenær lyfið var aftur væntanlegt.
Við flokkunina var farið eftir tímabilinu sem undanþágulyfið var samþykkt og borið saman við tímabilið sem lyfið var á bið vegna lyfjaskorts, dagsetningu afskráningar á skráðu lyfi og dagsetningu þegar skráð lyf var markaðssett hér á landi.
Samþykktar umsóknir eru þær umsóknir sem Lyfjastofnun samþykkti og urðu því aðgengilegar í lyfjagátt einstaklingsins. Hvert undanþágulyf hefur sitt norræna vörunúmer og innihélt hver umsókn því eitt norrænt vörunúmer. Á bak við hverja umsókn geta þó verið margar pakkningar og er því hver ávísun eitt lyf (tegund pakkningar/vörunúmer) óháð magni eða fjölda af þeirri pakkningu.
Heildarfjöldi samþykktra vörunúmera lýsir heildarfjölda sérlyfja sem samþykkt voru, en athuga verður að ákveðin sérlyf geta verið til í ólíkum pakkningum og formum. Þá ber það sama sérlyfjaheiti en annað vörunúmer.
Undanþágulyf í Svíþjóð
Gögn um undanþágulyfjaumsóknir frá Svíþjóð voru fengin frá sænsku lyfjastofnuninni. Aflað var upplýsinga fyrir hvert vörunúmer sem samþykkt var á undanþágu líkt og gert var fyrir Ísland. Út frá gögnunum sem safnað var saman var hvert vörunúmer sett í viðeigandi flokk eftir því hvort sambærilegt skráð lyf var fáanlegt eða hvort skráða lyfið var í tímabundnum skorti þegar undanþágan var samþykkt. Notaður var skortlisti á heimasíðu lyfjastofnunar í Svíþjóð til þess að finna upplýsingar um það hvaða lyf voru í tímabundnum skorti. Að auki var að finna á skortlistanum þau lyf sem höfðu verið afskráð. Til þess að sjá hvaða lyf voru markaðssett í Svíþjóð var skoðuð FASS (Farmacevtiska specialiteter i Sverige), sænska sérlyfjaskráin, þar sem leitað var eftir ATC-númeri.
Tölfræðileg úrvinnsla
Notað var Microsoft Excel við vinnslu, flokkun gagna og tölfræðiútreikninga. Microsoft Word var notað við myndvinnslu og gerð taflna.
Niðurstöður
Rannsóknarþýðið samanstóð af undanþágulyfjaumsóknum á Íslandi á tímabilinu 1. janúar 2020 til 31. desember 2021 ásamt undanþágulyfjaumsóknum í Svíþjóð frá 1. janúar til 31. desember 2020.
Undanþágulyf á Íslandi
Umfang undanþágulyfja
Heildarfjöldi undanþágulyfjaumsókna sem ávísað var í gegnum lyfjagátt Embættis landlæknis árið 2020 var 51.607, af þeim samþykkti Lyfjastofnun 49.161 umsóknir. Árið 2021 voru 48.453 undanþágulyfjaumsóknir og af þeim samþykkti Lyfjastofnun 46.581 umsóknir (munur á milli ára 6,1%).
Af samþykktum undanþágulyfjaumsóknum var heildarfjöldi norrænna vörunúmera 993 árið 2020, en árið 2021 voru þau 1093 talsins (munur á milli ára var 10%).
Ástæða fyrir ávísun undanþágulyfja
Ástæða fyrir ávísun undanþágulyfja var skoðuð fyrir hvert norrænt vörunúmer á árunum 2020 og 2021. Skoðað var hvort fáanlegt væri skráð lyf á markaði á Íslandi eða hvort skráða lyfið hafi skort á þeim tíma sem undanþágulyfið var samþykkt. Ástæður fyrir ávísun undanþágulyfja á árunum 2020 og 2021 má sjá á mynd 2.
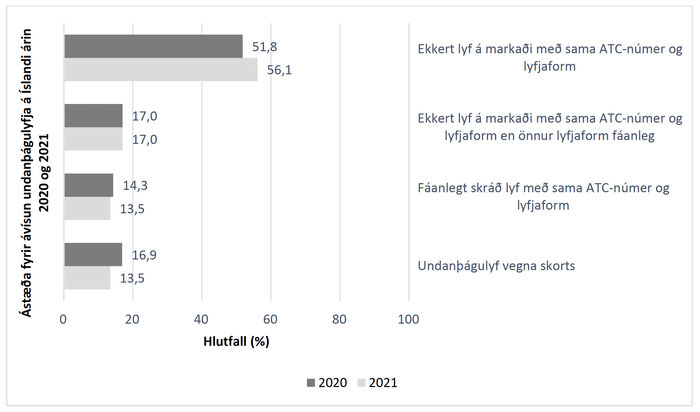
Mynd 2. Ástæða fyrir ávísun undanþágulyfja á Íslandi árin 2020 og 2021. Myndin sýnir hlutföll samþykktra undanþágulyfja fyrir hvern flokk. (ATC - Anatomical Therapeutic Chemical Code).
Á myndinni sést að rétt rúmur helmingur undanþágulyfja sem ávísað er á Íslandi á sér ekkert hliðstætt lyf á markaði með sama ATC-númer og lyfjaform. Hlutfallið hækkar milli ára, úr 51,8% árið 2020 í 56,1% árið 2021. Aðeins lítill hluti undanþágulyfja var samþykktur vegna skorts og þeim fækkaði milli ára.
Undanþágulyf samþykkt vegna skorts voru samþykkt af því að skráða lyfið skorti tímabundið ásamt þeim sem voru afskráð á árinu eða árinu á undan. Afskráð lyf voru flokkuð í tvo flokka, eftir því hvort þau voru samþykkt eftir að ár var liðið frá afskráningu eða áður en ár var liðið frá afskráningu. Flest þau undanþágulyf sem samþykkt voru vegna afskráningar í báðum hópum áttu sér ekkert lyf á markaði með sama ATC-númer og lyfjaform. Þau undanþágulyf sem samþykkt voru vegna þess að skráða lyfið skorti tímabundið var 8,8% árið 2020 og 7,6% árið 2021.
Mest ávísuðu undanþágulyfin á Íslandi árin 2020 og 2021
Þau 10 lyf sem mest var ávísað af undanþágulyfjum á Íslandi sem samþykkt voru af Lyfjastofnun árið 2020 má sjá í töflu I og fyrir árið 2021 í töflu II. 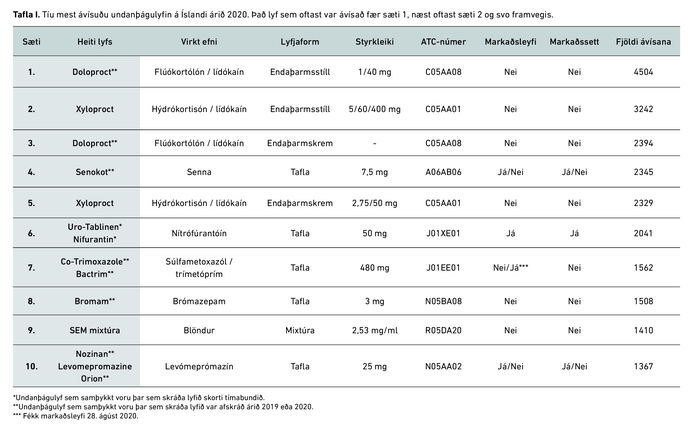
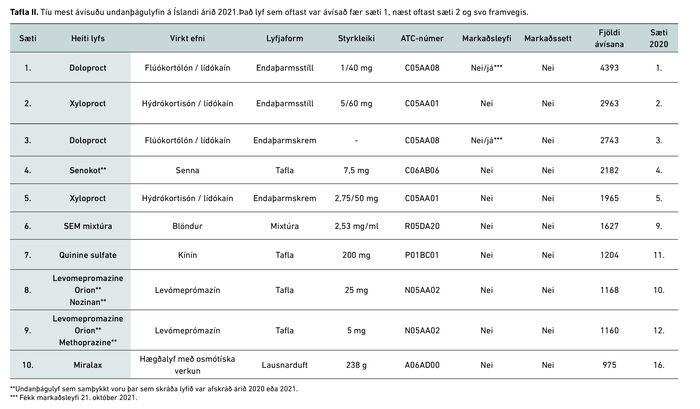
Það lyf sem oftast var ávísað fær sæti 1, næst oftast sæti 2 og svo framvegis. Af 10 mest ávísuðu undanþágulyfjunum árið 2020 var aðeins eitt lyf samþykkt þar sem skráða lyfið skorti tímabundið, samanborið við árið 2021 þegar ekkert lyf var samþykkt þar sem skráða lyfið skorti tímabundið. Tíu mest ávísuðu undanþágulyfin árið 2021 voru öll samþykkt árið 2020.
Í töflu I og II má einnig sjá hvort undanþágulyfið hafði lyf með markaðsleyfi á Íslandi og hvort það lyf var markaðssett hér. Árið 2020 var eitt lyf sem hlaut markaðsleyfi á árinu en það var ekki markaðssett fyrr en í byrjun árs 2021. Tvö lyf voru tekin af markaði og aðeins eitt lyf hafði markaðsleyfi og var markaðssett á árinu. Árið 2021 fékk Doloproct® markaðsleyfi fyrir bæði endaþarmsstíla og krem en var ekki markaðssett. Ekkert af 10 mest ávísuðu undanþágulyfjunum árið 2021 hafði markaðssett lyf á íslenskum markaði. Fimm mest ávísuðu undanþágulyfin voru þau sömu fyrir bæði árin.
Þegar horft var til 50 mest ávísuðu undanþágulyfjanna á Íslandi sem samþykkt voru af Lyfjastofnun árin 2020 og 2021 mátti sjá að 70% lyfjanna voru þau sömu bæði árin. Á mynd 3 má sjá ástæður fyrir ávísunum 50 mest ávísuðu undanþágulyfja á Íslandi árin 2020 og 2021.
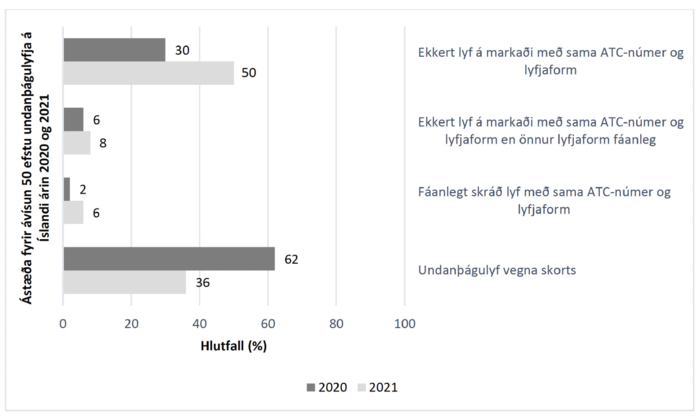
Mynd 3. Ástæður fyrir ávísunum 50 algengustu undanþágulyfja á Íslandi árin 2020 og 2021. Myndin sýnir hlutföll samþykktra undanþágulyfja fyrir hvern flokk. (ATC - Anatomical Therapeutic Chemical Code).
Undanþágulyf sem samþykkt voru vegna skorts voru þau undanþágulyf sem voru samþykkt af því að skráða lyfið skorti tímabundið ásamt þeim sem voru afskráð á árinu eða árinu á undan. Þau undanþágulyf sem ávísað var vegna þess að skráða lyfið skorti tímabundið voru 30% árið 2020 og 10% árið 2021.
Tíu, 30 og 50 mest ávísuðu undanþágulyfin eru stór hluti af heildarfjölda samþykktra umsókna árið 2020 og 2021. Tíu mest ávísuðu lyfin voru 46,8% af samþykktum umsóknum árið 2020 samanborið við árið 2021 þegar þau voru 43,8% af samþykktum umsóknum. Þrjátíu mest ávísuðu lyfin voru 70,7% árið 2020 og 67,3% árið 2021 og 50 mest ávísuðu lyfin voru 79,5% árið 2020 og 76,2% árið 2021.
Undanþágulyf í Svíþjóð árið 2020
Lyfjastofnun í Svíþjóð samþykkti 38.458 undanþágulyfjaumsóknir árið 2020. Í heildina voru samþykkt 1797 mismunandi vörunúmer.
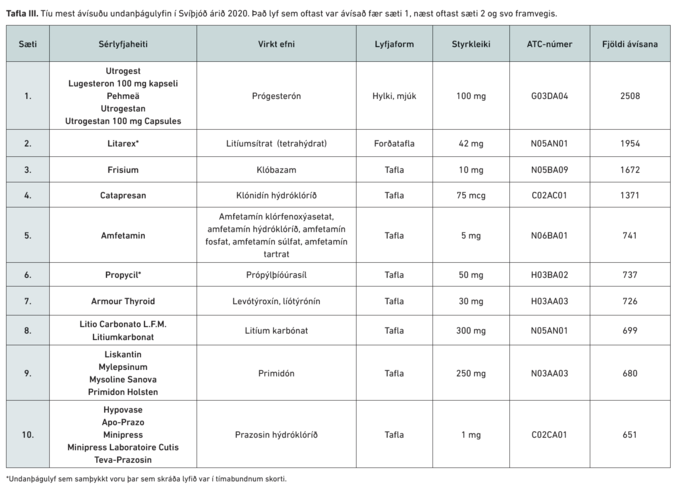
Í töflu III má sjá þau 10 undanþágulyf sem oftast var ávísað í Svíþjóð árið 2020. Mikill munur var á samþykktum umsóknum á sæti fjögur og fimm. Fjórum mest ávísuðu lyfin voru 19,5% af heildarfjölda samþykktra umsókna.
Þegar horft var til ástæðna fyrir ávísunum á 50 mest ávísuðu undanþágulyfin í Svíþjóð árið 2020 voru 12% undanþágulyfja samþykkt vegna þess að skráða lyfið skorti tímabundið. Þar sem ekkert lyf var á markaði með sama ATC-númer og lyfjaform var 46% af samþykktum undanþágum. Í 26% tilfella var undanþága samþykkt þar sem ekkert lyf var á markaði með sama ATC-númer og lyfjaform en annað lyfjaform var fáanlegt. Í 16% tilfella var undanþága samþykkt þar sem lyf með sama ATC-númer og lyfjaform var fáanlegt.. Meirihluti undanþágulyfja sem var mest ávísað í Svíþjóð árið 2020 voru samþykkt þar sem ekkert lyf var á markaði með sama ATC-númer og lyfjaform.
Ef heildarfjöldi samþykktra umsókna á 10, 30 og 50 mest ávísuðu lyfjunum er skoðaður fyrir árið 2020 sést að 10 algengustu lyfin voru 30,5%, 30 algengustu voru 50,5% og 50 efstu 59,4% af heildarfjölda. Fimmtíu efstu undanþágulyfin í Svíþjóð voru því meirihluti af heildarfjölda samþykktra umsókna.
Umræða
Undanþágulyf á Íslandi 2020-2021
Niðurstöður sýna að undanþágulyfjum fjölgaði en umsóknum fækkaði milli ára. Mikill meirihluti undanþágulyfja sem ávísað er á Íslandi eiga sér ekkert hliðstætt lyf á markaði með sama ATC-númer og lyfjaform og aðeins litlum hluta undanþágulyfja var ávísað vegna þess að skráða lyfið skorti tímabundið bæði árin. Þau undanþágulyf sem var mest ávísað bæði árin voru meira og minna sömu lyfin, og sömu lyfin skipa toppsætin ár frá ári. Þrátt fyrir mörg þúsund umsóknir er aðeins um nokkra tugi lyfja að ræða sem standa að baki heildarumfangi. Því myndi átaksverkefni með það að markmiði að hvetja til skráningar á 30-50 algengustu lyfjunum geta skilað talsverðri minnkun á heildarfjölda ávísana undanþágulyfja.
Ástæðan fyrir því að sömu lyfin eru efst ár frá ári ásamt því að meirihluti undanþágulyfja hefur ekkert skráð lyf með sama ATC-númer og lyfjaform gæti verið að markaðsleyfishafar hafi ekki áhuga á að markaðssetja ákveðin lyf hér á landi þar sem hagnaður er mögulega ekki jafn mikill og á öðrum mörkuðum eða lyfjum. Markaðsleyfishafar þurfa að greiða ýmis gjöld af þeim lyfjum sem þeir eru með markaðssett13 og ef sala er ekki mikil á lyfjunum geta markaðsleyfishafar séð sér meiri hag í því að halda slíkum lyfjum í undanþágulyfjakerfinu fremur en að markaðssetja þau og sleppa við ýmis gjöld er fylgja markaðssetningunni. Þetta getur verið varhugavert þar sem ávísun undanþágulyfja ætti einungis að koma til þegar rík nauðsyn krefur eða sérstakar ástæður. Til dæmis þegar skortur verður á skráðum lyfjum. Út frá þessum niðurstöðum má álykta að lítill hvati sé fyrir markaðsleyfishafa til þess að markaðssetja hér á landi þau lyf sem hefur mest verið ávísað á undanþágu undanfarin ár.
Lyfjaverð gæti einnig skipt máli, en hámarksverð lyfja í heildsölu á Íslandi er ákvarðað út frá ströngum kröfum og við ákvörðun er tekið mið af lægsta verði sömu lyfja á Norðurlöndunum.14 Í samanburði við Norðurlöndin reynist lyfjaverð á Íslandi almennt lágt,15 sem getur valdið því að íslenskur markaður sé ekki eins áhugaverður og aðrir markaðir. Þeim mun lægra sem lyfjaverð er, því meiri hætta er á skorti og ef verðið er of lágt er einnig minni ásókn í að koma lyfjum á markað.1
Staða undanþágulyfja á Íslandi samanborið við Svíþjóð árið 2020
Ávísun undanþágulyfja á Íslandi er fremur mikil samanborið við Svíþjóð þegar horft er á fólksfjölda. Svíþjóð er fjölmennast Norðurlandanna en íbúar árið 2020 í Svíþjóð voru 10.327.589 íbúar16 samanborið við Ísland þar sem voru 364.134 íbúar árið 2020.17 Merkilegt þykir því að samþykktar undanþágulyfja-umsóknir í Svíþjóð voru færri en á Íslandi árið 2020. Lyfjaframboð í löndunum tveimur getur haft áhrif á þennan mun milli landanna. Árið 2020 voru 3556 vörunúmer markaðssett á Íslandi samanborið við 14.859 vörunúmer í Svíþjóð. Það er því ljóst að lyfjaframboð er töluvert meira í Svíþjóð og neyðast læknar því ekki jafn oft til að sækja um undanþágu fyrir lyf þegar ekkert annað stendur til boða.
Mest ávísuðu undanþágulyfin eru stór hluti af heildarfjölda samþykktra umsókna bæði í Svíþjóð og á Íslandi. Ástæður fyrir ávísun á algengustu undanþágulyfin voru mismunandi milli landa, en undanþágulyf sem ávísað var vegna skorts voru fleiri á Íslandi en í Svíþjóð. Úrræði vegna lyfja sem skortur verður á eru líklega fleiri í Svíþjóð en á Íslandi og meiri möguleikar til að nota skráð lyf líkt og samheitalyf þar í landi. Sem dæmi má nefna að samþykktar umsóknir um mest ávísaða lyfið í Svíþjóð eru töluvert færri en á Íslandi en í Svíþjóð er það lyf fáanlegt á öðru lyfjaformi með sama ATC-númer og gæti það lyfjaform hentað meirihluta sjúklinga sem nota lyfið. Mest ávísaða undanþágulyfið á Íslandi er hins vegar ekki með neitt lyf á markaði með sama ATC-númer og lyfjaform: svo læknar hafa ekkert annað val.
Úrræði
Hvatakerfi fyrir lyf sem hafa verið í undanþágukerfinu með margar ávísanir í lengri tíma
Út frá niðurstöðum þessarar rannsóknar má sjá að ef það tækist að skrá hluta af mest ávísuðu undanþágulyfjunum, mætti fækka ávísunum undanþágulyfja um að minnsta kosti helming. Það myndi skila sér í minni óþægindum fyrir sjúklinga, lægri kostnaði vegna vinnu lækna, lyfjafræðinga og starfsfólks lyfjastofnunar. Kanna mætti hvort einhvers konar hvati eða breytingar á regluverki, hvað verð eða gjöld varðar, yrði til þess að fá umrædd lyf skráð. Það er verðugt verkefni og fer að sjálfsögðu mikið eftir því hverjar eru raunverulegar ástæður fyrir því að umrædd lyf eru ekki skráð. Augljóst er að markaðurinn virkar ekki eins og best verður á kosið fyrir þessi lyf, þar sem sömu lyfin sitja föst í efstu sætum, jafnvel þótt Lyfjastofnun hafi undanfarin ár sent út lista yfir mest ávísuðu undanþágulyfin og hvatt markaðsleyfishafa og umboðsmenn til að markaðssetja umrædd lyf. En stofnunin hefur tekið saman lista yfir mest ávísuðu lyfin og birt sem frétt á vefsíðu stofnunarinnar og sent til umboðsmanna og markaðsleyfishafa á Íslandi.18
Aukin heimild lyfjafræðinga til að einfalda afgreiðslu undanþágulyfja
Í dag er lyfjafræðingum heimilt að breyta hefðbundnum lyfseðli yfir í undanþágulyfið þegar Lyfjastofnun gefur heimild til.6 Sjúklingur þarf þá ekki að fara aftur til læknis til þess eins að fá undanþágulyfseðil. Heimildin einfaldar því ferlið fyrir undanþágulyf til muna og er góð lausn fyrir sjúklinga, lyfjafræðinga og lækna. Nýlega hafa lyfjafræðingar fengið slíka heimild veitta oftar þegar mikið notuð lyf skortir í landinu og ekkert annað samheitalyf með markaðsleyfi er fáanlegt. Líklegt er að áframhaldandi veiting þessarar heimildar muni einfalda sjúklingum og heilbrigðisstarfsfólki að takast á við það þegar mikið ávísuð lyf skortir með skömmum fyrirvara og eina lausnin er útvegun á undanþágulyfi. Það mun þó líklega ekki hafa mjög mikil áhrif á heildarumfang undanþágulyfja þar sem ávísanir vegna skorts eru ekki stór hluti ávísana á undanþágulyf.
Að einfalda ferlið eða fjölga slíkum heimildum getur einnig verið varhugavert ef aðgengi að undanþágulyfjum verður þá auðveldara. Það gæti ýtt undir afskráningu lyfja í sparnaðarskyni fyrir lyfjafyrirtæki ef þau gera ráð fyrir að lyfinu verði ávísað hvort sem er. Heimildina ætti því að reyna takmarka við tilvik þar sem klárlega er um að ræða skráð lyf sem skortir tímabundið og engin önnur meðferðarúrræði í boði.
Rafrænir fylgiseðlar
Dýrt getur verið fyrir lyfjafyrirtæki að markaðssetja lyf með íslenskum upplýsingum þar sem þau einskorðast aðeins við einn lyfjamarkað en samkvæmt lyfjalögum eiga fylgiseðlar að vera á íslensku og fylgja hverri lyfjapakkningu.19 Undanþágulyfjum fylgja ekki upplýsingar á íslensku, sem er erfitt fyrir marga sjúklinga. Í dag stendur yfir tilraunaverkefni um rafræna fylgiseðla fyrir lyf sem notuð eru á heilbrigðisstofnunum.20 Fari svo að lyfjaregluverk í Evrópu opni fyrir sveigjanleika hvað varðar atriði eins og rafræna fylgiseðla og aðrar merkingar, verður áhugavert að sjá hvort lyfjum fjölgar á markaði hér á landi með tilheyrandi fækkun undanþágulyfja. Þá gætu lyfjafyrirtæki mögulega í meira mæli samræmt pakkningar, sama fyrir hvaða markað þær eru.
Takmarkanir og styrkleikar rannsóknarinnar
Þetta er fyrsta rannsóknin á umfangi undanþágulyfja sem gerð er á Íslandi og gefur ákveðna mynd af stöðu undanþágulyfja hér á árunum 2020-2021 samanborið við Svíþjóð árið 2020. Rannsóknin byggir á áreiðanlegum gögnum og gefur einnig aukna möguleika á frekari rannsóknum.
Helsti veikleiki rannsóknarinnar er að rannsakað var umfang undanþágulyfja út frá ályktunum um ástæður fyrir ávísunum undanþágulyfja og flokkun eftir því hvort til var sambærilegt markaðssett lyf á markaði eða hvort markaðssett lyf skorti á ákveðnum tíma. Ekki voru skoðaðar sérstaklega ástæður fyrir ávísunum undanþágulyfja á Íslandi út frá rökstuðningi læknis fyrir ávísun þeirra. Enda þótt lyf hafi verið samþykkt á sama tíma og skráða lyfið skorti tímabundið, er ekki víst að allar umsóknir um það lyf hafi verið samþykktar vegna skorts, það gæti verið önnur ástæða fyrir ávísuninni. Þetta gæti skekkt niðurstöðurnar.
Ályktun
Niðurstöður sýna að mörg þeirra undanþágulyfja sem er mest ávísað á Íslandi eru þau sömu ár eftir ár og aðeins litlum hluta undanþágulyfja var ávísað vegna þess að skráða lyfið skorti tímabundið. Á lyfjamarkaðnum hérlendis er framboðið lítið í samanburði við Svíþjóð og eru tækifæri til staðar til að draga úr ávísunum undanþágulyfja á Íslandi til hagsbóta fyrir skjólstæðinga, lækna og lyfjafræðinga.
Þakkir
Lyfjastofnun Íslands og í Svíþjóð fá þakkir fyrir að veita aðgang að þeim gögnum sem þurfti við gerð rannsóknar.
Heimildir
| 1. Shukar S, Zahoor F, Hayat K, et al. Drug Shortage: Causes, Impact, and Mitigation Strategies. Front Pharmacol 9. júlí 2021; 12: 693426. https://doi.org/10.3389/fphar.2021.693426 PMid:34305603 PMCid:PMC8299364 |
||||
| 2. Bochenek T, Abilova V, Alkan A, et al. Systemic Measures and Legislative and Organizational Frameworks Aimed at Preventing or Mitigating Drug Shortages in 28 European and Western Asian Countries. Front Pharmacol 2018; 8: 942. https://doi.org/10.3389/fphar.2017.00942 PMid:29403372 PMCid:PMC5779072 |
||||
| 3. Undanþágulyf. Lyfjastofnun. lyfjastofnun.is/lyf/undanthagulyf/ - nóvember 2021. | ||||
| 4. Donovan G, Parkin L, Wilkes S. Special unlicensed medicines: what we do and do not know about them. Br J Gen Pract 2015 2021; 65: e861-3. https://doi.org/10.3399/bjgp15X688033 PMid:26622038 PMCid:PMC4655741 |
||||
| 5. European Commission. DIRECTIVE 2001/83/EC OF THEUROPEAN PARLIAMENT AND OF THE COUNCIL 2012. | ||||
| 6. Lyfjalög nr. 100, 2020. althingi.is/lagas/nuna/2020100.html - maí 2023. | ||||
| 7. Reglugerð um lyfjaávísanir og afhendingu lyfja nr. 740. reglugerd.is/reglugerdir/allar/nr/0740-2020 - maí 2023. | ||||
| 8. Áríðandi tilkynning til apóteka. Lyfjastofnun 2022. lyfjastofnun.is/frettir/aridandi-tilkynning-til-apoteka / - maí 2023. | ||||
| 9. Zitromax 500 mg og Azithromycin STADA 500 mg. Lyfjastofnun 2023. lyfjastofnun.is/lyfjaskortsfrettir/zitromax-500-mg-og-azithromycin-stada-500-mg/ - maí 2023. | ||||
| 10. Upplýsingar um undanþágulyf fyrir heilbrigðisstarfsfólk. Lyfjastofnun 2021. lyfjastofnun.is/lyf/undanthagulyf/upplysingar-um-undanthagulyf-fyrir-heilbrigdistarfsfolk/ - maí 2023. | ||||
| 11. Licens för läkemedel. Swedish Medical Products agency 2022. lakemedelsverket.se/sv/behandling-och-forskrivning/forskrivning/licenser - maí 2023. | ||||
| 12. ATC flokkun. Lyfjastofnun. serlyfjaskra.is/atc - maí 2023. | ||||
| 13. GJALDSKRÁ fyrir markaðsleyfi, árgjöld og önnur gjöld vegna lyfja sem Lyfjastofnun innheimtir nr. 1160. Lyfjastofnun 2018. lyfjastofnun.is/wp-content/eplica_media/lyfjastofnun/B_nr_1160_2018.pdf - maí 2023. | ||||
| 14. Reglugerð um verðlagningu lyfja og greiðsluþátttöku í lyfjum nr. 1414. 2020. island.is/reglugerdir/nr/1414-2020 - maí 2023. | ||||
| 15. Haraldsson G, Friðriksson KS, Skúlason MÁ. Rannsókn á lyfjamarkaði, verðlagning heildsölulyfja á Íslandi. Skýrsla Intellecon; 2018. old.frumtok.is/Media/intellecon-rannsokn-a-lyfjamarkadi.pdf - maí 2023. | ||||
| 16. Staðreyndir um Svíþjóð. Norrænt samstarf 2022. norden.org/is/information/stadreyndir-um-svithjod - maí 2023. | ||||
| 17. Lykiltölur mannfjöldans 1703-2022. Hagstofa Íslands 2022. hagstofa.is - maí 2023. | ||||
| 18. Undanþágulyf sem oftast var ávísað í nóvember 2022. Lyfjastofnun 2022. lyfjastofnun.is/frettir/undanthagulyf-sem-oftast-var-avisad-i-november-2022/ - maí 2023. | ||||
| 19. Reglugerð um markaðsleyfi sérlyfja, merkingar þeirra og fylgiseðla nr. 545. 2018. island.is/reglugerdir/nr/0545-2018 - maí 2023. | ||||
| 20. Rafrænir fylgiseðlar. Lyfjastofnun 2022. http://lyfjastofnun.is/lyf/rafraenir-fylgisedlar/ - maí 2023. | ||||