02. tbl. 108. árg. 2022
Fræðigrein
Nýgengi stokkasega á Íslandi frá 2008 til 2020
Ágrip
INNGANGUR
Stokkasegi er orsök um 0,5-1% allra heilablóðfalla. Stokkasegi getur valdið blæðingu og/eða heiladrepi auk hækkaðs innankúpuþrýstings. Erfitt getur reynst að greina stokkasega vegna fjölbreyttra einkenna og erfiðrar myndgreiningar á köflum. Markmið rannsóknarinnar var að rannsaka nýgengi stokkasega á Íslandi á tímabilinu 2008-2020, áhættuþætti, einkenni, meðferð og horfur.
EFNIVIÐUR OG AÐFERÐIR
Framkvæmd var lýsandi afturskyggn rannsókn án viðmiðunarhóps þar sem upplýsingum úr sjúkraskrám einstaklinga sem greindust með stokkasega á tímabilinu frá 1. janúar 2008 til 31. desember 2020 var safnað. Eftirfarandi þættir voru skoðaðir: kyn, greiningarár, aldur við greiningu, einkenni, þekktir áhættuþættir, rannsóknarniðurstöður, meðferðir og afdrif. Úrvinnsla fór fram í Excel og Rstudio.
NIÐURSTÖÐUR
Alls greindist 31 einstaklingar (22 konur). Meðalnýgengið var 0,72/100.000 manns á ári. Meðalaldur var 34,3 ár (14-63 ára). Algengasta einkennið var höfuðverkur (87%), önnur voru staðbundin taugaeinkenni, flog og skert meðvitund. Algengasti áhættuþátturinn meðal kvenna var notkun getnaðarvarnarlyfja (73%). Fjórir sjúklingar höfðu engan þekktan áhættuþátt. Í 74% tilfella var seginn í þverstokki. Stokkasegi var í tveimur eða fleiri bláæðastokkum í 58% tilfella. Allir sjúklingarnir voru settir á blóðþynningarmeðferð. Langoftast var byrjað á heparíni/léttheparíni og síðan tók við meðferð á warfaríni eða NOAC-lyfjum. Eftir þrjá mánuði mældust 87% sjúklinganna með 0-2 á modified Rankin-skalanum (mRS) og höfðu því enga eða væga fötlun eftir stokkasegann. Einn sjúklingur lést vegna stokkasega.
ÁLYKTANIR
Nýgengi stokkasega á Íslandi er í samræmi við erlendar rannsóknir. Höfuðverkur var algengasta einkennið og getnaðarvarnarlyf algengasti áhættuþátturinn meðal kvenna. Flestir sjúklinganna náðu góðum bata sem bendir til tímanlegrar greiningar og viðeigandi meðferðar á Íslandi.
Greinin barst til blaðsins 22. ágúst 2021, samþykkt til birtingar 5. janúar 2022.
Inngangur
Stokkasegi (cerebral venous and sinus thrombosis) er sjaldgæf orsök heilablóðfalls í bláæðakerfi heilans. Lengi vel greindist stokkasegi nær eingöngu við krufningar og var sjúkdómurinn því talinn vera orsök andláts í flestum tilfellum. Þökk sé aukinni þekkingu á áhættuþáttum, betri myndgreiningartækni og fleiri meðferðarmöguleikum er dánartíðni vegna stokkasega mun lægri en áður.1 Þrátt fyrir aukna þekkingu á stokkasega getur verið snúið að greina sjúkdóminn vegna fjölbreyttra einkenna og erfiðrar myndgreiningar á köflum. Greining stokkasega byggist á klínískri grunsemd og myndrannsóknum. Myndrannsóknir eru einnig meginaðferðin til að meta mögulega fylgikvilla stokkasega, til dæmis blæðingar, heiladrep eða þrýstingsáhrif innan höfuðkúpu sem geta haft áhrif á afdrif sjúklingsins. Mynd 1 sýnir helstu bláæðastokka heilans.2
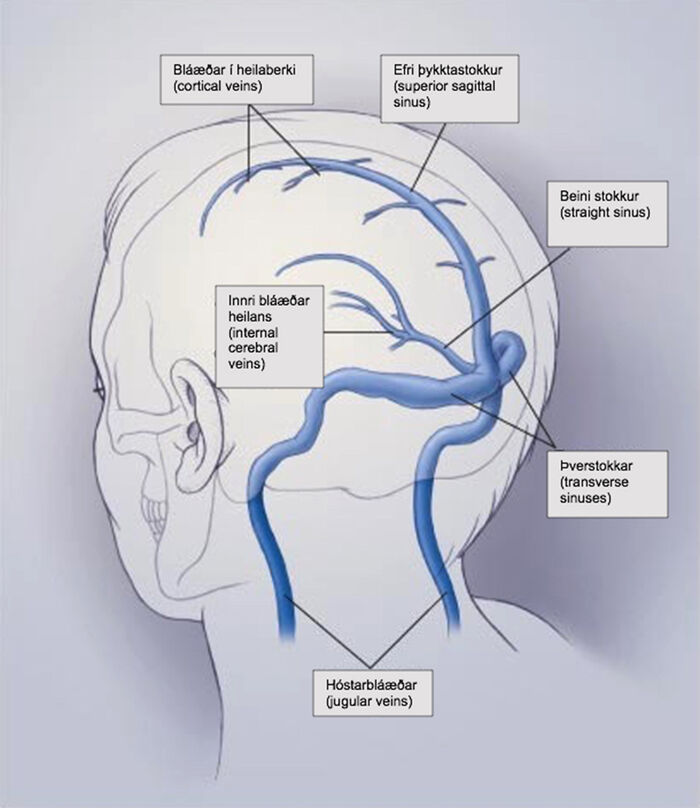 Mynd 1. Helstu bláæðar og bláæðastokkar heilans.
Mynd 1. Helstu bláæðar og bláæðastokkar heilans.
Erfitt hefur reynst að fullyrða með vissu um nýgengi stokkasega. Í fyrri rannsóknum hefur nýgengið verið á bilinu 0,2-2,02 á hverja 100.000 íbúa á ári, en talið er að stokkasegi sé orsök um 0,5-1% allra heilablóðfalla.3-7 Nýgengi stokkasega á Íslandi hefur aldrei áður verið kannað. Markmið rannsóknarinnar var að kortleggja nýgengi stokkasega og að kanna áhættuþætti, einkenni, greiningu, meðferð og horfur á Íslandi yfir tímabilið 2008-2020.
Efniviður og aðferðir
Framkvæmd var afturskyggn rannsókn sem náði yfir tímabilið frá 2008 til 2020. Þýðið samanstóð af þeim sem hlutu greiningarkóða I63.6 og I67.6 í samræmi við Alþjóðlegt flokkunarkerfi sjúkdóma og skyldra heilbrigðisvandamála 10 (International Classification of Diseases and Related Conditions 10, ICD 10). Upplýsinga var aflað úr Sögukerfi og Heilsugátt. Eftirfarandi gögnum var safnað: greiningarár, aldur við greiningu, kyn, áhættuþættir fyrir stokkasega (ættgengar segahneigðir, áunnar segahneigðir, meðganga og sængurlega, blóðsjúkdómar, bólgusjúkdómar, krabbamein, sýkingar, lyf og aðrir áhættuþættir), einkenni (höfuðverkur, ógleði og uppköst, flog (staðbundin, störu- eða alflog), skert meðvitund, sjóntruflanir og staðbundin taugaeinkenni (helftarlömun, málstol, verkstol)), rannsóknarniðurstöður úr myndrannsóknum (segulómun, tölvusneiðmynd), meðferð (lyfjagjöf, lengd meðferðar, sjúkrahúsinnlögn, gjörgæsluinnlögn, skurðaðgerðir og lengd sjúkrahúsvistar) og afdrif. Einkenni töldust bráð ef tíminn frá fyrstu einkennum til greiningar var styttri en 48 klukkustundir, meðalbráð ef tíminn var á milli 48 klukkustundir og 30 dagar og langvinn ef tíminn var lengri en 30 dagar. Afdrif sjúklinga voru miðuð við modified Rankin Scale (mRS) þremur mánuðum eftir greiningu.
Tölfræðiúrvinnsla
Rannsóknarupplýsingum var safnað í Microsoft Excel® skjal. Nýgengi stokkasega var reiknað með notkun mannfjöldatalna frá Hagstofu Íslands frá 1. júlí hvert ár frá 2008 til 2011 en frá öðrum ársfjórðungi hvers árs frá 2012 til 2020. Tölfræðileg úrvinnsla gagnanna og útreikningar voru framkvæmdir í Rstudio en Microsoft Word®, Microsoft Excel® og Rstudio voru notuð til að búa til töflur og gröf. Notað var Fisher tilgátupróf fyrir flokkabreytur en t-próf fyrir talnabreytur. Tölfræðileg marktækni var miðuð við p<0,05.
Leyfi frá vísindasiðanefnd (VSN-20-185) og vísindarannsóknar-nefnd Landspítala lágu fyrir við upphaf rannsóknar.
Niðurstöður
Rannsóknarþýðið samanstóð af 40 einstaklingum sem greindust með stokkasega á árunum 2008-2020 á Landspítala eða Sjúkrahúsinu á Akureyri. Fjórir reyndust hafa verið ranglega greindir eða ómögulegt að staðfesta greininguna. Ennfremur voru 5 sjúklingar erlendir ferðamenn sem greindust með stokkasega meðan á dvöl þeirra á Íslandi stóð. Þar sem þeir höfðu ekki búsetu á Íslandi og því ekki hluti af faraldsfræðilegri rannsókn, voru þeir undanskildir.
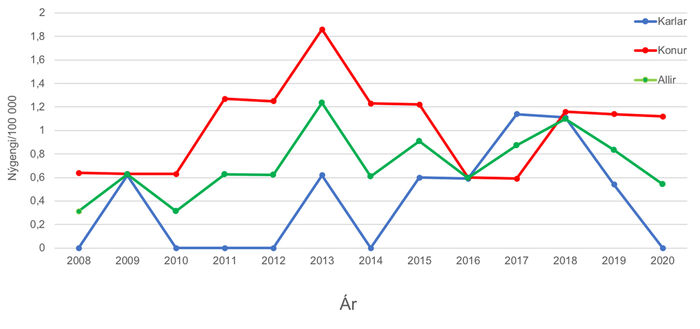 Mynd 2. Nýgengi á hverja 100.000 íbúa á ári. Græna línan sýnir nýgengi innan alls úrtaksins, rauða línan sýnir nýgengi meðal kvenna og bláa línan nýgengi meðal karla.
Mynd 2. Nýgengi á hverja 100.000 íbúa á ári. Græna línan sýnir nýgengi innan alls úrtaksins, rauða línan sýnir nýgengi meðal kvenna og bláa línan nýgengi meðal karla.
Alls greindist því 31 með stokkasega á árunum 2008–2020, eða um 1-4 á ári. Meðalfjöldi tilfella var 2,4 á ári. Meðalnýgengi stokkasega fyrir tímabilið var 0,7 tilfelli á hverja 100.000 íbúa á ári. Flestar greiningar stokkasega voru árin 2013 og 2018 en bæði árin voru tilfellin fjögur talsins. Mynd 2 sýnir nýgengi stokkasega fyrir hverja 100.000 íbúa á ári yfir rannsóknartímabilið, flokkað eftir kyni.
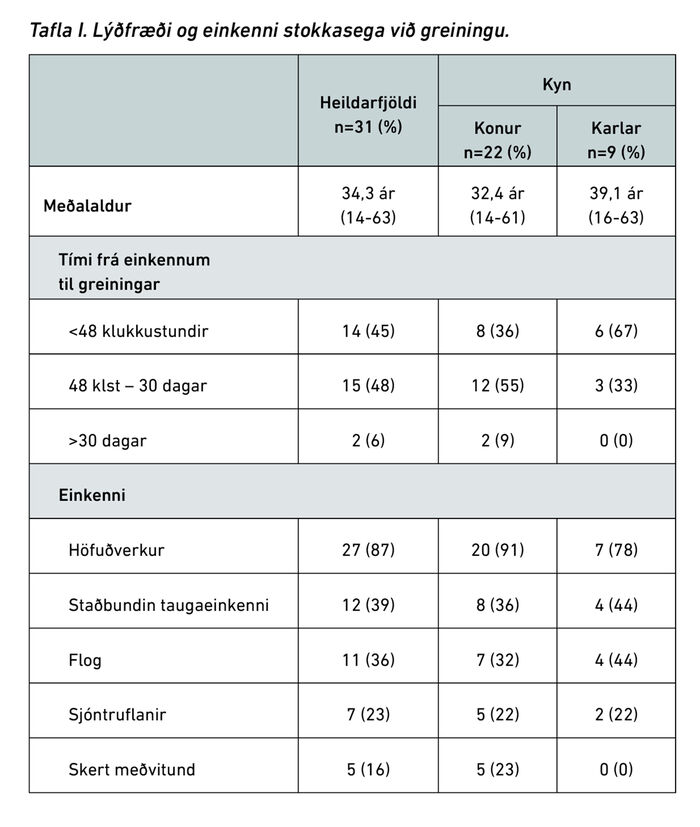 Tafla I sýnir lýðfræði og einkenni við greiningu. Um 70% úrtaksins voru konur (n=22). Kynjahlutfallið var 2,4:1. Meðalaldur var 34,3 ár en miðgildi aldurs var 30 ár, yngsti einstaklingurinn var 14 ára en sá elsti 63 ára. 74% sjúklinga voru yngri en 50 ára. Meðalaldur karla var 39,1 en 32,4 ár meðal kvenna (p=0,3). Einn sjúklingur hafði fyrri sögu um stokkasega. Fjórir sjúklingar höfðu fyrri sögu um bláæðasega af annarri gerð en stokkasega.
Tafla I sýnir lýðfræði og einkenni við greiningu. Um 70% úrtaksins voru konur (n=22). Kynjahlutfallið var 2,4:1. Meðalaldur var 34,3 ár en miðgildi aldurs var 30 ár, yngsti einstaklingurinn var 14 ára en sá elsti 63 ára. 74% sjúklinga voru yngri en 50 ára. Meðalaldur karla var 39,1 en 32,4 ár meðal kvenna (p=0,3). Einn sjúklingur hafði fyrri sögu um stokkasega. Fjórir sjúklingar höfðu fyrri sögu um bláæðasega af annarri gerð en stokkasega.
Algengustu einkennin voru höfuðverkur (87%), staðbundin taugaeinkenni (39%), flog (36%) og sjóntruflanir (23%). Höfuðverknum fylgdu ógleði og uppköst í um 70% tilfella. Staðbundin taugaeinkenni voru helftarlömun, málstol, verkstol og breytt snerti-skyn í andliti og/eða útlimum. Fjórir sjúklingar fengu staðbundin flog (13%), einn fékk störuflog (3%) en 10 fengu alflog (32%). Fimm sjúklingar (16%) voru með skerta meðvitund við komu á bráðamóttöku. Tími frá upphafi einkenna til staðfestrar greiningar var að meðaltali 9,2 dagar. Fjórtán manns (45%) höfðu bráð einkenni (<48 klst), 15 (48%) höfðu meðalbráð einkenni (48 klst-30 dagar) og tveir (6%) höfðu haft langvinn einkenni (>30 dagar) fram að greiningu.
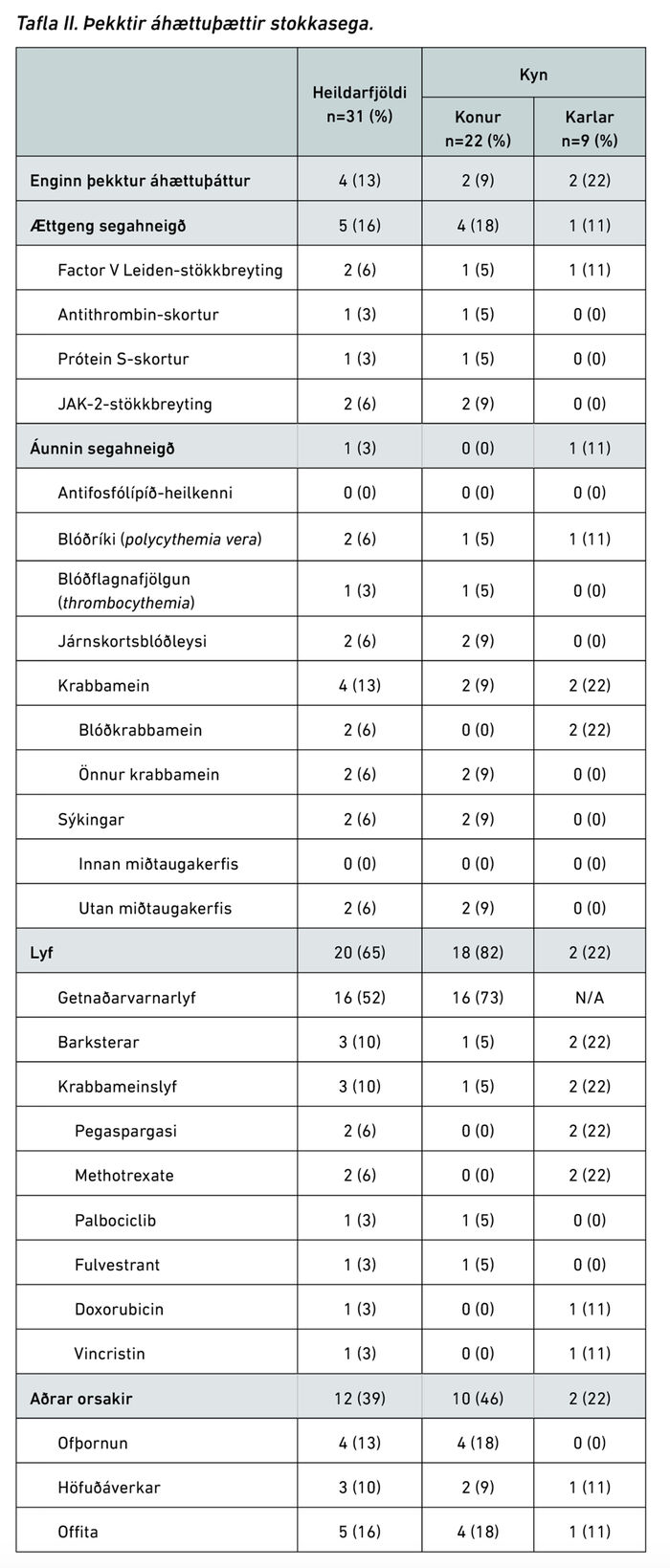 Yfirlit yfir þekkta áhættuþætti fyrir stokkasega má sjá á töflu II. Fjórir sjúklingar (13%) höfðu engan þekktan áhættuþátt. Fjórtán sjúklingar höfðu einn áhættuþátt (45%), 7 höfðu tvo áhættuþætti (23%) og 8 höfðu þrjá eða fleiri áhættuþætti (26%). Algengasti áhættuþátturinn var lyf (65%) og var þar marktækur munur á milli kynja (p=0,01) þar sem 73% kvenna sem greindust með stokkasega voru á getnaðarvarnarlyfjum.
Yfirlit yfir þekkta áhættuþætti fyrir stokkasega má sjá á töflu II. Fjórir sjúklingar (13%) höfðu engan þekktan áhættuþátt. Fjórtán sjúklingar höfðu einn áhættuþátt (45%), 7 höfðu tvo áhættuþætti (23%) og 8 höfðu þrjá eða fleiri áhættuþætti (26%). Algengasti áhættuþátturinn var lyf (65%) og var þar marktækur munur á milli kynja (p=0,01) þar sem 73% kvenna sem greindust með stokkasega voru á getnaðarvarnarlyfjum.
Fimm sjúklingar höfðu ættgenga segahneigð (16%). Af þeim höfðu tveir sjúklingar Factor V Leiden-stökkbreytingu (6%), einn sjúklingur hafði bæði antithrombín-skort og prótein S-skort (3%) og tveir höfðu JAK-2-stökkbreytingu (6%). Fimm sjúklingar voru með undirliggjandi blóðsjúkdóma (16%), þar af voru tveir með blóðríki (polycythemia vera), einn með blóðflagnafjölgun (essential thrombocythemia) og tveir með blóðleysi. Fjórir sjúklingar voru með krabbamein (13%), þar af tveir með bráðahvítblæði (6%). Tveir sjúklingar voru með undirliggjandi sýkingar (6%). Aðrir þekktir áhættuþættir stokkasega fundust hjá 12 sjúklingum (39%). Fjórir þeirra voru með ofþornun (13%), þrír voru með höfuðáverka (10%) og fimm voru með offitu (16%). Enginn sjúklingur var með bólgusjúkdóm og enginn var þungaður eða í sængurlegu.
Greining á stokkasega var staðfest með myndgreiningu hjá öllum sjúklingum. Einn sjúklingur fór í segulómun (3%) eingöngu, 13 (42%) fóru í tölvusneiðmynd (TS) og/eða TS bláæðamyndatöku og 17 (55%) einstaklingar fóru bæði í segulómun og tölvusneiðmynd. Algengasta staðsetningin fyrir stokkasega var í þverstokkum (transverse sinus) hjá 23 einstaklingum (74%) og efri þykktarstokki (superior sagittal sinus) hjá 14 manns (45%) (mynd 3). Stokkasegi kom fram í tveimur eða fleiri bláæðastokkum hjá 18 einstaklingum (58%). Fjórir sjúklingar sýndu merki um heiladrep við myndgreiningu (13%) og 8 sýndu merki um heilablæðingu (26%). Átta sjúklingar voru bæði með heiladrep og heilablæðingu (26%).
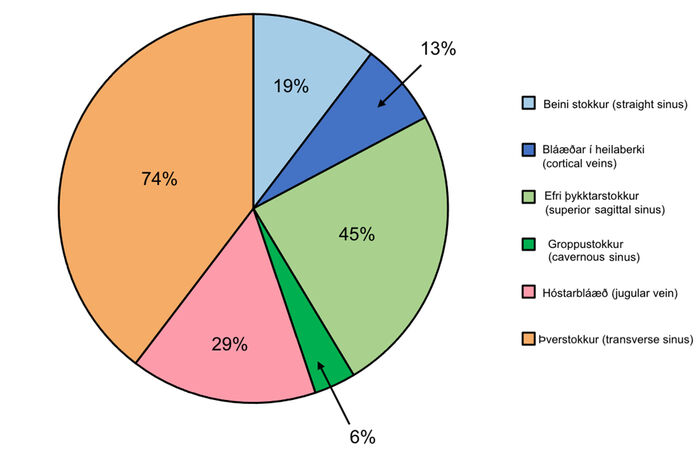 Mynd 3. Kökurit sem sýnir algengustu staðsetningar stokkasega.
Mynd 3. Kökurit sem sýnir algengustu staðsetningar stokkasega.
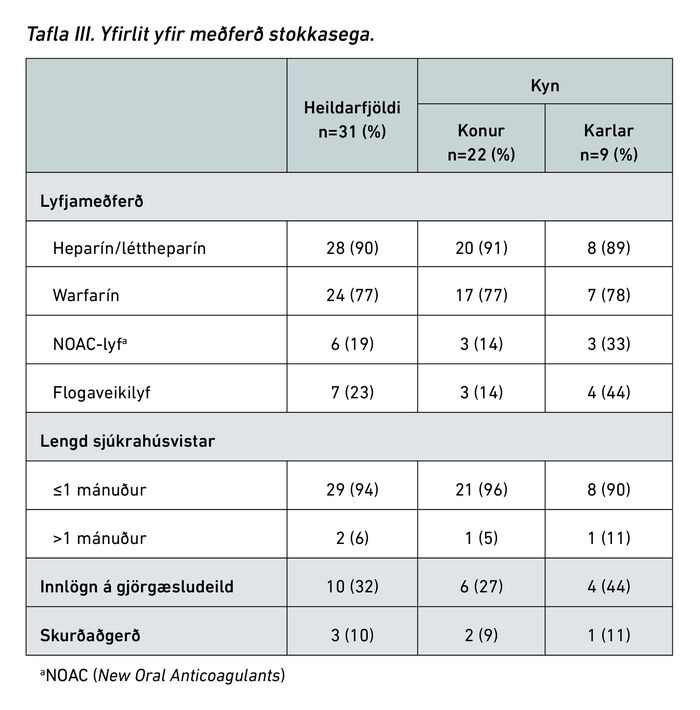 Yfirlit yfir meðferð sjúklinga sést í töflu III. Allir sjúklingarnir voru settir á blóðþynningarmeðferð, jafnvel þeir sem voru með heilablæðingu. Algengast var að hefja meðferð á heparíni eða léttheparíni og síðan tók við meðferð á warfaríni. Sex sjúklingar fóru á NOAC-lyf (New Oral Anticoagulants) (19%). Fimmtán sjúklingar (48%) voru á blóðþynningu í 6 mánuði eða skemur, en 16 voru á blóðþynningu lengur en 6 mánuði, þar af voru 9 sjúklingar settir á langtíma- eða ævilanga blóðþynningarmeðferð. Einnig voru allir sjúklingarnir lagðir inn á sjúkrahús. Meðallegutími var 15,3 dagar. Tíu voru lagðir inn á gjörgæslu í styttri eða lengri tíma (32%). Þrír sjúklingar (10%) þurftu á skurðaðgerð/-um að halda. Allir þrír gengust undir bráða kúpuopnun vegna blæðingar. Auk tæmingar á blæðingu voru framkvæmd brottnám á höfuðkúpubeini til þrýstingslækkunar (decompressive craniectomy) og hlutabrottnámi á heilavef (partial lobectomy) til þrýstingslækkunar.
Yfirlit yfir meðferð sjúklinga sést í töflu III. Allir sjúklingarnir voru settir á blóðþynningarmeðferð, jafnvel þeir sem voru með heilablæðingu. Algengast var að hefja meðferð á heparíni eða léttheparíni og síðan tók við meðferð á warfaríni. Sex sjúklingar fóru á NOAC-lyf (New Oral Anticoagulants) (19%). Fimmtán sjúklingar (48%) voru á blóðþynningu í 6 mánuði eða skemur, en 16 voru á blóðþynningu lengur en 6 mánuði, þar af voru 9 sjúklingar settir á langtíma- eða ævilanga blóðþynningarmeðferð. Einnig voru allir sjúklingarnir lagðir inn á sjúkrahús. Meðallegutími var 15,3 dagar. Tíu voru lagðir inn á gjörgæslu í styttri eða lengri tíma (32%). Þrír sjúklingar (10%) þurftu á skurðaðgerð/-um að halda. Allir þrír gengust undir bráða kúpuopnun vegna blæðingar. Auk tæmingar á blæðingu voru framkvæmd brottnám á höfuðkúpubeini til þrýstingslækkunar (decompressive craniectomy) og hlutabrottnámi á heilavef (partial lobectomy) til þrýstingslækkunar.
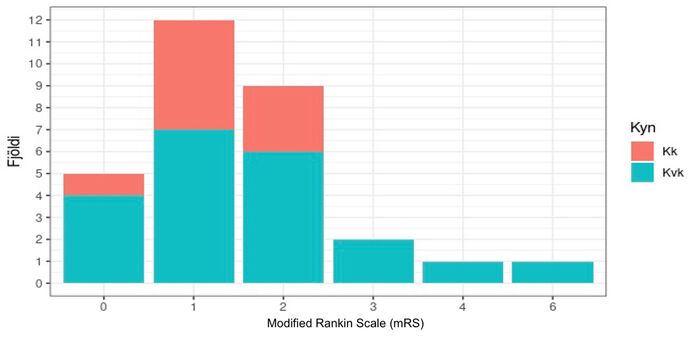
Einn sjúklingur lést vegna hnykiltjaldshaulunar í kjölfar stokkasega (3,3%). Fimm þróuðu flogaveiki í kjölfar stokkasegans (16%). Tveir sjúklingar fengu aftur stokkasega (6%) á eftirfylgdartímanum og þrír fengu bláæðasega af annarri gerð (10%). Upplýsingar um afdrif sjúklinga voru til staðar hjá 30 manns. Þremur mánuðum eftir greiningu mældust 26 sjúklingar með 0-2 á mRS skalanum (fullur/nær fullur bati (87%)), þrír mældust með 3-5 á mRS skala (10%) og einn sjúklingur lést (6 á mRS skala) (mynd 4).
Mynd 4. Afdrif einstaklinga með stokkasega þremur mánuðum eftir greiningu samkvæmt modified Rankin-skala.
Umræða
Á árunum 2008-2020 greindist 31 einstaklingur með staðfestan stokkasega, á bilinu 1-4 á ári. Meðalnýgengið var 0,7 á hverja 100.000 íbúa á ári. Nýgengið er í samræmi við erlendar rannsóknir, þar sem nýgengið hefur verið á bilinu 0,2-2,0 tilfelli á hverja 100.000 íbúa.3-6,8 Á Íslandi voru konur í miklum meirihluta, um 70%, sem er sambærilegt við aðrar rannsóknir (68-85%).9-12 Meðalaldurinn þýðisins var 34,3 ár sem er heldur lægra en í rannsóknum frá Argentínu, Túnis, Noregi og tveimur stærstu rannsóknum sem gerðar hafa verið á stokkasega – ISCVT- og VENOST-rannsóknunum (37,3-43,2 ár).9-11,13,14 Ekki var marktækur munur á meðalaldri milli kynja (p=0,3).
Í langflestum rannsóknum um stokkasega hafa yngri konur verið í meirihluta. Stokkasegi á sér oftar stað hjá ungu fólki en heilablóðföll vegna blóðsega í heilaslagæðum.15 Sennilegasta skýringin er sú að stærstu áhættuþættir stokkasega koma fram í konum á barneignaraldri: getnaðarvarnarlyf, meðganga og sængurlega.16-20 Algengustu áhættuþættir fyrir blóðsega í heilaslagæð eru hins vegar hjarta- og æðasjúkdómar á borð við æðakölkun, smáæðasjúkdóma, gáttatif og háþrýsting.21
Algengasta einkennið var höfuðverkur (87%). Hlutfallið samræmist erlendum rannsóknum (71-94%).9-14,22,23 Allar greiningar á stokkasega voru staðfestar með myndgreiningu: tölvusneiðmynd, segulómun eða bæði. Í þessari rannsókn voru heldur fleiri (55%) greindir með bæði tölvusneiðmynd og segulómun, miðað við erlendar rannsóknir (9-14%).10,11 Algengustu staðsetningarnar voru í þverstokki (74%) og efri þykktarstokki (45%), sem eru svipaðar niðurstöður og erlendis. 39% sjúklinga sýndu merki um heiladrep við myndgreiningu en 52% sýndu merki um heilablæðingu. Hlutfall einstaklinga með heiladrep er heldur hærra en í erlendum rannsóknum (11-33%)9,10,13,14 en hlutfall sjúklinga með heilablæðingu er töluvert hærra en í öðrum rannsóknum (3,8-10%).10,14 Við skoðun sjúkraskráa kom í ljós að mæling D-dímers í blóði var lítið sem ekkert notuð til greiningar á stokkasega.
Undirliggjandi þekktir áhættuþættir fundust hjá 87% sjúklinganna. Fjórir sjúklingar, eða 13% þýðisins, höfðu engan þekktan áhættuþátt. Er þetta í samræmi við stærstu rannsóknirnar þar sem áhættuþáttur fannst ekki hjá 12-24% tilfella.10,11,22 Ekki var marktækur munur á milli kynja með tilliti til áhættuþátta nema í einni breytu. Marktækur munur var á lyfjanotkun milli kynja (p=0,01). Ástæðan fyrir muninum er sú að getnaðarvarnarlyf voru langstærsti lyfjaflokkurinn, en 52% þýðisins (73% kvenna) voru á getnaðarvarnarlyfjum. Áhugavert er að enginn greindist með stokkasega í kjölfar meðgöngu eða sængurlegu. Erlendar rannsóknir hafa gefið upp afar mismunandi tölur varðandi þessa áhættuþætti, eða 2-35% sjúklinga.10-12,14,22 Ein möguleg skýring á þessu ósamræmi er smæð íslenska þýðisins. Á sama tíma náði rannsóknin yfir langt tímabil og því athyglisvert sé að enginn hafi fengið stokkasega á meðgöngu eða í sængurlegu á 12 ára tímabili.
Allir sjúklingarnir voru settir á blóðþynnandi meðferð, jafnvel þeir sem voru með heilablæðingu, sem er eftir viðteknum leiðbeiningum.7 Í langflestum tilfellum hófst meðferðin á heparíni eða léttheparíni áður en meðferð á warfaríni tók við. Sex sjúklingar (19%) voru settir á NOAC-lyf. Það er hærra hlutfall en í norskri rannsókn, þar sem 1,6% úrtaksins voru á NOAC-lyfjum.14 Nýlegar rannsóknir hafa sýnt fram á gagnsemi NOAC-lyfja við stokkasega.24,25 Tæplega helmingur sjúklinga (48%) var á blóðþynningu í 6 mánuði eða skemur. Það er í samræmi við leiðbeiningar frá ASA (American Stroke Association) en þar er mælt með blóðþynnandi meðferð í 3-6 mánuði fyrir sjúklinga með þekkta og tilfallandi undirliggjandi áhættuþætti.7 Þó ber að nefna að ESO (European Stroke Organization) mælir með blóðþynnandi meðferð í 3-12 mánuði.26 Níu sjúklingum (29%) var ráðlagt að vera á langtíma- eða ævilangri meðferð. Þeir sjúklingar voru flestir með blóðsjúkdóm eða ættgenga segahneigð.
Þrír sjúklingar (10%) þurftu á opinni kúpuaðgerð að halda. Í öllum þremur tilfellum var ástæðan fyrir skurðaðgerð merki um mikla heilablæðingu, miðlínuhliðrun og merki um yfirvofandi haulun. Hlutfall þeirra sem fóru í skurðaðgerð var heldur hærra en í öðrum rannsóknum, þar sem hlutfallið hefur verið á bilinu 1,25-3,7%.9,11-13,22 Enginn sjúklinganna fór í segabrottnám (thrombectomy) í þræðingu. Gæti það skýrst af smæð þýðisins og að segabrottnám varð fyrst valkostur á Íslandi í lok rannsóknartímabilsins.
Meðallegutími á sjúkrahúsi var 15,3 dagar, sem er svipaður meðallegutími og sést í öðrum rannsóknum (16,1 dagar – 20,4 dagar).11-13,22 Einn sjúklingur (3,3%) lést vegna stokkasega á árunum 2008-2020. Sá sjúklingur lést á gjörgæsludeild eftir 23 daga legu þrátt fyrir umfangsmikla meðferð. Hlutfallið er nokkuð svipað og í erlendum rannsóknum (3,4-7,7).9,11,12,22 Í fyrrnefndri ISCVT- rannsókn létust 4,3% sjúklinganna í bráðafasa sjúkdómsins og 3,4% létust innan 30 daga eftir að einkenni hófust.11 Algengasta dánarorsökin í þeirri rannsókn virtist vera hnykiltjaldshaulun (transtentorial herniation) vegna þrýstingsáhrifa á heilann, ýmist vegna blæðinga, dreps eða heilabjúgs.27
Horfur sjúklinga í íslensku rannsókninni voru almennt góðar. Þrátt fyrir að stór hluti þeirra hafi sýnt merki um heilablæðingu og/eða heiladrep, sem hvort tveggja eru vísbendingar um alvarlegri sjúkdómsmynd, mældust 87% sjúklinganna með 0-2 á mRS skalanum þremur mánuðum eftir greiningu. Það þýðir að 87% þeirra sem greindust með stokkasega voru með enga eða væga fötlun eftir sjúkdóminn. Þessar tölur eru almennt betri en margar aðrar rannsóknir en þá hefur á bilinu 66-85% þýðis náð góðum bata.9,11,12,22 VENOST-rannsóknin sýndi hins vegar fram á að 90% þýðisins hafði mælst 0-2 á mRS.10 Hið háa hlutfall þeirra sem náðu góðum bata hér á landi bendir til þess að sjúklingarnir hafi fengið tímanlega greiningu og árangursríka meðferð. Önnur ástæða gæti verið að okkar rannsókn ásamt þeirri norsku eru þær einu sannarlegu þýðis-rannsóknirnar (population based studies), sem minnkar valbjögun (selection bias) og eykur líkur á því að öll tilfelli séu tekin með á meðan alvarlegustu tilfellin eru frekar til staðar í spítala- eða fjölspítalarannsóknum (multi centered series).
Rannsóknin hefur ýmsa styrkleika. Í fyrsta lagi nær rannsóknin yfir heila þjóð og langt tímabil. Í öðru lagi er hún sú fyrsta sem kortleggur nýgengi og faraldsfræði stokkasega á Íslandi fyrir ákveðið tímabil. Gagnagrunnurinn sem búinn var til við gerð rannsóknarinnar og niðurstöður hennar gætu nýst sem grunnur fyrir frekari kortlagningu og eftirfylgd stokkasega á Íslandi. Ekki síst á þetta við ef stokkasegi reynist sjaldgæf en þó þekkt alvarleg aukaverkun vissra bóluefna gegn COVID-19.28
Rannsóknin hefur þó einnig veikleika. Stærð þýðisins er fremur lítið. Stokkasegi er sjaldgæfur sjúkdómur á heimsvísu og því er ekki óeðlilegt að sú staðreynd endurspeglist hér. Vegna þess hversu erfitt getur reynst að greina sjúkdóminn er ekki ólíklegt að einstaklingar hafi verið með stokkasega án staðfestrar greiningar eða að rangur greiningarkóði hafi verið notaður. Þá var gert ráð fyrir að allir sjúklingar með stokkasega á Íslandi hafi verið lagðir inn á Landspítala eða sjúkrahúsið á Akureyri. Ekki er hægt að útiloka þann möguleika að sjúklingar hafi fengið greiningu og meðferð við stokkasega á öðrum heilbrigðisstofnunum, þó svo að það sé afar ólíklegt. Þess ber einnig að geta að um var að ræða lýsandi rannsókn án viðmiðunarhóps. Því eru eingöngu skoðaðir þekktir áhættuþættir fyrir stokkasega.
Samantekt
Í þessari rannsókn var faraldsfræði stokkasega á Íslandi rannsökuð ásamt þekktum áhættuþáttum, einkennum, greiningu, meðferð og horfum. Stór hluti þeirra sem greindust með stokkasega á rannsóknartímabilinu voru konur yngri en 50 ára. Algengasta einkennið var höfuðverkur og algengasti áhættuþátturinn var notkun getnaðarvarnarlyfja. Voru allir sjúklingarnir settir á blóðþynnandi meðferð og flestir náðu góðum bata.
Heimildir
| 1. Luo Y, Tian X, Wang X. Diagnosis and Treatment of Cerebral Venous Thrombosis: A Review. Front Aging Neurosci 2018; 10: 2. https://doi.org/10.3389/fnagi.2018.00002 PMid:29441008 PMCid:PMC5797620 |
||||
| 2. Sveinsson ÓÁ, Kjartansson Ó, Valdimarsson EM. Stokkasegi - sjaldgæfur sjúkdómur en mikilvæg mismunagreining við höfuðverk, heilablóðfall og flog: Tilfellaröð með yfirliti. Læknablaðið 2013; 99: 189-95. https://doi.org/10.17992/lbl.2013.04.492 PMid:23695969 |
||||
| 3. Bousser MG, Ferro JM. Cerebral venous thrombosis: an update. Lancet Neurol 2007; 6: 162-70. https://doi.org/10.1016/S1474-4422(07)70029-7 |
||||
| 4. Coutinho JM, Zuurbier SM, Aramideh M, et al. The Incidence of Cerebral Venous Thrombosis: A Cross-Sectional Study. Stroke 2012; 43: 3375-7. https://doi.org/10.1161/STROKEAHA.112.671453 https://doi.org/10.1161/STROKEAHA.111.648162 |
||||
| 5. Devasagayam S, Wyatt B, Leyden J, et al. Cerebral Venous Sinus Thrombosis Incidence Is Higher Than Previously Thought. Stroke 2016; 7: 2180-2. https://doi.org/10.1161/STROKEAHA.116.013617 PMid:27435401 |
||||
| 6. Otite FO, Patel S, Sharma R, et al. Trends in incidence and epidemiologic characteristics of cerebral venous thrombosis in the United States. Neurology 2020; 95: e2200-e13. https://doi.org/10.1212/WNL.0000000000010598 PMid:32847952 PMCid:PMC7713788 |
||||
| 7. Saposnik G, Barinagarrementeria F, Brown RD, et al. Diagnosis and Management of Cerebral Venous Thrombosis: A Statement for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke 2011; 42: 1158-92. https://doi.org/10.1161/STR.0b013e31820a8364 PMid:21293023 |
||||
| 8. Stam J. Thrombosis of the Cerebral Veins and Sinuses. N Engl J Med 2005; 352: 1791-8. https://doi.org/10.1056/NEJMra042354 PMid:15858188 |
||||
| 9. Alet M, Ciardi C, Aleman A, et al. Cerebral venous thrombosis in Argentina: clinical presentation, predisposing factors, outcomes and literature review. J Stroke Cerebrovasc Dis 2020; 29: 105145. https://doi.org/10.1016/j.jstrokecerebrovasdis.2020.105145 PMid:32912503 |
||||
| 10. Duman T, Uluduz D, Midi I, et al. A Multicenter Study of 1144 Patients with Cerebral Venous Thrombosis: The VENOST Study. J Stroke Cerebrovasc Dis 2017; 26: 1848-57. https://doi.org/10.1016/j.jstrokecerebrovasdis.2017.04.020 PMid:28583818 |
||||
| 11. Ferro JM, Canhao P, Stam J, et al. Prognosis of Cerebral Vein and Dural Sinus Thrombosis: Results of the International Study on Cerebral Vein and Dural Sinus Thrombosis (ISCVT). Stroke 2004; 35: 664-70. https://doi.org/10.1161/01.STR.0000117571.76197.26 PMid:14976332 |
||||
| 12. Ruiz-Sandoval JL, Chiquete E, Banuelos-Becerra LJ, et al. Cerebral Venous Thrombosis in a Mexican Multicenter Registry of Acute Cerebrovascular Disease: The RENAMEVASC Study. J Stroke Cerebrovasc Dis 2012; 21: 395-400. https://doi.org/10.1016/j.jstrokecerebrovasdis.2011.01.001 PMid:21367622 |
||||
| 13. Sassi SB, Touati N, Baccouche H, et al. Cerebral Venous Thrombosis: A Tunisian Monocenter Study on 160 Patients. Clin Appl Thromb Hemost 2016; 23: 1005-9. https://doi.org/10.1177/1076029616665168 PMid:27582021 |
||||
| 14. Kristoffersen ES, Harper CE, Vetvik KG, et al. Incidence and Mortality of Cerebral Venous Thrombosis in a Norwegian Population. Stroke 2020; 51: 3023-9. https://doi.org/10.1161/STROKEAHA.120.030800 PMid:32883194 |
||||
| 15. Ferro JM, Canhao P, Aguiar De Sousa D. Cerebral venous thrombosis. La Presse Médicale 2016; 45: e429-e50. https://doi.org/10.1016/j.lpm.2016.10.007 PMid:27816347 |
||||
| 16. Amoozegar F, Ronksley PE, Sauve R, et al. Hormonal Contraceptives and Cerebral Venous Thrombosis Risk: A Systematic Review and Meta-Analysis. Front Neurol 2015; 6: 7. https://doi.org/10.3389/fneur.2015.00007 PMid:25699010 PMCid:PMC4313700 |
||||
| 17. Bajko Z, Motataianu A, Stoian A, et al. Gender Differences in Risk Factor Profile and Clinical Characteristics in 89 Consecutive Cases of Cerebral Venous Thrombosis. J Clin Med 2021; 10: 1382. https://doi.org/10.3390/jcm10071382 PMid:33808141 PMCid:PMC8036766 |
||||
| 18. de Bruijn SFTM, Stam J, Koopman MMW, et al. Case-control study of risk of cerebral sinus thrombosis in oral contraceptive users who are carriers of hereditary prothrombotic conditions. BMJ 1998; 316: 589-92. https://doi.org/10.1136/bmj.316.7131.589 PMid:9518910 PMCid:PMC28462 |
||||
| 19. Silvis SM, Lindgren E, Hiltunen S, et al. Postpartum Period Is a Risk Factor for Cerebral Venous Thrombosis: A Case-Control Study. Stroke 2019; 50: 501-3. https://doi.org/10.1161/STROKEAHA.118.023017 PMid:30621526 |
||||
| 20. Silvis SM, Middeldorp S, Zuurbier SM, et al. Risk Factors for Cerebral Venous Thrombosis. Semin Thromb Hemost 2016; 42: 622-31. https://doi.org/10.1055/s-0036-1584132 PMid:27272966 |
||||
| 21. Boehme AK, Esenwa C, Elkind MSV. Stroke Risk Factors, Genetics, and Prevention. Circ Res 2017; 120: 472-95. https://doi.org/10.1161/CIRCRESAHA.116.308398 PMid:28154098 PMCid:PMC5321635 |
||||
| 22. Narayan D, Kaul S, Ravishankar K, et al. Risk factors, clinical profile, and long-term outcome of 428 patients of cerebral sinus venous thrombosis: Insights from Nizam's Institute Venous Stroke Registry, Hyderabad (India). Neurol India 2012; 60: 154-9. https://doi.org/10.4103/0028-3886.96388 PMid:22626695 |
||||
| 23. Wasay M. Cerebral Venous Thrombosis: Analysis of a Multicenter Cohort From the United States. J Stroke Cerebrovasc Dis 2008; 17: 49-54. https://doi.org/10.1016/j.jstrokecerebrovasdis.2007.10.001 PMid:18346644 |
||||
| 24. Ferro JM, Coutinho JM, Dentali F, et al. Safety and Efficacy of Dabigatran Etexilate vs Dose-Adjusted Warfarin in Patients With Cerebral Venous Thrombosis: A Randomized Clinical Trial. JAMA Neurol 2019; 76: 1457-65. https://doi.org/10.1001/jamaneurol.2019.2764 PMid:31479105 PMCid:PMC6724157 |
||||
| 25. Li H, Yao M, Liao S, et al. Comparison of Novel Oral Anticoagulants and Vitamin K Antagonists in Patients With Cerebral Venous Sinus Thrombosis on Efficacy and Safety: A Systematic Review. Front Neurol 2020; 11: 597623. https://doi.org/10.3389/fneur.2020.597623 PMid:33362699 PMCid:PMC7758340 |
||||
| 26. Ferro JM, Bousser MG, Canhao P, et al. European Stroke Organization guideline for the diagnosis and treatment of cerebral venous thrombosis - Endorsed by the European Academy of Neurology. Eur J Neurol 2017; 24: 1203-13. https://doi.org/10.1111/ene.13381 PMid:28833980 |
||||
| 27. Canhao P, Ferro JM, Lindgren AG, et al. Causes and Predictors of Death in Cerebral Venous Thrombosis. Stroke 2005; 36: 1720-25. https://doi.org/10.1161/01.STR.0000173152.84438.1c PMid:16002765 |
||||
| 28. Ghosh R, Roy D, Mandal A, et al. Cerebral venous thrombosis in COVID-19. Diabetes Metab Syndr 2021; 15: 1039-45. https://doi.org/10.1016/j.dsx.2021.04.026 PMid:34015627 PMCid:PMC8128714 |
||||