12. tbl. 110. árg. 2024
Fræðigrein
Rannsókn. SGLT2-hemlar – Nýir meðferðarmöguleikar við langvinnum nýrnasjúkdómi og hjartabilun
Ágrip
SGLT2-hemlar auka útskilnað á natríum og glúkósa í þvagi. Auk blóðsykurslækkunar leiðir það meðal annars til skilvirkari orkuefnaskipta í nýrum og hjarta, blóðþrýstingslækkunar, lækkunar þrýstings í nýrnagauklum, aukningu á myndun rauðra blóðkorna, auk þess að minnka bólgu og bandvefsmyndun í hjarta og nýrum. Stórar slembiraðaðar rannsóknir hafa verið gerðar á sjúklingum með hjartabilun með og án skerðingu á útfallsbili hjartans og NYHA klass II-IV. Hafa þær sýnt fram á lægri tíðni versnana af völdum hjartabilunar og dauða af völdum hjarta-og æðasjúkdóma hjá sjúklingum sem fá meðferð med SGLT2 hemlum miðað við samanburðarhóp.
Rannsóknir hafa einnig verið gerðar á sjúklingum með langvinnan nýrnasjúkdóm og sýnt hefur verið fram á að lyfin hægja á framgangi nýrnabilunar og lækka tíðni lokastigs nýrnabilunar ásamt dauða af völdum hjarta- og æðasjúkdóma. Hafa sjúklingar með hjartabilun og nýrnasjúkdóma því sterka ábendingu fyrir lyfjunum. Með aukinni útbreiðslu þessara lyfja verður að hafa í huga frábendingar sem eru meðal annars sykurýki af gerð 1. Einnig þarf að hafa vakandi auga fyrir sjaldséðum, alvarlegum aukaverkunum sem eru ketónblóðsýring með eðlilegum blóðsykri og Forniers ýldudrep (gangrene).
Inngangur
Bakgrunnur
SGLT2 (sodium-glucose cotransporter 2) hemlar auka útskilnað á natríum og glúkósa í þvagi með því að hemja frásog á natríum og glúkósa í nærpíplum nýrna. Í nærpíplum nýrna eru bæði SGLT1 og SGLT2 jónagöng en SGLT2 jónagöngin eru afkastameiri og sjá um 90% af frásogi glúkósa. SGLT1 jónagöngin eru einnig í smáþörmunum.1 Árið 1835 byrjuðu menn fyrst að nota efnið flórizín, sem var meðal annars unnið úr börk eplatrjáa og var ósértækur SGLT2-hemill, í læknisfræðilegum tilgangi. Efnið var notað við meðhöndlun sýkinga, sérstaklega malaríu. Fljótlega uppgötvuðust áhrif flórizíns á nýrun og efnið var notað við tilraunir á lífeðlisfræði nýrna í byrjun 20. aldar.2 Sú hugmynd vaknaði að nýta þennan verkunarmáta og þróaðist lyfjaflokkur við sykursýki af gerð 2 sem kallast glíflózín og eru öll lyf í þessum flokki sértækir SGLT2-hemlar nema lyfið sótaglíflózín sem hemur bæði SGLT1 og SGLT2 jónagöngin.3 Á Íslandi eru tvö þessara lyfja á markaði, dapaglíflózín (Forxiga) og empaglíflózín (Jardiance). Komið hefur í ljós lækkun á langtímablóðsykri um ~7-10 mmól/mól hjá sjúklingum með sykursýki af gerð 2.4 Virkni hemilsins á SGLT2 jónagöngin er háð blóðsykri og minnkar virknin ef blóðsykur er eðlilegur. Einnig auka lyfin ný-myndun glúkósa í lifur og nýrum. Þetta gerir það að verkum að lyfin valda ein og sér ekki blóðsykursfalli.5 Við skerðingu á nýrnastarfsemi minnkar magn glúkósa sem er síaður um nýrun og sést þess vegna engin lækkun á langtímablóðsykri hjá sjúklingum með skerta nýrnastarfsemi6,7 Höfðu lyfin því einungis ábendingu hjá sjúklingum með sykursýki af gerð 2 með gaukulsíunarhraða >45 ml/mín/1,73m2, sem olli því að einungis takmarkaður hópur sjúklinga fékk meðhöndlun með þessum lyfjaflokki.
Öryggisrannsóknir
Þar sem sjúklingar með sykursýki eru í aukinni áhættu á hjarta- og æðasjúkdómum eru nú gerðar kröfur um rannsóknir á öryggi nýrra sykursýkislyfja til að tryggja að lyfin auki ekki áhættuna á hjartasjúkdómum enn frekar. Rannsóknirnar EMPA-REG8, CANVAS9 og DECLARE–TIMI 5810 voru stórar slembiraðaðar samanburðarrannsóknir sem voru gerðar á sjúklingum með sykursýki af gerð 2 og voru annað hvort með þekktan hjarta- og æðasjúkdóm eða í hárri áhættu á hjarta- og æðasjúkdómi. Gerð var krafa um reiknaðan gaukulsíunar-hraða (rGSH) > 30mL/mín/1,73m2 hjá sjúklingunum í þessum rannsóknum. Þessar rannsóknir voru hannaðar til að sýna að verkunin var ekki lakari en hjá lyfleysuhópnum. Rannsóknirnar sýndu að ekki var aukin áhætta á samsettum endapunkti: dauða vegna hjartasjúkdóms, bráðri kransæðastíflu eða heilablóðfalli með notkun þessara lyfja þegar þau voru borin saman við lyfleysu. Meirihluti sjúklinga (70-80%) fékk meðhöndlun með metformíni og RAAS (renín-angíótensín-aldosteron -system) hemli samhliða meðferð með SGLT2-hemli. Lítið var um meðhöndlun með GLP-1 hliðstæðum eða einungis hjá 2-3% sjúklinga. Meðferð með SGLT2-hemlunum leiddi til þyngdartaps, minnkunar á mittismáli og lækkunar á blóðþrýstingi auk lækkunar á langtímablóðsykri.8-10
Rannsóknirnar gáfu vísbendingar um að lyfin fækkuðu sjúkrahúsinnlögnum vegna versnunar á hjartabilun og hefðu nýrnaverndandi áhrif.8-10 Þörf var á frekari rannsóknum til að staðfesta niðurstöðurnar þar sem rannsóknirnar voru ekki hannaðar til að svara ofangreindum rannsóknarspurningum um hjarta- og nýrnabilun.
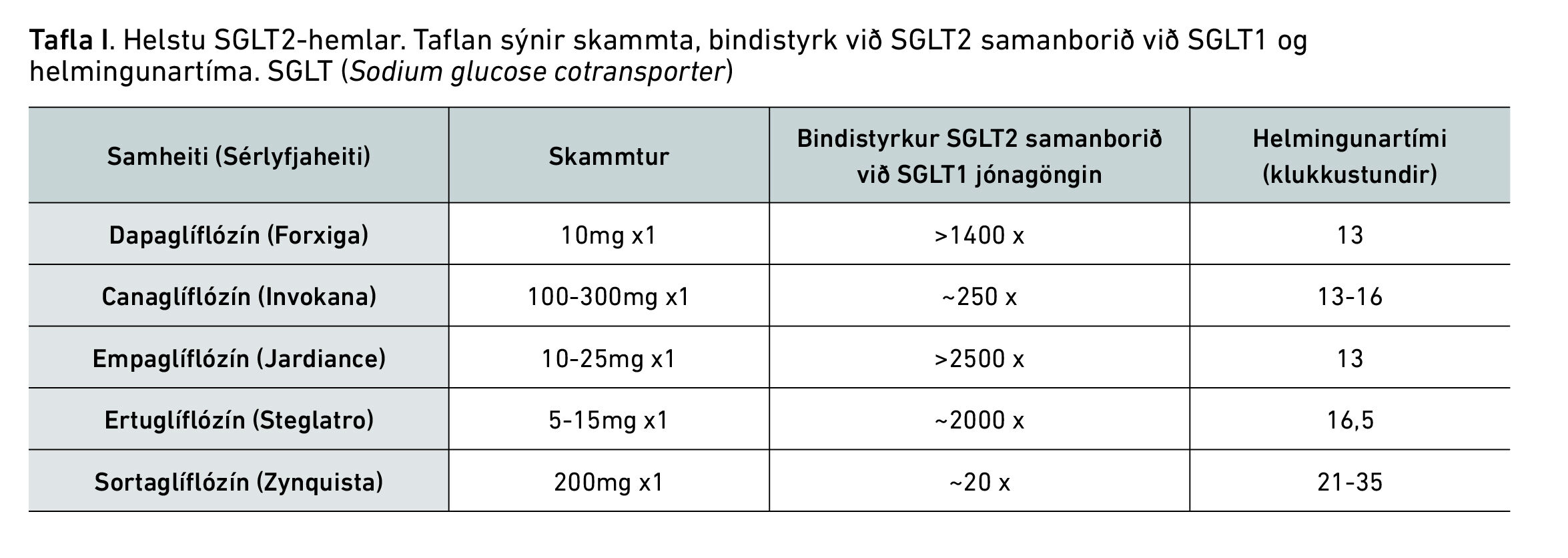 Tafla I. Helstu SGLT2-hemlar. Taflan sýnir skammta, bindistyrk við SGLT2 samanborið við SGLT1 og helmingunartíma. SGLT (Sodium glucose cotransporter)
Tafla I. Helstu SGLT2-hemlar. Taflan sýnir skammta, bindistyrk við SGLT2 samanborið við SGLT1 og helmingunartíma. SGLT (Sodium glucose cotransporter)
Nýrnabilun
Í ofangreindum öryggisrannsóknum voru sjúklingarnir með góða nýrnastarfsemi, gaukulsíunarhraðinn var ca 70-85 mL/mín/1,73m2 að meðaltali. Þó voru ca 30% sjúklinganna með öralbúmínmigu og 10% með albúmínmigu.
Hafnar voru sérhannaðar rannsóknir á nýrnaverndandi áhrifum SGLT2-hemlana. CREDENCE var fyrsta rannsóknin sem kom út og var hún gerð á canaglíflózín en einungis á sjúklingum með langvinnan nýrnasjúkdóm stig 2-3 (rGSH 30-89 mL/mín/1,73m2) af völdum sykurýki týpu 2.11 DAPA-CKD12 og EMPA-KIDNEY13 komu í kjölfarið þar sem sjúklingar með langvinnan nýrnasjúkdóm með og án sykursýki af gerð 2 fengu að taka þátt. Rannsóknirnar voru allar hannaðar þannig að SGLT2-hemli var bætt ofan á að minnsta kosti eins mánaðar meðhöndlum með RAAS-hemli. Endapunktarnir voru samsettir og innifalið í þeim var lokastigs nýrnabilun, versnun á nýrnastarfsemi (> 40-50% lækkun á gaukulsíunarhraða), dauði af völdum nýrnabilunar eða hjarta- og æðasjúkdóms. Sjúklingunum var fylgt eftir í 2-3 ár. Sjúklingarnir sem fengu meðferð með SGLT2-hemlum í þessum rannsóknum höfðu 30-44% lægri áhættu (relative risk) að fá ofangreindan samsettan endapunkt samanborið við sjúklinga í lyfleysuhópunum.11-13 Þessar rannsóknir voru stöðvaðar vegna svo jákvæðra áhrifa á nýrnastarfsemi hjá hópnum sem fékk SGLT2-hemlana að ekki þótti siðferðislega rétt að halda þeim áfram.
Hjartabilun
Hjartabilun með skertu útfallsbroti
Sömu sögu má segja um SGLT2-hemla og áhrif á versnun hjartabilunar. EMPEROR-reduced (empaglíflózín) 14 og DAPA-HF (dapaglíflózín)15 voru stórar slembiraðaðar rannsóknir sem voru gerðar á sjúklingum með hjartabilun með skertu útfallsbroti ≤ 40% og NYHA klass II-IV. Þær rannsökuðu tíðni versnunar á hjartabilun og dauða af völdum hjarta- og æðasjúkdóma. SGLT2-hemli var í þessum rannsóknum bætt við fulla hjartabilunarmeðferð þar sem nær allir sjúklingar voru meðhöndlaðir með beta-blokkerum, 80-90% með RAAS-hemli með eða án neprilysín-hemils (með um 10%) og 70% með aldósterón-viðtakahemli.
Fjöldi sjúklinga sem þurfti að meðhöndla með SGLT2-hemli til að koma í veg fyrir þennan samsetta endapunkt var í báðum þessum rannsóknum um 20 sem var auðvitað tölfræðilega marktækur munur. Í klínísku leiðbeiningunum frá Evrópsku hjartalæknasamtökunum um meðferð hjartabilunar frá 2021 er nú mælt með fjögurra lyfja meðferð hjá sjúklingum með hjartabilun með skertu útfallsbroti, með beta-blokker, RAAS hemli með eða án neprilysín-hemils, aldósterón-viðtakahemli og SGLT2-hemli.16
Ekki er þó vitað hvort það borgi sig að setja inn þessa meðferð strax eftir bráða kransæðastíflu þar sem rannsóknin EMPACT-MI var nýlega birt sem sýndi ekki fram á lægri tíðni versnunar á hjartabilun hjá sjúklingum sem hófu meðferð innan 14 daga frá bráðri kransæðatíflu og voru með útfallsbrot <45%. Var þó einungis um 1 árs eftirfylgni að ræða.17
Hjartabilun með varðveittu og vægt skertu útfallsbroti
Þar sem gagnreyndir meðferðarmöguleikar við hjartabilun með eðlilegu útfallsbroti hafa hingað til verið mjög takmarkaðir voru talsverðar vonir bundnar við SGLT2-hemlana, hvort þeir gætu gagnast þessum sjúklingahópi. Rannsóknirnar EMPEROR-Preserved18 og DELIVER19 leituðst við að svara þeirri spurningu. Voru þær gerðar á sjúklingum með útfallsbrot >40% og NYHA klass II-IV. Um þriðjungur sjúklinga voru með útfallsbrot <50%. Endapunktarnir voru versnun á hjartabilun og dauði af völdum hjarta- og æðasjúkdóma. Þó áhrifin væru ekki jafn mikil og hjá sjúklingum með hjartabilun með skertu útfallsbroti sást þó virkni lyfjanna hjá þessum sjúklingahópi líka en hér þurfti að meðhöndla 33 sjúklinga til að koma í veg fyrir endapunktinn. Í EMPEROR-Preserved rannsókninni virtist ávinningurinn vera meiri hjá þeim sem voru með útfallsbrot milli 40-50%18 en í DELIVER virtust áhrifin ekki vera síðri en hjá þeim sem voru með útfallsbrot >60%.19 Sjúklingar með hjartabilun með eðlilegu eða vægt skertu útfallsbroti hafa því einnig ábendingu fyrir SGLT2-hemli.20
Virkni
En hvernig valda SGLT2-hemlarnir þessum verndandi áhrifum á starfsemi hjarta og nýrna?
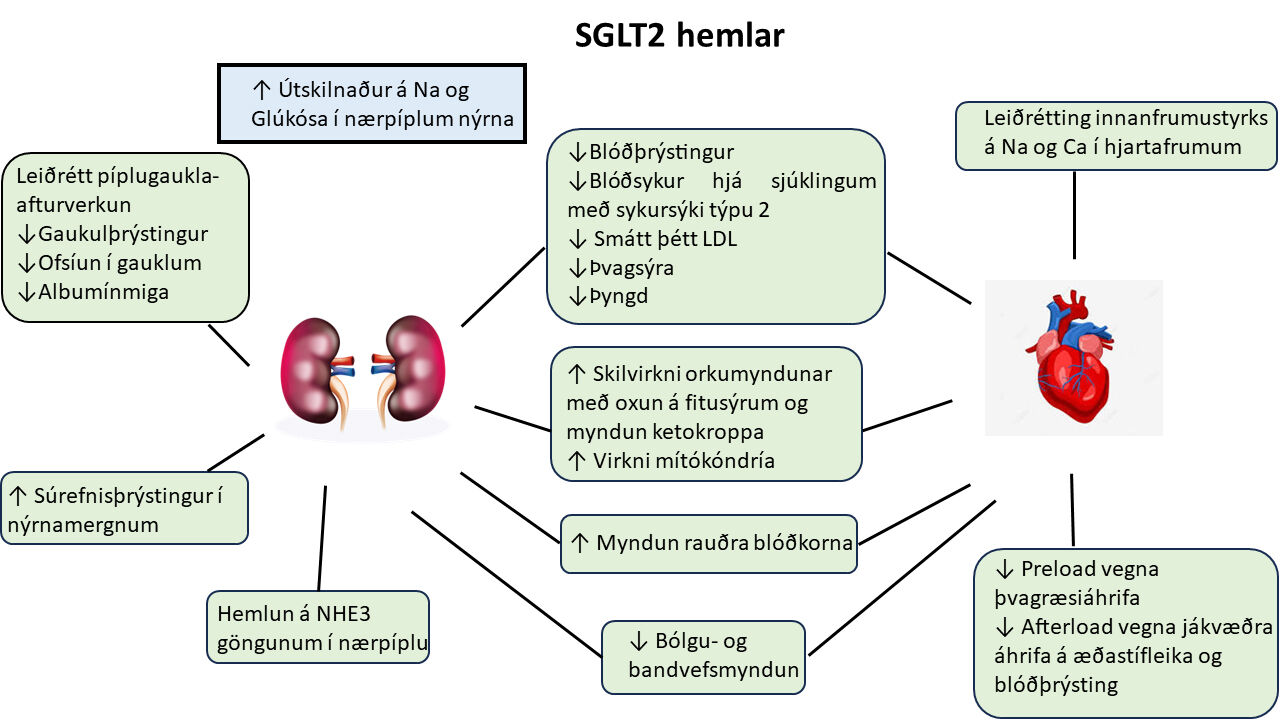 Mynd 1. Verkunarmáti SGLT2-hemla.
Mynd 1. Verkunarmáti SGLT2-hemla.
Rannsóknir hafa sýnt að virknin sést bæði hjá sjúklingum með og utan sykursýki af gerð 2 og er óháð lækkun á langtímablóðsykri12,21 (mynd 1). Eftirtaldir mekan-ismar hafa verið nefndir:
a) Með því að hemja SGLT2-jónagöngin berst aukið magn af natríum til fjærpíplanna og leiðir til herpingar á aðlægum slagæðlingi í nýrnagauklunum vegna aukinnar píplugaukla afturverkunar (tubuloglomerular feedback). Þetta lækkar þrýsting í nýrnagauklunum og kemur í veg fyrir ofsíun sem er mjög algengt við nýrnamein af völdum sykursýki en sést einnig í öðrum nýrnasjúkdómum.22
b) Samhliða lækkun á gaukulþrýstingi minnkar albúmínmiga. Pódócýtar eru frumur í grunnhimnu gaukla sem koma í veg fyrir að albúmín komist í gegn um grunnhimnuna. Rannsóknir á músum hafa sýnt að SGLT2-jónagöng eru á pódócýtum svo ekki er útilokað að SLGT2-hemlarnir hafi bein áhrif á pódócýtana og orsaki þannig minnkun á albúmínmigu.23
c) Samhliða hemlun á SGLT2-jónagöngunum verður einnig hemlun á NHE3-göngum í nærpíplu nýrna sem hafa það hlutverk að frásoga natríum í skiptum fyrir vetnisjónir. Fjöldi NHE3-jónaganganna er aukinn hjá rottum með hjartabilun, sem er líklega hluti af svari nýrnanna við minnkuðu hjartaútfalli. Þetta getur að hluta til skýrt virkni lyfsins hjá sjúklingum með eðlilegan blóðsykur.24
d) Það er orkufrekt að frásoga natríum og glúkósa í nýrunum og því eykur hemlun á SGLT2-jónagöngunum súrefnisþrýsting í nýrunum.25
e) Hjartabilun veldur brenglaðri stjórnun á innanfrumustyrk natríum- og kalsíumjóna.26 SGLT2-hemlar virðast minnka innanfrumustyrk natríum í hjartavöðvafrumum og leiðrétta innanfrumstyrk á natríum og kalsíum. Þetta veldur minnkun á virkum súrefnissamböndum, betri samdráttarhæfni og minnkar hættu á hjartsláttartruflunum.27
f) Þvagræsandi áhrif leiða til lækkunar á fylliþrýstingi hjartans (preload).28,29
g) SGLT2-hemlar valda einnig lækkun á slagæðaþrýstingi (afterload) með því að draga úr æðastífleika. Blóðþrýstingslækkun gæti átt þátt í skýringunni en einnig er um að ræða áhrif á vanstjórnun endóþels.30
h) Lækkun á blóðþrýstingi (3-5 mmHg lækkun á slagbilsþrýstingi) hefur bæði hjarta- og nýrnaverndandi áhrif.31 Engin aukning sést á hjartsláttartíðni svo kenningar hafa verið uppi um hvort lyfin hemji sympatíska taugavirkni.32
i) Áhrif á aðra áhættuþætti hjarta- og æðasjúkdóma og þar með einnig nýrnasjúkdóma. Lyfin valda lækkun á blóðsykri hjá þeim með sykursýki.33 Einnig sést lækkun á þvagsýru í blóði sem er í sjálfu sér ekki áhættuþáttur en er líklega marki á bólgumyndun og oxunarstress.34 Lyfin valda einnig þyngdartapi.35 Áhrif á blóðfitur eru misvísandi. Flestar rannsóknir sýna örlitla hækkun á LDL (low density lipoprotein) en nánari skoðun hefur leitt í ljós að lækkun verður á smáu þéttu LDL sem veldur frekar æðakölkun og að meirihluti þessa LDL er af stærri gerðinni sem veldur síður æðakölkunum.36 Aukning verður á HDL og lækkun á þríglyseríðum.37
j) Við aukningu á útskilnaði á glúkósa breytast efnaskiptin í líkamanum og líkjast þeim sem líkaminn notar þegar hann fastar. Eykst þá oxun á fitusýrum og myndun ketókroppa á kostnað glýkólýsu og leiðir til þess að orkumyndun frumna í hjarta og nýrum verður skilvirkari. Auk þess auka lyfin virkni hvatbera.38
k) SGLT2-hemlar koma í veg fyrir bólgu og bandvefsmyndun í hjarta og nýrum. Um víðtæk áhrif er að ræða og áhrifum á marga marka og boðleiðir hefur verið lýst.39
l) SGLT2-hemlar auka myndun hemóglóbíns með því að auka myndun erýtrópóetíns og þar með rauðra blóðkorna. Lækkar einnig styrkur hepsidíns í blóði sem leiðir til aukinnar járnnýtingar í líkamanum.40 Hepsidín er hormón sem hækkar oft í bólguástandi og leiðir til þess að ekki er hægt að ná í járn úr járnbirgðum líkamans í lifrinni og dregur úr frásogi járns frá þarminum.
Frábendingar og aukaverkanir
Algengustu aukaverkanir af lyfjunum eru þvagfærasýkingar og sveppasýkingar í leggöngum hjá konum.8-10 Flestar sýkinganna eru þó einfaldar blöðrubólgur sem svara vel sýklalyfjameðferð. Mikilvægt er því að gefa sjúklingum almennar leiðbeiningar um hreinlæti í kring um þvagrás og kynfæri. Í CANVAS-rannsókninni kom fram aukin áhætta á aflimun og beinbrotum hjá hópi sjúklinga sem fengu canagliflózín9 en aðrar rannsóknir hafa ekki staðfest þessar niðurstöður.4,8,10 Tveimur alvarlegum en mjög sjaldgæfum aukaverkunum hefur verið lýst eftir að lyfin fóru á markað. Önnur er Forniers ýldudrep (gangrene) sem er mjög alvarleg bakteríusýking á spangarsvæði sem getur breiðst hratt út. Árið 2022 var búið að skrá 491 tilfelli af Fourniers ýldudrepi hjá sjúklingum á SGLT2-hemli þar sem einungis 16 sjúklingar voru ekki með sykurýki. Hér er þó að sjálfsögðu enginn samanburðarhópur.41 Hin alvarlega og sjaldgæfa aukaverkunin er ketónblóðsýring (ketoacidosis) með eðlilegum blóðsykri. Tíðnin er ca 0,16-0,76/1000 mannár.42 Það að blóðsykurinn er eðlilegur gerir greiningu þessa ástands oft erfiða og verða læknar að muna eftir þessari mismunagreiningu og mæla ketóna í blóði til að fá greininguna. Er þessi aukaverkun nánast einungis þekkt hjá sjúklingum með sykursýki en ekki óhugsandi hjá sjúklingum í langvarandi svelti. Áhættuþættir eru minnkuð insúlínframleiðsla, vannæring, þyngdartap, áfengishólneysla og sýkingar. Meinalífeðlisfræðin er ekki þekkt að öllu leyti en talið er að aukið fituniðurbrot leiði til aukinnar myndunar ketóna í lifur og lægri insulínseyting auki geymslu á ketónafurðum.42 Mikilvægt er því að upplýsa sjúklinga um að stöðva tímabundið töku lyfjanna við bráð veikindi þar sem hætta er á ofþornun, svo sem háan hita, niðurgang eða uppköst.
Þess ber að geta að SGLT2-hemlar valda ekki of lágum blóðsykri og bráður nýrnaskaði hefur í flestum rannsóknum sýnt sig vera sjaldgæfari í SGLT2-hemla hópnum miðað við í lyfleysuhópnum.11-13 Líkt og eftir að hafin er meðferð með RAAS-hemlum getur maður átt von á að sjá um 30% hækkun á kreatíníni eftir að meðferð er hafin með SGLT2-hemli.12,13 Þetta endurspeglar lækkaðan gaukulþrýsting og er oft talið jákvætt merki um að lyfin hafi tilætluð áhrif á nýrun.
Frábendingar fyrir SGLT2-hemlum eru sykursýki af gerð 1 þar sem talin er aukin hætta á ketónblóðsýringu. Sjúklingahópar sem ekki tóku þátt í rannsóknum um nýrnaverndandi árhif lyfjanna voru sjúklingar með blöðrunýrnasjúkdóm og sjúklingar á ónæmisbælandi meðferð.11-13 Sjúklingar með gaukulsíunarhraða niður í 20-30 mL/mín/1,73m2 voru með í EMPA-KIDNE13 og DAPA-CKD12 svo ekki er vitað um nýrnaverndandi áhrif við að hefja meðferð á lyfinu við lægri gaukulsíunarhraða. Hins vegar var meðferð ekki hætt þótt nýrnastarfsemin versnaði og héldu sjúklingar áfram á lyfinu þó þeir þyrftu á skilun að halda. Þess vegna eru engin skýr mörk gaukulsíunarhraða, hvenær leyfilegt er að hefja meðferð hjá sjúklingum með hjartabilun og þarf að meta hvert tilfelli fyrir sig . Ekki er þörf á að stöðva inntöku lyfjanna þó rGSH fari undir 20mL/mín/1,73m2.
Hafa þarf í huga að meðalaldur í flestum rannsóknum var á milli 60 og 70 ár og þess vegna eru lyfin ekki rannsökuð hjá háöldruðum. Gerð hefur verið safngreining á undirhópum stærstu rannsóknanna sem sýnir að lyfið gagnast einnig öldruðum en þá voru skoðaðir hópar >75 ára.43 Hafa þarf í huga aukna áhættu á aukaverkunum hjá eldri sjúklingum, sérstaklega ef þeir nærast illa. Einnig gæti aukin tíðni beinbrota sem sást í CANVAS-rannsókninni9 verið vegna aukinnar tíðni byltna vegna ofþurrks og þarf sérstaklega að gæta að því hjá eldri einstaklingum.
Lokaorð
Af ofangreindu er ljóst að sjúklingar með hjartabilun og sjúklingar með langvinna nýrnabilun ber að meðhöndla með SGLT2-hemlum óháð því hvort þeir séu með sykurýki af gerð 2 eða ekki, nema að klár frábending sé til staðar. Lyfin fækka sjúkrahúsinnlögnum vegna hjartabilunar og dauða af völdum hjarta- og æðasjúkdóma, hægja á framgangi nýrnabilunar og lækka tíðni lokastigs nýrnabilunar. Hafa verður þó í huga frábendingar meðferðar og þar sem áhætta af meðferðinni er aukin, það er að segja sjúklingar með sykursýki af gerð 1, vannærðir sjúklingar og sjúklingar í mikilli byltuhættu. Þurfa læknar sérstaklega að vera vakandi fyrir ketónblóðsýringu með eðlilegum blóðsykri. Með aukinni notkun lyfjanna er mikilvægt að senda inn tilkynningar um aukaverkanir svo hægt sé að gera sér betur grein fyrir tíðni þessara sjaldséðu aukaverkana.
| 1. Lee WS, Kanai Y, Wells RG, et al. The high affinity Na+/glucose cotransporter. Re-evaluation of function and distribution of expression. J Biol Chem 1994; 269(16): 12032-9. https://doi.org/10.1016/S0021-9258(17)32677-7 PMid:8163506 |
||||
| 2. Ehrenkranz JR, Lewis NG, Kahn CR, et al. a review. Diabetes Metab Res Rev 2005; 21(1): 31-8. https://doi.org/10.1002/dmrr.532 PMid:15624123 |
||||
| 3. Lapuerta P, Zambrowicz B, Strumph P, et al. Development of sotagliflozin, a dual sodium-dependent glucose transporter 1/2 inhibitor. Diabetes Metab Res Rev 2015; 12(2): 101-10. https://doi.org/10.1177/1479164114563304 PMid:25690134 |
||||
| 4. Zaccardi F, Webb DR, Htike ZZ, et al. Efficacy and safety of sodium-glucose co-transporter-2 inhibitors in type 2 diabetes mellitus: systematic review and network meta-analysis. Diabetes Obes Metabm 2016; 18(8): 783-94. https://doi.org/10.1111/dom.12670 PMid:27059700 |
||||
| 5. Merovci A, Solis-Herrera C, Daniele G, et al. Dapagliflozin improves muscle insulin sensitivity but enhances endogenous glucose production. J Clin Invest 2014; https://doi.org/10.1172/JCI70704 PMid:24463448 PMCid:PMC3904617 |
||||
| 124(2): 509-14. | ||||
| 6. Ferrannini E, Veltkamp SA, Smulders RA, et al. Renal glucose handling: impact of chronic kidney disease and sodium-glucose cotransporter 2 inhibition in patients with type 2 diabetes. Diabetes care 2013; 36(5): 1260-5. https://doi.org/10.2337/dc12-1503 PMid:23359360 PMCid:PMC3631866 |
||||
| 7. Kohan DE, Fioretto P, Tang W, et al. Long-term study of patients with type 2 diabetes and moderate renal impairment shows that dapagliflozin reduces weight and blood pressure but does not improve glycemic control. Kidney Int 2014; 85(4): 962-71. https://doi.org/10.1038/ki.2013.356 PMid:24067431 PMCid:PMC3973038 |
||||
| 8. Zinman B, Wanner C, Lachin JM, et al. Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med 2015; 373(22): 2117-28. https://doi.org/10.1056/NEJMoa1504720 PMid:26378978 |
||||
| 9. Neal B, Perkovic V, Mahaffey KW, et al. Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. N Engl J Med 2017; 377(7): 644-57. https://doi.org/10.1056/NEJMoa1611925 PMid:28605608 |
||||
| 10. Wiviott SD, Raz I, Bonaca MP, et al. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2019; 380(4): 347-57. https://doi.org/10.1056/NEJMoa1812389 PMid:30415602 |
||||
| 11. Perkovic V, Jardine MJ, Neal B, et al. Canagliflozin and Renal Outcomes in Type 2 Diabetes and Nephropathy. N Engl J Med 2019; 380(24): 2295-306. https://doi.org/10.1056/NEJMoa1811744 PMid:30990260 |
||||
| 12. Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med 2020; 383(15): 1436-46. https://doi.org/10.1056/NEJMoa2024816 PMid:32970396 |
||||
| 13. Herrington WG, Staplin N, Wanner C, et al. Empagliflozin in Patients with Chronic Kidney Disease. N Engl J Med 2023; 388(2): 117-27. https://doi.org/10.1056/NEJMoa2204233 PMid:36331190 PMCid:PMC7614055 |
||||
| 14. Packer M, Anker SD, Butler J, et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. N Engl J Med 2020; 383(15): 1413-24. https://doi.org/10.1056/NEJMoa2022190 PMid:32865377 |
||||
| 15. McMurray JJV, Solomon SD, Inzucchi SE, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med 2019; 381(21): 1995-2008. https://doi.org/10.1056/NEJMoa1911303 PMid:31535829 |
||||
| 16. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) With the special contribution of the Heart Failure Association (HFA) of the ESC. Rev Esp Cardiol (Engl Ed) 2022; 75(6): 523. https://doi.org/10.1016/j.rec.2022.05.005 PMid:35636830 |
||||
| 17. Butler J, Jones WS, Udell JA, et al. Empagliflozin after Acute Myocardial Infarction. The N Engl J Med 2024; 390(16): 1455-66. https://doi.org/10.1056/NEJMoa2314051 PMid:38587237 |
||||
| 18. Anker SD, Butler J, Filippatos G, et al. Empagliflozin in Heart Failure with a Preserved Ejection Fraction. N Engl J Med 2021; 385(16): 1451-61. https://doi.org/10.1056/NEJMoa2107038 PMid:34449189 |
||||
| 19. Solomon SD, McMurray JJV, Claggett B, et al. Dapagliflozin in Heart Failure with Mildly Reduced or Preserved Ejection Fraction. N Engl J Med 2022; 387(12): 1089-98. https://doi.org/10.1056/NEJMoa2206286 PMid:36027570 |
||||
| 20. McDonagh TA, Metra M, Adamo M, et al. 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the task force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) With the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail 2024; 26(1): 5-17. https://doi.org/10.1002/ejhf.3024 PMid:38169072 |
||||
| 21. Wanner C, Inzucchi SE, Lachin JM, et al. Empagliflozin and Progression of Kidney Disease in Type 2 Diabetes. The N Engl J Med 2016; 375(4): 323-34. https://doi.org/10.1056/NEJMoa1515920 PMid:27299675 |
||||
| 22. Kidokoro K, Cherney DZI, Bozovic A, et al. Evaluation of Glomerular Hemodynamic Function by Empagliflozin in Diabetic Mice Using In Vivo Imaging. Circulation 2019; 140(4): 303-15. https://doi.org/10.1161/CIRCULATIONAHA.118.037418 PMid:30773020 |
||||
| 23. Cassis P, Locatelli M, Cerullo D, et al. SGLT2 inhibitor dapagliflozin limits podocyte damage in proteinuric nondiabetic nephropathy. JCI insight 2018; 3(15). https://doi.org/10.1172/jci.insight.98720 PMid:30089717 PMCid:PMC6129124 |
||||
| 24. Inoue BH, dos Santos L, Pessoa TD, et al. Increased NHE3 abundance and transport activity in renal proximal tubule of rats with heart failure. Am J Physiol Regul Integr Comp Physiol 2012; 302(1): R166-74. https://doi.org/10.1152/ajpregu.00127.2011 PMid:22031782 |
||||
| 25. Hesp AC, Schaub JA, Prasad PV, et al. The role of renal hypoxia in the pathogenesis of diabetic kidney disease: a promising target for newer renoprotective agents including SGLT2 inhibitors? Kidney Int 2020; 98(3): 579-89. https://doi.org/10.1016/j.kint.2020.02.041 PMid:32739206 PMCid:PMC8397597 |
||||
| 26. Baartscheer A, Schumacher CA, van Borren MM, et.al. Increased Na+/H+-exchange activity is the cause of increased [Na+]i and underlies disturbed calcium handling in the rabbit pressure and volume overload heart failure model. Cardiovasc Res 2003; 57(4): 1015-24. https://doi.org/10.1016/S0008-6363(02)00809-X PMid:12650879 |
||||
| 27. Baartscheer A, Schumacher CA, Wüst RC, et al. Empagliflozin decreases myocardial cytoplasmic Na(+) through inhibition of the cardiac Na(+)/H(+) exchanger in rats and rabbits. Diabetologia 2017; 60(3): 568-73. https://doi.org/10.1007/s00125-016-4134-x PMid:27752710 PMCid:PMC6518059 |
||||
| 28. Jensen J, Omar M, Kistorp C, et al. Effects of empagliflozin on estimated extracellular volume, estimated plasma volume, and measured glomerular filtration rate in patients with heart failure (Empire HF Renal): a prespecified substudy of a double-blind, randomised, placebo-controlled trial. Lancet Diabetes Endocrinol 2021; 9(2): 106-16. https://doi.org/10.1016/S2213-8587(20)30382-X PMid:33357505 |
||||
| 29. Mullens W, Martens P, Testani JM, et al. Renal effects of guideline-directed medical therapies in heart failure: a consensus document from the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2022; 24(4): 603-19. https://doi.org/10.1002/ejhf.2471 PMid:35239201 |
||||
| 30. Bosch A, Ott C, Jung S, et al. How does empagliflozin improve arterial stiffness in patients with type 2 diabetes mellitus? Sub analysis of a clinical trial. Cardiovasc Diabetol 2019; 18(1): 44. https://doi.org/10.1186/s12933-019-0839-8 PMid:30922297 PMCid:PMC6440009 |
||||
| 31. Georgianos PI, Agarwal R. Ambulatory Blood Pressure Reduction With SGLT-2 Inhibitors: Dose-Response Meta-analysis and Comparative Evaluation With Low-Dose Hydrochlorothiazide. Diabetes care 2019; 42(4): 693-700. https://doi.org/10.2337/dc18-2207 PMid:30894383 PMCid:PMC6429633 |
||||
| 32. Dimova R, Tankova T. Does SGLT2 Inhibition Affect Sympathetic Nerve Activity in Type 2 Diabetes? Horm Metab Res 2021; 53(2): 75-84. https://doi.org/10.1055/a-1298-4205 PMid:33202429 |
||||
| 33. Thomas MC, Cherney DZI. The actions of SGLT2 inhibitors on metabolism, renal function and blood pressure. Diabetologia 2018; 61(10): 2098-107. https://doi.org/10.1007/s00125-018-4669-0 PMid:30132034 |
||||
| 34. Zhao Y, Xu L, Tian D, et al. Effects of sodium-glucose co-transporter 2 (SGLT2) inhibitors on serum uric acid level: A meta-analysis of randomized controlled trials. Diabetes Obes Metab 2018; 20(2): 458-62. https://doi.org/10.1111/dom.13101 PMid:28846182 |
||||
| 35. Brown E, Wilding JPH, Barber TM, et al. Weight loss variability with SGLT2 inhibitors and GLP-1 receptor agonists in type 2 diabetes mellitus and obesity: Mechanistic possibilities. Obes Rev 2019; 20(6): 816-28. https://doi.org/10.1111/obr.12841 PMid:30972878 |
||||
| 36. Hayashi T, Fukui T, Nakanishi N, et al. Correction to: Dapagliflozin decreases small dense low-density lipoprotein-cholesterol and increases high-density lipoprotein 2-cholesterol in patients with type 2 diabetes: comparison with sitagliptin. Cardiovasc Diabetol 2017; 16(1): 149. https://doi.org/10.1186/s12933-017-0608-5 https://doi.org/10.1186/s12933-016-0491-5 |
||||
| 37. Filippas-Ntekouan S, Tsimihodimos V, Filippatos T, et al. SGLT-2 inhibitors: pharmacokinetics characteristics and effects on lipids. Expert Opin Drug Metab Toxicol 2018; 14(11): 1113-21. https://doi.org/10.1080/17425255.2018.1541348 PMid:30360662 |
||||
| 38. Maejima Y. SGLT2 Inhibitors Play a Salutary Role in Heart Failure via Modulation of the Mitochondrial Function. Front Cardiovasc Med 2019; 6: 186. https://doi.org/10.3389/fcvm.2019.00186 PMid:31970162 PMCid:PMC6960132 |
||||
| 39. Bray JJH, Foster-Davies H, Stephens JW. A systematic review examining the effects of sodium-glucose cotransporter-2 inhibitors (SGLT2is) on biomarkers of inflammation and oxidative stress. Diabetes Res Clin Pract 2020; 168: 108368. https://doi.org/10.1016/j.diabres.2020.108368 PMid:32800932 |
||||
| 40. Ghanim H, Abuaysheh S, Hejna J, et al. Dapagliflozin Suppresses Hepcidin And Increases Erythropoiesis. J Clin Endocrinol Metab 2020; 105(4). https://doi.org/10.1210/clinem/dgaa057 PMid:32044999 |
||||
| 41. Tran BA, Updike WH, Bullers K, et al. Sodium-Glucose Cotransporter 2 Inhibitor Use Associated With Fournier's Gangrene: A Review of Case Reports and Spontaneous Post-Marketing Cases. Clin Diabetes 2022; 40(1): 78-86. https://doi.org/10.2337/cd21-0015 PMid:35221476 PMCid:PMC8865791 |
||||
| 42. Goldenberg RM, Berard LD, Cheng AYY, et al. SGLT2 Inhibitor-associated Diabetic Ketoacidosis: Clinical Review and Recommendations for Prevention and Diagnosis. Clin Ther 2016; 38(12): 2654-64.e1. https://doi.org/10.1016/j.clinthera.2016.11.002 PMid:28003053 |
||||
| 43. Scheen AJ, Bonnet F. Efficacy and safety profile of SGLT2 inhibitors in the elderly: How is the benefit/risk balance? Diabetes Metab 2023; 49(2): 101419. https://doi.org/10.1016/j.diabet.2023.101419 PMid:36640828 |
||||
English summary
Doi 10.17992/lbl.2024.12.817
SGLT2 inhibitors - A novel treatment for congestive heart failure and chronic kidney disease.
Sigridur Birna Eliasdottir
MD, MS. Sahlgrenska University Hospital, Gothenburg, Sweden.
Correspondence: sigridur.eliasdottir@vgregion.se
Key words: SGLT2 inhbitors, Congestive heart failure, Chronic kidney disease, Diabetes type 2,
Mechanism
SGLT2 inhibitors increase renal excretion of sodium and glucose by blocking the SGLT2 transporters in the proximal tubule. Not only do they lower blood sugars levels but also have positive effects on blood pressure and weight. They lead to more efficient energy metabolism in the heart and kidneys, increase the production of red blood cells and decrease fibrosis and inflammation in the heart and the kidneys. Large double blind randomized trials have shown both cardiac and renal protective effects. Patient with heart failure, both with reduced and preserved ejection fraction have shown to benefit from treatment with SGLT2 inhibitors. They have lower risk of death due to cardiovascular causes and decreased risk of hospitalization because of heart failure compared to patient treated with placebo both with and without diabetes type 2. SGLT2 inhibitors are shown to decrease risk of chronic kidney disease stage 5 and dialysis, death due of cardiovascular events and doubling of serum creatinine in patients with chronic kidney disease both with and without diabetes type 2.
They are now recommended for treatment of heart failure and chronic kidney disease with the highest evidence grade. SGLT2 inhibitors do not increase risk of hypoglycemia or acute kidney injury but do have a serious uncommon adverse effect that are normoglycemic ketoacidosis and Fournier's gangrene that physicians need to be alert to.

