12. tbl. 106. árg. 2020
Fræðigrein
MS og barnsburður: Sjúkdómsvirkni og útkoma meðgöngu og fæðingar
Ágrip
INNGANGUR
MS (multiple sclerosis) er langvinnur bólgusjúkdómur í miðtaugakerfi sem einkennist af köstum, einkum hjá ungu fólki, konum frekar en körlum. Meðgöngu- og fæðingarsaga íslenskra kvenna með MS hefur ekki verið rannsökuð áður. Markmið rannsóknarinnar var tvíþætt, annars vegar að skoða sjúkdómsmynd MS á meðgöngu og fyrstu mánuðum eftir fæðingu og hins vegar að kanna útkomu meðgöngu og fæðingar kvenna með MS og bera saman við hóp kvenna sem ekki hafa greinst með MS eða annan langvinnan sjúkdóm.
EFNIVIÐUR OG AÐFERÐIR
Afturskyggn rannsókn á gögnum úr sjúkraskrá Landspítala og Fæðingaskráningu Embættis landlæknis sem náði til kvenna með greininguna MS (ICD-10: G35) á árunum 2009-2018 og fæðinga þeirra á tímabilinu 1999-2018, alls 91 konu og 137 fæðinga.
NIÐURSTÖÐUR
Köstum fækkaði á fyrsta og öðrum þriðjungi meðgöngu miðað við árið fyrir þungun. Rúmlega helmingur kvennanna var á fyrirbyggjandi lyfjameðferð fyrir meðgöngu og hættu þær allar meðferðinni um eða fyrir getnað. Konur með MS fæddu oftar með keisaraskurði án fæðingarsóttar. Meðgöngulengd kvenna með MS var sambærileg við samanburðarhóp þegar sótt hófst sjálfkrafa. Ekki var munur á fjölda léttbura eða þungbura milli hópa. Apgar-stigun var sambærileg milli hópa.
ÁLYKTUN
Við teljum að rannsókn okkar endurspegli vel meðgöngu- og fæðingarsögu kvenna með MS á Íslandi og að niðurstöður sýni að þær skeri sig lítt úr almennu þýði. Niðurstöður okkar samrýmast erlendum rannsóknum um lægri kastatíðni á meðgöngu en munurinn er þó sá að í okkar rannsókn eru þau áhrif bundin við fyrsta og annan þriðjung meðgöngu.
Greinin barst til blaðsins 10. september 2020, samþykkt til birtingar 10. nóvember 2020.
Inngangur
MS (multiple sclerosis) er langvinnur bólgusjúkdómur sem herjar á miðtaugakerfið og einkennist af bólgufrumuíferð, eyðingu mýelínslíðurs og fækkun taugasíma. Áætlað er að MS hrjái um 2,3 milljónir manna um heim allan en algengi er breytilegt milli landa.1 Tíðnin er há á Íslandi; algengið var 167/100.000 í desember 2007.2 Klínísk einkenni endurspegla líffærafræðilega staðsetningu bólgubletta í miðtaugakerfinu en ekki valda þó allir bólgublettir einkennum. Sjúkdómurinn kemur oftast fram í köstum taugakerfiseinkenna.1,3, 4
Áður fyrr voru konur með MS lattar til þess að ganga með börn vegna gruns um neikvæð áhrif meðgöngu á sjúkdóm móðurinnar og slæm afdrif barnanna.5 Viðhorf til barneigna kvenna með MS er að breytast og nú virðist sem fæðingum þeirra fjölgi.6 Þar sem sjúkdómurinn greinist helst hjá konum á barneignaraldri er mikilvægt að þekking liggi fyrir um afdrif þessa hóps á meðgöngu og í fæðingu. Flest bendir til þess að lítil áhætta fylgi meðgöngu og fæðingu þessara kvenna en nokkurt misræmi hefur þó einkennt niðurstöður rannsókna.1,7
Nú er nokkuð vel staðfest að MS-köstum fækkar á meðgöngu, sérstaklega á síðasta þriðjungi (trimester) og að tíðni þeirra eykst á fyrstu mánuðum eftir fæðingu. Í evrópskri fjölþjóðarannsókn, PRIMS (Pregnancy In Multiple Sclerosis)8 1998 var fyrst sýnt fram á þessar breytingar í sjúkdómsvirkni MS í kringum barnsburð og hafa fleiri rannsóknir síðari tíma stutt þær niðurstöður.9,10 Áhrif brjóstagjafar á tíðni kasta eru þó umdeild; í sumum rannsóknum hefur verið sýnt fram á verndandi áhrif brjóstagjafar,11 en í öðrum reyndist hún hvorki veita vernd né auka áhættu.12
Miklar framfarir hafa orðið í fyrirbyggjandi meðferð (disease modifying treatment) við MS frá því fyrstu lyfin voru tekin í notkun fyrir um 25 árum. Almenna reglan er að þeim hefur ekki verið beitt á meðgöngu eða með brjóstagjöf.5,13 Samtök breskra taugalækna gáfu nýverið út leiðarvísi þar sem fram kemur að nauðsynlegt sé að vega og meta þá áhættu og ávinning sem felst í lyfjameðferð á meðgöngu en að hún komi til greina í sumum tilvikum.14
Meðgöngu- og fæðingarsaga íslenskra kvenna með MS hefur ekki verið rannsökuð áður. Markmið rannsóknarinnar var tvíþætt, annars vegar að skoða sjúkdómsmynd MS á meðgöngu og fyrstu mánuðum eftir fæðingu og hins vegar að kanna útkomu meðgöngu og fæðingar kvenna með MS og bera saman við hóp kvenna sem ekki hafa greinst með MS eða annan langvinnan sjúkdóm.
Efni og aðferðir
Rannsóknin náði til kvenna með greininguna MS (ICD-10: G35) í sjúkraskrárkerfi Landspítala á árunum 2009-2018 og fæðinga þeirra á tímabilinu 1999-2018 eftir greiningu sjúkdómsins, alls 137 fæðinga hjá 91 konu. Útilokaðar voru konur eldri en 65 ára og fæðingar sem áttu sér stað fyrir greiningu sjúkdómsins. Þegar rannsóknarhópurinn var borinn saman við viðmiðunarhóp voru fjölburafæðingar einnig útilokaðar og fæðingar þar sem ekki fundust viðeigandi viðmið. Samanstóð sá undirhópur af 87 konum með MS sem höfðu fætt 129 börn í jafnmörgum fæðingum (mynd 1).
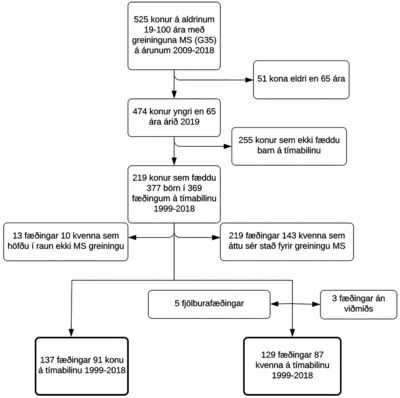
Mynd 1. Flæðirit yfir val rannsóknarþýðis.
Upplýsingum var safnað úr sjúkraskrám Landspítala og Fæðingaskrá Embættis landlæknis. Skoðaður var aldur við greiningu og fæðingu, svo hægt væri að útiloka þær fæðingar sem áttu sér stað fyrir MS-greiningu. Kastatíðni var skráð árið fyrir meðgöngu, á þremur þriðjungum meðgöngu og fyrsta hálfa árið eftir fæðingu. Einungis voru talin þau köst sem voru skilgreind sem slík af taugalækni. Hefð er fyrir því að meðgöngu sé skipt í þrjá mislanga þriðjunga og var ákveðið að halda þeirri tímalengd þegar kastatíðni var borin saman milli þriðjunga. Fyrsti þriðjungur er 12 vikur, annar er 16 vikur og sá þriðji er yfirleitt 12 vikur, ef miðað er við 40 vikna meðgöngu. Skráð var lyfjameðferð móður fyrir og á meðgöngu og eftir fæðingu, hvenær henni var hætt og hvenær hún hófst aftur eftir fæðingu (innan 6 mánaða). Tímalengd brjóstagjafar var skráð í heilum vikum.
Í Fæðingaskrá Embættis landlæknis fengust gögn um meðgöngur og fæðingar kvennanna og börn þeirra. Eftirfarandi breytur voru notaðar til samanburðar á rannsóknarhóp og viðmiðunarhóp: Aldur móður, bæri (parity), kyn barns, fjöldi forskoðana, meðgöngulengd samkvæmt ómun, upphaf fæðingar, fæðingarþyngd nýbura og Apgar-stig við 5 mínútna aldur. Allar ICD (International Classification of Diseases) og NCSP (Nomesco Classification of Surgical Procedures) greiningar móður á meðgöngu og í fæðingu fengust sömuleiðis frá Fæðingaskránni og voru kóðarnir nýttir til þess að skilgreina eftirfarandi breytur til samanburðar: Inngrip vegna fósturstreitu, barnabik í legvatni, áhaldafæðing, valkeisaraskurður, bráðakeisaraskurður, lengt 1. stig fæðingar, lengt 2. stig fæðingar, mænurótardeyfing (epidural anesthesia) og mænudeyfing (spinal anesthesia).
Viðmiðunarhópur (n=129) fékkst með því að para eina fæðingu, fyrir hverja fæðingu í rannsóknarhópnum (n=129), sem átti sér stað næst á eftir í tíma hjá móður af sama bæri og á svipuðum aldri (+/- 1 ár). Mæður sem höfðu aðrar ICD-10 greiningar en þær sem tilheyrðu flokki O (þungun, barnsburður og sængurlega) og Z (þættir sem hafa áhrif á heilbrigðisástand og samskipti við heilbrigðisþjónustu) í Fæðingaskrá voru útilokaðar úr samanburðarhópnum. Með þeim hætti var ætlunin að útiloka mæður sem höfðu langvinna sjúkdóma. Af sömu ástæðu voru konur sem höfðu greiningarnar O10.0 (fyrirverandi háþrýstingur), O24.0 (fyrir-verandi sykursýki) og O11 (meðgöngueitrun ofan á langvinnan háþrýsting) útilokaðar úr samanburðarhópnum. Þessar útilokanir voru ekki gerðar í rannsóknarhópnum.
Tölfræðiúrvinnsla fór fram í forritinu R. Kastatíðni var skoðuð með Poisson-meðaltölum með almennri línulegri aðhvarfsgreiningu. Kastatíðnin fyrir hvert tímabil var umreiknuð í kastatíðni á ári svo hægt væri að bera hana saman milli mismunandi tímabila, þar sem þau voru mislöng. Við samanburð á flokkabreytum var kí-kvaðrat- eða Fisher-próf notað. Við samanburð á lengd brjóstagjafar, meðgöngulengd, Apgar og fæðingarþyngd var ýmist notað t-próf eða Wilcoxon-próf. Tvíkosta aðhvarfsgreining var notuð til þess að reikna gagnlíkindahlutfall (odds ratio, OR) við samanburð á rannsóknar- og viðmiðunarhóp. Til þess að koma í veg fyrir gruggunaráhrif var leiðrétt fyrir meðgöngueitrun, meðgöngusykursýki og meðgönguháþrýstingi þegar OR var reiknað fyrir fyrirburafæðingu, keisaraskurð og framköllun fæðingar. Við samanburð á fæðingarþyngd milli hópa var leiðrétt fyrir meðgöngulengd. Línuleg aðhvarfsgreining var notuð til leiðréttingar. Notast var við 95% öryggisbil (ÖB) og tölfræðileg marktækni miðaðist við p<0,05.
Fyrir lágu leyfi Vísindasiðanefndar (VSN-b20190-10038/03.01), Persónuverndar (2019010098ÞS), Embættis landlæknis (1901171-/5.6.1/gkg) og vísindarannsóknanefndar Landspítala (16).
Niðurstöður
Kastatíðni, lyfjameðferð og brjóstagjöf
Rannsóknarhópurinn taldi 91 konu sem fæddu 142 börn í 137 fæðingum; þar af voru 5 tvíburafæðingar og ein andvana fæðing. Meðalaldur kvennanna við greiningu MS-sjúkdóms var 25 ár og meðalaldur við fæðingu var 31,3 ár. Mynd 2 sýnir dreifingu á fjölda fæðinga kvennanna yfir tímabilið. Flestar voru fæðingarnar árið 2014, 14 talsins (10,2%). Árið 2003 reyndust fæðingar kvenna með MS vera fæstar; aðeins ein fæðing (0,7%).
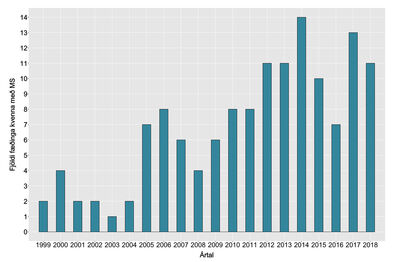
Mynd 2. Fjöldi fæðinga kvenna með MS á ári (1999-2018).
Í töflu I má sjá kastatíðni eftir tímabilum. Kastatíðnin var hæst hálfa árið eftir fæðingu og lægst á fyrsta þriðjungi meðgöngunnar. Á meðgöngu í heild sinni var kastatíðni lægri en árið fyrir meðgöngu (p=0,01). Ekki var breyting á tíðni kasta á síðasta þriðjungi meðgöngu (p=0,483) eða fyrsta hálfa árið eftir fæðingu (p=0,159) miðað við árið fyrir meðgöngu. Á mynd 3 má sjá hvernig kastatíðni á ári breyttist á meðgöngu og eftir fæðingu, miðað við árið fyrir þungun.
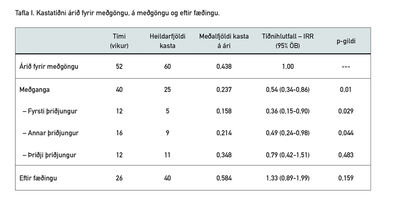
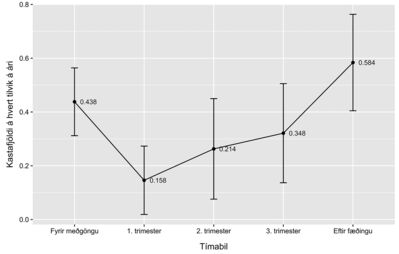
Mynd 3. Tíðni kasta á ári á hverja fæðingu árið fyrir meðgöngu, á meðgöngu og hálfa árið eftir fæðingu. Kastafjöldi á hverju tímabili er umreiknaður í tíðni á ári.
Í rúmlega helmingi tilfella (51,1%) var móðir á fyrirbyggjandi lyfjameðferð fyrir meðgöngu. Allar konur hættu þeirri meðferð fyrir meðgönguna eða við greiningu þungunar. Yfir 90% kvennanna sem voru á lyfjameðferð voru á eftirtöldum lyfjum: interferón beta, natalízúmab, glatiramerasetat, dímetýlfúmarat (tafla II). Í 7 meðgöngum fékk móðir sterameðferð.
 Í 76 tilvikum (55,5%) var tímalengd brjóstagjafar skráð í sjúkraskrá. Í 14 þeirra varði brjóstagjöf skemur en í viku. Meðaltímalengd skráðrar brjóstagjafar var 13,3 vikur. Móðir hætti brjóstagjöf áður en fyrirbyggjandi lyfjameðferð hófst eftir fæðingu í öllum tilvikum, nema einu. Í þeim hópi þar sem tímalengd brjóstagjafar var þekkt var hlutfall þeirra sem hófu lyfjameðferð eftir fæðingu rúmlega tvöfalt miðað við þann hóp þar sem tímalengd var ekki þekkt (72,4% á móti 32,8%, p=0,008). Eins var um hlutfall þeirra sem fengu kast eftir fæðingu (32,9% á móti 16,4%, p=0,045).
Í 76 tilvikum (55,5%) var tímalengd brjóstagjafar skráð í sjúkraskrá. Í 14 þeirra varði brjóstagjöf skemur en í viku. Meðaltímalengd skráðrar brjóstagjafar var 13,3 vikur. Móðir hætti brjóstagjöf áður en fyrirbyggjandi lyfjameðferð hófst eftir fæðingu í öllum tilvikum, nema einu. Í þeim hópi þar sem tímalengd brjóstagjafar var þekkt var hlutfall þeirra sem hófu lyfjameðferð eftir fæðingu rúmlega tvöfalt miðað við þann hóp þar sem tímalengd var ekki þekkt (72,4% á móti 32,8%, p=0,008). Eins var um hlutfall þeirra sem fengu kast eftir fæðingu (32,9% á móti 16,4%, p=0,045).
Útkoma meðgöngu og fæðingar
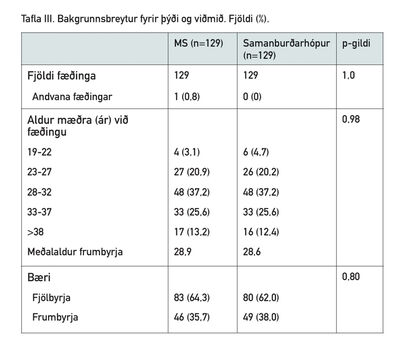
Í töflu III og IV sést samanburður á breytum hjá rannsóknar- og viðmiðunarhóp. Munur var á upphafi fæðinga milli hópanna (p=0,03); konur með MS fóru sjaldnar í sjálfkrafa sótt (51,9% á móti 68,2%, p<0,01). Konur með MS fóru oftar í keisaraskurð án fæðingarsóttar (10,1% á móti 3,1%, p=0,04). Ekki var munur milli hópanna á fjölda forskoðana á meðgöngu.
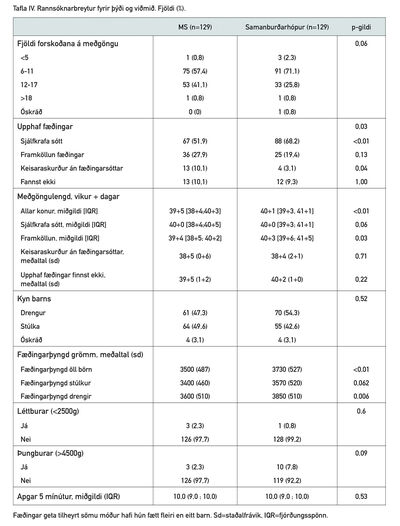 Samanburður á miðgildi meðgöngulengdar milli hópa sýndi að meðganga kvenna með MS var ívið styttri (39v5d miðað við 40v1d, p<0,01) (tafla IV). Meðganga kvenna með MS var styttri þegar fæðing var framkölluð (39v4d miðað við 40v3d, p=0,03) en hvorki þegar sótt hófst sjálfkrafa né við keisaraskurð án fæðingarsóttar.
Samanburður á miðgildi meðgöngulengdar milli hópa sýndi að meðganga kvenna með MS var ívið styttri (39v5d miðað við 40v1d, p<0,01) (tafla IV). Meðganga kvenna með MS var styttri þegar fæðing var framkölluð (39v4d miðað við 40v3d, p=0,03) en hvorki þegar sótt hófst sjálfkrafa né við keisaraskurð án fæðingarsóttar.
Munur var á fæðingarþyngd nýbura milli hópa (tafla IV); nýburar kvenna með MS voru léttari (3500g á móti 3720g, p<0,01). Munurinn var enn marktækur eftir leiðréttingu fyrir meðgöngulengd (p=0,025). Þegar fæðingarþyngd var skipt upp eftir kyni reyndist aðeins munur á fæðingarþyngd drengja milli hópa en ekki stúlkna. Sá þyngdarmunur reyndist ekki marktækur eftir leiðréttingu fyrir meðgöngulengd (p=0,06). Ekki var munur á fjölda léttbura eða þungbura milli hópa. Miðgildi Apgar-stiga við 5 mínútna aldur var hið sama í hópunum (tafla IV).
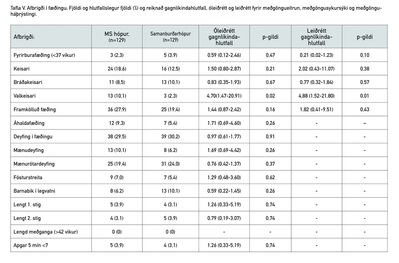
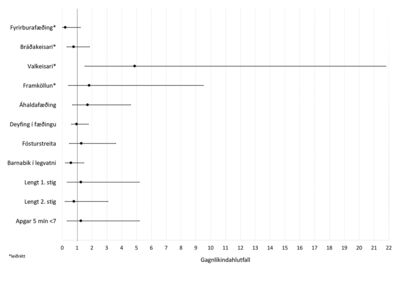
Mynd 4. Afbrigði í fæðingu. Myndræn framsetning á reiknuðu gagnlíkindahlutfalli.
Hlutfallslegan fjölda og gagnlíkindahlutföll (odds ratio) fyrir afbrigði í fæðingu má sjá í töflu V og á mynd 4. Konur með MS fóru í valkeisara í 10,1% tilfella en konur í samanburðarhópnum einungis í 2,3% tilfella. Gagnlíkindahlutfall fyrir valkeisara reyndist hátt, bæði fyrir og eftir leiðréttingu (4,70 [1,47-20,91] og 4,88 [1,52-21,80]).
Umræður
Í þessari rannsókn á fæðingasögu íslenskra kvenna með MS á 20 ára tímabili kom fram að köstum fækkaði á meðgöngu miðað við árið fyrir þungun. Rúmlega helmingur kvennanna var á fyrirbyggjandi lyfjameðferð fyrir meðgöngu og hættu þær allar meðferðinni um eða fyrir getnað. Upplýsingar um tímalengd brjóstagjafar lágu fyrir í rúmlega helmingi tilfella og varði hún að meðaltali í 13,3 vikur. Lyfjameðferð var fátíðari og kastatíðni minni hjá þeim konum þar sem upplýsingar um brjóstagjöf voru ekki skráðar. Konur með MS fóru sjaldnar í sjálfkrafa sótt en konur í samanburðarhópi. Meðganga var ívið styttri hjá rannsóknarhópnum en ekki var aukin hætta á fyrirburafæðingum. Konur með MS voru líklegri til þess að enda meðgönguna með valkeisara. Ekki var aukin hætta á áhaldafæðingu, lengdri fæðingu, framköllun fæðingar, bráðakeisara, barnabiki í legvatni né á inngripi vegna fósturstreitu hjá konum með MS miðað við samanburðarhóp. Ekki var sýnt fram á mun á Apgar milli hópa.
Þegar litið er á heildarfjölda fæðinga á ári á tveggja áratuga rannsóknartímabilinu virðist þeim fara fjölgandi. Þessi þróun samrýmist niðurstöðum bandarískrar rannsóknar Houtchens og félaga þar sem tíðni fæðinga kvenna með MS jókst á árunum 2006-2014.6 Ein möguleg skýring gæti verið að greiningarskilmerki fyrir MS breyttust á tímabilinu, þröskuldur þess að fá staðfesta greiningu lækkaði15, það er konur greinast með vægari sjúkdóm og eru yngri við greiningu sjúkdómsins.7,15 Sú þróun sem orðið hefur í meðferð með fyrirbyggjandi lyfjum, og bætt lífsgæði í kjölfar þess, hafa mögulega virkað hvetjandi á barneignir. Rannsóknir hafa líka sýnt að tíðni MS á Íslandi fer vaxandi og þá ekki síst meðal kvenna.2,16
Kastatíðni lækkaði á meðgöngu miðað við árið fyrir þungun og var lækkunin mest á fyrsta þriðjungi. Þetta er önnur niðurstaða en rannsóknir hafa sýnt, en þá er kastatíðnin yfirleitt lægst á síðasta þriðjungi meðgöngu en þar reyndist munurinn ekki marktækur í okkar rannsókn. Möguleg skýring þessa er að okkar rannsókn er afturskyggn en PRIMS-rannsóknin, sem helst er vísað í varðandi þennan þátt, var framskyggn.8 Í afturskyggnri rannsókn gæti frekar verið um vanskráningu kasta að ræða snemma á meðgöngu, sérstaklega kasta í vægari kantinum, í ljósi þess að á þeim tíma er síst æskilegt að gefa stera og taka segulómmynd með skuggaefni.14,17 Með öðrum orðum gæti verið að skráningu kasta sé seinkað fram á seinni hluta meðgöngu í okkar þýði og niðurstaðan um mun snemma í meðgöngu því ekki raunveruleg. Um helmingur kvennanna í rannsóknarhópi okkar var á fyrirbyggjandi lyfjameðferð fyrir meðgöngu. Hugsanlegt er að áhrifa þessarar meðferðar hafi gætt inn í fyrsta þriðjung meðgöngu og dregið úr kastatíðni. Einnig má benda á að vitað er að natalízúmab, sem 15,3% kvennanna var á fyrir meðgöngu, getur haft svokölluð rebound áhrif sem felast í aukinni kastatíðni þegar um þrír mánuðir eru liðnir frá því að natalízúmab-meðferð er hætt.18,19 Þær niðurstöður okkar að kastatíðni jókst ekki eftir fæðingu eru úr takti við það sem PRIMS-rannsóknin og fleiri rannsóknir hafa sýnt. 8,10 Mögulegt er að þessi munur skýrist af aukinni notkun fyrirbyggjandi lyfja á síðustu árum. Í nýlegri rannsókn Langer-Gould og félaga frá 2019 var ekki sýnt fram á aukna kastatíðni eftir fæðingu.9
Þróun fyrirbyggjandi lyfjameðferðar við MS hefur verið hröð og mikil síðustu árin.20 Við upphaf rannsóknartímabilsins, 1999, voru interferón beta og glatíramerasetat einu lyfin. Með tilkomu natalízúmabs hérlendis árið 2008 jókst fyrirbyggjandi lyfjameðferð og hafa ný lyf bæst við um leið og dregið hefur úr notkun þeirra eldri. Á rannsóknartímabilinu var almennt mælt með að lyfjameðferð væri hætt fyrir ráðgerða þungun eða við greiningu hennar og endurspeglast það í niðurstöðum okkar. Sú ráðlegging gildir áfram fyrir flest nýrri lyfin og vísast þar til nýlegra breskra ráðlegginga.14
Tímalengd brjóstagjafar var einungis skráð í rannsóknarhópi okkar í rúmlega helmingi tilvika og var um þrír mánuðir. Brjóstagjöf samanburðarhóps var ekki könnuð en óbirt gögn úr Heilsusögubanka Krabbameinsfélags Íslands gefa til kynna mun lengri meðaltalsbrjóstagjöf íslenskra barna (frumburða) fæddra á fyrsta áratug þessarar aldar, eða 7-8 mánuðir.21 Við athugun á lengd brjóstagjafar kom í ljós að meðal þeirra kvenna þar sem hún var skráð var hlutfall þeirra sem hófu fyrirbyggjandi lyfjameðferð og þeirra sem fengu kast eftir fæðingu rúmlega tvöfalt á við hinar. Telja verður líklegt að lengd brjóstagjafar annarra MS-kvenna sé lengri, þegar hvorki þarf að taka tillit til sterameðferðar við kasti né fyrirbyggjandi lyfjameðferðar.
Fyrri rannsóknir sýna að ekki er munur á meðgöngulengd kvenna með MS og annarra.22-26 Í okkar rannsókn reyndust konur með MS hafa ívið styttri meðgöngu. Það átti þó ekki við þegar sótt hófst sjálfkrafa, einungis þegar fæðing var framkölluð. Áhugavert væri að skoða hverjar ábendingar fyrir framköllun eru, hvort fötlun vegna MS sé þar á meðal og hvort einhverjar fæðingar séu framkallaðar vegna MS-greiningarinnar einnar, án fötlunar.
Tölulegur munur á tíðni framköllunar reyndist ekki marktækur milli hópanna (MS 27,9%; borið saman við 19,4%; p=0,13). Til samanburðar má geta þess að 27,7% allra fæðinga á landinu 2016-2018 voru framkallaðar.27 Erlendar rannsóknir hafa sýnt mismunandi niðurstöður um tíðni framköllunar hjá konum með MS, allt frá 4,9% upp í 49,6%.25,26,28,29 Ólíkir rannsóknarhópar, til dæmis hvað tímabil, fötlun og almennt heilbrigði varðar, sem og ólík vinnubrögð milli landa, gætu skýrt misræmi milli niðurstaðna rannsókna.
Meðgöngur kvenna með MS voru líklegri til að enda í valkeisara en ekki í bráðakeisara miðað við samanburðarhóp. Þetta samrýmist niðurstöðum norskrar rannsóknar sem tók til tímabilsins 1981-2002.30 Hins vegar hafa tvær aðrar rannsóknir, kanadísk sem tók til tímabilsins 1998-2009 og finnsk sem tók til áranna 2003-2005, sýnt að konur með MS voru ekki líklegri til að enda meðgöngu með valkeisara miðað við samanburðarhópa.24,25 Óljóst er hvort skýra megi niðurstöður rannsóknar okkar um valkeisara með MS-tengdri fötlun kvennanna, óska þeirra um að fæða ekki um leggöng, viðhorfi lækna eða með öðrum fæðingafræðilegum ábendingum. Þessum niðurstöðum þarf þó að taka með fyrirvara þar sem gagnlíkindahlutfall kvenna með MS í rannsókn okkar á að enda meðgöngu með valkeisara gæti reynst uppblásið. Tíðni valkeisara í samanburðarhópnum er töluvert lægri en í hinu almenna þýði, eða um 2,3%, tíðni valkeisara var að meðaltali 6,1% á Íslandi á árunum 2003-2015.31 Það gæti verið afleiðing þess að samanburðarhópurinn er heilbrigðari en allt þýðið.
Fjöldi mænu- og mænurótardeyfinga var sambærilegur milli hópa í okkar rannsókn. Norskar og finnskar niðurstöður sýna sömuleiðis að konur með MS fá þessar deyfingar á pari við viðmið.25,32 Almenn skoðun fræðimanna er að notkun mænu- og mænurótardeyfinga sé örugg hjá þunguðum konum með MS.33
Mæður með MS voru hvorki í meiri hættu á inngripum vegna fósturstreitu í fæðingu né á barnabiki í legvatni. Eftir því sem næst verður komist hefur aðeins ein rannsókn frá árinu 2002 skoðað sömu breytur meðal kvenna með MS og voru niðurstöður hennar samhljóða okkar.23
Tilgátur hafa verið uppi í fyrri rannsóknum um lengt annað stig fæðingar (að lokinni útvíkkun) hjá konum með MS,32 sem jafnvel aukist með alvarleika fötlunar,24 en niðurstöður þeirra hafa þó verið neikvæðar. Niðurstöður okkar styðja heldur ekki slíkar tilgátur, en hvorki var munur á hlutfallslegri hættu á lengdu 1. né 2. stigi fæðingar milli hópa. Taka verður þó niðurstöðum um lengda fæðingu með fyrirvara þar sem ekki er miðað við neina ákveðna eðlilega tímalengd þegar greiningin er sett heldur veltur hún á huglægu mati læknis og greiningin er nær eingöngu notuð þegar hún leiðir til inngrips í fæðinguna til þess að ljúka henni.
Apgar-stigun var sambærileg milli hópa og samrýmist það flestum fyrri rannsóknum.22-24,26,32
Helstu styrkleikar rannsóknarinnar eru þeir að líklegt er að mikill meirihluti kvenna með MS sem fæddu barn á Íslandi á rannsóknartímabilinu hafi verið með í rannsókninni, þar sem Landspítali er stærsta sjúkrahúsið á landinu og flestir MS-sjúklingar eru í meðferð þar. Unnið var með gögn úr Fæðingaskrá Embættis landlæknis og verður það einnig að teljast til styrkleika. Skráin geymir gögn um allar fæðingar á Íslandi síðustu áratugi.
Helstu takmarkanir rannsóknarinnar má telja að hún var afturskyggn og treysti á rétta og nákvæma skráningu á öllum breytum en sjúkraskrá er ekki færð með rannsóknarhagsmuni í huga. Misbrestur var á skráningu á nokkrum breytum og hafði það hugsanlega áhrif á athuganir og tölfræðilegan samanburð. Þetta sést til dæmis á vanskráningu brjóstagjafar. Einnig var ætlunin að athuga fötlunarstig MS-hópsins (svokallað EDSS – Expanded Disability Status Scale) en skráningu þess reyndist mjög ábótavant. Því var ekki hægt að skoða meðgöngu- og fæðingatengdar breytur með tilliti til fötlunarstigs. Einnig mætti teljast veikleiki að hugsanlega er munur á heilbrigði milli hópa þar sem langvinnir sjúkdómar voru aðeins útilokaðir úr samanburðarhópnum en ekki rannsóknarhópnum.
Ráðgjöf um barneignir sem veitt er konum með MS verður alltaf einstaklingsbundin, en gott er þó að hafa niðurstöður þessarar rannsóknar að styðjast við. Við teljum að rannsóknarhópur okkar endurspegli vel raunverulega meðgöngu- og fæðingasögu kvenna með MS á Íslandi, og að niðurstöður sýni að meðgöngur og fæðingar íslenskra kvenna með MS skeri sig lítt úr heilbrigðu þýði íslenskra kvenna. Niðurstöður okkar samrýmast erlendum rannsóknum um verndandi þátt meðgöngu á kastatíðni MS en munurinn er þó sá að í okkar rannsókn eru þau áhrif bundin við fyrsta og annan þriðjung meðgöngu.
Af rannsókn okkar verða þó ekki dregnar ályktanir um þær konur með MS sem ekki eignuðust börn, og voru því undanskildar í endanlega rannsóknarhópnum, hvorki um frjósemi þeirra almennt né hugsanlegar aðrar skýringar á barnleysi þeirra.
Þakkir
Þakkir fá starfsmenn tölfræðiráðgjafar heilbrigðisvísindasviðs Háskóla Ísland fyrir veitta ráðgjöf, starfsmenn Embættis landlæknis og starfsmenn Landspítala sem unnu að undirbúningi gagnasafna.
Heimildir
| 1. Filippi M, Bar-Or A, Piehl F, et al. Multiple sclerosis. Nat Rev Dis Primers 2018; 4: 43. https://doi.org/10.1038/s41572-018-0050-3 https://doi.org/10.1038/s41572-018-0041-4 PMid:30410033 |
||||
| 2. Eliasdottir O, Kjartansson O, Olafsson E. Prevalence of Multiple Sclerosis in Iceland. Neuroepidemiology 2018; 51: 50-6. https://doi.org/10.1159/000489472 PMid:29940573 |
||||
| 3. Dendrou CA, Fugger L, Friese MA. Immunopathology of multiple sclerosis. Nat Rev Immunol 2015; 15: 545-58. https://doi.org/10.1038/nri3871 PMid:26250739 |
||||
| 4. Frohman EM, Racke MK, Raine CS. Medical progress: Multiple sclerosis - The plaque and its pathogenesis. New Engl J Med 2006; 354: 942-55. https://doi.org/10.1056/NEJMra052130 PMid:16510748 |
||||
| 5. Vukusic S, Marignier R. Multiple sclerosis and pregnancy in the 'treatment era'. Nat Rev Neurol 2015; 11: 280-9. https://doi.org/10.1038/nrneurol.2015.53 PMid:25896084 |
||||
| 6. Houtchens MK, Edwards NC, Schneider G, et al. Pregnancy rates and outcomes in women with and without MS in the United States. Neurology 2018; 91: e1559-e69. https://doi.org/10.1212/WNL.0000000000006384 PMid:30266889 PMCid:PMC6205683 |
||||
| 7. Bove R, Alwan S, Friedman JM, et al. Management of multiple sclerosis during pregnancy and the reproductive years: a systematic review. Obstet Gynecol 2014; 124: 1157-68. https://doi.org/10.1097/AOG.0000000000000541 PMid:25415167 |
||||
| 8. Confavreux C, Hutchinson M, Hours MM, et al. Rate of Pregnancy-Related Relapse in Multiple Sclerosis. N Engl J Med 1998; 339: 285-91. https://doi.org/10.1056/NEJM199807303390501 PMid:9682040 |
||||
| 9. Langer-Gould A, Smith JB, Albers KB, et al. Pregnancy-related relapses and breastfeeding in a contemporary multiple sclerosis cohort. Neurology 2020; 94: e1939-e1949. https://doi.org/10.1212/WNL.0000000000009374 PMid:32284359 PMCid:PMC7274922 |
||||
| 10. Houtchens MK, Edwards NC, Phillips AL. Relapses and disease-modifying drug treatment in pregnancy and live birth in US women with MS. Neurology 2018; 91: e1570-e8. https://doi.org/10.1212/WNL.0000000000006382 PMid:30266887 PMCid:PMC6205686 |
||||
| 11. Langer-Gould A, Huang SM, Gupta R, et al. Exclusive Breastfeeding and the Risk of Postpartum Relapses in Women With Multiple Sclerosis. Arch Neurol 2009; 66: 958-63. https://doi.org/10.1001/archneurol.2009.132 https://doi.org/10.1001/archneurol.2009.282 PMid:19506118 |
||||
| 12. Amato MP, Portaccio E. Fertility, pregnancy and childbirth in patients with multiple sclerosis: impact of disease-modifying drugs. CNS drugs 2015; 29: 207-20. https://doi.org/10.1007/s40263-015-0238-y PMid:25773609 |
||||
| 13. Tintore M, Vidal-Jordana A, Sastre-Garriga J. Treatment of multiple sclerosis - success from bench to bedside. Nat Rev Neurol 2019; 15: 53-8. https://doi.org/10.1038/s41582-018-0082-z PMid:30315270 |
||||
| 14. Dobson R, Dassan P, Roberts M, et al. UK consensus on pregnancy in multiple sclerosis: 'Association of British Neurologists' guidelines. Pract Neurol 2019; 19: 106. https://doi.org/10.1136/practneurol-2018-002060 PMid:30612100 |
||||
| 15. Thompson AJ, Banwell BL, Barkhof F, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018; 17: 162-73. https://doi.org/10.1016/S1474-4422(17)30470-2 https://doi.org/10.1016/S1474-4422(18)30168-6 |
||||
| 16. Eliasdottir OJ, Olafsson E, Kjartansson O. Incidence of multiple sclerosis in Iceland, 2002-2007: a population-based study. Mult Scler 2011; 17: 909-13. https://doi.org/10.1177/1352458511402112 PMid:21511690 |
||||
| 17. Sellebjerg F, Barnes D, Filippini G, et al. EFNS guideline on treatment of multiple sclerosis relapses: report of an EFNS task force on treatment of multiple sclerosis relapses. Eur J Neurol 2005; 12: 939-46. https://doi.org/10.1111/j.1468-1331.2005.01352.x PMid:16324087 |
||||
| 18. Papeix C, Vukusic S, Casey R, et al. Risk of relapse after natalizumab withdrawal: Results from the French TYSEDMUS cohort. Neurol Neuroimmunol Neuroinflamm 2016; 3: e297-e. https://doi.org/10.1212/NXI.0000000000000297 PMid:27844037 PMCid:PMC5087255 |
||||
| 19. Prosperini L, Kinkel RP, Miravalle AA, et al. Post-natalizumab disease reactivation in multiple sclerosis: systematic review and meta-analysis. Ther Adv Neurol Disord 2019; 12: 1756286419837809. https://doi.org/10.1177/1756286419837809 PMid:30956686 PMCid:PMC6444403 |
||||
| 20. Kretzschmar B, Pellkofer H, Weber MS. The Use of Oral Disease-Modifying Therapies in Multiple Sclerosis. Curr Neurol Neurosci Rep 2016; 16: 38. https://doi.org/10.1007/s11910-016-0639-4 PMid:26944956 |
||||
| 21. Krabbameinsskrá Krabbameinsfélags Íslands. Heilsusögubanki. | ||||
| 22. Goldacre A, Pakpoor J, Goldacre M. Perinatal characteristics and obstetric complications in mothers with multiple sclerosis: Record-linkage study. Mult Scler Relat Disord 2017; 12: 4-8. https://doi.org/10.1016/j.msard.2016.11.011 PMid:28283105 |
||||
| 23. Mueller BA, Zhang JY, Critchlow CW. Birth outcomes and need for hospitalization after delivery among women with multiple sclerosis. Am J Obstet Gynecol 2002; 186: 446-52. https://doi.org/10.1067/mob.2002.120502 PMid:11904605 |
||||
| 24. van der Kop ML, Pearce MS, Dahlgren L, et al. Neonatal and Delivery Outcomes in Women with Multiple Sclerosis. Ann Neurol 2011; 70: 41-50. https://doi.org/10.1002/ana.22483 PMid:21710652 PMCid:PMC3625744 |
||||
| 25. Jalkanen A, Alanen A, Airas L, et al. Pregnancy outcome in women with multiple sclerosis: results from a prospective nationwide study in Finland. Mult Scler 2010; 16: 950-5. https://doi.org/10.1177/1352458510372629 PMid:20542921 |
||||
| 26. Lu E, Zhu F, van der Kop M, et al. Labor induction and augmentation in women with multiple sclerosis. Mult Scler J 2013; 19: 1182-9. https://doi.org/10.1177/1352458512474090 PMid:23386429 |
||||
| 27. Jonasdottir E, V.H. The Icelandic Birth Registration, annual reports for the years 2016, 2017 and 2018 (Skýrsla frá Fæðingaskráningunni). 2016-2018. | ||||
| 28. Dahl J, Myhr KM, Daltveit AK, et al. Pregnancy, delivery and birth outcome in mothers prior to debut of multiple sclerosis. Eur J Neurol 2006; 13: 28-9. | ||||
| 29. Fong A, Chau CT, Quant C, et al. Multiple sclerosis in pregnancy: prevalence, sociodemographic features, and obstetrical outcomes. J Matern Fetal Neonatal Med 2018; 31: 382-7. https://doi.org/10.1080/14767058.2017.1286314 PMid:28139946 |
||||
| 31. Landspítali. Skýrslur Fæðingarskráningarinnar á Íslandi 2003-2015. | ||||
| 30. Dahl J, Myhr KM, Daltveit AK, et al. Pregnancy, delivery, and birth outcome in women with multiple sclerosis. Neurology 2005; 65: 1961-3. https://doi.org/10.1212/01.wnl.0000188898.02018.95 PMid:16380620 |
||||
| 32. Dahl J, Myhr KM, Daltveit AK, et al. Planned vaginal births in women with multiple sclerosis: delivery and birth outcome. Acta Neurol Scand 2006; 113: 51-4. https://doi.org/10.1111/j.1600-0404.2006.00616.x PMid:16637930 |
||||
| 33. Yurashevich M, Brown J. Anesthetic Considerations for Pregnant Women with Multiple Sclerosis. Í: Anaesthesiologists WFoSo, ritstj. Anaesthesia tutorial of the week 2017. | ||||