05. tbl. 106. árg. 2020
Fræðigrein
Fyrsta meðferð með tocilizumab við COVID-19 hérlendis – sjúkratilfelli
ÁGRIP
Rúmlega fimmtugur karlmaður sem hafði verið á ferðalagi erlendis veiktist við komuna til landsins með flensulíkum einkennum og greindist með COVID-19. Nokkrum dögum síðar versnandi honum af öndunarfæraeinkennum og lagðist inn á Landspítala. Hann reyndist vera súrefnisháður og með útbreiddar íferðir í lungum. Eftir innlögn fékk hann versnandi öndunarbilun og var fluttur á gjörgæsludeild þar sem hann var meðal annars meðhöndlaður með tocilizumab (IL-6 hemill). Hann sýndi batamerki í kjölfarið og þurfti ekki að fara í öndunarvél.
Greinin barst til blaðsins 16. apríl 2020, samþykkt til birtingar 21. apríl 2020.
Inngangur
Síðastliðna mánuði hefur heimsfaraldur með nýrri kórónuveiru, (Severe Acute Respiratory Syndrome Coronavirus-2, SARS-CoV-2) lagt tugi þúsunda að velli og valdið gríðarlegum skaða. Sjúkdómurinn sem veiran veldur er kallaður kórónuveirusjúkdómur, eða COVID-19 á ensku (coronavirus disease 2019). SARS-CoV-2 er af flokki betakórónuveira (betacoronavirus).1 Meginsmitleið er um öndunarveg þar sem veiran hefur innrás sína í þekjuvef meðal annars í gegnum ACE-2 viðtaka (angiotensin converting enzyme 2).2 Faraldurinn hófst í borginni Wuhan í Hubei-héraði í Kína síðla árs 2019 og hefur síðan breiðst hratt um heiminn. Eins og annars staðar hefur faraldurinn leikið almenning hér á landi grátt, auk verulegs efnahagslegs skaða fyrir íslenskt samfélag sem enn sér ekki fyrir endann á. Samhliða þessu hefur þurft að umturna skipulagi og framkvæmd heilbrigðisþjónustu í landinu. Þegar þetta er skrifað hafa tæplega 1800 staðfest smit verið greind hérlendis, samkomubann er enn í gildi, auk annarra samfélagslegra takmarkana með víðtæk áhrif á starfsemi fyrirtækja og stofnana. Stofnuð hefur verið sérstök COVID-göngudeild á Landspítala sem hefur sinnt hátt í 1800 manns. Þar af hafa nálægt 100 einstaklingar verið lagðir inn á spítalann, 13 farið í öndunarvél og 10 eru látin. Enn er mikil óvissa um bestu meðferð þessarar sýkingar og engin gagnreynd lyfjameðferð í boði, en margs konar klínískar prófanir í gangi víðs vegar um heiminn.
Sjúkratilfelli
Rétt rúmlega fimmtugur karlmaður sem hafði verið á ferðalagi erlendis veiktist með flensulíkum einkennum við komuna til landsins og fór strax í sjálfskipaða sóttkví. Maðurinn var í yfirþyngd (BMI 32, líkamsþyngdarstuðull, Body Mass Index) og með fyrri sögu um barnaastma og háþrýsting sem var vel meðhöndlaður með lósartan, hýdróklórtíazíði og amlódipíni. Veikindin byrjuðu með vægum hita, hálssærindum, þurrum hósta og hlustarverk. Daginn eftir komuna til landsins reyndist nefkoksstrok jákvætt fyrir SARS-CoV-2.
Í fyrstu var manninum fylgt eftir með reglulegum símtölum frá COVID-teymi Landspítala. Á 8. degi veikinda var hann kominn með sótthita, mikinn hósta, máttleysi og mæddist við gang. Næstu daga var hann að mestu hitalaus en með þrálátan hósta, lystarleysi, ógleði, uppköst og niðurgang. Á 14. degi hækkaði hitinn og hann fann fyrir takverk og þyngslum fyrir brjósti, höfuðverk og þrýstingi út í eyru. Einnig var hóstinn nú með uppgangi. Hann var lagður inn á smitsjúkdómadeild Landspítala til frekari rannsókna, greiningar og meðferðar.
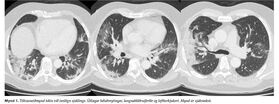
Við komu á sjúkrahús var maðurinn veikindalegur, talmóður og með mikinn hósta. Hann var með 38°C hita og súrefnismettun var 88% á andrúmslofti en fór upp í 95% á 4 L/mín súrefnis í nös. Öndunartíðni var 20-22/mínútur en önnur lífsmörk voru innan eðlilegra marka. Við lungnahlustun heyrðist fíngert brak yfir báðum lungum, mest neðarlega. Að öðru leyti var líkamsskoðun eðlileg. Blóðrannsókn ( tafla I ) sýndi hækkuð hvít blóðkorn, CRP (>200 mg/L) og ferritín (>2000 μg/L), lengdar blæðingarprufur og saltbrenglanir. Fengin var tölvusneiðmynd af brjóstholi sem sýndi dreifðar útlægar þéttingar í öllum lungnablöðum; bæði hélubreytingar (ground glass) og íferðir í lungnablöðrum (alveolar consolidation) með loftberkjukortum (air bronchogram), sem voru taldar geta samrýmst COVID-19 lungnabólgu ( mynd 1 ). Vegna möguleika á bakteríuyfirsýkingu var hafin meðferð með ceftríaxóni í æð og azitrómýsíni um munn. Jafnframt var hafin 5 daga meðferð með hýdroxýklórókíni um munn sem meðferð við COVID-19. Daginn eftir var sjúklingur með allt að 40°C hita, slæm hóstaköst og með mikla þreytu og þróttleysi. Hann var með versnandi hypoxíska öndunarbilun með súrefnismettun 88% á 5-6 L/mín súrefnis í hvíld, sem féll enn frekar við hóstaköst og áreynslu. Öndunartíðni var í kringum 20/mín en blóðþrýstingur og hjartsláttartíðni voru innan eðlilegra marka. Vegna versnandi ástands, áhættuþátta verri útkomu COVID-19-sjúkdóms og vaxandi bólgumyndunar í blóði (CRP og ferritín) var ákveðið að flytja sjúkling á gjörgæsludeild. Næstu klukkustundirnar hélt klínískt ástand áfram að versna og barkaþræðing með innri öndunarvélarmeðferð var yfirvofandi. Hann var talinn vera með boðefnafár (cýtókín storm) og að höfðu samráði smitsjúkdóma- og gjörgæslulækna var ákveðið að hefja meðferð með tocilizumab (IL-6 hemill), 400 mg í æð. Fyrir upphaf meðferðar voru bólguboðefni mæld (17 efna pakki). Þar kom í ljós hækkun á IL-6 (22,04 pg/ml, viðmið <3,66 pg/ml), CD40L (5861 pg/ml, viðmið <4336 pg/ml) og MIP-3a (25 pg/ml, viðmið <4 pg/ml). Önnur bólguboðefni, þar með talið IL-1β og TNFα, voru eðlileg ( tafla II ). Á fyrstu klukkustund eftir lyfjagjöf fór líðan hans batnandi og hann varð hitalaus. Í kjölfarið fóru önnur lífsmörk batnandi og blóðprufur snérust til betri vegar. Á 20. degi var hann fluttur aftur á smitsjúkdómadeild. Sjúklingur þurfti þá 5 L/mín súrefnis í nös til halda súrefnismettun yfir 93%. Hann var inniliggjandi í 5 daga til viðbótar og á þeim tíma jókst þrek hans smám saman og lífsmörk og blóðprufur löguðust. Í kjölfar útskriftar var honum fylgt eftir af COVID-teymi Landspítala og hann var orðinn einkennalaus 34 dögum eftir að veikindi hófust.
Umræða
Á síðustu tveimur áratugum hafa orðið þrír faraldrar sem nýjar kórónuveirur hafa valdið. COVID-19 faraldurinn er sá eini sem hefur orðið að heimsfaraldri, en hinir tveir voru SARS (Severe Acute Respiratory Syndrome) árin 2002-2004 og MERS (Middle Eastern Respiratory Syndrome) sem greindist fyrst 2012 og er enn að skjóta upp kollinum.2,3
COVID-19 varð fyrst vart í kínversku borginni Wuhan í árslok 2019 þegar fjöldi fólks veiktist af lungnabólgu af óljósum toga. Síðan þá hefur sjúkdómurinn breiðst út og var skilgreindur sem heimsfaraldur af Alþjóðaheilbrigðisstofnuninni (WHO) þann 11. mars 2020. SARS-CoV-2 veiran er talin komast inn í frumur mannslíkamans með því að bindast ACE-2 viðtaka á frumuhimnum.2 Þessi viðtaki er meðal annars tjáður í nýrum, hjarta, meltingarvegi, æðakerfi og þekjufrumum í lungnablöðrum (alveolar type 2 cells).2
Meðgöngutími er að meðaltali 4 dagar.6 Sjúkdómurinn byrjar með ósértækum einkennum eins og hita, hósta, máttleysi, mæði og bragð- eða lyktarskynstruflunum1,2,4,7 ( tafla III ). Yfirleitt eru þessi einkenni væg og ganga yfir. Í um 20% tilfella fá einstaklingar alvarlegri einkenni og lungnabólgu, sem að meðaltali koma fram á fimmta degi veikinda.2,6 Eingöngu helmingur sjúklinga er með hita við innlögn en næstum 90% fá hita í sjúkrahúslegunni.6,7 Tölvusneiðmynd af lungum sýnir oftast hélubreytingar útlægt í báðum lungum.8
Blóðprufur í sjúklingum með alvarlega sýkingu sýna gjarnan eitilfrumnafæð, mikla hækkun á LDH, ferritíni, CRP og D-dimer, auk eðlilegs eða vægs hækkaðs prókalsítóníns ( tafla IV ). Greining á SARS-CoV-2-sýkingu byggir á kjarnsýrumögnun erfðaefnis veirunnar í háls- og nefkokstroki, en næmið er ekki þekkt og því er mælst til að endurtaka sýnatöku ef einstaklingur reynist neikvæður en klínískur grunur er fyrir hendi.2 Hjá sjúklingum sem hafa lagst inn á Landspítala virðast einkenni frá meltingarvegum vera tiltölulega algeng, en fremur óalgeng samkvæmt erlendum uppgjörum (3,8%).6
Meðferð við COVID-19 er fyrst og fremst stuðningsmeðferð. Fara ætti varlega með vökvagjöf í æð þar sem SARS-CoV-2 getur skaðað hjartavöðvann auk þess sem leitast er við að halda neikvæðu vökvajafnvægi við meðferð á bráðu andnauðarheilkenni, ARDS (acute respiratory distress syndrome), sem er vel þekktur fylgikvilli COVID-19.2,7,9 Þar sem prókalsítónín er almennt ekki hækkað í COVID-19 er einkum stuðst við það til að meta þörf á sýklalyfjum, en prókalsítónín er talið hækka sérstaklega í bakteríusýkingum. Samkvæmt meðferðarleiðbeiningum Landspítala ber að forðast notkun ytri öndunarvéla og háflæðis súrefnisgjafar vegna hættu á að framkalla loftborið smit, sem veldur aukinni sýkingarhættu fyrir starfsfólk og aðra sjúklinga. Í Kína voru 3,7% smitaðra heilbrigðisstarfsfólk.10 Innlagðir sjúklingar á Landspítala hafa verið meðhöndlaðir með hýdroxýklórókíni samkvæmt ráðleggingum WHO,11 auk þess að azitrómýsíni er oft bætt við. Bæði þessi lyf geta valdið lengingu á QT-bili í leiðslukerfi hjartans og því þarf að taka hjartalínurit til eftirlits. Takmarkaðar rannsóknir eru til um virkni hýdroxýklórókíns en fram hafa komið rannsóknir sem sýna að lyfið hindri SARS-CoV-2 in vitro.12 Auk þess eru vísbendingar um að sé hýdroxýklórókín og azitrómýsín gefið saman geti það flýtt fyrir að nefkoksstrok sjúklinga verði PCR-neikvætt.13 Forðast ætti notkun stera við meðhöndlun á COVID-lungnabólgum utan gjörgæslu. Rannsóknir á MERS og SARS sýndu engan ávinning við sterameðferð, en þvert á móti aukið magn veiru í blóði, lengt veirublæði (viremia) og verri klíníska endapunkta.14,15 Þar að auki eykur sterameðferð dánartíðni í inflúensu.16
Um 15% þeirra sem leita á sjúkrahús verða bráðveikir með alvarlega öndunarbilun, lágþrýsting eða fjölkerfabilun sem krefst gjörgæslumeðferðar.6 Versnun verður að meðaltali 7-12 dögum frá upphafi veikinda.2,6,7,10 Reynslan erlendis er að versnun beri oft hratt að með litlum fyrirboða.17 Þekkt er að sýktir einstaklingar geta fengið mikla súrefnisþurrð án sértækra öndunarfæraeinkenna, sérstaklega aldraðir.18 Af þessum sökum er fylgst náið með súrefnismettun innlagðra og reynt að setja þá sem eru með váleg rannsóknargildi (tafla III) í sírita.
Sjúkdómurinn er frábrugðinn öðrum veirusjúkdómum að því leyti að yfirsýkingar af völdum baktería eru ekki sterkur drifkraftur þessara alvarlegu veikinda.7 Hin bráðu veikindi eru talin stafa af mikilli bólguvirkni eða boðefnafári. Heilkenni boðefnafárs stafar af ofræsingu á bólgusvari ónæmiskerfisins sem einkennist af óheftri framleiðslu boðefna, efnatoga og vaxtarþátta.19 Þetta lýsir sér með viðvarandi hita, eitilfrumnafæð, hækkandi ferritíni, CRP og D-dímer og klínískri mynd sem getur samrýmst bráðu andnauðarheilkenni.2,19,20 Þessi gríðarlega bólgusvörun getur einnig valdið auknu gegndræpi æða og vanstjórnun á storkukerfi.20 Boðefnafári hefur verið lýst í kjölfar SARS-CoV og nú einnig SARS-CoV-2 sýkinga.21 Samhliða þessu geta sumir fengið rauðkornaátsheilkenni, tengt smiti (secondary haemophagocytic lymphohistiocytosis) sem einkennist af viðvarandi háum hita, hvítkornafæð, og hækkuðu ferritíni, auk þess sem lungnabólga (þar með talið ARDS) sést í um það bil helmingi tilfella.19,20
Fjölmargar leiðir hafa verið reyndar við meðhöndlun boðefnafárs, meðal annars með mótefnum gegn IL-1β og viðtökum IL-6.19,20 Báðar meðferðarleiðir hafa verið notaðar á Íslandi og víðar. Enn hafa ekki verið birtar niðurstöður samanburðarrannsókna varðandi virkni IL-6 hemla í COVID-19, aðeins tilfellaraðir og einstök sjúkratilfelli.22,23 IL-6 hemlar hafa þó gefist ágætlega í meðferð annarra sjúkdóma sem valda boðefnafári.20 Það er ekki að ástæðulausu að menn hafa gripið til slíkra tilraunameðferða hjá sjúklingum sem veikjast alvarlega af COVID-19, þar sem nýlegar rannsóknir sýna að dánartíðni er 50-70% meðal þeirra sem leggjast inn á gjörgæsludeildir erlendis.2,7 Um 80% andláta eru á meðal einstaklinga eldri en 60 ára með undirliggjandi sjúkdóma á borð við háþrýsting, hjartasjúkdóma, sykursýki, langvinna lungnasjúkdóma, krabbamein og langvinna nýrnabilun.2,7 Þessir sjúklingar þurfa oft langa sjúkrahúslegu með tilheyrandi álagi á heilbrigðiskerfið. Meðaltími veikinda að andláti eru um 2-8 vikur en meðaltími að bata hjá innlögðum sjúklingum er 6-8 vikur.2
Enn mun nokkur tími líða þar til viðunandi árangur næst í meðferð einstaklinga með boðefnafár í kjölfar COVID-19. Hluti af þeirri meðferð gæti orðið ónæmisbælandi lyfjameðferð sem myndi endurstilla bólgusvarið svo að hinn græðandi hluti ónæmissvarsins nái yfirhöndinni, líkt og hér virðist hafa gerst.
Heimildir
| 1. Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J, et al. Clinical Characteristics of 138 Hospitalized Patients with 2019 Novel Coronavirus-Infected Pneumonia in Wuhan, China. JAMA 2020; Feb 7. https://doi.org/10.1001/jama.2020.1585 PMid:32031570 PMCid:PMC7042881 |
||||
| 2. Phua J, Weng L, Ling L, Egi M, Lim CM, Divatia JV, et al. Intensive care management of coronavirus disease 2019 (COVID-19): challenges and recommendations. Lancet Respir Med 2020; Apr 6. |
||||
| 3. World Health Organization. MERS situation update, January 2020. | ||||
| 4. Giacomelli A, Pezzati L, Conti F, Bernacchia D, Siano M, Oreni L, et al. Self-reported olfactory and taste disorders in SARS-CoV-2 patients: a cross-sectional study. Clin Infect Dis 2020; Mar 26. | ||||
| 5. Wu C, Chen X, Cai Y, Xia J, Zhou X, Xu S, et al. Risk Factors Associated with Acute Respiratory Distress Syndrome and Death in Patients with Coronavirus Disease 2019 Pneumonia in Wuhan, China. JAMA Intern Med 2020; Mar 13. |
||||
| 6. Guan W, Ni Z, Hu Y, Liang WH, Ou CQ, He JX, et al. Clinical Characteristics of Coronavirus Disease 2019 in China. N Engl J Med 2020; Feb 28. | ||||
| 7. Bhatraju PK, Ghassemieh BJ, Nichols M, Kim R, Jerome KR, Nalla AK, et al. Covid-19 in Critically Ill Patients in the Seattle Region - Case Series. N Engl J Med 2020; Mar 30. https://doi.org/10.1056/NEJMoa2004500 PMid:32227758 PMCid:PMC7143164 |
||||
| 8. Shi H, Han X, Jiang N, Cao Y, Alwalid O, Gu J, et al. Radiological findings from 81 patients with COVID-19 pneumonia in Wuhan, China: a descriptive study. Lancet Infect Dis 2020; Apr 20. |
||||
| 9. Keddissi JI, Youness HA, Jones KR, Kinasewitz GT. Fluid management in Acute Respiratory Distress Syndrome: A narrative review. Can J Respir Ther 2018; 55: 1-8. https://doi.org/10.29390/cjrt-2018-016 PMid:31297439 PMCid:PMC6591787 |
||||
| 10. Aylward, Bruce (WHO), Liang W (PRC). Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19). WHO-China Jt Mission Coronavirus Dis 2019. 2020. | ||||
| 11. World Health Organization. Clinical management of severe acute respiratory infection when novel coronavirus (2019-nCoV) infection is suspected: interim guidance, 28 January 2020. World Heal Organ. | ||||
| 12. Yao X, Ye F, Zhang M, Cui C, Huang B, Niu P, et al. In Vitro Antiviral Activity and Projection of Optimized Dosing Design of Hydroxychloroquine for the Treatment of Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2). Clin Infect Dis 2020; Mar 9. https://doi.org/10.1093/cid/ciaa237 PMid:32150618 PMCid:PMC7108130 |
||||
| 13. Gautret P, Lagier J-C, Parola P, Hoang VT, Meddeb L, Mailhe M, et al. Hydroxychloroquine and azithromycin as a treatment of COVID-19: results of an open-label non- randomized clinical trial. Int J Antimicrob Agents 2020; Mar 20: 105949. https://doi.org/10.1016/j.ijantimicag.2020.105949 PMid:32205204 PMCid:PMC7102549 |
||||
| 14. Arabi YM, Mandourah Y, Al-Hameed F, Sindi AA, Almekhlafi GA, Hussein MA, et al. Corticosteroid therapy for critically ill patients with middle east respiratory syndrome. Am J Respir Crit Care Med 2018; 197: 757-67. https://doi.org/10.1164/rccm.201706-1172OC PMid:29161116 |
||||
| 15. Stockman LJ, Bellamy R, Garner P. SARS: Systematic review of treatment effects. PLoS Med 2006; 3: e343. https://doi.org/10.1371/journal.pmed.0030343 PMid:16968120 PMCid:PMC1564166 |
||||
| 16. Lansbury L, Rodrigo C, Leonardi-Bee J, Nguyen-Van-Tam J, Lim WS. Corticosteroids as adjunctive therapy in the treatment of influenza. Cochrane Database Syst Rev 2019; 2: CD010406. https://doi.org/10.1002/14651858.CD010406.pub3 PMid:30798570 PMCid:PMC6387789 |
||||
| 17. Rosenbaum L. Facing Covid-19 in Italy - Ethics, Logistics, and Therapeutics on the Epidemic's Front Line. N Engl J Med 2020; Mar 18. https://doi.org/10.1056/NEJMp2005492 PMid:32187459 |
||||
| 18. Xie J, Tong Z, Guan X, Du B, Qiu H, Slutsky AS. Critical care crisis and some recommendations during the COVID-19 epidemic in China. Intensive Care Med 2020; Mar 2. |
||||
| 19. Mehta P, McAuley DF, Brown M, Sanchez E, Tattersall RS, Manson JJ. COVID-19: consider cytokine storm syndromes and immunosuppression. Lancet 2020; 395: 1033-4. |
||||
| 20. Tanaka T, Narazaki M, Kishimoto T. Immunotherapeutic implications of IL-6 blockade for cytokine storm. Immunotherapy 2016; 8: 959-70. https://doi.org/10.2217/imt-2016-0020 PMid:27381687 |
||||
| 21. Zhou Y, Fu B, Zheng X, Wang D, Zhao C, qi Y, et al. Pathogenic T cells and inflammatory monocytes incite inflammatory storm in severe COVID-19 patients. Natl Sci Rev 2020; Mar. https://doi.org/10.1093/nsr/nwaa041 PMCid:PMC7108005 |
||||
| 22. Zhang X, Song K, Tong F, Fei M, Guo H, Lu Z, et al. First case of COVID-19 in a patient with multiple myeloma successfully treated with tocilizumab. Blood Adv 2020; 4: 1307-10. https://doi.org/10.1182/bloodadvances.2020001907 PMid:32243501 PMCid:PMC7160284 |
||||
| 23. Luo P, Liu Y, Qiu L, Liu X, Liu D, Li J. Tocilizumab treatment in COVID-19: a single center experience. J Med Virol 2020; Apr 6. https://doi.org/10.1002/jmv.25801 PMCid:PMC7166592 |
||||