05. tbl. 106. árg. 2020
Fræðigrein
ÁGRIP
MS (multiple sclerosis) er algengasti bólgusjúkdómurinn í miðtaugakerfi og ein algengasta orsök fötlunar hjá ungu og miðaldra fólki. MS er sjálfsofnæmissjúkdómur sem orsakast af flóknu samspili erfða og umhverfis. Miklar framfarir hafa orðið í greiningu og meðferð sjúkdómsins á síðustu árum og mikilvægt er að læknar séu vel upplýstir um einkenni og meðferðarmöguleika til að tryggja skjóta greiningu og viðeigandi meðferð. Í þessari grein ræðum við nýjungar í orsökum, greiningu og meðferð MS.
Greinin barst til blaðsins 23. janúar 2020, samþykkt til birtingar 14. apríl 2020.
Þessi grein er að hluta byggð á greininni MS-Sjúkdómurinn anno 2018 eftir Hauk Hjaltason í MS-blaðinu 2018. Birt með góðfúslegu leyfi MS-blaðsins.
Inngangur
MS (multiple sclerosis) er algengasti bólgusjúkdómurinn í miðtaugakerfi og ein algengasta orsök fötlunar hjá ungu og miðaldra fólki. Samfélagslegur kostnaður vegna MS hefur verið hár, ekki síst vegna atvinnufjarveru.1 Með bættri meðferð mun þessi kostnaður hugsanlega minnka.2 MS er sjálfsofnæmissjúkdómur sem orsakast af flóknu samspili erfða og umhverfis.3 Miklar framfarir hafa orðið í greiningu, ekki síst snemmgreiningu, og meðferð MS á síðustu árum og mikilvægt er að læknar séu vel upplýstir um einkenni og meðferðarmöguleika til að tryggja skjóta greiningu og viðeigandi meðferð. Eldra yfirlit um sjúkdóminn birtist í Læknablaðinu árið 2009.4 Í þessari grein ræðum við nýjungar í orsökum, greiningu og meðferð MS.
Tíðni sjúkdóms og áhættuþættir
Einn af hverjum 500-1000 greinist með MS á lífsleiðinni (0,1-0,2%).5 Tíðni er breytileg eftir löndum og svæðum, en er há á Íslandi. Á árunum 2002-2007 var nýgengi MS á Íslandi 7,6 á hverja 100.000 íbúa á ári, og algengi í lok árs 2007 167/100.000 íbúa.6,7 Ef þessar tölur eru heimfærðar upp á fjölda Íslendinga í dag (350.000) samrýmast þær því að fjöldi MS-sjúklinga sé nú 585 og að 27 einstaklingar greinist árlega. MS-greining er algengust á aldursbilinu 20-40 ára, en kemur fyrir meðal barna og eldra fólks en er þó fátíð eftir 60 ára aldur.8 Eins og í flestum öðrum sjálfsofnæmissjúkdómum eru konur í meiri áhættu en karlar (3:1).5
Orsök MS er ekki fyllilega þekkt enda ólíklega um eina orsök að ræða. Allt bendir til þess að MS sé sjálfsofnæmissjúkdómur.3 Hvað nákvæmlega setur í gang sjálfsofnæmisferlið er ekki vitað. Eins og í öðrum slíkum sjúkdómum eru til staðar umhverfis- og erfðaþættir sem magna upp hver annan.9 MS svipar þannig til annarra sjálfsofnæmissjúkdóma eins og iktsýki og sóríasis.
Nokkrar stórar rannsóknir á mikilvægi erfða í MS hafa verið gerðar á undanförnum árum.10 Sterkastur er erfðaþátturinn hjá eineggja tvíburum, um 30%.11 Annars er áhættan hjá fyrstu gráðu ættingja á bilinu 3-5% (rúmlega tíföld miðað við almenning).10 Niðurstöður sýna að HLA-vefjagerðin hefur þar mesta þýðingu.10 HLA inniheldur hundruð gena sem staðsett eru á litningi 6, og mörg þeirra gegna lykilhlutverki í starfsemi ónæmiskerfisins. HLA-afbrigðið DR-15 eykur líkurnar á MS og er algengt hjá norðlægum þjóðum, sem útskýrir að hluta hærra algengi sjúkdómsins meðal þessara þjóða. Til viðbótar við HLA-vefjagerðina hafa vísindamenn greint yfir 200 aðrar erfðabreytur sem auka áhættuna á MS.10,12 Hver og ein þeirra hefur þó takmarkaða áhættuaukningu í för með sér. Þetta styður að margar mismunandi erfðabreytur hafi samanlögð áhrif á arfgengi MS.10 Það hefur þó takmarkað gildi að framkvæma einstaklingserfðapróf til að meta MS-áhættu, til að mynda hjá nánum ættingjum MS-sjúklinga. Þessi erfðaþekking hefur hins vegar töluverða þýðingu fyrir skilning okkar á orsökum sjúkdómsins þar sem flest genin hafa þýðingu fyrir starfsemi ónæmiskerfisins, sem er frekari vísbending um að MS sé sjálfsofnæmissjúkdómur. Til lengri tíma litið gæti þessi þekking verið mikilvæg fyrir þróun nýrra meðferða og hugsanlega getur erfðasamsetning hvers og eins spáð fyrir um hvaða fyrirbyggjandi lyf virka best í hverju tilviki.
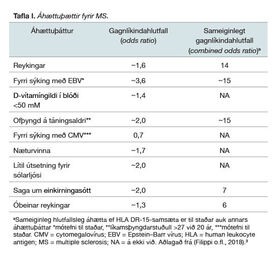
Fjarlægð frá miðbaug virðist skipta máli í tíðni á MS og líklegt að sólarljós komi þar við sögu.5 Lágt D-vítamíngildi í blóði er áhættuþáttur fyrir því að greinast með MS (tafla I).9,13 Vísbendingar eru um að hið virka form D vítamíns (1,25-dihydroxycholecalciferol) hafi ónæmisbælandi áhrif.9,13 Langflestir einstaklingar með MS bera með sér Epstein Barr-veiruna.14 Að hafa veikst af einkirningasótt eykur áhættuna á MS enn frekar (tafla I).9 Á síðustu árum hefur komið í ljós að reykingar bæði auka áhættuna á MS8 og ýta undir verri horfur.15 Því er mikilvægt að hvetja MS-sjúklinga til reykbindindis.16 Athyglisvert er að ofþyngd, sérstaklega á unglingsárum, er einnig áhættuþættur.9 Sjá má þekkta áhættuþætti og samspil þeirra í töflu I . Þó að hver áhættuþáttur sé tiltölulega vægur breytist áhættan til muna ef fleiri áhættuþættir fara saman. Sem dæmi: ef viðkomandi reykir er áhættuaukningin 1,6 (60%) en að viðbættri HLA DR-15 genasamsætunni eykst áhættan fimmtánfalt (tafla 1).17 Ef viðkomandi hefur ofannefnda vefjagerð og fyrri sögu um EBV-sýkingu verður sextánföld áhætta18 og hið sama má segja um samspil vefjagerðarinnar og ofþyngdar á unglingsárum.19
Einkenni og sjúkdómsgangur
MS einkennist af bólgu í miðtaugakerfi. Bólgan er án merkja um sýkingu3, kemur endurtekið en leggst mismunandi á sjúklinga. Bólgan veldur köstum en sjúkdómsgangur er breytilegur eftir því hversu títt bólgublettir myndast, staðsetningu þeirra og umfangi. Þó að sjúklingar geti náð sér vel eftir köst, skilja þau ávallt eftir sig einhvern vefjaskaða og stundum viðvarandi einkenni (sjá mynd 1 ). Með hækkandi aldri dregur oftast úr kastatíðni. Síðkomin versnun, versnun án kasta, (sjá gulu línuna í neðsta hluta myndar 1 ) kemur fram hjá hluta sjúklinga, yfirleitt allmörgum árum eftir greiningu.20 Ekki er vitað hvað kemur henni af stað en líklega skiptir magn vefjaskemmda máli, bæði þeirra sem sjáanlegar eru með segulómun og annarra.21,22 Rannsóknir benda til þess að með því að halda kastatíðni niðri (eins og gert er með fyrirbyggjandi meðferð í dag) megi komast hjá eða seinka slíkri síversnun.3 Um 10-15% sjúklinga eru hins vegar án dæmigerðs kastaforms sjúkdómsins frá upphafi, oft nefnt frumkomin síversnun (primary progressive MS). Einkenni þeirra sjúklinga verða verri með tímanum og ganga ekki til baka eins og yfirleitt er þegar um kastaeinkenni er að ræða. Síversnunin, af hvorri tegundinni sem er, getur hins vegar verið mismunandi hröð. Þegar verst lætur er versnunin hröð, með tilheyrandi fötlun á tiltölulega skömmum tíma.
Köst hafa lengstum verið afgerandi í mati á sjúkdómsvirkni. Á undanförnum árum hefur hins vegar komið í ljós að köstin eru eingöngu toppurinn á ísjakanum.23 Sjúklingar geta verið með nýjar bólgubreytingar á segulómun (skuggaefnishlaðandi eða nýtilkomnar breytingar) án þess að finna til einkenna eða vera í kasti. Talið er að 9 af hverjum 10 nýjum skellum leiði ekki til kasts en skaði miðtaugakerfisvef þegar til lengri tíma er litið og ýti að öllum líkindum undir síversnun.24 Því er mikilvægt að leggja áherslu á hugtakið sjúkdómsvirkni, sem metin er með tíðni og alvarleika kasta og tilkomu nýrra breytinga á segulómun. Vaxandi áhersla er á að mat á sjúkdómsvirkni með þessum hætti eigi að vera leiðandi í ákvarðanatöku um meðferð.3 Eftir að meðferð er hafin og við breytingar á henni er oft miðað við að segulómun sé framkvæmd að minnsta kosti einu sinni á ári en þann tíma má fljótlega lengja ef vel gengur. Nýjar rannsóknir benda til að sjúkdómsvirkni megi ennfremur meta með mælingu á prótíninu neurofilament light, sem er niðurbrotsefni taugaþráða, hvort sem er í mænuvökva eða sermi.25 Almenn notkun þessara mælinga er þó enn takmörkuð.26
Greining
Sú regla fyrir MS-greiningu sem lengstum hefur verið miðað við er að sjúklingur hafi fengið tvö köst aðskilin í tíma og rúmi og að aðrar skýringar hafi verið útilokaðar. Sú regla gildir áfram en með tilkomu segulómunar og nýrra greiningarskilmerkja sem fyrst birtust 2001, en hafa verið endurskoðuð nokkrum sinnum, síðast 2017,27 er nú hægt að greina MS þegar eftir eitt kast. Miðað er við að kastaeinkennin hafi varað í að minnsta kosti einn sólarhring og séu dæmigerð fyrir MS.28 Sem dæmi er sjóntap og verkur við augnhreyfingar en það eru einkenni um sjóntaugabólgu sem er algeng í MS. Höfuðverkur og flog myndu hins vegar ekki flokkast undir dæmigerð einkenni. Einkenni kasts byrja yfirleitt ekki skyndilega og standa í daga eða vikur, jafnvel mánuði. Hafi sjúklingur fengið í fyrsta sinn dæmigerð einkenni og þar með sitt fyrsta kast auk þess að segulómun sýni að minnsta kosti eina breytingu á að minnsta kosti tveimur af fjórum tilgreindum svæðum, eins og sést á mynd 2 (útbreiðsla í rúmi), er hægt að setja MS-greininguna að því tilskildu að aðrar skýringar séu útlokaðar. Annað skilyrði tekur til tímaþáttar (útbreiðsla í tíma) og felst í að við segulómun sjáist misgamlar breytingar (með og án skuggaefnis), eða nýjar breytingar frá einni segulómunarmynd til þeirrar næstu, eða þá að bólgubönd sjáist í mænuvökva sjúklings. Eins og sést á þessu skiptir segulómun miklu við snemmgreiningu á MS.
Dæmigerð klínísk einkenni eru forsenda MS-greiningar. Stundum greinast hins vegar MS-líkar breytingar á segulómun hjá sjúklingum án nokkurra slíkra einkenna (til dæmis sjúklingar sem hafa farið í segulómun vegna brjóskloss eða höfuðverkja). Í þessum tilvikum er talað um að sjúklingar hafi Radiological Isolated Syndrome, RIS. 29 Framskyggnar rannsóknir skortir á þessum hópi en afturskyggnar athuganir benda til að allt að þriðjungur þessara einstaklinga fái einkenni og greinist með MS næstu 5 ár eftir RIS-greiningu.30 Mikilvægt er því að fylgja einstaklingum eftir klínískt og myndrænt með reglulegu millibili sem ræðst af aldri og hversu sterkur grunur er um MS út frá myndrannsóknum.30
Meðferð
Meðferð við MS má skipta í þrennt:
- Meðferð við köstum
- Fyrirbyggjandi meðferð
- Meðferð gegn viðvarandi einkennum (svo sem þreytu, verkjum,
aukinni vöðvaspennu og þvagblöðrutruflunum)
Sterameðferð við köstum (í formi inndælingar eða töflumeðferðar) er einkum beitt þegar kastaeinkenni trufla daglegt líf sjúklings eða gætu skilið eftir sig fötlun.3 Mikilvægt er að útiloka sýkingar því að í slíkum tilvikum getur sterameðferð verið hættuleg. Hafa skal í huga að sýkingar, jafnvel vægar sýkingar eins og þvagfærasýkingar og ýmsar veirusýkingar, geta kallað fram eða ýft upp fyrri MS-einkenni. Þótt það sé ekki alltaf auðvelt, er mikilvægt að mistúlka ekki slíkt sem raunveruleg köst eða merki um aukna sjúkdómsvirkni. Við afar slæmum köstum sem ekki svara háskammtasterameðferð er hægt að beita blóðvökvaskiptum (plasma exchange).3
Ekki verður frekar farið út í meðferð gegn viðvarandi einkennum en þó minnst á lyfið famprídín (Fampyra®) sem er tiltölulega nýlega komið á markað hér. Lyfið virkar hemjandi á flæði kalíum-jóna yfir frumuhimnur og hafa rannsóknir sýnt að það getur í sumum tilvikum bætt göngugetu MS-sjúklinga.31 Krafist er lyfjaskírteinis þar sem koma þarf fram niðurstaða sjúkraþjálfara um skerta göngugetu sjúklings.
Fyrirbyggjandi meðferð
Tilgangur fyrirbyggjandi meðferðar er að minnka sjúkdómsvirkni:
- Fyrirbyggja köst
- Koma í veg fyrir nýjar breytingar á segulómun
- Fyrirbyggja fötlun og síversnun
Þessa þrjá þætti er oftast miðað við í rannsóknum á gagnsemi lyfja við MS. Á töflu II má sjá núverandi fyrirbyggjandi meðferð við MS á Íslandi. Interferón beta (Avonex®, Betaferon®, Rebif®, Plegridy®) og glatíramerasetat (Copaxone®, Remurel®) eru sprautulyf sem notuð hafa verið í um tvo áratugi. Þau veita um 30% vörn gegn köstum en dæmi eru um sjúklinga sem verið hafa á þessum lyfjum í mörg ár með góðum árangri.32,33 Góð reynsla er af þessum lyfjum með tilliti til öryggis. Helsta aukaverkun interferón beta lyfjanna eru flensulík einkenni.3 Tíðni notkunar er allt frá vikulegum gjöfum í vöðva upp í að sjúklingar sprauti sig daglega undir húð þegar um glatírameracetat meðferð er að ræða. Lyf um munn, teriflúnómíð (Aubagio®) og dímetýlfúmarat (Tecfidera®), eru dæmi um önnur lyf í flokki 1 (sjá töflu II ). Fyrirbyggjandi áhrif dímetýlfúmarats á MS eru meiri en hjá interferón beta og glatíramerasetati.34 Algengustu aukaverkanir eru húðroði og hitakennd, og meltingarfæraóþægindi geta komið fyrir í upphafi meðferðar og hamlað áframhaldandi notkun. Vegna fæðar á eitilfrumum sem getur orðið á dímetýlfúmarat-meðferð er mælt með blóðprufum fjórum sinnum á ári. Þekkt eru örfá tilvik heilabólgu (sjá neðar) sem hafa tengst mikilli eitilfrumufæð. Fyrirbyggjandi árangur teriflúnómíðs er svipaður og hjá eldri sprautulyfjunum, lítil áhætta er á alvarlegum aukaverkunum nema að lyfið getur valdið skaðlegum áhrifum á fóstur35 og vegna mögulegra áhrifa á lifur kallar teríflúnómíð á blóðprufur aðra hverja viku í byrjun.
Meginviðmiðið er að sjúklingur fari í fyrstu á eitthvert lyf í flokki 1 en dugi það ekki til að hefta sjúkdómsvirkni er skipt yfir í lyf í flokki 2.36 Til lyfja í þeim flokki er reyndar stundum gripið strax í byrjun ef sjúkdómsvirkni er mikil, til dæmis ef sjúklingur hefur fengið tvö fatlandi köst á innan við einu ári.37 Þessi lyf (eins og lyf í flokki 1) hafa öll með einum eða öðrum hætti áhrif á ónæmiskerfi sjúklings. Sum hefta för hvítra blóðkorna úr blóðrás yfir í miðtaugakerfi og varna með því bólguviðbrögðum (natalízumab).
Viss lyf hefta flutning eitilfrumna úr eitlum inn í blóðrásina (fingolimod) og önnur tilurð eitilfrumna (rítúxímab). Með tilkomu natalízúmabs (Tysabri®) 2006 urðu viss straumhvörf í meðferð MS38 en það var þá fyrsta viðbót við eldri sprautulyfin sem getið er að ofan. Natalízumab er árangursrík meðferð, gefin í æð mánaðarlega, en getur líka valdið hættulegri heilabólgu af völdum JC-veiru (progressive multifocal leucoencephalpathy, PML). Þessarar tegundar heilabólgu hefur líka orðið vart hjá öðrum lyfjum (dímetýlfúmarat og fingolimod) en ekki í sama mæli. Hægt er að mæla mótefni í sermi gegn JC-veirunni og séu þau ekki til staðar eru hverfandi líkur á umræddri heilabólgu og talið óhætt að halda áfram natalízumab-meðferð.
Rannsóknir í grannlöndum okkar sýna að um helmingur fólks hefur smitast af JC-veirunni. Við meðferð með natalízumabi eru blóðprufur teknar tvisvar á ári, meðal annars til að fylgjast með hugsanlegri tilkomu JC-mótefna hjá áður neikvæðum sjúklingum. Fingolimod (Gilenya®) er töflumeðferð sem hefur betri sjúkdómshemjandi áhrif en interferón beta og glatíramerasetat.39 Aukaverkanir eru meðal annars fækkun hvítra blóðkorna, sérstaklega eitilfrumna, sem kallar á reglubundnar blóðprufur, og getur aukið hættu á sýkingum, meðal annars umræddri heilabólgu en miklu sjaldnar en hjá natalízumabi. Í mjög sjaldgæfum tilvikum getur verið hætta á alvarlegum hjartsláttartruflunum og á þetta sérstaklega við eftir fyrsta lyfjaskammt. Sjúklingar eru því undir sérstöku eftirliti fyrstu klukkustundirnar eftir að meðferð er hafin. Verði af einhverjum ástæðum hlé á lyfjagjöf getur þurft að hafa sama háttinn á þegar meðferð hefst að nýju. Rétt er að benda á að samfara fingolimod-notkun á ekki að nota lyf sem áhrif hafa á leiðslukerfi í hjarta.
Viss hætta er á bólgu í sjónhimnu (macular edema) sem kemur aðallega fram hjá sjúklingum með sykursýki. Þetta kallar á augnbotnaeftirlit eftir þriggja mánaða meðferð. Rítúxímab (MabThera®, Blitzima®, Truxima®) er eldra lyf sem einkum hefur verið notað við ýmsum gigtar- og blóðsjúkdómum. Lyfið hefur ekki gengið í gegnum stóra fasa-3 rannsókn við MS en á undanförnum árum hafa Svíar engu að síður mjög beitt þessari meðferð við MS með mjög góðum árangri40 og höfum við hér á landi gert slíkt hið sama.
Svíar hafa gert viðamiklar rannsóknir á rítúxímabi sem sýna góðan árangur og gott öryggi í samanburði við önnur MS-lyf.40 Helstu aukaverkanir eru innrennslistengdar (gefið í byrjun í æð tvisvar á ári) auk vissrar áhættu á sýkingum vegna ónæmisbælingar.
Ocrelizumab (Ocrevus®) er hins vegar nýrra lyf sem svipar mjög til rítúxímabs. Bæði bæla lyfin B-eitilfrumur. Auk góðrar virkni á kastasjúkdóm MS41 er ocrelizumab fyrsta lyfið sem rannsóknir hafa sýnt að skilar árangri í MS við frumkomna síversnun.42 Þó hafði fyrri rannsókn á rítúxímab einnig sýnt fram á árangur hjá sjúklingum með frumkomna síversnun væru þeir undir 50 ára aldri og merki væru um virkan sjúkdóm á segulómun.43 Ocrelizumab er tiltölulega nýlega komið á markað á Íslandi en greiðsluþátttaka liggur þó eingöngu fyrir varðandi notkun þess við frumkomið síversnunarform MS. Alemtuzimab (Lemtrada®) er eldra lyf sem hefur verið notað í allmörg ár en þó ekki hér á landi.44 Gjöf þess er nokkru flóknari en hinna og aukverkanir, ekki síst frá skjaldkirtli, eru algengar.
Kladríbín (Mavenclad®) er krabbameinslyf sem var nýlega skráð sem MS-lyf á Íslandi og er gefið í tveimur kúrum á ári á tveimur árum, svo er beðið átekta með frekari lyfjagjöf næstu tvö árin. Rannsóknir hafa sýnt að lyfið er áhrifaríkara en beta-interferón og glatíramerasetati, virðist þolast vel og lítið um aukaverkanir nema helst hætta á ristli (varicella zoster).45
Stofnfrumumeðferð með blóðmyndandi frumum (hematopoietic stem cell transplantation) hefur verið beitt við MS. Þegar um yngri sjúklinga er að ræða með mikla bólguvirkni og fjölda kasta sem ekki ræðst við með hefðbundinni lyfjameðferð, virðist fátt eins áhrifaríkt og stofnfrumumeðferð en hún er ekki hættulaus og reynir á sjúklinginn.47 Stofnfrumumeðferð hefur ekki skilað árangri við síversnunarformi MS.47 Vísbendingar eru um að inntaka háskammta D-vítamíns geti minnkað líkur á að greinast með MS48 og geti hugsanlega minnkað sjúkdómsvirkni eftir að sjúkdómurinn er kominn fram.49 Því er oft mælt með inntöku 1000-2000 eininga daglega hjá sjúklingum með MS, ekki síst yfir vetrarmánuði og ef gildi D-vítamíns er lágt.
Þróun fyrirbyggjandi lyfjameðferðar við MS hefur verið hröð undanfarin ár. Vaxandi áhersla hefur verið lögð á að byrja á fyrirbyggjandi lyfjameðferð sem fyrst og fylgjast vel með og breyta henni nái hún ekki að halda sjúkdómsvirkni niðri. Nýrri og bættri meðferð er ástæða til að fagna um leið og ganga þarf götuna með gát. Ekki er langt síðan hætt var að nota nýtt lyf við MS vegna alvarlegra aukaverkana sem komu í ljós eftir skamma notkun þess.46
Lyfjameðferð við MS er að langmestu leyti sinnt á göngudeild taugadeildar Landspítala. Þar fer einnig fram eftirlit lækna, og ekki síður hjúkrunarfræðinga, með göngudeildarkomum og símaþjónustu. Þessi þjónusta hefur vaxið mjög mikið síðustu árin en að sama skapi hefur komum á bráðamóttökur og innlögnum á sjúkrahús fækkað mikið. Auk beinnar lyfjagjafar felst göngudeildarþjónusta í einkenna- og aukaverkanaeftirliti, tilheyrandi blóðprufum og ýmissi ráðgjöf, auk þess sem segulómskoðanir skipta miklu máli og samskipti við röntgendeild því mikilvæg.
Lokaorð
Á síðustu tveimur áratugum hefur orðið bylting í þekkingu á MS-sjúkdómnum. Aukinn skilningur hefur fengist á áhættuþáttum sjúkdómsins. Greiningarhæfnin hefur aukist til muna en síðast en ekki síst eru fjölmargir áhrifaríkir meðferðarmöguleikar komnir fram á sjónarsviðið, ekki síst við kastaformi MS. Þróunin verður líklega áfram hröð og innan fárra ára munu langtímaáhrif bættrar meðferðar koma í ljós, til að mynda hvort síðkomin versnun verði fátíðari. Einnig er þörf á betri meðferð við síversnunarformum sjúkdómsins auk betri vitneskju um hve lengi eigi að halda meðferð áfram hjá sjúklingum án sjúkdómsvirkni í langan tíma.50
Heimildir
| 1. Kobelt G, Thompson A, Berg J, Gannedahl M, Eriksson J; MSCOI Study Group; European Multiple Sclerosis Platform. New insights into the burden and costs of multiple sclerosis in Europe. Mult Scler 2017; 23: 1123-36. https://doi.org/10.1177/1352458517694432 PMid:28273775 PMCid:PMC5476197 |
||||
| 2. Chen AY, Chonghasawat AO, Leadholm KL. Multiple sclerosis: frequency, cost, and economic burden in the United States. J Clin Neurosci 2017; 45: 180-6. https://doi.org/10.1016/j.jocn.2017.06.005 PMid:28676312 |
||||
| 3. Filippi M, Bar-Or A, Piehl F, Preziosa P, Solari A, Vukusic S, et al. Multiple sclerosis. Nat Rev Dis Primers 2018; 4: 43. https://doi.org/10.1038/s41572-018-0050-3 https://doi.org/10.1038/s41572-018-0041-4 PMid:30410033 |
||||
| 4. Elíasdóttir OJ, Olafsson E, Kjartansson O. Multiple Sclerosis - yfirlit um einkenni, greiningu og meðferð. Læknablaðið 2009; 95: 583-9. | ||||
| 5. Koch- Henriksen N. Sorensen PS. The changing demographic pattern of multiple sclerosis epidemiology. Lancet Neurol 2010; 9: 520-32. |
||||
| 6. Elíasdóttir Ó, Kjartansson Ó, Olafsson E. Prevalence of Multiple Sclerosis in Iceland. Neuroepidemiology 2018; 51: 50-6. https://doi.org/10.1159/000489472 PMid:29940573 |
||||
| 7. Eliasdottir OJ, Olafsson E, Kjartansson O. Incidence of multiple sclerosis in Iceland, 2002-2007: a population-based study. Mult Scler 2011; 17: 909-13. https://doi.org/10.1177/1352458511402112 PMid:21511690 |
||||
| 8. Yeshokumar AK, Narula S, Banwell B. Pediatric multiple sclerosis. Curr Opin Neurol 2017; 30: 216-21. https://doi.org/10.1097/WCO.0000000000000452 PMid:28323645 |
||||
| 9. Olsson T, Barcellos LF, Alfredsson L. Interactions between genetic, lifestyle and environmental risk factors for multiple sclerosis. Nat Rev Neurol 2017; 13: 25-36. https://doi.org/10.1038/nrneurol.2016.187 PMid:27934854 |
||||
| 10. Baranzini SE, Oksenberg JR. The genetics of multiple sclerosis: from 0 to 200 in 50 years. Trends Genet 2017; 33: 960-70. https://doi.org/10.1016/j.tig.2017.09.004 PMid:28987266 PMCid:PMC5701819 |
||||
| 11. Harirchian MH, Fatehi F, Sarraf P, Honarvar NM, Bitarafan S. Worldwide prevalence of familial multiple sclerosis: a systematic review and metaanalysis. Mult Scler Relat Disord 2017; 20: 43-7. https://doi.org/10.1016/j.msard.2017.12.015 PMid:29291483 |
||||
| 12. Hafler DA, Compston A, Sawcer S, Lander ES, Daly MJ, De Jager PL, et al. Risk alleles for multiple sclerosis identified by a genomewide study. N Engl J Med 2007; 357: 851-62. https://doi.org/10.1056/NEJMoa073493 PMid:17660530 |
||||
| 13. Pierrot-Deseilligny C, Souberbielle JC. Vitamin D and multiple sclerosis: an update. Mult Scler Relat Disord 2017; 14: 35-45. https://doi.org/10.1016/j.msard.2017.03.014 PMid:28619429 |
||||
| 14. Haahr S, Plesner AM, Vestergaard BF, Hollsberg P. A role of late Epstein-Barr virus infection in multiple sclerosis. Acta Neurol Scand 2004; 109: 270-5. https://doi.org/10.1046/j.1600-0404.2003.00221.x PMid:15016009 |
||||
| 15. Healy BC, Ali EN, Guttmann CR, Chitnis T, Glanz BI, Buckle G, et al. Smoking and disease progression in multiple sclerosis. Arch Neurol 2009; 66: 858-64. https://doi.org/10.1001/archneurol.2009.122 PMid:19597087 PMCid:PMC2754172 |
||||
| 16. Amato MP, Derfuss T, Hemmer B, Liblau R, Montalban X, Soelberg Sørensen P, et al. Environmental modifiable risk factors for multiple sclerosis: report from the 2016 ECTRIMS focused workshop. Mult Scler 2017; 24: 590-603. https://doi.org/10.1177/1352458516686847 PMid:28671487 |
||||
| 17. Hedstrom AK, Sundqvist E, Bäärnhielm M, Nordin N, Hillert J, Kockum I, et al. Smoking and two human leukocyte antigen genes interact to increase the risk for multiple sclerosis. Brain 2011; 134: 653-64. https://doi.org/10.1093/brain/awq371 PMid:21303861 |
||||
| 18. Sundqvist E, Sundström P, Lindén M, Hedström AK, Aloisi F, Hillert J, et al. Epstein-Barr virus and multiple sclerosis: interaction with HLA. Genes Immun 2012; 13: 14-20. https://doi.org/10.1038/gene.2011.42 PMid:21776012 |
||||
| 19. Hedstrom AK, Lima Bomfim I, Barcellos L, Gianfrancesco M, Schaefer C, Kockum I, et al. Interaction between adolescent obesity and HLA risk genes in the etiology of multiple sclerosis. Neurology 2014; 82: 865-72. https://doi.org/10.1212/WNL.0000000000000203 PMid:24500647 PMCid:PMC3959752 |
||||
| 20. Lublin FD, Reingold SC. Defining the clinical course of multiple sclerosis: results of an international survey. Neurology 1996; 46: 907-11. https://doi.org/10.1212/WNL.46.4.907 PMid:8780061 |
||||
| 21. Willis MA, Fox RJ. Progressive Multiple Sclerosis. Continuum (Minneap Minn) 2016; 22: 785-98. https://doi.org/10.1212/CON.0000000000000323 PMid:27261682 |
||||
| 22. Fisniku LK, Brex PA, Altmann DR, Miszkiel KA, Benton CE, Lanyon R, et al. Disability and T2 MRI lesions: a 20-year follow- up of patients with relapse onset of multiple sclerosis. Brain 2008;131: 808-17. https://doi.org/10.1093/brain/awm329 PMid:18234696 |
||||
| 23. Wattjes MP, Rovira À, Miller D, Yousry TA, Sormani MP, de Stefano MP, et al. Evidence- based guidelines: MAGNIMS consensus guidelines on the use of MRI in multiple sclerosis - establishing disease prognosis and monitoring patients. Nat Rev Neurol 2015; 11: 597-606. https://doi.org/10.1038/nrneurol.2015.157 PMid:26369511 |
||||
| 24. Frohman EM, Racke MK, Raine CS. Multiple sclerosis--the plaque and its pathogenesis. N Engl J Med 2006; 354: 942-55. https://doi.org/10.1056/NEJMra052130 PMid:16510748 |
||||
| 25. Lycke J, Zetterberg H. The role of blood and CSF biomarkers in the evaluation of new treatments against multiple sclerosis. Expert Rev Clin Immunol 2017; 13: 1143-53. https://doi.org/10.1080/1744666X.2017.1400380 PMid:29090607 |
||||
| 26. Novakova L, Zetterberg H, Sundström P, Axelsson M, Khademi M, Gunnarsson M, et al. Monitoring disease activity in multiple sclerosis using serum neurofilament light protein. Neurology 2017; 89: 2230-7. https://doi.org/10.1212/WNL.0000000000004683 PMid:29079686 PMCid:PMC5705244 |
||||
| 27. Thompson AJ, Banwell BL, Barkhof F, Carroll WM, Coetzee T, Comi G, Correale J, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol 2018; 17: 162-73. |
||||
| 28. Brownlee WJ, Hardy TA, Fazekas F, Miller DH. Diagnosis of multiple sclerosis: progress and challenges. Lancet 2017; 389: 1336-46. |
||||
| 29. De Stefano N, Giorgio A, Tintoré M, Pia Amato M, Kappos L, Palace J, et al. Radiologically isolated syndrome or subclinical multiple sclerosis: MAGNIMS consensus recommendations. Mult Scler 2018; 24: 214-21. https://doi.org/10.1177/1352458517717808 PMid:29451440 |
||||
| 30. Lebrun C. The radiologically isolated syndrome. Rev Neurol (Paris) 2015; 171: 698-706. https://doi.org/10.1016/j.neurol.2015.05.001 PMid:26410363 |
||||
| 31. Goodman AD, Brown TR, Krupp LB, Schapiro RT, Schwid SR, Cohen R, et al. Sustained-release oral fampridine in multiple sclerosis: a randomised, doubleblind, controlled trial. Lancet 2009; 373: 732-8. |
||||
| 32. Johnson KP, Brooks BR, Cohen JA, Ford CC, Goldstein J, Lisak RP, et al. Copolymer 1 reduces relapse rate and improves disability in relapsing- remitting multiple sclerosis: results of a phase III multicenter, doubleblind placebo- controlled trial. Neurology 1995; 45: 1268-76. https://doi.org/10.1212/WNL.45.7.1268 PMid:7617181 |
||||
| 33. Ebers GC, PRISMS Study Group. Randomised double- blind placebo- controlled study of interferon β-1a in relapsing/remitting multiple sclerosis. Lancet 1998; 352: 1498-504. |
||||
| 34. Gold R, Kappos L, Arnold DL, Bar-Or A, Giovannoni G, Selmaj K, et al. Placebo-controlled phase 3 study of oral BG-12 for relapsing multiple sclerosis. N Engl J Med 2012; 367: 1098-107. https://doi.org/10.1056/NEJMoa1114287 PMid:22992073 |
||||
| 35. O'Connor P, Wolinsky JS, Confavreux C, Comi G, Kappos L, Olsson TP, et al. Randomized trial of oral teriflunomide for relapsing multiple sclerosis. N Engl J Med 2011; 365: 1293-303. https://doi.org/10.1056/NEJMoa1014656 PMid:21991951 |
||||
| 36. Montalban X, Gold R, Thompson AJ, Otero-Romero S, Amato MP, Chandraratna D, et al. ECTRIMS/EAN guideline on the pharmacological treatment of people with multiple sclerosis. Mult Scler 2018; 24: 96-120. https://doi.org/10.1177/1352458517751049 PMid:29353550 |
||||
| 37. Rae- Grant A, Day GS, Marrie RA, Rabinstein A, Cree BAC, Gronseth GS, et al. Practice guideline recommendations summary: Disease- modifying therapies for adults with multiple sclerosis. Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology. Neurology 2018; 90: 777-88. https://doi.org/10.1212/WNL.0000000000005345 https://doi.org/10.1212/WNL.0000000000005347 PMid:29686116 |
||||
| 38. Polman CH, O'Connor PW, Havrdova E, Hutchinson M, Kappos L, Miller DH, et al. A randomized, placebo- controlled trial of natalizumab for relapsing multiple sclerosis. N Engl J Med 2006; 354: 899-910. https://doi.org/10.1056/NEJMoa044397 PMid:16510744 |
||||
| 39. Kappos L, Radue EW, O'Connor P, Polman C, Hohlfeld R, Calabresi P, et al. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis. N Engl J Med 2010; 362: 387-401. https://doi.org/10.1056/NEJMoa0909494 PMid:20089952 |
||||
| 40. Granqvist M, Boremalm M, Poorghobad A, Svenningsson A, Salzer J, Frisell T, et al. Comparative effectiveness of rituximab and other initial treatment choices for multiple sclerosis. JAMA Neurol 2018; 75: 320-7. https://doi.org/10.1001/jamaneurol.2017.4011 PMid:29309484 PMCid:PMC5885857 |
||||
| 41. Hauser SL, Bar-Or A, Comi G, Giovannoni G, Hartung HP, Hemmer B, et al. Ocrelizumab versus interferon beta- 1a in relapsing multiple sclerosis. N Engl J Med 2017; 376: 221-34. https://doi.org/10.1056/NEJMoa1601277 PMid:28002679 |
||||
| 42. Montalban X, Hauser SL, Kappos L, Arnold DL, Bar-Or A, Comi G, et al. Ocrelizumab versus placebo in primary progressive multiple sclerosis. N Engl J Med 2017; 376: 209-20. https://doi.org/10.1056/NEJMoa1606468 PMid:28002688 |
||||
| 43. Hawker K, O'Connor P, Freedman MS, Calabresi PA, Antel J, Simon J, et al. Rituximab in patients with primary progressive multiple sclerosis: results of a randomized double-blind placebo-controlled multicenter trial. Ann Neurol 2009; 66: 460-71. https://doi.org/10.1002/ana.21867 PMid:19847908 |
||||
| 44. Coles AJ, Twyman CL, Arnold DL, Cohen JA, Confavreux C, Fox EJ, et al. Alemtuzumab for patients with relapsing multiple sclerosis after disease-modifying therapy: a randomised controlled phase 3 trial. Lancet 2012; 380: 1829-39. |
||||
| 45. Giovannoni G, Comi G, Cook S, Rammohan K, Rieckmann P, Soelberg Sørensen P, et al. A placebo-controlled trial of oral cladribine for relapsing multiple sclerosis. N Engl J Med 2010; 362: 416-26. https://doi.org/10.1056/NEJMoa0902533 PMid:20089960 |
||||
| 46. Kappos L, Wiendl H, Selmaj K, Arnold DL, Havrdova E, Boyko A, et al. Daclizumab HYP versus interferon beta- 1a in relapsing multiple sclerosis. N Engl J Med 2015; 373: 1418-28. https://doi.org/10.1056/NEJMoa1501481 PMid:26444729 |
||||
| 47. Burman J, Iacobaeus E, Svenningsson A, Lycke J, Gunnarsson M, Nilsson P, et al. Autologous haematopoietic stem cell transplantation for aggressive multiple sclerosis: the Swedish experience. J Neurol Neurosurg Psychiatry 2014; 85: 1116-21. https://doi.org/10.1136/jnnp-2013-307207 PMid:24554104 |
||||
| 48. Amato MP, Derfuss T, Hemmer B, Liblau R, Montalban X, Soelberg Sørensen P, et al. Environmental modifiable risk factors for multiple sclerosis: report from the 2016 ECTRIMS focused workshop. Mult Scler 2017; 24: 590-603. https://doi.org/10.1177/1352458516686847 PMid:28671487 |
||||
| 49. Sintzel MB, Rametta M, Reder AT. Vitamin D and multiple sclerosis: a comprehensive review. Neurol Ther 2018; 7: 59-85. https://doi.org/10.1007/s40120-017-0086-4 PMid:29243029 PMCid:PMC5990512 |
||||
| 50. Piehl F. A changing treatment landscape for multiple sclerosis: challenges and opportunities. J Intern Med 2014; 275: 364-81. https://doi.org/10.1111/joim.12204 PMid:24444084 |
||||