03. tbl. 111. árg. 2025
Fræðigrein
Rannsókn. Aðgerðir vegna taugainnkirtlaæxla í efri hluta meltingarvegar á Landspítala
Ágrip
Inngangur
Taugainnkirtlaæxli eru sjaldgæf æxli upprunnin frá taugainnkirtlavef. Þau geta átt uppruna sinn frá ýmsum líffærum, en eru algengust í lungum og meltingarvegi. Æxlin eru ólík eftir því frá hvaða líffæri þau eiga upptök sín og hversu vel þroskuð þau eru. Taugainnkirtlaæxli geta framleitt hormón eða verið óvirk.
Efniviður og aðferðir
Gerð var afturskyggn rannsókn þar sem skoðaðir voru sjúklingar sem fóru í aðgerð vegna taugainnkirtlaæxlis í efri hluta meltingarvegar á árunum 2010-2020. Farið var yfir uppruna æxla, aðgerðir og aðgerðartengda þætti svo sem fylgikvilla og legutíma. Bæði 30 daga og 5 ára lifun var skoðuð. Með voru sjúklingar sem gengust undir aðgerð á frumæxli, en einnig þeir sem gengust undir aðgerð vegna meinvarpa. Fengnar voru upplýsingar úr sjúkraskrárkerfum Landspítala. Notast var við lýsandi tölfræði ásamt lifunartölfræði, þar sem notast var við tölfuforritin Excel og GraphPad Prism. Viðeigandi leyfi voru fengin áður en rannsókn var hafin.
Niðurstöður
Alls gengust 31 sjúklingur undir aðgerð vegna taugainnkirtlaæxlis í efri hluta meltingarvegar á þessum árum þar sem var gert brottnám æxlis hjá 29 sjúklingum sem mynduðu rannsóknarþýði. 34% sjúklinga hlaut fylgikvilla sem krafðist inngrips eða gjörgæslulegu. Enginn lést innan 30 daga frá aðgerð. Heildarlifun sjúklinga var 88% eftir fimm ár og sjúkdóms sértæk lifun 95%.
Ályktun
Fáir sjúklingar fara í aðgerð vegna taugainnkirtlaæxla í efri hluta meltingarvegar. Aðgerðir voru árangursríkar og fimm ára lifun var góð sem er í samræmi við erlendar niðurstöður.
Inngangur
Taugainnkirtlaæxli (neuroendocrine tumors, NETs) eru upprunnin frá taugainnkirtlavef (neuroendocrine system). Nýgengi taugainnkirtlaæxla í meltingarfærum á Íslandi er 3,65 á hverja 100.000, með heildar fimm ára lifun (overall survival) 75% fyrir staðbundinn sjúkdóm.1 Nýgengi er sambærileg og hefur verið lýst í Bandaríkjunum.2 Æxlin geta átt upptök sín í flestum líffærum líkamans, en eru ólík og hegða sér á mismunandi hátt eftir því í hvaða líffæri þau eiga upptök sín.3 Taugainnkirtlaæxli eru oftast stakstæð (sporadic) en það kemur fyrir að þau fylgi erfðatengdum heilkennum eins og MEN1 (Multiple endocrine neoplasia type 1), von Hippel-Lindau og neurofibromatosis.4
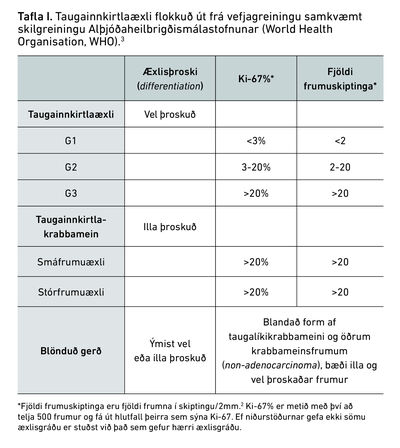
Vefjafræðilega eru æxlin flokkuð eftir því hversu þroskuð þau eru. Frumur taugainnkirtlaæxla framleiða prótein (t.d. krómógranín A, krómógranín B og synaptófysín). Þessi prótein eru notuð til greiningar og mats á þroska æxlis. Vel þroskuð (well differentiated) æxli eru skilgreind sem taugainnikirtlaæxli en illa þroskuð (poorly differentiated) sem taugainnkirtlakrabbamein (neuroendocrine carcinoma). Taugainnkirtlakrabbamein skiptast í smáfrumu- (small cell neuroendocrine carcinoma) og stórfrumuæxli (large cell neuroendocrine carcinoma),3 sjá töflu I. Þessi flokkun á við óháð því hvaðan æxlið er upprunnið.5 Taugainnkirtlaæxli eru mun algengari en taugainnkirtlakrabbamein.6 Æxlisgráða er skilgreind sem G1-G3 (grade, G) eftir ónæmisfræðilegri litun. Hún er metin út frá fjölda frumuskiptinga (mitotic rate) eða Ki-67% (antigen Kiel 67, Ki-67) (Tafla I).
(Tafla II)
Taugainnkirtlaæxli með gráðu G1 og G2 eru algengust, en G3 æxli eru sjaldgæf og lítið rannsökuð.5 Meirihluti taugainnkirtlaæxla eru einkennalaus og uppgötvast oft fyrir tilviljun.7 Líkt og á við um önnur æxli geta einkenni komið fram seint í sjúkdómsferlinu vegna massaáhrifa eða fjarmeinvarpa.4 Taugainnkirtlaæxli eru algengust í lungum og af líffærum efri hluta meltingarvegar er algengast að taugainnkirtlaæxli greinist í brisi.4 Um 90% taugainnkirtlaæxla í brisi (pNET) eru ekki hormónavirk. Almennt er talið að horfur séu verri ef æxlin eru ekki hormónavirk, en það er líklega vegna þess að þau valda litlum eða engum einkennum og greinast því oft seint.
Af heilkennum sem fylgja hormónavirkum æxlum er krabbalíkiheilkenni (carcinoid syndrome) algengast og kemur fram ef ofseyting serótóníns á sér stað. Algengast er að heilkennið komi fram hjá sjúklingum með lifrarmeinvörp, en dæmi eru um krabbalíkiheilkenni án lifrarmeinvarpa.8 Einkenni þess geta verið margþætt sem gerir greiningu erfiða, en algengust eru niðurgangur, roði á húð og hitaköst (flushing), astma-lík einkenni frá lungum og dökkir blettir á húð (hyperpigmentation).8
Hægt er að nota prótein sem æxlin framleiða, eins og krómógranín A, sem æxlisvísa (tumor markers) til að fylgja eftir svörun við meðerð. Það er þó ekki áreiðanlegt eitt og sér til greiningar. Hormónamælingar þarf ekki að gera hjá öllum sjúklingum, heldur eingöngu þar sem er grunur um hormónavirkt æxli.8 Myndrannsóknir eru mikilvægar til að fá sem nákvæmasta stigun við greiningu og til að meta skurðtæki.8
Litlum æxlum í brisi, undir tveimur sentimetrum, er talið óhætt að fylgja eftir með eftirliti. Æxli yfir þremur sentimetrum er ráðlagt að fjarlægja ásamt aðliggjandi eitlum. Ef sjúkdómur er talinn staðbundinn og ekki greind eitlameinvörp eða litlar líkur taldar á eitlameinvörpum er ráðlagt að íhuga vefjasparandi aðgerð (parenchyma-sparing) og taka eingöngu æxlið og sem minnst af aðliggjandi vef. Þetta á við æxli milli tveggja og þriggja sentimetra að stærð og ef ekki eru merki um víkkun á brisgangi.8 Ef æxli í brisi eru skurðtæk er fimm ára lifun 70-80%.8 Svipuð nálgun er við æxli í maga og skeifugörn (GiNET). Algengasta tegund þessara æxla (75-80% af GiNET) eru æxli sem koma í kjölfar magabólgu með visnun (chronic atropic gastritis). Þar er mælt með eftirfylgd á æxlum upp að einum sentímetra. Stærri æxli er mælt með að fjarlægja, hvort sem það er gert í speglun (endoscopic resection) eða með skurðaðgerð.9
Mjög sjaldgæft er að taugainnkirtlaæxli eigi upptök sín í lifur. Ef taugainnkirtlaæxli finnst í lifur er yfirleitt um meinvörp að ræða. Hægt er að grípa til ýmissa meðferða hjá sjúklingum með lifrarmeinvörp, svo sem skurðaðgerð. Einnig er hægt að beita krabbameinslyfjameðferð, lyfjameðferð með sómatóstatín eða interferón, viðtakamiðaðri geislameðferð (Peptide receptor radionuclide therapy PRRT) eða segameðferð með æðaþræðingu (embolization).10 Skurðaðgerð vegna meinvarpa í lifur er gerð annað hvort til að minnka æxlisbyrði og einkenni eða sem læknandi meðferð í völdum tilfellum. Brottnám meinvarpa taugainnkirtlaæxla í lifur er almennt talin kjörmeðferð en ekki hafa verið gerðar rannsóknir þar sem mismunandi meðferðir eru bornar saman. Ef hægt er að fjarlægja allan æxlisvöxt úr lifur er 5 ára lifun nálægt 100%.10
Nýgengi á taugainnkirtlaæxlum hefur aukist síðustu áratugi. Líklega má rekja það til aukinnar notkunar myndrannsókna og speglunarrannsókna, þar sem æxlin greinast fyrir tilviljun. Horfur hafa þó ekki breyst.6
Tilgangur rannsóknarinnar var að skoða árangur skurðaðgerða á taugainnkirtlaæxlum í efri hluta meltingarvegar á Íslandi, sem og horfur sjúklingahópsins sem gengst undir aðgerð.
Efniviður og aðferðir
Gerð var afturskyggn gagnarannsókn sem náði til áranna 2010-2020. Rannsóknarþýði mynduðu þeir sjúklingar, 18 ára og eldri, sem höfðu gengist undir brottnám taugainnkirtlaæxlis í efri hluta meltingarvegar. Hún tekur til æxla í maga, skeifugörn, brisi og lifur.
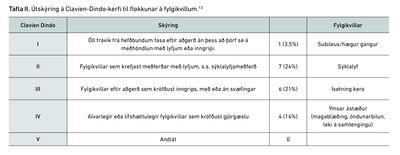
Upplýsingar um sjúklinga voru fengnar úr sjúkraskrá Landspítala. Skoðaðar voru vefjagreiningarniðurstöður og þeir sjúklingar sem höfðu staðfest taugainnkirtlaæxli í vefjagreiningu mynduðu rannsóknarþýði. Skoðaður var aldur, kyn, dagsetning aðgerðar, tímalengd aðgerðar og aðgerðartegund. Stigun eftir aðgerð var framkvæmd samkvæmt TNM stigunarkerfi, fjölda frumuskiptinga og æxlisgráðu sem metin var út frá Ki-67% og frumuskiptingum í smásjárskoðun eftir aðgerð. Skráð var hvort einkenni leiddu til greiningar og um hvers konar einkenni var að ræða, hvort sjúklingur var með hormónavirkt æxli og skráð hverjir voru greindir með MEN1 heilkenni. Einnig var skoðaður legutími, fylgikvillar, meðferð fylgikvilla, skurðdauði, eða dauði á rannsóknartímabilinu, og hvort sjúklingar voru ræddir á samráðsfundi. Fylgikvillar voru flokkaðir eftir Clavien-Dindo flokkunarkerfi en það flokkar sjúklinga í fimm flokka út frá alvarleika fylgikvilla og meðhöndlun (tafla I). Sérstaklega verður fjallað um sjúklinga sem höfðu alvarlegri fylgikvilla eða fylgikvilla sem kröfðust inngrips (Clavien-Dindo ≥III).13 Við úrvinnslu gagna og tölfræði var notuð lýsandi tölfræði ásamt lifunartölfræði. Stuðst var við forritin Excel og GraphPad Prism. Viðeigandi leyfi hjá Siðanefnd heilbrigðisrannsókna á Landspítala og Vísindarannsóknarnefnd heilbrigðisrannsókna voru fengin áður en rannsókn hófs.
Niðurstöður
Alls gengust 31 sjúklingur undir skurðaðgerð vegna taugainnkirtlaæxlis í efri hluta meltingarvegar á árunum 2010-2020. Tveir af þeim voru með óskurðtækan sjúkdóm og ekki gert brottnám á æxli. Þessir tveir sjúklingar voru því ekki hafðir með í rannsókninni og rannsóknarþýði því 29 sjúklingar. 27 sjúklingar (93%) gengust undir aðgerð vegna frumæxlis. Þar af var æxlið staðsett í brisi hjá 22 sjúklingum (81%), í maga hjá fjórum (15%) og hjá einum (4%) í skeifugörn. Tveir sjúklingar gengust undir brottnám á meinvörpum taugainnkirtlaæxlis í lifur. Þeir höfðu áður gengist undir aðgerð þar sem frumæxli var fjarlægt, annað frá dausgörn og hitt frá lunga. Miðgildi aldurs var 58 ár (bil 24-77). Alls 15 (52%) karlar og 14 konur (48%).
Flestir sjúklinganna voru einkennalausir (n=12, 44%) eða höfðu almenn, óljós einkenni svo sem slappleika, þyngdartap og meltingartruflanir (n=12, 44%). Fimm (12%) voru með hormónavirkt æxli og einkenni tengd því. Fjórir sjúklingar greindust með eða voru með þekkt MEN1-heilkenni (multiple endocrine neoplasia type 1) og voru þeir allir nema einn með hormónavirk æxli.
Hormónamælingar voru gerðar hjá þeim sjúklingum sem voru með hormónavirk æxli, en almennt fundust ekki skráðar hormónamælingar fyrir aðra sjúklinga. Á umræddu tímabili heyrði til undantekninga að samráðsfundarnóta fyndist fyrir sjúklinga í þýðinu.
Aðgerðir
Af þeim 27 sjúklingum sem gengust undir aðgerð á frumæxli (Mynd 1) gengust fimm sjúklingar undir hlutabrottám á brisi með brottnámi á brishöfði (pancreaticoduodenectomy/Whipple), 14 fóru í aðgerð á brisskotti (distal pancreatectomy). Tveir fóru í staðbundið brottnám (enucleation) á æxli í brisi og einn í hlutabrottnám á miðhluta briss (central pancreatectomy). Fjórir sjúklingar gengust undir hlutabrottnám á maga (partial gastrectomy) og einn hlutabrottnám á skeifugörn (duodenectomy). Aðgerðartími var mislangur eftir tegund aðgerða, en var á bilinu 90-460 mínútur (miðgildi: 204 mínútur)
Fylgikvillar og legutími
Sjúklingar með fylgikvilla sem falla í flokk III til IV í Clavien-Dindo-kerfinu voru alls tíu (34%) Enginn lést innan 30 daga (Clavien Dindo V). Einn þurfti enduraðgerð innan 30 daga. Legutími var að meðaltali 58 dagar (bil: 2-232) og miðgildi 8 dagar.
Niðurstöður meinafræðirannsókna og lifun
Flestir sjúklinganna, eða 59%, voru með TNM-stigun II -eftir aðgerð. Skurðbrúnir voru fríar hjá 92,6% sjúklinga. 18,5% höfðu eitlameinvörp. Öll æxlin voru lággráðu, það er af gráðu G1 (74%) eða G2 (26%). Mítósuhraða og Ki-67% vantaði hjá einum sjúklingi og æxlisgráða því ekki metin. Fylgikvillar voru algengari hjá sjúklingum með æxli í brisi en þeim sem höfðu æxli í maga eða skeifugörn (tafla III).
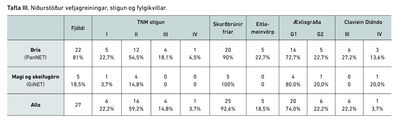
Heildarlifun sjúklinga var 93% eftir þrjú ár og 88% eftir fimm ár. Fyrir sjúklinga með æxli frumkomið í brisi var fimm ára lifun 85% og 100% fyrir sjúklinga með frumkomið æxli í maga eða skeifugörn (mynd 2). Aðeins einn sjúklingur lést vegna taugainnkirtlasjúkdóms og var sjúkdómssértæk lifun (disease specific survival) 95%.
Sjúklingum var almennt fylgt eftir af skurðlæknum nema eftir aðgerðir á lifur eða sjúklingar fengu endurkomu. Þá var eftirfylgd í höndum krabbameinslækna. Við MEN1-heilkenni eða önnur innkirtlavandamál var eftirfylgd í höndum lyflækna. Í heildina greindust fimm sjúklingar með meinvörp eða endurkomu sjúkdóms innan fimm ára (mynd 4). Fjórir af þeim voru með frumæxli í brisi og greindust síðar með meinvörp í lifur. Einn sjúklingur með gastrínæxli (gastrinoma) greindist með meinvarp í eitli sem var fjarlægt. Þeir sjúklingar sem fengu meinvörp í lifur fengu allir sandóstatín-meðferð í læknandi tilgangi. Fimm ára sjúkdómslaus lifun (disease free survival) var 85% fyrir þá sem voru með frumæxli í efri hluta meltingarvegar.
Umræður
Rannsókn eins og þessi þar sem skoðaðar eru útkomur eftir aðgerð vegna taugainnkirtlaæxlis í efri hluta meltingarvegar hefur ekki verið framkvæmd áður á Íslandi. Hér er því um ákveðið yfirlit að ræða yfir sérhæfðar aðgerðir við taugainnkirtlaæxli á 10 ára tímabili. Almennt er talað um taugainnkirtlaæxli sem góðkynja sjúkdóm og í flestum tilfellum hagar hann sér á þann hátt. Mikilvægt er þó að hafa í huga að hann getur hagað sér líkt og illkynja krabbamein.11 Mikilvægt er því að ræða umræddan sjúklingahóp á samráðsfundi.12 Á Landspítala hafa undanfarin ár verið starfræktir samráðsfundir fyrir góðkynja breytingar í brisi sem er að mestu leyti ætlaður sjúklingum með blöðruæxli eða belgmein í brisi (pancreatic cyst). Þar hafa þessir sjúklingar verið ræddir, sem og á samráðsfundi um illkynja krabbamein. Ekki liggja fyrir ákveðnir verkferlar á Íslandi fyrir hópinn í heild sinni og mikilvægt að hópur sérfræðinga mismunandi sérgreina myndi hóp sem fer fyrir þessum sjúklingum, bæði í efri- og neðri hluta meltingarvegar. Stuðst hefur verið við alþjóðlegar leiðbeiningar á samráðsfundum en ekki hafa allir sjúklingar verið ræddir þar.11,9 Þetta er mikilvægt, einnig þegar tekið er tillit til þess að eins og í þessari rannsókn fer hluti sjúklinga í aðgerð vegna meinvarpa sem einkennameðferð eða læknandi meðferð í ákveðnum hópi. Fáir sjúklingar gengust undir aðgerð vegna frumæxlis í efri hluta meltingarvegar á tímabilinu.11,9 Einnig gangast fáir sjúklingar undir aðgerð á lifur vegna meinvarpa taugainnkirtlaæxla og vekur það upp spurningar um hvort allir sjúklingar séu ræddir á samráðsfundi. Gæðaskráning greindra tilfella taugainnkirtlaæxla, sem skráð væri í rauntíma, gæti gefið nákvæmari mynd af árangri meðferðar hérlendis. Kostur rannsóknarinnar er að í þýðinu eru allir sjúklingar á Íslandi sem gengust undir þessar aðgerðir á þessum árum, þar sem aðgerðir við taugainnkirtlaæxli í efri hluta meltingarvegar eru einungis framkvæmdar á Landspítala. Á sama tíma er ókostur að rannsóknin er afturskyggn og úrtak sjúklinga er lítið, eins og kemur vel í ljós þegar reiknuð er lifun í lok tímabils fyrir þrjú eða fimm ár. Fáar aðgerðir eru gerðar árlega vegna taugainnkirtlaæxlis í efri hluta meltingarvegar, en algengastar eru aðgerðir á brisi. Um þriðjungur sjúklinga fékk alvarlega fylgikvilla en enginn sjúklingur lést eftir aðgerð. Lifun var sambærileg við niðurstöður erlendra rannsókna.11,9 Endurkomutíðni er lág en ljóst er að skerpa þarf á verkferlum á Íslandi fyrir umræddan sjúklingahóp.
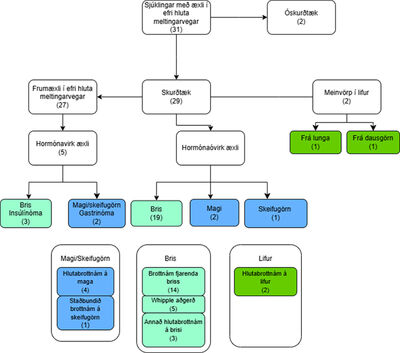
Mynd 1. Yfirlit yfir staðsetningu æxla og tegund aðgerða.
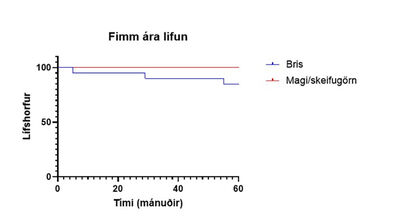
Mynd 2. Kaplan-Meier-rit yfir fimm ára lifun sjúklinga með frumkomið æxli í efri hluta meltingarvegar.
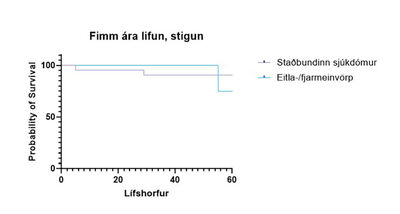
Mynd 3. Kaplan-Meier-rit yfir fimm ára lifun allra sjúklinga, flokkað eftir stigun.
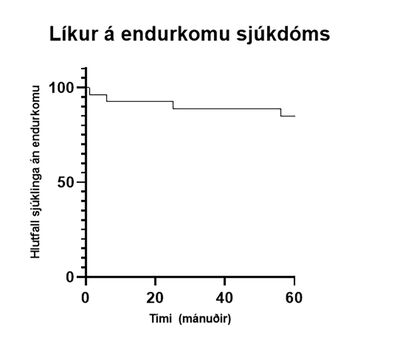
Mynd 4. Hlutfall sjúklinga með frumæxli í efri hluta meltingarvegar án endurkomu sjúkdóms.
Heimildir
| 1.
Gudmundsdottir H, Möller PH, Jonasson JG, et al. Gastroenteropancreatic
neuroendocrine tumors in Iceland: a population-based study. Scand J
Gastroenterol. 2019;54(1):69-75. https://doi.org/10.1080/00365521.2018.1553061 PMid:30638086 | ||||
| | ||||
| 2.
Das S, Dasari A. Epidemiology, Incidence, and Prevalence of
Neuroendocrine Neoplasms: Are There Global Differences? Curr Oncol Rep.
2021;23(4) 43. https://doi.org/10.1007/s11912-021-01029-7 PMid:33719003 PMCid:PMC8118193 | ||||
| | ||||
| 3.
Rindi G, Klimstra DS, Abedi-Ardekani B, et al. A common classification
framework for neuroendocrine neoplasms: an International Agency for
Research on Cancer (IARC) and World Health Organization (WHO) expert
consensus proposal. Modern Pathology. 2018;31(12):1770-1786. https://doi.org/10.1038/s41379-018-0110-y PMid:30140036 PMCid:PMC6265262 | ||||
| | ||||
| 4. Modlin IM, Oberg K, Chung DC, et al. Gastroenteropancreatic neuroendocrine tumours. Lancet Oncol. 2008;9(1):61-72. https://doi.org/10.1016/S1470-2045(07)70410-2 PMid:18177818 | ||||
| | ||||
| 5.
Nagtegaal ID, Odze RD, Klimstra D, et al. The 2019 WHO classification
of tumours of the digestive system. Histopathology. 2020;76(2):182-188. https://doi.org/10.1111/his.13975 PMid:31433515 PMCid:PMC7003895 | ||||
| | ||||
| 6. Gonzalez RS. Diagnosis and Management of Gastrointestinal Neuroendocrine Neoplasms. Surg Pathol Clin. 2020;13(3):377-397. https://doi.org/10.1016/j.path.2020.04.002 PMid:32773190 | ||||
| | ||||
| 7.
Herrera MF, Åkerström G, Angelos P, et al. Aace/Ace Disease State
Clinical Review: Pancreatic Neuroendocrine Incidentalomas. Endocrine
Practice. 2015;21(5):546-553 https://doi.org/10.4158/EP14465.DSC PMid:25962093 PMCid:PMC4975928 | ||||
| | ||||
| 8.
Ito T, Lee L, Jensen RT. Carcinoid-syndrome: recent advances, current
status and controversies. Curr Opin Endocrinol Diabetes Obes 2018
Feb;25(1):22-35. https://doi.org/10.1097/MED.0000000000000376 PMid:29120923 PMCid:PMC5747542 | ||||
| | ||||
| 9.
Panzuto F, Ramage J, Pritchard DM, et al. European Neuroendocrine Tumor
Society (ENETS) 2023 guidance paper for gastroduodenal neuroendocrine
tumours (NETs) G1-G3. J Neuroendocrinol. 2023;35(8):e13306. https://doi.org/10.1111/jne.13306 PMid:37401795 | ||||
| | ||||
| 10. Saeed A, Buell JF, Kandil E. Surgical treatment of liver metastases in patients with neuroendocrine tumors. Ann Transl Med. 2013;1(1):6. | ||||
| | ||||
| 11.
Kos-Kudła B, Castaño JP, Denecke T, et al. European Neuroendocrine
Tumour Society (ENETS) 2023 guidance paper for nonfunctioning pancreatic
neuroendocrine tumours. J Neuroendocrinol. 2023;35(12):e13343. https://doi.org/10.1111/jne.13343 PMid:37877341 | ||||
| | ||||
| 12.
Rogers MJ, Matheson L, Garrard B, et al. Comparison of outcomes for
cancer patients discussed and not discussed at a multidisciplinary
meeting. In: Public Health. Vol 149. Elsevier B.V.; 2017:74-80. https://doi.org/10.1016/j.puhe.2017.04.022 PMid:28575751 | ||||
