01. tbl. 94. árg. 2008
Fræðigrein
Trefjavefslungnabólga - yfirlitsgrein og helstu niðurstöður íslenskra rannsókna
Organising Pneumonia - a review and results from Icelandic studies
Ágrip
Trefjavefslungnabólga er sjúkdómur í lungum, skilgreindur með klínískum einkennum, myndgreiningarrannsóknum og vefjameinafræðilegum breytingum í sameiningu. Klínísk einkenni eru hósti, mæði, hækkaður líkamshiti og almennur slappleiki. Algengt er að einkennin hafi verið til staðar í nokkrar vikur áður en greining fæst. Myndgreiningarrannsóknir geta sýnt fjölbreytt mynstur, til dæmis dreifðar millivefsíferðir, afmarkaðar lungnablöðruíferðir eða staka hnúða. Yfirleitt svarar sjúkdómurinn vel meðferð með barksterum en tekur sig upp hjá um fimmtungi sjúklinga.
Inngangur
Trefjavefslungnabólga (organising pneumonia, OP) er sjúkdómur í lungum, skilgreindur með klínískum einkennum, myndrannsóknum og vefjameinafræðilegum breytingum í sameiningu (1). Enda þótt trefjavefslungnabólga hafi lengi verið þekkt sem vefjagreining var það fyrst á níunda áratug liðinnar aldar sem hún öðlaðist sess sem klínískt heilkenni (2-3).
Trefjavefslungnabólga hefur einnig verið kölluð berkjungastífla með trefjavefslungnabólgu (bronchiolitis obliterans organising pneumonia, BOOP) en nýlega hefur verið mælt með því að nota frekar orðið trefjavefslungnabólga (organising pneumonia) og greina í tvo flokka, trefjavefs-?lungnabólgu óþekktra (TÓO) og þekktra orsaka (TÞO) (4) (cryptogenic organising pneumonia, COP, secondary organising pneumonia, SOP). BOOP nafngiftin var óheppileg, ekki síst vegna þess að annar óskyldur lungnasjúkdómur heitir Bronchiolitis obliterans (BO). Það er alvarlegur loftvegateppusjúkdómur sem kemur helst í tengslum við ígræðslu lungna- og beinmergs en sést einnig hjá sjúklingum með iktsýki. BO hefur afar slæmar horfur, öfugt við trefjavefs-lungnabólgu. Hið eina sameiginlega er að báðir sjúkdómar leggjast á berkjunga. Undanfarin ár hefur trefjavefslungnabólga verið rannsökuð hér á landi. Í greininni er yfirlit yfir hana og sagt frá helstu niðurstöðum íslenskra rannsókna á sjúkdómnum (5-7).
Meingerð
Margt er á huldu um orsakir og meingerð trefjavefslungnabólgu en töluvert hefur miðað í átt að aukinni þekkingu á síðustu árum. Það sem talið er setja ferilinn í gang er áverki á lungnablöðrufrumum. Skaðinn leiðir til þess að lungnablöðrufrumur losna frá grunnhimnunni og lungnablöðruþekjan flagnar. Þó að holur myndist í grunnhimnunni er það veigamikið atriði að himnan eyðileggst ekki, auk þess sem æðaþelsfrumurnar í háræðum undir grunnhimnunni eru aðeins lítið skaddaðar. Storkuprótein leka gegnum holur í grunnhimnu og fíbrín myndast. Myndun fíbríns orsakast af misvægi milli storku og fíbrínleysandi ferla sem endar með storknun (8). Aukið magn af trombín virkjandi fíbrínleysandi hemjara (thrombin activable fibrinolysis inhibitor) og prótein C hemjara, sem hvort tveggja hemla fibrínólýsu, hafa fundist í berkjuskoli frá sjúklingum með trefjavefs-lungnabólgu (9). Það er að koma betur í ljós að storkuþættirnir virðast eiga allstóran þátt í meingerðinni. Þeir búa til bráðabirgða-uppistöðuefni fyrir flutning frumna og stuðla að fíbrínmyndun (10). Í dýralíkönum þar sem heparín eða úrókínasi er gefinn myndast ekki trefjavefslungnabólga, sem styður þá hugmynd enn frekar (11, 12).
Næsta skref einkennist af myndun sprota úr græðsluvef og bólguvilsu (fibro-inflammatory buds). Fíbrínið er brotið niður og nú fara trefjakímfrumur (fibroblastar) úr millivefnum inn í lungnablöðrurnar í gegnum götin á grunnhimnunni. Þar setjast þær að í fíbrínleifum og fjölga sér. Í kjölfarið fara trefjakímfrumurnar í gegnum frekari breytingar, sérstaklega myndun umfrymisþráða og verða sumar trefjakímfrumurnar að frumum sem hafa einnig eiginleika sléttra vöðvafrumna (myofibroblasta) og retíkúlín grind byggist upp í utanfrumuefninu (12). Fjölgun lungnablöðrufrumna á sér stað og leiðir af sér endurnýjun þekju í lungnablöðruþekjunni og því viðhelst rétt uppbygging lungnablöðrunnar sem er afar mikilvægt (12). Auk þessa eru merki æðanýmyndunar sem minnir á græðsluvef (granulation tissue) eftir sáramyndun til staðar. Er það annað merki þess að hér sé um afturkræfa bandvefs- og bólguvilsu-meinsemd (fibro-inflammatory lesion) að ræða (12, 13). Öfugt við lungnatrefjun af óþekktri orsök (usual interstitial pneumonitis) þar sem kollagen I er ráðandi efni, er sambland af kollagen III, fíbrónektíni og próteóglíkönum algengara að finna í trefjavefslungnabólgu. Auð svæði í utanfrumuefninu gera millifrumuefnið að lausgerðum bandvef. Fullyrða má að slíkur bandvefur sé viðkvæmari fyrir niðurbroti og eyðingu, sem gerir horfur mun betri í trefjavefslungnabólgu en ella (12, 14-15).
Lokastigið í viðgerðarferlinu einkennist af myndun þroskaðra bandvefssprota. Á þessu stigi hafa bólgufrumurnar nánast alveg horfið í flestum sprotunum og ekki er lengur neitt fíbrín í lungnablöðruholinu. Einkennandi fyrir þetta stig eru fyrrum trefjakímfrumur sem eru nú frumur með eiginleika sléttvöðvafrumna, sem mynda sammiðja hringi með víxlandi lögum af bandvef.
Dýralíkön sem gerð hafa verið til að líkja eftir trefjavefslungnabólgu sýna að það er stærðargráða áverkans sem ræður miklu hvort úr verður trefjavefslungnabólga eða útbreiddur lungna-?blöðruskaði (diffuse alveolar damage) (12, 16). Kemur þar einnig í ljós að sterar virðast ekki aðeins ná að stöðva trefjunina heldur snúa henni við. Hvorugt gerist í útbreiddum lungnablöðruskaða (12, 17).
Meinafræði
Vefjabreytingar sem einkenna trefjavefslungna-bólgu geta einnig sést í öðrum lungnasjúkdómum (1). Til þess að geta greint trefjavefslungnabólgu þurfa vefjabreytingarnar að vera megin meinafræðilegu breytingarnar í vefjasýninu, ekki aðeins breytingar á jöðrum eða sem fylgifiskur annarra sjúkdóma eins og eósínófíl lungnabólgu, ofurnæmislungnabólgu (hypersensitivity pneumonitis), krabbameins eða annarra sjúkdóma (1). Mikilvægt er að leita vel að mögulegum orsökum eins og sýkingum, meðal annars með sérlitunum á vefjasýnum. Enginn munur var á vefjameinafræði eftir því hvort orsök var þekkt eða óþekkt í íslensku rannsókninni.
Í vefjasýni sjást í fjarlægum loftvegum sprotar af nýmynduðum græðsluvef sem spanna fíbrínseytur til lausgerðs bandvefs með einstöku trefjakímfrumum, en án kollagens, ásamt vægri langvinnri bólgufrumuíferð í millivef. Oftast eru breytingarnar í lungnablöðrum, en geta einnig verið til staðar í holi fjarlægra berkjunga og kallast það berkjungastífla (1). Þetta mynstur er ekki dæmigert fyrir ákveðinn sjúkdóm eða orsök heldur endurspeglar það ákveðna gerð af bólgusvari eftir lungnaskaða (1).

Mynd I. Meinafræði trefjavefslungnabólgu á fyrri stigum. Hér má sjá lausgerðan bandvef (gul ör) og virkjaðar lungnablöðrufrumur (græn ör) og stöku trefjakímfrumur (svört ör). Einnig sést væg bólga í millivef (rauðar örvar).
Lýsa má þróun trefjavefslungnabólgu með tveimur dæmum af vefjasýnum. Á fyrstu myndinni sést lausgerður bandvefur með fáeinum trefjakímfrumum. Einnig sést væg bólga í millivef (mynd I). Á næstu mynd sést meiri græðsluvefur, aukinn fjöldi trefjakímfrumna og nýmyndun æða (mynd II).
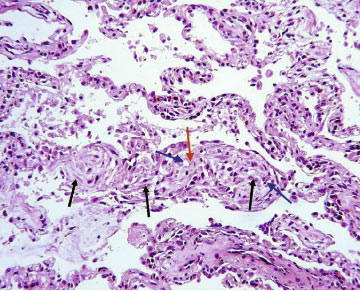
Mynd II. Meinafræði trefjavefslungnabólgu á síðari stigum. Hér sést meiri græðsluvefur (rauð ör), aukinn fjöldi trefjakímfrumna (svartar örvar) og nýmyndun æða (bláar örvar).
Flokkun trefjavefslungnabólgu
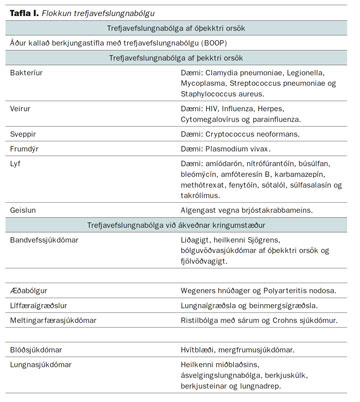
Hægt er að flokka trefjavefslungnabólgu eftir því hvort orsökin er þekkt (TÞO), óþekkt (TÓO) eða hvort hún komi fram við ákveðnar kringumstæður eins og sýnt er í töflu I. Einnig getur verið um svokallaða hratt vaxandi form trefjavefslungna-bólgu (rapidly progressive organising pneu-monia) að ræða og getur hún komið undir öllum flokkunum þremur.
Fjöldi sjúkdóma hefur verið tengdur við trefjavefslungnabólgu. Líta má á flokkunina sem nálgun. Með skiptinguna í þekktar eða óþekktar orsakir að vopni verða rannsóknir, greining og meðferð sjúkdómsins markvissari fyrir vikið. Þó að flokkað sé sem óþekktar orsakir er alls ekki sagt að TÓO hafi ekki orsök. Orsökin hefur aðeins ekki verið fundin né skýrð. Því er alls ekki útilokað að flokkunin taki breytingum og ætti í raun að gera það eftir því sem þekkingin vex. Til þess að trefjavefslungnabólga sé talin vera af þekktum orsökum (TÞO) þarf að sýna fram á náin tengsl við einhvern af neðangreindum flokkum:
Af þekktri orsök
Eftir sýkingu: Fjöldi sýkinga getur valdið trefjavefslungnabólgu (sjá töflu I). Til þess að geta sýnt fram á tengsl við sýkingu þarf sjúklingurinn að hafa klínísk og myndræn einkenni í samræmi við sýkinguna og svara ekki hefðbundinni meðferð með sýklalyfjum. Nauðsynlegt er að sýna fram á þekktan orsakavald með sterkt jákvæðri ræktun örvera, blóðvatnsprófum eða mótefnamælingum.
Lyfjatengt: Tímatengsl upphafs sjúkdóms og lyfjainntöku gefa vísbendingu um orsakasamband (sjá töflu I). Dæmi um lyf sem geta valdið trefjavefslungnabólgu eru búsúlfan, nitrófurantóín og bleómýcín auk fjölda annarra (18). Sérstök athygli er vakin á hjartalyfinu amíódarón, ekki síst vegna þess að notkun þess er útbreidd hér á landi sem og annars staðar (19-20). Fengu þrír einstaklingar trefjavefslungnabólgu í tengslum við amíódarón í okkar rannsókn (6). Dæmigert er sjá svokallaðar froðuátfrumur (foamy macro-?phages) á vefjasýni undir þessum kringumstæðum. Erfitt getur reynst að greina annars vegar á milli lyfs sem orsakavalds fyrir sjúkdómnum eða hins vegar bandvefssjúkdóma, krabbameins eða blóðsjúkdóma. Ekki síst þegar lyf sem geta valdið trefjavefslungnabólgu eru notuð gegn sjúkdómi eins og iktsýki sem einnig getur valdið trefjavefs-lungnabólgu. Það að einkennin hjaðni við að lyfjainntaka sé stöðvuð er besta vísbendingin um að orsakasamband sé til staðar.
Geislun: Ef upphaf sjúkdómsins er í tengslum við geislun á brjóstkassa (og ekki er hægt að finna aðra nærtækari skýringu) gæti verið um trefjavefslungnabólgu orsakaða af geislun að ræða. Það hefur lengi verið þekkt að geislun á brjósthol getur valdið geislunarlungnabólgu (radiation pneumonitis), en trefjavefslungnabólgu hefur aðeins verið lýst á síðustu 10-15 árum í tengslum við geislun, sérstaklega vegna brjóstakrabbameins (21-24).
Trefjavefslungnabólga af þekktri orsök við ákveðnar kringumstæður
Bandvefssjúkdómar: Þekkt er að margir bandvefssjúkdómar geta lagst á lungun og meðal annars valdið trefjavefslungnabólgu. Helst eru það iktsýki, Sjögrens heilkenni og vöðvabólgusjúkdómar (inflammatory myopathies) sem valda trefjavefslungnabólgu en rauðir úlfar eða herslishúð (scleroderma) síður, en þekkist þó (25-28). Nauðsynlegt er að um virkan bandvefssjúkdóm sé að ræða ef greina á trefjavefslungnabólgu.
Aðrar kringumstæður
Trefjavefslungnabólga er þekkt í tengslum við fjölda annarra sjúkdóma. Meðal þeirra eru sáraristilbólga, Crohns sjúkdómur, fjölvöðvagigt, Behcet´s sjúkdómur, lifrarbólga af C gerð, Sweets heilkenni og ýmsar gerðir blóðsjúkdóma á borð við hvítblæði, mergmisþroska (myelodysplasia) og mergofvöxt (myeloproliferative disorders) (sjá töflu I) (26). Í flestum tilfellum er aðeins um að ræða fáein birt sjúkratilfelli og því óljóst hvort um orsakasamhengi sé að ræða eða aðeins tímalegt samhengi. Hugsanlega gæti verið um að ræða ógreinda sýkingu eða lyf sem í raun valda trefjavefslungnabólgunni.
Í íslensku rannsókninni voru sýkingar algengasta orsökin fyrir TÞO, meðal þeirra voru bæði bakteríu- og veirusýkingar. Lyf sem orsökuðu TÞO voru amíódarón, nítrófurantóín, metótrexat and búsúlfan. Brjóstakrabbamein var algengasta krabbameinið í tengslum við TÞO. Einnig voru allar þær konur sem greindust með TÞO í tengslum við geislun með brjóstakrabbamein. Iktsýki, fjölvöðvagigt og heilkenni Sjögrens voru algengustu bandvefssjúkdómarnir í tengslum við TÞO (7).
Öllum undirgerðum af TÞO í rannsókn okkar hefur áður verið lýst (12). Enn er þó nokkuð óljóst hver er algengasti undirhópur af TÞO. Í rannsókn Lohr et al. voru bandvefssjúkdómar algengasta undirtegund TÞO (29). Í íslensku rannsókninni var sýking af ýmsu tagi algengasta orsökin.Teljum við líklegt að stór hluti af trefjavefslungnabólgu af óþekktri orsök sé einnig orsakaður af sýkingu, það er að sýking setji ferilinn í gang. Af hverju greinist þá ekki trefjavefslungnabólga eftir sýkingu oftar? Líklega eru tvær ástæður. Í fyrsta lagi er ekki alltaf leitað nógu ítarlega, til að mynda með blóðvatnsprófum og mótefnamælingum. Í öðru lagi er líklegt að sýkingin og jafnvel ummerki hennar séu gengin yfir.
Faraldsfræði og lýðfræðilegir þættir
Ekki eru til margar rannsóknir á faraldsfræði trefjavefslungnabólgu og stærsta og eina faraldsfræðirannsóknin sem gerð hefur verið á heilli þjóð, svo vitað sé, er á Íslandi (5). Um að ræða rannsókn sem tók yfir 20 ára tímabil, frá 1984-2003 og greindust 104 sjúklingar með trefjavefslungnabólgu, þar af 58 með TÓO og 46 með TÞO. Í rannsókninni mældist meðalnýgengi trefjavefslungnabólgu 1,97 á hverja 100.000 íbúa yfir tímabilið þar af 1,10 fyrir TÓO og 0,87 fyrir TÞO. Fór nýgengið stigvaxandi allt tímabilið og var komið í 3,06 síðustu fjögur ár rannsóknirnar. Jókst því nýgengið marktækt á tímabilinu (p<0,0001), í það heila um 8,1% á ári yfir tímabilið. Sýndi rannsóknin því fram á hærra nýgengi trefjavefslungnabólgu en fyrri rannsóknir hafa gert þrátt fyrir að nota ströng skilmerki. Í rannsókn frá Olmstead sýslu í Minnesóta fylki í Bandaríkjunum reyndist nýgengið vera 0,85 (29). Vaxandi nýgengi hér á landi gæti haft ýmsar skýringar. Í fyrsta lagi er aukin vitund um sjúkdóminn en stutt er síðan honum var lýst fyrst sem klínísku heilkenni af Epler á árunum 1984-85. Í öðru lagi hefur orðið fjölgun á lungnasérfræðingum og þar með berkjuspeglunum á Íslandi á tímabilinu. Í þriðja lagi er aukin notkun lyfja og meðferðar sem gæti hugsanlega aukið fjölda greindra TÞO. Í fjórða lagi má nefna hækkandi aldur þjóðarinnar.
Tilfellin hér á landi dreifðust nokkuð jafnt um landið. Flest tilfelli voru á Reykjavíkursvæðinu. (sjá mynd III). Hæst var tíðnin í Vestmannaeyjum, alls sjö tilfelli. Ekki er einföld skýring á því, en eyjan hefur fengið reglulegar heimsóknir frá lungnalæknum, sem gæti verið hluti af skýringunni.
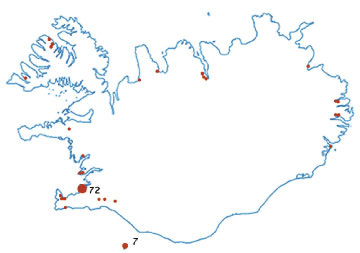
Mynd III. Dreifing trefjavefslungnabólgu um landið.
Í trefjavefslungnabólgu er yfirleitt um nokkuð jafnt kynjahlutfall að ræða (12). Aldur við greiningu getur spannað vítt tímabil en flestir eru á aldrinum 60-70 ára. Öfugt við marga aðra lungnasjúkdóma hefur ekki verið hægt að sýna fram á tengsl við reykingar (12).
Klínísk einkenni og teikn
Sjúkdómseinkenni lýsa sér venjulega sem hósti án uppgangs, mæði, hækkaður líkamshiti, þyngdartap og almennur slappleiki. Brjóstverkir og nætursviti koma einnig fyrir. Blóðhósti er afar sjaldgæfur. Mæðin er venjulega frekar væg nema í einstaka tilfellum, sérstaklega þegar um er að ræða hratt vaxandi form sjúkdómsins. Einkennin hafa gjarnan verið til staðar í nokkrar vikur fyrir greiningu nema á hratt vaxandi forminu, þar sem þau geta verið til staðar í fáeina daga. Almenn líkamsskoðun getur verið eðlileg en brak yfir þéttingarsvæðum við lungnahlustun var algengasta teiknið við skoðun (7). Reyndist brak marktækt algengara í TÞO hópnum (73%) en í TÓO hópnum (49%) en að öllum líkindum hefur það enga þýðingu.
Blóðrannsóknir
Ekki eru til sértæk blóðpróf sem greina trefjavefs-lungnabólgu sem slíka, en bólgupróf eins og sökk og CRP eru yfirleitt hvort tveggja töluvert hækkuð. Til að gefa til kynna hve mikið bólguástand er til staðar í líkamanum, var meðaltals-sökk 69 mm/klst og meðaltals-CRP 115 mg/L í íslensku rannsókninni (7). Einnig er oft um að ræða væga hækkun á hvítum blóðkornum, mest hlutleysiskyrningum (neutrophils). Stundum sést vægur blóðskortur og lækkun á albúmíni sem endurspeglar bólguástandið í líkamanum.
Berkjuskol
Berkjuskol og deilitalning þess getur verið gagnleg í greiningu trefjavefslungnabólgu til aðgreiningar frá öðrum sjúkdómum. Almennt sýnir deilitalning skolsins í trefjavefslungnabólgu nokkuð blandaða mynd; um er að ræða aukningu á eitilfrumum (20-40%), en hlutleysiskyrningar eru um 10% og um 5% eru eósínófílar (30-32). Í trefjavefslungnabólgu er fjöldi eitilfrumna því hærri en fjöldi eósínófíla. Eitilfrumurnar eru virkjaðar og CD4/CD8 hlutfall eitilfrumna í berkjuskoli er lækkað í trefjavefs-lungnabólgu (12). Berkjuskolið er ekki sértækt fyrir trefjavefslungnabólgu. Ef fjöldi eósínófíla er aukinn er eósínófíl lungnabólga líklegri en sé hlutfall hlutleysiskyrninga hækkað er lungnatrefjun (pulmonary fibrosis) líklegri.
Öndunarmælingar
Væg til meðalsvæsin herpa á öndunarprófum er algeng í trefjavefslungnabólgu. Loftskiptapróf sýna minnkuð loftskipti fyrir kolmónoxíði (DLCO). Vægur súrefnisskortur er algengur og yfir-?leitt sýna blóðgös væga til meðalsvæsna súrefnisbilun. Þekkt er svæsin súrefnisbilun í trefjavefs-lungnabólgu, ekki síst í hratt versnandi trefjavefs-lungnabólgu (12).
Myndrannsóknir
Nokkur breytileiki getur verið á mynstri þéttinga í trefjavefslungnabólgu en tölvusneiðmynd af lungum getur gefið greininguna sterklega til kynna þó svo að vefjasýni sé ávallt æskilegt. Tölvusneiðmynd hefur mikið gildi fram yfir hefðbundna röntgenmynd af lungum. Gagnlegt er að flokka myndbreytingar í þrennt:
1) Dreifðar lungnablöðruþéttingar
Þetta er algengasta mynd trefjavefslungnabólgu með dreifðum þéttingum af lungnablöðrugerð (sjá mynd IV). Þéttingar eru oft útlægar og beggja vegna. Stærð þéttinganna getur verið nokkuð breytileg, allt frá nokkrum sentimetrum yfir í heilt lungnablað og stundum flakkandi (migratory) (12). Að sama skapi getur þéttleiki íferðanna verið nokkuð misjafn, allt frá hélun (ground glass) yfir í þéttingu með loftberkjukorti (air bronchogram). Algengt er að tölvusneiðmynd leiði í ljós fjölda þéttinga sem ekki sjást með hefðbundinni rönt-genmynd. Dæmi um sjúkdóma með svipað mynstur þéttinga eru langvinn eósínófíl lungnabólga, hægt vaxandi eitlakrabbamein og lungnakrabbamein, ekki síst af berkju- og lungnablöðru (bronchoalveolar) gerð (12, 33).
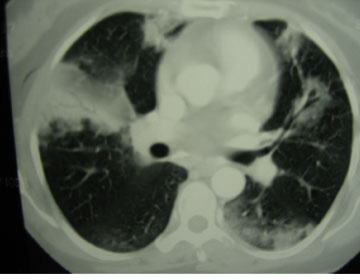
Mynd IV. a) Röntgenmynd af lungum og b) tölvusneiðmynd af lungum sýna útlægar og dreifðar þéttingar beggja vegna af lungnablöðrugerð (12). (Birt með leyfi European Respiratory Journal.)
2) Dreifðar millivefsþéttingar
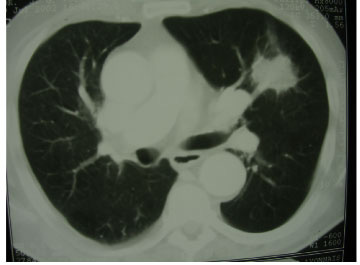
Mynd V. Tölvusneiðmynd af lungum sem sýnir dreifðar millivefsbreytingar beggja vegna (12). (Birt með leyfi European Respiratory Journal.)
Önnur myndgerð er þar sem dreifðar millivefsþéttingar eru ráðandi, yfirleitt beggja vegna ásamt vægum lungnablöðruþéttingum (sjá mynd V). Þessi gerð hefur verið tengd bandvefssjúkdómum og verri horfum. Hér er því mikilvægt að greina trefjavefslungnabólgu frá öðrum millivefsjúkdómum á borð við útbreiddar skemmdir á lungnablöðrum (diffuse alveolar damage) eða lungnatrefjun (34-35). Hugsanlega getur verið um skörun við þessa sjúkdóma að ræða í sumum tilfellum.
3) Staðbundinn hnúður
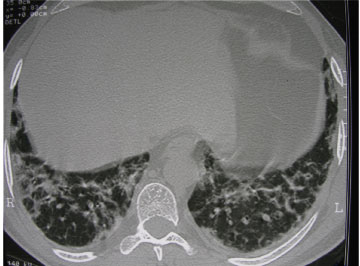
Mynd VI. Sýnir hnúð í hægra lunga sem reyndist vera trefjavefslungna-bólga (12). (Birt með leyfi European Respiratory Journal.)
Þriðja myndgerð trefjavefslungnabólgu er staðbundinn hnúður (sjá mynd VI). Hér fæst greiningin oft eftir að hnúðurinn hefur verið fjarlægður vegna gruns um krabbamein (12). Hafa þessir sjúklingar minni almenn einkenni, sem og minni einkenni frá lungum. Líklegt er að hér sé um að ræða eftirstöðvar af lungnabólgu í mörgum tilfellum (12, 36).
Sýnataka
Sýnataka með skurðaðgerð er talin æskilegust en sýnataka við berkjuspeglun (transbronchial) er einnig talin vera nægilega góð (29, 31, 37). Nokkuð er þetta efni þó umdeilt í hópi lungnalækna og meinafræðinga. Í íslensku rannsókninni voru flestir sjúklinganna greindir með sýnatöku við berkjuspeglun eða um 81% en 19% voru greindir með sýnatöku með skurðaðgerð (7). Gætu sumir talið það vera veikleika rannsóknarinnar hversu fáir voru greindir með sýni fengnu með skurðaðgerð. En gegn því mætti segja að þá hefðu færri verið greindir því þröskuldurinn í vegi fyrir því að framkvæma skurðaðgerð til að ná í sýni er ?yfirleitt hærri en að framkvæma berkjuspeglun og sýnataka með þeim hætti. Sýnt hefur verið fram á að sýnataka með berkjuspeglun hefur um 64% næmi og 86% sértækni (31). Almennt er trefjavefs-lungnabólga ekki greind án vefjasýnis. Kemur þó til greina að meðhöndla án sýnatöku mjög veika sjúklinga eða aðra þá sem ekki þola sýnatöku af einhverjum sökum. Sérstaklega á það við ef klínísk einkenni og myndræn teikn eru dæmigerð fyrir trefjavefslungnabólgu. Ef slíkir sjúklingar svara ekki háskammta sterameðferð á stuttum tíma er nauðsynlegt að endurmeta greininguna. Æskilegast er að taka vefjasýnið áður en meðferð hefst eða á fyrsta sólarhring meðferðar.
Meðferð
Bati án meðferðar er sjaldgæfur en þekkist þó (38-39). Ónæmisbælandi meðferð á formi barkstera er meginmeðferð við sjúkdómnum en árangur af sýklalyfinu erythrómýcín þekkist einnig og voru þrír sjúklingar meðhöndlaðir með lyfinu í íslensku rannsókninni og fengu allir bót af sínum einkennum (7). Talið er að lyfið hafi bólgueyðandi áhrif auk sýkladrepandi verkunar (40). Flestir voru meðhöndlaðir með barksterum, 69% í TÓO og 72% í TÞO og var upphafsskammtur Prednisólóns að meðaltali 42 mg fyrir báða hópana (7). Ekki eru menn fyllilega sammála um skammtastærðir stera. Sumir höfundar mæla með stórum upphafsskömmtum á bilinu 1-1,5 mg/kg á dag (41-42) en algengara er að mælt sé með upphafsskömmtum í kringum 0,75 mg/kg á dag (12) og er því meðferðin á Íslandi nær hinu síðarnefnda. Yfirleitt er svörunin við sterum skjót og góð, þó ekki eins hröð og í eósínófíl lungnabólgu (43). Algengt er að sjúklingar finni fyrir bata strax á fyrstu dögum meðferðar og breytingar til batnaðar sjáist á lungnamynd á næstu dögum/vikum. Fullur bati sést eftir vikur eða mánuði. Þegar um er að ræða hratt vaxandi gerð trefjavefslungnabólgu er mælt með því að nota háa skammta af sterum í æð (til dæmis 250 mg af methýlprednisólón á sex klukkustunda fresti) (44).
Sjaldan eru ónæmisbælandi lyf á borð við cýklófosfamíð og azatíóprín notuð við trefjavefs-lungnabólgu en gildi slíkra lyfja er óvíst og hefur lítið verið rannsakað (45). Aðeins er um tilfellalýsingar að ræða. Helst eru þessi lyf gefin sem viðbót við stera vegna þráláts sjúkdóms.
Endurkoma trefjavefslungnabólgu
og tímalengd meðferðar
Það er vel þekkt að trefjavefslungnabólga getur tekið sig upp og gerðist það hjá 20% sjúklinganna í rannsókn okkar en nánast allir (20/21) svöruðu endurtekinni meðferð (7). Aðrar rannsóknir hafa sýnt fram á bæði lægri og hærri endurkomutíðni (29, 46-47). Engin regla virðist vera á bakslagi. Breytingarnar geta tekið sig upp á sama stað eða annars staðar í lungunum. Ekki er óalgengt að sjúkdómurinn taki sig upp aftur þegar steraskammtar eru minnkaðir eða notkun þeirra er hætt. Erfitt getur því verið að spá fyrir um tímalengd meðferðar. Mikilvægt er því að upplýsa sjúklinga um að þeir geti átt von á bakslagi þrátt fyrir góða meðferðarsvörun. Hefðbundin meðferðarlengd er 6-12 mánuðir. Tímalengd meðferðar ræðst þó ávallt af einkennum hvers sjúklings. Sumir þurfa viðhaldsskammt af sterum til lengri tíma þó það sé ekki æskilegt vegna aukaverkana. Því er mikilvægt að huga að beinvernd frá upphafi.
Dánartíðni og lífslíkur
Almennt eru horfur fyrir trefjavefslungnabólgu taldar góðar og í íslensku rannsókninni lést aðeins einn sjúklingur úr trefjavefslungnabólgu (5). Hafði hann hratt vaxandi trefjavefslungnabólgu. Eigi að síður sýndi okkar rannsókn að sjúklingar með trefjavefslungnabólgu höfðu hærri dánartíðni en aldurs- og kyn staðlaður almenningur (sjá mynd VII). Er það því nokkur ráðgáta af hverju sjúklingarnir hafa styttri lífslíkur. Þetta hefur ekki verið rannsakað mikið. Ástæðurnar gætu verið tvær. Í fyrsta lagi gæti hið mikla bólguástand sem skapast í trefjavefslungnabólgu haft áhrif á ýmis líffæri líkamans, meðal annars hjarta og æðakerfið. Í öðru lagi eru sjúklingar með trefjavefslungnabólgu oft með annan alvarlegan sjúkdóm eins og langvinna lungnateppu, krabbamein eða bandvefssjúkdóm.
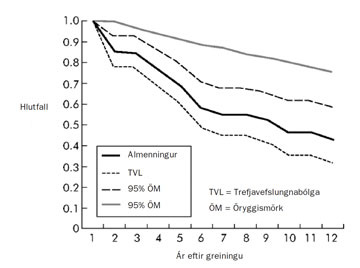
Mynd VII. Lifun sjúklinga með trefjavefslungnabólgu í samanburði við aldursstaðlað þýði á Íslandi (5).
Samantekt
Þrátt fyrir að trefjavefslungnabólga sé enn sjaldgæfur sjúkdómur er hún algengari en áður var talið og hefur tíðnin farið vaxandi. Mikilvægt er að hafa hana í huga hjá sjúklingum með þéttingar sem svara ekki hefðbundinni meðferð. Trefjavefslungnabólga er nú vel skilgreindur sjúkdómur með einkennandi klínískum, myndrænum og vefjameinafræðilegum breytingum. Þó að meðferð með sykursterum sé áhrifarík er erfitt að spá fyrir um hverjir muni þurfa stera til lengri tíma og hverjir fá bakslag sjúkdóms síðar. Auk þess er erfitt að segja til um æskilegan byrjunarskammt stera og hve lengi á að meðhöndla. Sjúkdómurinn er í eðli sínu breytilegur og verður meðferðin ávallt að stjórnast af því.
Þörf er á frekari vísindalegum rannsóknum sem leiða til betri skilnings á meingerð sjúkdómsins. Skilgreina þarf betur hvernig takmarkaður viðgerðarferill í lungum breytist yfir í viðvarandi bólguviðbrögð sem svara þó sterum.
Þakkir
Höfundar þakka Inger Helene Bóasson ljósmyndara aðstoð við myndvinnslu.
Heimildir
1. Colby TV. Pathologic aspects of bronchiolitis obliterans organizing pneumonia. Chest 1992; 102: 38-43.
2. Davison AG, Heard BE, McAllister WAC, et al. Cryptogenic organizing pneumonitis. Q J Med 1983; 52: 382-94.
3. Epler GR, Colby TV, McLoud TC, et al. Bronchiolitis obliterans organizing pneumonia. N Engl J Med 1985; 312: 152-8.
4. American Thoracic Society/European Respiratory Society Classification of the idiopathic interstitial pneumonias: international multidisciplinary consensus. American Thoracic Society/European Respiratory Society. Am J Respir Crit Care Med 2002; 165: 277-304.
5. Guðmundsson G, Sveinsson ÓÁ, Ísaksson HJ, et al. Organizing pneumonia in Iceland. A nationwide population based epidemiological study. Thorax 2006; 61: 805-8.
6. Sveinsson ÓÁ, Ísaksson HJ, Guðmundsson G. Trefjavefslungnabólga tengd notkun lyfsins amíódaón. Sjúkratilfelli og yfirlit. Læknablaðið 2006; 92: 385-8.
7. Sveinsson ÓÁ, Ísaksson, Sigvaldason A, et al. Clinical features in secondary and cryptogenic organizing pneumonia. Int J Tubercul Lung Dis 2007; 11: 989-94.
8. Nesheim M. Thrombin and fibrinolysis. Chest 2003; 124: Suppl. 3, 33-9.
9. Fujimoto H, Gabazza EC, Hataji O, et al. Thrombin-activatable fibrinolysis inhibitor and protein C inhibitor in interstitial lung disease. Am J Respir Crit Care Med 2003; 167: 1687-94.
10. Loskutoff DJ, Quigley JP. PAI-1, fibrosis, and the elusive provisional fibrin matrix. J Clin Invest 2000; 106: 1441-3.
11. Gunthe A, Lubke N, Ermert M, et al. Prevention of bleomycin-induced lung fibrosis by aerosolization of heparin or urokinase in rabbits. Am J Respir Crit Care Med 2003; 168: 1358-65.
12. Cordier J. Cryptogenic organising pneumonia. Eur Respir J 2006; 28: 422-46.
13. Lappi-Blanco E, Kaarteenaho-Wiik R, Soini Y, et al. Intraluminal fibromyxoid lesions in bronchiolitis obliterans organizing pneumonia are highly capillarized. Hum Pathol 1999; 30: 1192-6.
14. Peyrol S, Cordier JF, Grimaud JA. Intra-alveolar fibrosis of idiopathic bronchiolitis obliterans-organizing pneumonia. Cell-matrix patterns. Am J Pathol 1990; 137: 155-70.
15. Kuhn C 3rd, Boldt J, King TE, et al. An immunohistochemical study of architectural remodeling and connective tissue synthesis in pulmonary fibrosis. Am Rev Respir Dis 1989; 140: 1693-703.
16. London L, Majeski EI, Paintlia MK, et al. Respiratory reovirus 1/L induction of diffuse alveolar damage: a model of acute respiratory distress syndrome. Exp Mol Pathol 2002; 72: 24-36.
17. London L, Majeski EI, Altman-Hamamdzic S, et al. Respiratory reovirus 1/L induction of diffuse alveolar damage: pulmonary fibrosis is not modulated by corticosteroids in acute respiratory distress syndrome in mice. Clin Immunol 2002; 103: 284-95.
18. Epler GR. Drug-induced bronchiolitis obliterans organizing pneumonia. Clin Chest Med 2004; 25: 89-94.
19. Valle JM, Alvarez D, Antunez J, et al. Bronchiolitis obliterans organizing pneumonia secondary to amiodarone: a rare aetiology. Eur Respir J 1995; 8: 470-1.
20. Camus P, Martin WJ 2nd. Rosenow EC 3rd. Amiodarone pulmonary toxicity. Clin Chest Med 2004; 25: 65-75.
21. Camus P, Fanton A, Bonniaud P, et al. Interstitial lung disease induced by drugs and radiation. Respiration 2004; 71: 301-26.
22. Crestani B, Kambouchner M, Soler P, et al. Migratory bronchiolitis obliterans organizing pneumonia after unilateral radiation therapy for breast carcinoma. Eur Respir J 1995; 8: 318-21.
23. Crestani B, Valeyre D, Roden S, et al, and the Groupe d?Etudes et de Recherche sur les Maladies Orphelines Pulmonaires (GERM?O?P). Bronchiolitis obliterans organizing pneumonia syndrome primed by radiation therapy to the breast. Am J Respir Crit Care Med 1998; 158: 1929-35.
24. Arbetter KR, Prakash UBS, Tazelaar HD, et al. Radiation-induced pneumonitis in the "nonirradiated" lung. Mayo Clin Proc 1999; 74: 27-36.
25. Cordier JF. Organising pneumonia. Thorax 2000; 55: 318-28.
26. Imasaki T, Yoshii A, Tanaka S, et al. Polymyositis and Sjogren's syndrome associated with bronchiolitis obliterans organizing pneumonia. Intern Med 1996; 35: 231-5.
27. Rees JH, Woodhead MA, Sheppard MN, et al. Rheumatoid arthritis and cryptogenic organising pneumonitis. Respir Med 1991; 85: 243-6.
28. Gammon RB, Bridges TA, al-Nezir H, et al. Bronchiolitis obliterans organizing pneumonia associated with systemic lupus erythematosus. Chest 1992; 102: 1171-4.
29. Lohr RH, Boland BJ, Douglas WW, et al. Organizing pneumonia: features and prognosis of cryptogenic, secondary, and focal variants. Arch Intern Med 1997; 157: 1323-9.
30. Costabel U, Teschler H, Guzman J. Bronchiolitis obliterans organizing pneumonia (BOOP): the cytological and immunocytological profile of bronchoalveolar lavage. Eur Respir J 1992; 5: 79-7.
31. Poletti V, Cazzato S, Minicuci N, et al. The diagnostic value of bronchoalveolar lavage and transbronchial lung biopsy in cryptogenic organizing pneumonia. Eur Respir J 1996; 9: 2513-6.
32. Nagai S, Aung H, Tanaka S, et al. Bronchoalveolar lavage cell findings in patients with BOOP and related diseases. Chest 1992; 102: Suppl. 1/ 32-7.
33. Preidler KW, Szolar DM, Moelleken S, et al. Distribution pattern of computed tomography findings in patients with bronchiolitis obliterans organizing pneumonia. Invest Radiol 1996; 31: 251-5.
34. Fukuda Y, Ishizaki M, Masuda Y, et al. The role of intraalveolar fibrosis in the process of pulmonary structural remodeling in patients with diffuse alveolar damage. Am J Pathol 1987; 126: 171-82.
35. Svee K, White J, Vaillant P, et al. Acute lung injury fibroblast migration and invasion of a fibrin matrix is mediated by CD44. J Clin Invest 1996; 98: 1713-27.
36. Kohno N, Ikezoe J, Johkoh T, et al. Focal organizing pneumonia: CT appareance. Radiology 1993; 189: 119-23.
37. Azzam ZS, Bentur L, Rubin AH, et al. Bronchiolitis obliterans organizing pneumonia. Diagnosis by transbronchial biopsy. Chest 1993; 104: 1899-901.
38. Bellomo R, Finlay M, McLaughlin P, et al. Clinical spectrum of cryptogenic organising pneumonitis. Thorax 1991; 46: 554-8.
39. Akira M, Yamamoto S, Sakatani M. Bronchiolitis obliterans organizing pneumonia manifesting as multiple large nodules or masses. AJR 1998; 170: 291-5.
40. Ichikawa Y, Ninomiya H, Katsuki M, et al. Long-dose/long-term erythromycin for treatment of bronchiolitis obliterans organizing pneumonia (BOOP). Kurume Med J 1993; 40: 65-7.
41. Epler GR. Heterogeneity of bronchiolitis obliterans organizing pneumonia. Curr Opin Pulm Med 1998; 4: 93-7.
42. Wright L, King TE. Cryptogenic organizing pneumonia (idiopathic bronchiolitis obliterans organizing pneumonia): an update. Clin Pulm Med 1997; 4: 152-8.
43. Sveinsson ÓÁ, Guðmundsson G, Ísaksson HJ. Langvinn eósínófíl lungnabólga á Íslandi. Faraldsfræði, klínísk einkenni og yfirlit. Læknablaðið 2007; 93: 111-6.
44. Cohen AJ, King TE Jr, Downey GP. Rapidly progressive bronchiolitis obliterans with organizing pneumonia. Am J Respir Crit Care Med 1994; 149: 1670-5.
45. Purcell IF, Bourke SJ, Marshall SM. Cyclophosphamide in severe steroid-resistant bronchiolitis obliterans organizing pneumonia. Respir Med 1997; 91: 175-7.
46. Lazor R, Vandevenne A, Pelletier A, et al. The Groupe d?Etudes et de Recherche sur les Maladies ?Orphelines? Pulmonaires (GERM?O?P). Cryptogenic organizing pneumonia: characteristics of relapses in a series of 48 patients. Am J Respir Crit Care Med 2000; 162: 571-7.
47. Oymak FS, Demirbas HM, Mavili E, et al. Bronchiolitis obliterans organizing pneumonia. Clinical and roentgenological features in 26 cases. Respiration 2005; 72: 254-62.
