05. tbl 93. árg. 2007
Fræðigrein
Sjálfkrafa loftbrjóst - Yfirlitsgrein
Ágrip
Sjálfkrafa loftbrjóst er tiltölulega algengur sjúkdómur sem oftast greinist hjá ungu og annars hraustu fólki. Horfur eru yfirleitt góðar og flesta er hægt að lækna með brjóstholskera sem tengdur er við sog. Endurtekið loftbrjóst og viðvarandi loftleki eru þó tíðir fylgikvillar eftir slíka meðferð og getur þurft að grípa til skurðaðgerða. Hér eru rakin einkenni sjálfkrafa loftbrjósts, aðferðir til greiningar og meðferð. Sérstök áhersla er lögð á mismunandi meðferðarúrræði og ábendingar fyrir skurðaðgerð.
Skilgreining og faraldsfræði
Loftbrjóst kallast það þegar loft safnast fyrir innan fleiðruholsins. Árlegt aldursstaðlað nýgengi á Vesturlöndum er í kringum 7,4-18/100.000 fyrir karla og 1,2-6/100.000 fyrir konur (1, 2). Þessar tölur miðast eingöngu við sjúklinga sem ekki hafa þekktan lungnasjúkdóm, en að þeim viðbættum er tíðni sjálfkrafa loftbrjósts allt að tvöfalt hærri (2). Flestir sjúklingar eru á bilinu 20-30 ára og karlmenn í meirihluta (3, 4). Loftbrjóst er einnig mun algengara hjá reykingafólki (1), eða allt að 20 sinnum algengara en hjá þeim sem aldrei hafa reykt. Hér á landi eru ekki til nákvæmar tölur um nýgengi loftbrjósts. Nokkrar íslenskar rannsóknir eru þó til, þar á meðal doktorsritgerð eftir Jón G. Hallgrímsson frá árinu 1978 (5), og tvær rannsóknir birtar í Læknablaðinu. Í þeirri fyrri var greint frá afdrifum 118 sjúklinga sem gengust undir skurðaðgerð vegna loftbrjósts á Landspítalanum á tímabilinu 1975-1984 (6). Síðari greinin birtist í þessu tölublaði Læknablaðsins og er yfirlit yfir árangur loftbrjóstaðgerða á Landspítala á árunum 1991-2005 (7).
Lífeðlisfræði, meingerð og orsakir loftbrjósts
Undir venjulegum kringumstæðum er neikvæður þrýstingur í fleiðruholi sem eykst við innöndun. Þessi neikvæði fleiðruholsþrýstingur er meiri við lungnatoppa en neðar í fleiðruholi. Í hávöxnu fólki er þrýstingsmunur enn meiri og getur hugsanlega skýrt hærri tíðni loftbrjósts hjá þeim (8). Þegar samgangur verður á milli loftvega lungna og fleiðruhols flæðir loft í átt að neikvæðum þrýstingi uns hann jafnast út. Loft getur borist í fleiðruhol með þrennum hætti. Langalgengast er að rof verði á yfirborði lunga og loft streymi út um yfirborð þess vegna rofs á lungnablöðrum. Í öðru lagi getur loft borist í gegnum brjóstvegg vegna utanaðkomandi áverka á brjóstholi, til dæmis eftir hnífstungu. Í þriðja lagi getur sýking í fleiðruholi með gasmyndandi sýklum myndað loft í fleiðru.
Sjúklingar með sjálfkrafa loftbrjóst geta haft þekktan lungnasjúkdóm sem á þátt í orsök þess (secondary pneumothorax, SSP) (8). Tíðni loftbrjósts er aukin í nánast öllum lungnasjúkdómum. Rof verður á yfirborði lunga og loft berst út í fleiðruhol. Lungnaþemba og krónískt berkjukvef eru algengustu sjúkdómarnir (9) en hlutfall loftbrjóstssjúklinga með þessa lungnasjúkdóma er yfirleitt á bilinu 10-40% (10-12). Þessi tegund loftbrjósts getur verið lífshættuleg þar sem þessir sjúklingar eru oft eldri og hafa skerta lungnastarfsemi (13, 14). Er dánarhlutfall þeirra allt að fjórfalt hærra en hjá sjúklingum með loftbrjóst án undirliggjandi lungnasjúkdóms (15). Aðrir og sjaldgæfari lungnasjúkdómar sem valdið geta sjálfkrafa loftbrjósti eru meðal annars histiocytosis X (Langerhans cell granulomatosis) (16) og lymph-angioleiomyomatosis (17).
Mun algengara er þó að sjúklingar með sjálfkrafa loftbrjóst hafi ekki greinst með lungnasjúkdóm (primary spontaneous pneumothorax, PSP). Ástæða loftbrjósts er þá rof á smáum blöðrum sem staðsettar eru undir fleiðru lungans (subpleural blebs). Blöðrurnar eru yfirleitt minni en 2 cm í þvermál og eru langoftast á toppi efra lungnablaðs eða á toppi þess neðra (18). Í langflestum tilvikum (>90%) er blöðrur að finna í báðum lungum (19, 20). Um er að ræða eins konar staðbundið lungnaþan (localised emphysema) sem veldur staðbundinni veilu í lungum sem að öðru leyti eru eðlileg. Myndun blaðranna er hugsanlega tengd niðurbroti á teygjuþráðum (elastic fibers) og eru þeir taldir brotna niður vegna ójafnvægis milli próteasa og antipróteasa annars vegar og oxunarefna og andoxunarefna hins vegar (21). Einnig er talið að hvítfrumur (neutrophils) og átfrumur (macrophages) hafi hlutverki að gegna, en aukinn fjöldi bólgufrumna er til staðar hjá reykingafólki (22). Afleiðingin er eyðing lungnavefs og bandvefsummyndun, þar á meðal í aðlægri fleiðru. Er talið hugsanlegt að efni í tóbaksreyk ræsi þetta ferli (23). Einnig hefur verið sett fram sú tilgáta að sjálfkrafa loftbrjóst geti verið afleiðing einhvers konar bandvefsgalla og blöðrurnar því meðfæddar. Til dæmis er loftbrjóst mjög algengt hjá sjúklingum með Marfans heilkenni (24) og sjúklingar með míturlokuleka (25) og nárakviðslit hafa hærri tíðni en aðrir (26).
Loks má nefna svokallað tíðaloftbrjóst (catamenial pneumothorax). Það sést endurtekið í tengslum við tíðablæðingar, oftast innan 48-72 klukkustunda frá upphafi þeirra (27). Þetta er afar sjaldgæf tegund loftbrjósts en er hugsanlega vangreind, til dæmis er til rannsókn þar sem 3-6% kvenna með loftbrjóst á aldrinum 20-30 ára reyndust vera með tíðaloftbrjóst (3). Yfirleitt eru þessi loftbrjóst hægra megin og erfitt getur verið að greina þau, enda eru þau oftast lítil (21, 28). Orsakir tíðaloftbrjósts eru á huldu (29) en í sumum tilfellum er það talið geta tengst legslímu-flakki (endometriosis) (30).


Klínísk skipting
Loftbrjóst er flokkað í sjálfkrafa loftbrjóst, áverkaloftbrjóst og loftbrjóst af læknisvöldum (tafla I) (31, 32). Sjálfkrafa loftbrjóst er sjúkdómur þar sem ekki er saga um áverka (9). Það er síðan flokkað í „prímert“ loftbrjóst þar sem lungnasjúkdómur er ekki fyrir hendi, og „sekúndert“ loftbrjóst, þar sem sjúklingurinn hefur þekktan lungnasjúkdóm (tafla II).
Einkenni og skoðun
Einkenni loftbrjósts er langoftast takverkur eða mæði sem versnar við áreynslu (33). Stundum fylgir þurr hósti. Einkenni geta gert vart við sig í áreynslu en algengara er að þau komi í hvíld, jafnvel í svefni (34). Sumir sjúklingar hafa engin einkenni, sérstaklega ef loftbrjóstið er lítið (35). Á hinn bóginn geta sjúklingar með lungnasjúkdóm haft alvarleg einkenni lungnabilunar þótt loftbrjóstið sé lítið. Mæði er yfirleitt mest áberandi hjá þessum sjúklingum og getur verið erfitt að aðgreina einkenni loftbrjósts frá lungnasjúkdómnum (14, 36).
Við skoðun sjúklinga með sjálfkrafa loftbrjóst er oft lítið að finna ef um lítið loftbrjóst er að ræða. Við stærra loftbrjóst getur sjúklingurinn orðið móður og hjartsláttur hraður. Í slíkum tilvikum eru minnkuð öndunarhljóð yfir samfallna lunganu og aukinn banktónn (heyrist best í holhönd með sjúklinginn í uppréttri stöðu).
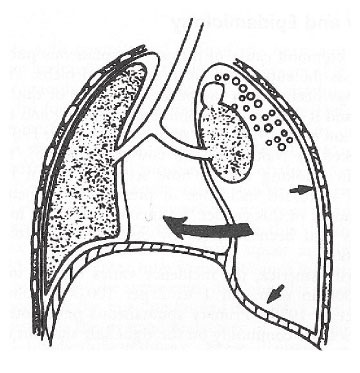
Mynd 1. Skematísk mynd af þrýstiloftbrjósti. Loft streymir út í fleiðruholið í gegnum einstefnuloka. Þrýstingur í fleiðruholinu hækkar smám saman og leiðir til þess að miðmæti færist til og þrýstingur verður á hjarta, stóru æðarnar í miðmæti og gagnstætt lunga.
Þrýstiloftbrjóst (tension pneumothorax) getur sést hjá öllum gerðum loftbrjósts en þá verður þrýstingur innan fleiðruhols í útöndun hærri en loftþrýstingur (37). Eins konar loki hefur þá myndast sem aðeins hleypir loftinu aðra leiðina. Loft safnast því fyrir í fleiðruholinu þar sem það kemst ekki út aftur (mynd 1). Við þetta getur orðið tilfærsla á miðmæti og loftbrjóstið þrýst á hjarta, miðmætisæðar og hitt lungað. Þrýstiloftbrjósti fylgja oftast mikil einkenni, svo sem andnauð, blámi og lost. Þetta er lífshættulegt ástand og krefst skjótra viðbragða sem felast í því að létta á þrýstingnum, til dæmis með ísetningu brjóstholskera eða með því að stinga nál í gegnum brjóstvegginn (38).
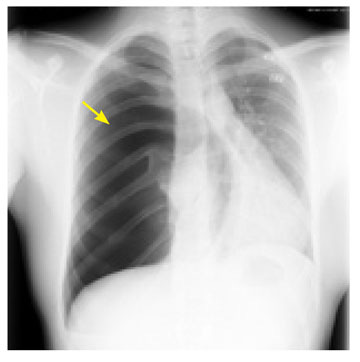
Mynd 2. Lungnamynd sem sýnir loftbrjóst hægra megin.

Greining
Oftast gefur saga sjúklings sterkar vísbendingar um greiningu. Mismunagreiningar eru þó margar (tafla III) og í sumum tilvikum getur verið um alvarlega sjúkdóma að ræða, eins og til dæmis bráða kransæðastíflu. Því er mikilvægt að staðfesta greininguna sem fyrst og er það gert með hefðbundinni lungnamynd. Auðveldast er að greina loftbrjóst á lungnamynd með sjúklinginn í uppréttri stöðu og útöndun (mynd 2) (39). Á lungnamynd sést samfall á lunga og loft milli þess og brjóstveggjar. Er hægt að meta gróflega stærð loftbrjóstsins.
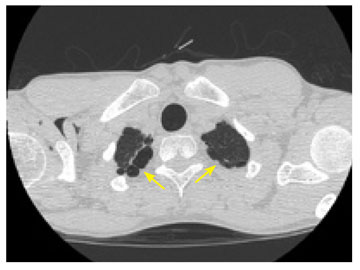
Mynd 3. Tölvusneiðmyndir af lungum sem sýna litlar blöðrur á toppi beggja lungna. Slíkar blöðrur eru dæmigerðar hjá sjúklingum með sjálfkrafa loftbrjóst (PSP).
Stundum eru einnig teknar tölvusneiðmyndir, sérstaklega í vafatilfellum (40, 41). Ekki er þó talin þörf á tölvusneiðmyndum sem rútínurannsókn við greiningu sjálfkrafa loftbrjósts. Á tölvusneiðmynd er auðvelt að sjá loftbrjóst sem getur verið erfitt að greina á lungnamynd, til dæmis þegar um er að ræða lítið loftbrjóst framan við lungað (41). Einnig er auðvelt að greina blöðrur á lungnatoppum og átta sig þannig betur á umfangi þeirra (mynd 3). Sumir sjúklingar hafa stóra blöðru eða blöðrur á lunga og getur verið mjög erfitt að aðgreina þær frá loftbrjósti á venjulegri lungnamynd. Í slíkum tilvikum geta tölvusneiðmyndir verið hjálplegar, ekki síst til að meta betur hvort ástæða sé til lungnaskurðaðgerðar (40).
Þrýstiloftbrjóst er fyrst og fremst klínísk greining, enda er oft sem ekki gefst tími til að senda slíka sjúklinga í myndrannsóknir (41). Mikilvæg mismunagreining er hjartaþröng (cardiac tamponade) (tafla III), en mjög erfitt getur verið að greina það frá þrýstiloftbrjósti.

Meðferð
Meðferð loftbrjósts felst aðallega í tvennu; annars vegar að fjarlægja loft úr fleiðruholinu og draga þannig út lungað og hins vegar að fyrirbyggja endurtekið loftbrjóst (31). Meðferðarúrræði eru mörg og eru þau helstu sýnd í töflu IV.
Bíða og sjá til: Meðferð ræðst bæði af stærð loftbrjóstsins og einkennum sjúklingsins. Ef minna en 20% samfall hefur orðið á lunganu kemur oft til greina að bíða og sjá til (31, 32, 42). Þetta á þó eingöngu við um sjúklinga með lítil eða engin einkenni. Ef sjúklingar eru hafðir undir eftirliti í nokkrar klukkustundir og loftbrjóst helst lítið er hægt að senda þessa sjúklinga heim og er þá fengin lungnamynd daginn eftir og önnur viku síðar. Ef loftleki hefur stöðvast sést hvernig loftbrjóstið minnkar strax á fyrstu tveimur sólarhringunum og yfirleitt er loftbrjóstið horfið innan viku (frásog lofts er í kringum 2% á sólarhring) (43). Inniliggjandi sjúklinga er æskilegt að meðhöndla með súrefni í nös, en súrefni frásogast hraðar en andrúmsloft og flýtir því frásogi loftbrjóstsins (43, 44).
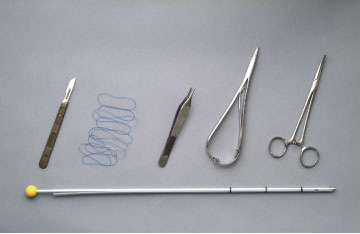
Mynd 4. Brjóstholskeri ásamt verkfærum fyrir ísetningu.

Mynd 5. Sogflaska.
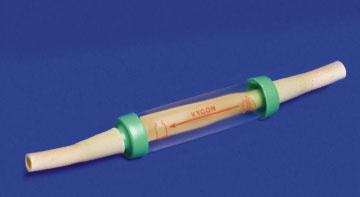
Mynd 6. Heimlich-loki.
Brjóstholskeri: Hjá sjúklingum með stórt loftbrjóst er fyrsta meðferð yfirleitt brjóstholskeri (45) sem tengdur er við sog (oftast -20 cm H2O) (myndir 4, 5). Yfirleitt er notast við tiltölulega svera kera (16F-22F). Hægt er að notast við minni kera (7F-14F) (46, 47) og getur þá verið hentugt að koma þeim fyrir í gegnum 2. rifjabil þar sem stutt er að toppi lungnanna. Hafa ber þó í huga að grannir kerar stíflast frekar en sverir. Sogið er oftast tengt við vegg og er sjúklingurinn þá bundinn við sjúkrastofuna. Til eru sérstök rafmagnssog sem unnt er að tengja við rafhlöður og eru sjúklingarnir þá frjálsari ferða sinna (48). Ekki er nauðsynlegt að beita sogi í meðferð loftbrjósts (31, 32, 42, 49). Til dæmis er hægt er að tengja kerann við Heimlich®-loku sem er einstefnuloki (50) og hóstar sjúklingurinn þá loftinu úr fleiðruholinu (mynd 6). Heimlich®-loki á þó ekki við ef loftleki er mikill. Í dag er til fjöldi loka á markaði sem svipar til Heimlich®-loka, til dæmis McSwain-loki® (51). Þessir lokar eru flestir fyrirferðarminni en Heimlich®-loki en galli við þá flesta er að þeir ráða illa við mikinn loftleka og eiga til að stíflast (31, 42). Þessir lokar eiga því síður við í meðferð sjúklinga með alvarlega lungnasjúkdóma og frekar er mælt með því að slíkir sjúklingar séu lagðir inn og meðhöndlaðir með brjóstholskera sem tengdur er við sog (42).
Oftast stöðvast loftleki eftir nokkurra daga sogmeðferð, eða í 80-90% tilvika við fyrsta loftbrjóst (52). Þetta hlutfall lækkar við hvert endurtekið loftbrjóst, til dæmis stöðvast loftleki einungis hjá 15% sjúklinga með þriðja loftbrjóst sömu megin (52). Meðferð með brjóstholskera er því árangursrík meðferð við fyrsta loftbrjósti og hún er talin vænlegri til árangurs en eingöngu lofttæming með nál (31, 32, 42). Þá er nál (til dæmis Kugelbergsnál®) (mynd 7) stungið í fleiðruholið og loftið sogað út með sprautu (53). Gallinn við þessa meðferð er sá að hún bregst í allt að helmingi tilfella (54), sérstaklega hjá eldri sjúklingum og þeim sem eru með stórt loftbrjóst (>2,5 L) (55). Almennt er því lofttæming með nál talin síðri kostur en meðferð með kera og sogi (42).
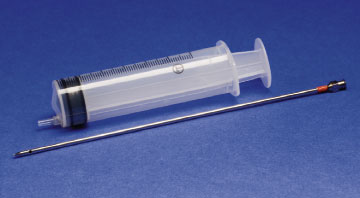
Mynd 7. Kugelbergsnál sem nota má til að tæma loft úr fleiðruholi.
Brjóstholskeri er oftast hafður í að minnsta kosti tvo sólarhringa. Þetta er þó umdeilt og sumir fjarlægja kerann fyrr ef loftleki hefur stöðvast (49). Þegar liðnar eru 12-24 klukkustundir án þess að loftleki hafi gert vart við sig er yfirleitt óhætt að fjarlægja kerann. Auðvelt er að sjá hvort loftleki er til staðar með því að kíkja eftir loftbólum í vatnslásnum á sogflöskunni þegar sjúklingurinn er látinn hósta. Algengast er að loka fyrir kerann áður en hann er fjarlægður (42) en slíkt er ekki nauðsynlegt (56). Síðan er lungnamynd með sjúklinginn í uppréttri stöðu fengin nokkrum klukkustundum síðar. Greinist loftbrjóst ekki á þessum myndum er kerinn fjarlægður. Auðveldast er að fjarlægja kerannn með því að draga hann út um leið og sjúklingurinn hóstar. Daginn eftir eru lungun mynduð og aftur viku síðar. Einnig er æskilegt að fá nýja lungnamynd að mánuði liðnum. Ef sjúklingur er einkennalaus er yfirleitt ekki talin þörf á frekara eftirliti.

Þótt ekki sé um stórt inngrip að ræða getur ísetning brjóstholskera haft fylgikvilla í för með sér, eða í allt að fjórðungi tilfella eftir rannsóknum ( 45, 57). Oftast er þó um minniháttar fylgikvilla að ræða, svo sem verki og blæðingar (tafla V). Einnig getur komið fyrir að keranum sé stungið í gegnum þindina og þaðan í lifur eða milta. Endurtekið loftbrjóst og viðvarandi loftleki eru þó algengari fylgikvillar. Til dæmis er talið að í kringum 30% sjúklinga (16-52% eftir rannsóknum) fái loftbrjóst að nýju eftir meðferð með brjóstholskera og er algengast að það greinist 6-48 mánuðum frá upphaflega loftbrjóstinu (58-61). Tíðni endurtekins loftbrjósts hækkar við hvert endurtekið loftbrjóst (62) og eftir þriðja loftbrjóst eru líkur á endurteknu loftbrjósti meiri en 50% (5, 63). Sýnt hefur verið fram á að ungt fólk og þeir sem reykja eru í aukinni hættu á endurteknu loftbrjósti (59, 60).
Annar algengur fylgikvilli er viðvarandi loftleki og er talið að í kringum þriðjungur sjúklinga (20-39%) hafi loftleka eftir viku meðferð með brjóstholskera (32, 64). Þetta hlutfall lækkar óverulega eftir 10 daga meðferð. Flestir brjóstholsskurðlæknar telja því loftleka sem varað hefur lengur en 4-7 daga vera ábendingu fyrir skurðaðgerð (sjá nánar síðar) (42, 65, 66). Annað úrræði í meðferð viðvarandi loftleka er að sprauta efnum (sclerosing agents) í gegnum kerann sem örva myndun samvaxta í fleiðruholinu (chemical pleurodesis). Hægt er að nota ýmis efni, til dæmis mepacrine, tetracyklín (67, 68), talkúm (69, 70) eða blóð (71). Árangur hjá sjúklingum með loftbrjóst er hins vegar lakari en fyrir önnur meðferðarúrræði (til dæmis vegna fleiðruvökva af völdum krabbameina), og allt að 25% sjúklinga (8-25%) fá endurtekið loftbrjóst innan fimm ára (58, 73). Í stað ertandi efna er því frekar mælt með skurðaðgerð hjá sjúklingum með viðvarandi loftleka (8, 32, 42).
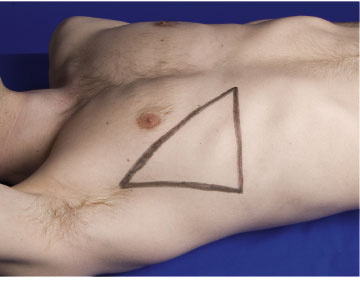
Mynd 8. „Öruggi þríhyrningurinn“ fyrir ísetningu brjóstholskera.
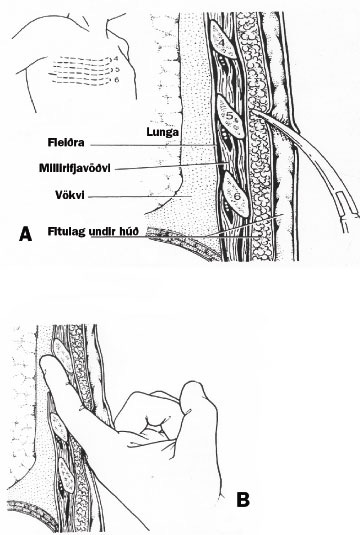
Mynd 9 A og B. Skematísk mynd af opinni aðferð við að koma fyrir brjóstholskera.
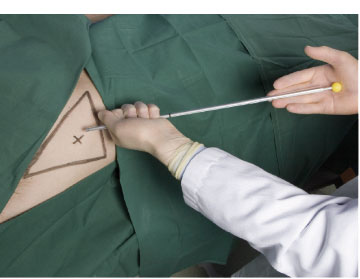
Mynd 10. Yfirlitsmynd af ísetningu brjóstholskera. Mikilvægt er að halda vinstri hendi þétt að keranum tiltölulega nálægt spjótsendanum. Með þessu er verið að fyrirbyggja að spjótið stingist of djúpt og skaði innri líffæri við ísetninguna.
Ísetning brjóstholskera
Brjóstholskera er yfirleitt komið fyrir í 4. eða 5. rifjabili fyrir miðri holhönd. Mikilvægt er að halda sig innan ?örugga þríhyrningsins? sem af afmarkast af þremur vöðvum, pectoralis major að framan, latissimus dorsi að aftan og þind að neðan (mynd 8) (74). Einnig er hægt að koma keranum fyrir í 2. rifjabili undir miðju viðbeini. Áður var þetta algengasta staðsetningin en nú er mælt með 4. eða 5. rifjabili (75). Ástæðan er minni hætta á blæðingu (aðallega frá a. thoracica interna) og að í ?örugga þríhyrningnum? þarf ekki að fara í gegnum eins þykka vöðva.
Við ísetningu er húðin þrifin með sótthreinunarlausn til að minnka líkur á sýkingu. Síðan er staðdeyfingu (til dæmis lidocaini) sprautað í rifjabilið. Mikilvægt er að deyfa fleiðruna á innanverðum brjóstvegg en þar er næmt sársaukaskyn. Auðveldast er að stinga sprautunni beint inn í fleiðruholið (loft sogast í sprautuna) og bakka henni síðan í gegnum brjóstvegg um leið og deyfingu er sprautað í vöðva og mjúkvef. Nálinni er alltaf stungið höfuðmegin (ofan) við rifið til að forðast æðar og taugar. Kerinn er lagður langt inn þannig að endinn liggi efst í fleiðruholinu.
Keranum er hægt að koma fyrir með opinni aðferð og með tækni þar sem notast er við spjót (trochar) (45, 75, 76). Erlendis er víða mælt með opnu aðferðinni (75, 76), sérstaklega ef um alvarlega fjöláverka er að ræða og ef lungnamynd liggur ekki fyrir. Einnig er mælt með henni fyrir lækna sem hafa takmarkaða reynslu af ísetningu brjóstholskera. Hún er talin öruggari og minnkar líkur á stunguáverkum á líffæri í brjóstholinu (til dæmis á hjarta og holæð). Á hinn bóginn er skurður við opnu aðferðina stærri og ör meira áberandi (75, 77).
Við opna aðferð er gerður lítill húðskurður (3-4 cm) og æðatöng notuð til að útbúa lítil göng í gegnum brjóstvegg (mynd 9A). Fingri er stungið gegnum göngin sem gerir kleift að þreifa eftir yfirborði lungans og leita að samvöxtum í fleiðruholi (mynd 9B) (75). Því næst er keranum stýrt á rétt-an stað með því að stinga töng inn í hliðargöt á keranum.
Við hina aðferðina er spjóti komið fyrir inni í keranum (mynd 10) og því síðan stungið í gegnum í brjóstvegg ofan við rifbein. Áður hefur verið útbúið gat með æðatöng til að auðvelda stungu með spjótinu. Annarri hendi er haldið við spjótsendann og hinni um kerann nálægt brjóstveggnum. Þannig eru minni líkur til þess að oddhvass spjótsendinn stingist of djúpt inn í brjóstholið. Spjótsendinn er eingöngu notaður til að komast í gegnum brjóstvegg og er honum síðan bakkað nokkra cm. Spjótið er engu að síður hægt að nota til að stýra keranum á réttan stað í fleiðruholi að því gefnu að oddhvassa endanum hafi áður verið hnikað nokkra cm til baka frá enda kerans.

Mynd 11. Talkúm-duft. Duftinu er blandað við deyfivökva og lausninni sprautað inn í brjóstholið í gegnum brjóstholskerann
Skurðaðgerð (og fleiðruerting)
Eins og áður kom fram er algengt að loftleki stöðvist ekki og þarf þá að grípa til skurðaðgerðar (8). Algengasta ábending fyrir skurðaðgerð er þó síðkomið endurtekið loftbrjóst sömu megin. Áður fyrr var skurðaðgerð beitt við þriðja loftbrjóst, það er aðra endurtekningu. Í dag eru hins vegar margir þeirrar skoðunar að fyrsta endurtekning sé ábending fyrir skurðaðgerð (8, 32, 42). Skurðaðgerð á einnig við hjá sjúklingum með loftbrjóst beggja vegna (78) og ef saga er um þrýstiloftbrjóst (8). Atvinna og búseta getur einnig skipt máli, til dæmis getur fyrsta loftbrjóst verið ábending fyrir skurðaðgerð hjá flugmönnum, sjómönnum og köfurum sem og hjá sjúklingum sem búa afskekkt (79, 80).
Sjúklingar með þekktan lungnasjúkdóm eru ekki síður taldir hafa gagn af skurðaðgerð, jafnvel eftir fyrsta loftbrjóst (32). Skurðaðgerð kemur þó einungis til greina ef áhætta við svæfingu og aðgerð er ekki talin of mikil vegna lungnasjúkdómsins (81, 82). Í slíkum tilvikum kemur til greina að nota talkúm og er því sprautað inn í kerann ásamt staðdeyfingarlausn (mynd 11). Talkúm er öflugt þéttiefni og yfirleitt er nóg að notast við 2 grömm í stað stærri skammta (5g) líkt og gert er þegar talkúm er notað til að fyrirbyggja fleiðruvökva (83). Talkúm er tiltölulega hættulítið efni en sjúklingar geta fengið heiftarlega verki (84, 85). Nota má utanbastsdeyfingu til að minnka verki. Þar sem lítið er vitað um langtímaáhrif talkúms, til dæmis hvað varðar verki, er yfirleitt ekki mælt með notkun þess hjá ungum einstaklingum (8, 42).
Helsta markmið skurðaðgerða er að uppræta loftlekann. Í sömu aðgerð er síðan hægt að örva samvexti og koma þannig í veg fyrir endurtekið loftbrjóst. Sá hluti lungans sem lekur er numinn brott með heftibyssu (fleygskurður). Sumir telja fleygskurð duga (86), aðrir ekki (87-89). Hægt er að mynda samvexti með því að fjarlægja hluta fleiðrunnar á innanverðu brjóstholinu (partial pleurectomy) (90, 91), en algengara er að erta fleiðruna með grisju eða sandpappír (mechanical pleurodesis) (92). Einnig kemur til greina að notast við ertandi efni, til dæmis talkúm (sjá áður).
Skurðaðgerðir er bæði hægt að framkvæma með opinni aðgerð og brjóstholsspeglun. Í dag eru speglunaraðgerðir mun algengari en opnar aðgerðir (11, 88, 93). Þær eru yfirleitt taldar hagkvæmari en þetta er þó umdeilt (65). Sjúklingarnir hafa í flestum rannsóknum minni verki eftir brjóstholsspeglunaraðgerð og útskrifast fyrr af sjúkrahúsi (11, 88, 93-98). Endurtekið loftbrjósts er þó algengara eftir brjóstholsspeglun (2-14%) (11, 12, 93, 99) en við hefðbundna opna aðgerð (0-7%) (86, 100, 101), eða allt að þrefalt algengara. Þetta hefur meðal annars verið staðfest með nýlegri íslenskri rannsókn (7). Hins vegar eru krónískir verkir algengari eftir opna aðgerð (97, 102) og ör meira áberandi. Til eru margar erlendar rannsóknir þar sem þessar aðgerðir hafa verið bornar saman (97, 100, 101). Fæstar þeirra eru þó slembaðar og oft er um tiltölulega lítinn efnivið að ræða. Ljóst er að frekar rannsókna er að fleiri og ítarlegri rannsókna er þörf.
Brjóstholsspeglunaraðgerð: Sjúklingarnir eru svæfðir með tvöfaldri berkjupípu (double lumen intubation). Þannig er að hægt að fella saman lungað sem verið er að laga í aðgerðinni. Sjúklingur er lagður í 90° hliðarlegu og lunganu haldið samanföllnu með CO2 sem blásið er inn í fleiðruholið. Síðan er þremur holstingjum (trocars) komið fyrir í brjóstholinu, þar af er einum fyrir myndavél sem tengd er við brjóstholssjá (mynd 12) (80).
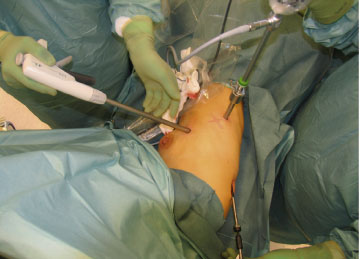
Mynd 12. Brjósthols-speglunaraðgerð við sjálfkrafa loftbrjósti. Sjá nánari lýsingu á aðgerðinni í texta.
Töngum og öðrum verkfærum er síðan komið fyrir í gegnum hin götin, meðal annars sérstakri heftibyssu. Heftibyssan er notuð til að hefta fyrir og fjarlægja þær blöðrur sem finnast á lunganu (fleygskurður). Oft er fleiðran ert auk fleygskurðarins, ýmist með sandpappír eða grisju og í einstaka tilfellum með talkúmi (eldri einstaklingar). Loks er hægt að fjarlægja hluta fleiðrunnar, oftast fyrir ofan lungnatoppana.
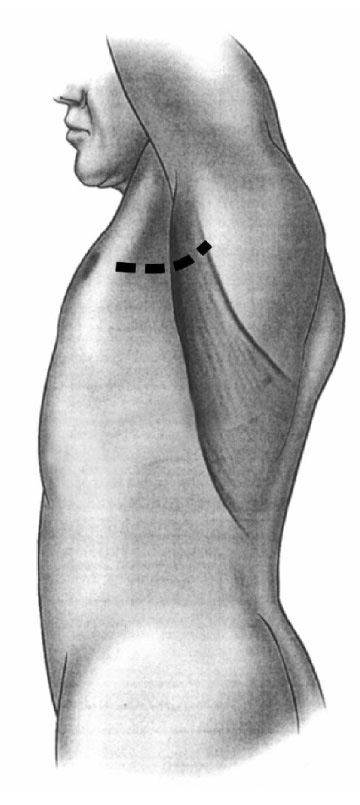
Mynd 13. Opinn brjóstholsskurður (lateral/axillary mini-thoracotomy). Sjá nánar í texta.
Opnar aðgerðir: Svæfing og uppstilling sjúklings er svipuð og í brjóstholsspeglunaraðgerð. Yfirleitt er gerður 6-10 cm brjóstveggsskurður (mynd 13), langoftast í gegnum 3.-4. millirifjabil (mini-?axillary thoracotomy) (103). Lungað er lekaprófað með vatni og síðan framkvæmdur fleygskurður, með eða án fleiðruertingar, á svipaðan hátt og í brjóstholsspeglunaraðgerð.
Fylgikvillar skurðaðgerða: Opnar aðgerðir og aðgerðir með brjóstholssjá verða að teljast mjög öruggar. Til dæmis lést enginn af 234 sjúklingum í íslensku rannsókninni sem áður var getið (7). Erlendis er skurðdauði (dánir <30 daga frá aðgerð) yfirleitt í kringum 0-2% (11, 12, 65, 88, 93). Rétt er þó að geta þess að dánartíðni í mismunandi rannsóknum fer mjög eftir því hversu hátt hlutfall er af sjúklingum með alvarlega lungnasjúkdóma og þetta hlutfall er frekar lágt hér á landi (5% samanborið við 10-40% í erlendum rannsóknum)(10-12). En þótt fáir látist eftir aðgerð eru skurðaðgerðir við loftbrjósti ekki lausar við fylgikvilla. Blæðingar og sýkingar geta gert vart við sig enda þótt þær séu tiltölulega sjaldgæfar (<3%). Mun algengari eru viðvarandi loftleki (3-15%) (11, 80, 88, 93) og endurtekið loftbrjóst (3-8%) (11, 12, 87, 88, 93) sem oftast krefjast skurðaðgerðar, sérstaklega eftir brjóstholsspeglun. Þrefalt hærri tíðni enduraðgerða eftir brjóstholsspeglun er áhyggjuefni og getur haft þýðingu þegar velja á aðgerð, til dæmis hjá sjúklingum þar sem endurtekið loftbrjóst er mjög óæskilegt (svo sem hjá flugmönnum og köfurum) eða hættulegt (sjúklingar með alvarlegan lungnasjúkdóm). Það er þó ekki þar með sagt að brjóstholsspeglunaraðgerðir eigi ekki rétt á sér. Eins og áður sagði eru þessar aðgerðir yfirleitt taldar þægilegri fyrir sjúklingana þar sem þær valda minni verkjum (97, 98) og ör eru minna áberandi. Hvort tveggja hefur átt sinn þátt í því að speglunaraðgerðir hafa rutt sér til rúms á kostnað hefðbundinna opinna aðgerða (11, 88, 93). Þar að auki liggja þessir sjúklingar skemur á sjúkrahúsi og margir komast fyrr til vinnu (93, 97). Á móti kemur aukinn kostnaður í tengslum við endurinnlagnir og enduraðgerðir.
Lokaorð
Í flestum tilvikum er loftbrjóst frekar hættulítill sjúkdómur sem greinist í ungum einstaklingum, hraustum að öðru leyti. Í tilteknum tilvikum getur hins vegar verið um hættulegan sjúkdóm að ræða, til dæmis hjá sjúklingum með þrýstiloftbrjóst og þeim sem hafa alvarlega lungnasjúkdóma. Þessir sjúklingar geta verið í lífshættu og skjót greining og meðferð skipta sköpum. Loftbrjóst er auðvelt að greina á hefðbundinni lungnamynd en í vafatilfellum er hægt að notast við tölvusneiðmyndir. Ef um stórt loftbrjóst er að ræða er brjóstholskeri sem tengdur er við sog yfirleitt fyrsta meðferð. Slík meðferð dugar þó ekki alltaf og við endurtekið loftbrjóst eða viðvarandi loftleka verður oft að grípa til skurðaðgerðar. Í skurðaðgerðum er loftleki stöðvaður með því að fjarlægja blöðrur á lungnatoppum og samvaxtamyndun í fleiðruholi örvuð. Skurðaðgerðir er hægt að framkvæma bæði með opinni aðgerð og brjóstholsspeglun. Síðarnefndu aðgerðirnar valda minni verkjum, sjúklingarnir dvelja skemur á sjúkrahúsi og komast fyrr til vinnu. Hins vegar er tíðni endurtekins loftbrjósts og viðvarandi loftleka umtalsvert hærri eftir brjóstholsspeglunaraðgerðirnar og mikilvægt að finna lausn á því í nánustu framtíð.
Þakkir
Fær Þórdís Erla Ágústsdóttir ljósmyndari á Landspítala fyrir töku ljósmynda. Gunnhildur Jóhannsdóttir ritari á skurðdeild Landspítala og Bjarni Geir Viðarsson deildarlæknir fá einnig þakkir fyrir aðstoð við öflun heimilda og gerð mynda.
Heimildir
- Bense L, Eklund G, Wiman LG. Smoking and the increased risk of contracting spontaneous pneumothorax. Chest 1987; 92: 1009-12.
- Melton LJ, 3rd, Hepper NG, Offord KP. Incidence of spontaneous pneumothorax in Olmsted County, Minnesota: 1950 to 1974. Am Rev Respir Dis 1979; 120: 1379-82.
- Nakamura H, Konishiike J, Sugamura A, Takeno Y. Epidemiology of spontaneous pneumothorax in women. Chest 1986; 89: 378-82.
- Primrose WR. Spontaneous pneumothorax: a retrospective review of aetiology, pathogenesis and management. Scott Med J 1984; 29: 15-20.
- Hallgrímsson JG. Spontaneous pneumothorax in Iceland with special reference to the idiopathic type: a clinical and epidemiological investigation. Scand J Thorac Cardiovasc Surg 1978; Suppl 21: 1-74.
- Steinbach R, Ólafsson G. Sjúklingar með sjálfkrafa loftbrjóst vistaðir á Landspítalanum 1975-1984. Læknablaðið 1986; 73: 88-92.
- Tómasdóttir G, Torfason B, Ísaksson H, Guðbjartsson T. Samanburður á opnum aðgerðum og aðgerðum með brjóstholssjá við sjálfkrafa loftbrjósti. Læknablaðið 2007; 93: 403-10.
- Pearson FG, Cooper JD, Deslaurier JG. Thoracic Surgery. 2nd ed. Philadelphia: Churchill Livingstone; 2002.
- Light RW. Management of spontaneous pneumothorax. Am Rev Respir Dis 1993; 148: 245-8.
- Gupta D, Hansell A, Nichols T, Duong T, Ayres JG, Strachan D. Epidemiology of pneumothorax in England. Thorax 2000; 55: 666-71.
- Mouroux J, Elkaim D, Padovani B, Myx A, Perrin C, Rotomondo C, et al. Video-assisted thoracoscopic treatment of spontaneous pneumothorax: technique and results of one hundred cases. J Thorac Cardiovasc Surg 1996; 112: 385-91.
- Passlick B, Born C, Haussinger K, Thetter O. Efficiency of video-assisted thoracic surgery for primary and secondary spontaneous pneumothorax. Ann Thorac Surg. 1998; 65: 324-7.
- George RB, Herbert SJ, Shames JM, Ellithorpe DB, Weill H, Ziskind MM. Pneumothorax complicating pulmonary emphysema. JAMA 1975; 234: 389-93.
- Shields TW, Oilschlager GA. Spontaneous pneumothorax in patients 40 years of age and older. Ann Thorac Surg 1966; 2: 377-83.
- Videm V, Pillgram-Larsen J, Ellingsen O, Andersen G, Ovrum E. Spontaneous pneumothorax in chronic obstructive pulmonary disease: complications, treatment and recurrences. Eur J Respir Dis 1987; 71: 365-71.
- Mendez JL, Nadrous HF, Vassallo R, Decker PA, Ryu JH. Pneumothorax in pulmonary Langerhans cell histiocytosis. Chest 2004; 125: 1028-32.
- Johnson SR. Lymphangioleiomyomatosis. Eur Respir J 2006; 27: 1056-65.
- Edge J, Simon G, Reid L. Peri-acinar (paraseptal) emphysema: its clinical, radiological, and physiological features. Br J Dis Chest 1966;60: 10-8.
- Baronofsky ID, Warden HG, Kaufman JL, Whatley J, Hanner JM. Bilateral therapy for unilateral spontaneous pneumothorax. J Thorac Surg 1957; 34: 310-9; discussion 9-22.
- Ikeda M, Uno A, Yamane Y, Hagiwara N. Median sternotomy with bilateral bullous resection for unilateral spontaneous pneumothorax, with special reference to operative indications. J Thorac Cardiovasc Surg 1988; 96: 615-20.
- Sabiston, Spencer. Surgery of the Chest. 5th ed; 1990.
- Hunninghake GW, Crystal RG. Cigarette smoking and lung destruction. Accumulation of neutrophils in the lungs of cigarette smokers. Am Rev Respir Dis 1983; 128: 833-8.
- Robbins RA, Gossman GL, Nelson KJ, Koyama S, Thompson AB, Rennard SI. Inactivation of chemotactic factor inactivator by cigarette smoke. A potential mechanism of modulating neutrophil recruitment to the lung. Am Rev Respir Dis 1990; 142: 763-8.
- Teoh PC. Bronchiectasis and spontaneous pneumothorax in Marfan‘s syndrome. Chest 1977; 72: 672-3.
- Margaliot SZ, Barzilay J, Bar-David M, Lewis BS, Froom P, Forecast D, et al. Spontaneous pneumothorax and mitral valve prolapse. Chest 1986; 89: 93-4.
- Mattei P, Wiebke E, Lipsett P. Tension pneumothorax as a presentation of traumatic diaphragmatic hernia. South Med J 1992; 85: 847-50.
- Joseph J, Sahn SA. Thoracic endometriosis syndrome: new observations from an analysis of 110 cases. Am J Med 1996; 100: 164-70.
- Carter EJ, Ettensohn DB. Catamenial pneumothorax. Chest 1990; 98: 713-6.
- Fonseca P. Catamenial pneumothorax: a multifactorial etiology. J Thorac Cardiovasc Surg 1998; 116: 872-3.
- Marshall MB, Ahmed Z, Kucharczuk JC, Kaiser LR, Shrager JB. Catamenial pneumothorax: optimal hormonal and surgical management. Eur J Cardiothorac Surg 2005; 27: 662-6.
- Griffith Pearson JDC F, Deslaurier J, Ginsberg RJ, et al. Thoracic Surgery 2nd ed. Philadelphia: Churchill Livingstone; 2002.
- Sahn SA, Heffner JE. Spontaneous pneumothorax. N Engl J Med 2000; 342: 868-74.
- DeVries WC, Wolfe WG. The management of spontaneous pneumothorax and bullous emphysema. Surg Clin North Am 1980; 60: 851-66.
- Bense L, Wiman LG, Hedenstierna G. Onset of symptoms in spontaneous pneumothorax: correlations to physical activity. Eur J Respir Dis 1987; 71: 181-6.
- Seremetis MG. The management of spontaneous pneumothorax. Chest 1970; 57: 65-8.
- Tanaka F, Itoh M, Esaki H, Isobe J, Ueno Y, Inoue R. Secondary spontaneous pneumothorax. Ann Thorac Surg 1993; 55: 372-6.
- Gustman P, Yerger L, Wanner A. Immediate cardiovascular effects of tension pneumothorax. Am Rev Respir Dis 1983; 127: 171-4.
- Rivarola C. Tension pneumothorax. Philadelphia: Mosby-Year Book; 1990.
- Bradley M, Williams C, Walshaw MJ. The value of routine expiratory chest films in the diagnosis of pneumothorax. Arch Emerg Med 1991; 8: 115-6.
- Bourgouin P, Cousineau G, Lemire P, Hebert G. Computed tomography used to exclude pneumothorax in bullous lung disease. J Can Assoc Radiol 1985; 36: 341-2.
- O‘Connor AR, Morgan WE. Radiological review of pneumothorax. BMJ 2005; 330: 1493-7.
- Baumann MH, Strange C, Heffner JE, Light R, Kirby TJ, Klein J, et al. Management of spontaneous pneumothorax: an American College of Chest Physicians Delphi consensus statement. Chest 2001; 119: 590-602.
- Northfield TC. Oxygen therapy for spontaneous pneumothorax. BMJ 1971; 4: 86-8.
- Hill RC, DeCarlo DP, Jr., Hill JF, Beamer KC, Hill ML, Timberlake GA. Resolution of experimental pneumothorax in rabbits by oxygen therapy. Ann Thorac Surg 1995; 59: 825-7; discussion 7-8.
- Miller KS, Sahn SA. Chest tubes. Indications, technique, management and complications. Chest 1987; 91: 258-64.
- Conces DJ, Jr., Tarver RD, Gray WC, Pearcy EA. Treatment of pneumothoraces utilizing small caliber chest tubes. Chest 1988; 94: 55-7.
- Martin T, Fontana G, Olak J, Ferguson M. Use of pleural catheter for the management of simple pneumothorax. Chest 1996; 110: 1169-72.
- Curran JF, Stanek KS, Kacmarek RM. Portable airway-suction systems: a comparison of performance. Respir Care 1991; 36: 259-66.
- So SY, Yu DY. Catheter drainage of spontaneous pneumothorax: suction or no suction, early or late removal? Thorax 1982; 37: 46-8.
- Mercier C, Page A, Verdant A, Cossette R, Dontigny L, Pelletier LC. Outpatient management of intercostal tube drainage in spontaneous pneumothorax. Ann Thorac Surg 1976; 22: 163-5.
- Wayne MA, McSwain NE, Jr. Clinical evaluation of a new device for the treatment of tension pneumothorax. Ann Surg 1980; 191: 760-2.
- Jain SK, Al-Kattan KM, Hamdy MG. Spontaneous pneumothorax: determinants of surgical intervention. J Cardiovasc Surg 1998; 39: 107-11.
- Kugelberg J. [Blunt needle for easier pleura punction]. Lakartidningen 1969; 66: 4715.
- Delius RE, Obeid FN, Horst HM, Sorensen VJ, Fath JJ, Bivins BA. Catheter aspiration for simple pneumothorax. Experience with 114 patients. Arch Surg 1989; 124: 833-6.
- Soulsby T. British Thoracic Society guidelines for the management of spontaneous pneumothorax: do we comply with them and do they work? J Accid Emerg Med 1998; 15: 317-21.
- Miller AC, Harvey JE. Guidelines for the management of spontaneous pneumothorax. Standards of Care Committee, British Thoracic Society. BMJ 1993; 307: 114-6.
- Etoch SW, Bar-Natan MF, Miller FB, Richardson JD. Tube thoracostomy. Factors related to complications. Arch Surg 1995; 130: 521-5; discussion 5-6.
- Light RW, O‘Hara VS, Moritz TE, McElhinney AJ, Butz R, Haakenson CM, et al. Intrapleural tetracycline for the prevention of recurrent spontaneous pneumothorax. Results of a Department of Veterans Affairs cooperative study. JAMA 1990; 264: 2224-30.
- Lippert HL, Lund O, Blegvad S, Larsen HV. Independent risk factors for cumulative recurrence rate after first spontaneous pneumothorax. Eur Respir J 1991; 4: 324-31.
- Sadikot RT, Greene T, Meadows K, Arnold AG. Recurrence of primary spontaneous pneumothorax. Thorax 1997; 52: 805-9.
- Committee BTSR. Comparison of simple aspiration with intercostal drainage in the management of sontaneous pneumothorax. Thorax 1993: 48: 430-31.
- Schramel FM, Postmus PE, Vanderschueren RG. Current aspects of spontaneous pneumothorax. Eur Respir J 1997; 10: 1372-9.
- Cran IR, Rumball CA. Survey of spontaneous pneumothoraces in the Royal Air Force. Thorax 1967; 22: 462-5.
- Schoenenberger RA, Haefeli WE, Weiss P, Ritz RF. Timing of invasive procedures in therapy for primary and secondary spontaneous pneumothorax. Arch Surg 1991; 126: 764-6.
- Baumann MH, Strange C. Treatment of spontaneous pneumothorax: a more aggressive approach? Chest 1997; 112: 789-804.
- Granke K, Fischer CR, Gago O, Morris JD, Prager RL. The efficacy and timing of operative intervention for spontaneous pneumothorax. Ann Thorac Surg 1986; 42: 540-2.
- Alfageme I, Moreno L, Huertas C, Vargas A, Hernandez J, Beiztegui A. Spontaneous pneumothorax. Long-term results with tetracycline pleurodesis. Chest 1994; 106: 347-50.
- Chen JS, Hsu HH, Chen RJ, Kuo SW, Huang PM, Tsai PR, et al. Additional minocycline pleurodesis after thoracoscopic surgery for primary spontaneous pneumothorax. Am J Respir Crit Care Med 2006; 173: 548-54.
- Cardillo G, Carleo F, Giunti R, Carbone L, Mariotta S, Salvadori L, et al. Videothoracoscopic talc poudrage in primary spontaneous pneumothorax: a single-institution experience in 861 cases. J Thorac Cardiovasc Surg 2006; 131: 322-8.
- Milanez JR, Vargas FS, Filomeno LT, Fernandez A, Jatene A, Light RW. Intrapleural talc for the prevention of recurrent pneumothorax. Chest 1994; 106: 1162-5.
- Robinson CL. Autologous blood for pleurodesis in recurrent and chronic spontaneous pneumothorax. Can J Surg 1987; 30: 428-9.
- Tan C, Sedrakyan A, Browne J, Swift S, Treasure T. The evidence on the effectiveness of management for malignant pleural effusion: a systematic review. Eur J Cardiothorac Surg 2006; 29: 829-38.
- Almind M, Lange P, Viskum K. Spontaneous pneumothorax: comparison of simple drainage, talc pleurodesis, and tetracycline pleurodesis. Thorax 1989; 44: 627-30.
- Peek GJ, Morcos S, Cooper G. The pleural cavity. BMJ 2000; 320: 1318-21.
- Advanced Trauma Life Support for Doctors. In: Trauma ACoSCo, editor. Student course manual. 6th ed; 1997: 129.
- Almquist M, Palsson B, Gyllstedt E. Pleural drainage in trauma. Lakartidningen 2004; 101: 2016-8, 21-2.
- Ivert T, Orre L. A chest tube can be inserted safely utilizing standard technique. Minithoracotomy should not be performed routinely. Lakartidningen 2003; 100: 2366-9.
- Graf-Deuel E, Knoblauch A. Simultaneous bilateral spontaneous pneumothorax. Chest 1994; 105: 1142-6.
- Clark TA, Hutchison DE, Deaner RM, Fitchett VH. Spontaneous pneumothorax. Am J Surg 1972; 124: 728-31.
- Ingólfsson IG, Gyllstedt E, Pikwer A, Lillo-Gil R, Jönsson P, Guðbjartsson T. Reoperations are common following VATS for spontaneous pneumothorax: study of risk factors. Interact CardioVasc Thorac Surg 2006; 5: 602-7.
- Graham AN, McManus KG, McGuigan JA. Videothoracoscopy and spontaneous pneumothorax. Ann Thorac Surg 1995; 59: 266-7.
- Waller DA, Forty J, Soni AK, Conacher ID, Morritt GN. Videothoracoscopic operation for secondary spontaneous pneumothorax. Ann Thorac Surg 1994; 57: 1612-5.
- Kennedy L, Sahn SA. Talc pleurodesis for the treatment of pneumothorax and pleural effusion. Chest 1994; 106: 1215-22.
- Kennedy L, Vaughan LM, Steed LL, Sahn SA. Sterilization of talc for pleurodesis. Available techniques, efficacy, and cost analysis. Chest 1995; 107: 1032-4.
- Froudarakis ME, Klimathianaki M, Pougounias M. Systemic inflammatory reaction after thoracoscopic talc poudrage. Chest 2006; 129: 356-61.
- Korner H, Andersen KS, Stangeland L, Ellingsen I, Engedal H. Surgical treatment of spontaneous pneumothorax by wedge resection without pleurodesis or pleurectomy. Eur J Cardiothorac Surg 1996; 10: 656-9.
- Inderbitzi RG, Leiser A, Furrer M, Althaus U. Three years‘ experience in video-assisted thoracic surgery (VATS) for spontaneous pneumothorax. J Thorac Cardiovasc Surg 1994; 107: 1410-5.
- Lang-Lazdunski L, Chapuis O, Bonnet PM, Pons F, Jancovici R. Videothoracoscopic bleb excision and pleural abrasion for the treatment of primary spontaneous pneumothorax: long-term results. Ann Thorac Surg 2003; 75: 960-5.
- Massard G, Thomas P, Wihlm JM. Minimally invasive management for first and recurrent pneumothorax. Ann Thorac Surg 1998; 66: 592-9.
- Caes F, Cham B, Van den Brande P, Welch W. Transaxillary thoracotomy for treatment of spontaneous pneumothorax. Acta Chir Belg 1987; 87: 137-41.
- Weeden D, Smith GH. Surgical experience in the management of spontaneous pneumothorax, 1972-82. Thorax 1983; 38: 737-43.
- Pairolero P, Payne S. The surgical management of recurrent of persistent pneumothorax: Abrasive pleurodesis. In: Kittle F, editor. Current Controversies in Thoracic Surgery. Philadelphia: WB Saunders; 1986: 43.
- Bertrand PC, Regnard JF, Spaggiari L, Levi JF, Magdeleinat P, Guibert L, et al. Immediate and long-term results after surgical treatment of primary spontaneous pneumothorax by VATS. Ann Thorac Surg 1996; 61: 1641-5.
- De Giacomo T, Rendina EA, Venuta F, Ciriaco P, Lena A, Ricci C. Video-assisted thoracoscopy in the management of recurrent spontaneous pneumothorax. Eur J Surg 1995; 161: 227-30.
- Dumont P, Diemont F, Massard G, Toumieux B, Wihlm JM, Morand G. Does a thoracoscopic approach for surgical treatment of spontaneous pneumothorax represent progress? Eur J Cardiothorac Surg 1997; 11: 27-31.
- Melvin WS, Krasna MJ, McLaughlin JS. Thoracoscopic management of spontaneous pneumothorax. Chest 1992; 102: 1877-9.
- Waller DA, Forty J, Morritt GN. Video-assisted thoracoscopic surgery versus thoracotomy for spontaneous pneumothorax. Ann Thorac Surg 1994; 58: 372-6; discussion 6-7.
- Waller DA, Yoruk Y, Morritt GN, Forty J, Dark JH. Videothoracoscopy in the treatment of spontaneous pneumothorax: an initial experience. Ann R Coll Surg Engl 1993; 75: 237-40.
- Yim AP, Liu HP. Video assisted thoracoscopic management of primary spontaneous pneumothorax. Surg Laparosc Endosc 1997; 7: 236-40.
- Crisci R, Coloni GF. Video-assisted thoracoscopic surgery versus thoracotomy for recurrent spontaneous pneumothorax. A comparison of results and costs. Eur J Cardiothorac Surg 1996; 10: 556-60.
- Horio H, Nomori H, Fuyuno G, Kobayashi R, Suemasu K. Limited axillary thoracotomy vs video-assisted thoracoscopic surgery for spontaneous pneumothorax. Surg Endosc 1998; 12: 1155-8.
- Landreneau RJ, Hazelrigg SR, Mack MJ, Dowling RD, Burke D, Gavlick J, et al. Postoperative pain-related morbidity: video-assisted thoracic surgery versus thoracotomy. Ann Thorac Surg 1993; 56: 1285-9.
- Murray KD, Matheny RG, Howanitz EP, Myerowitz PD. A limited axillary thoracotomy as primary treatment for recurrent spontaneous pneumothorax. Chest 1993; 103: 137-42.
