03. tbl 93. árg. 2007
Fræðigrein
Langvinnur nýrnasjúkdómur - nýjar áherslur í greiningu og meðferð
Advances in detection, evaluation and management of chronic kidney disease
Ágrip
Nýgengi nýrnabilunar á lokastigi hefur aukist jafnt og þétt um allan heim á undanförnum áratugum. Því hafa augu manna beinst að því að greina langvinnan nýrnasjúkdóm snemma svo draga megi úr áþján og kostnaði sem fylgir lokastigsnýrnabilun. Samkvæmt nýlegum leiðbeiningum er langvinnur nýrnasjúkdómur skilgreindur sem gaukulsíunarhraði (GSH) undir 60 ml/mín./1,73 m2 og/eða merki um skemmdir í nýrum samkvæmt þvag- eða myndgreiningarrannsóknum, í að minnsta kosti þrjá mánuði. Jafnframt er langvinnum nýrnasjúkdómi skipt í fimm stig eftir starfshæfni nýrna, frá stigi 1 sem er skilgreint sem eðlilegur GSH eða yfir 90 ml/mín./1,73 m2, og upp í stig 5, þegar GSH er kominn niður fyrir 15 ml/mín./1,73 m2 en það telst vera lokstigsnýrnabilun. Gaukulsíunarhraða er hægt að mæla beint en mun hentugra er að reikna hann út frá kreatíníni í sermi með því að nota jöfnur sem hafa reynst vera nokkuð áreiðanlegar. Hins vegar er kreatínín í sermi eitt sér frekar ónákvæmur mælikvarði á nýrnastarfsemi. Faraldsfræðilegar rannsóknir sem byggja á framangreindri skilgreiningu hafa sýnt að tíðni langvinns nýrnasjúkdóms er 5-10% á Vesturlöndum og er því víða farið að líta á hann sem lýðheilsuvandamál. Einnig hefur verið sýnt fram á að langvinnum nýrnasjúkdómi fylgir aukin hætta á hjarta- og æðasjúkdómum. Á þessu ári mun rannsóknastofa í klínískri lífefnafræði á Landspítala hefja þá nýbreytni að gefa upp reiknaðan GSH ásamt kreatíníngildum. Mikilvægt er að læknar kynni sér gildi reiknaðs GSH og nýti hann við dagleg störf. Þannig verður greining og meðferð sjúklinga með langvinnan nýrnasjúkdóm markvissari og verður vonandi hægt að koma í veg fyrir að sjúkdómurinn þróist yfir í lokastigsnýrnabilun auk þess að draga úr hættu á hjarta- og æðasjúkdómum.
Inngangur
Á undanförnum áratugum hefur orðið gífurleg fjölgun einstaklinga sem gangast undir lífsnauðsynlega meðferð vegna nýrnabilunar á lokastigi, ýmist með skilun eða ígræðslu á nýra. Það stafar meðal annars af hækkandi aldri fólks, auknum lífslíkum og bættu aðgengi að meðferð við lokastigsnýrnabilun. Aukningin hefur haldist í hendur við fjölgun sjúklinga með aðra langvinna sjúkdóma, svo sem háþrýsting, sykursýki, offitu og hjarta- og æðasjúkdóma. Alþjóðaheilbrigðismálastofnunin hefur metið að fjöldi dauðsfalla í heiminum árið 2005 hafi verið 58 milljónir, þar af 35 milljónir vegna langvinnra sjúkdóma www.who.int/chp/chronic_disease_report/part1/en/index1.html Þó langvinnur nýrnasjúkdómur sé ekki nefndur þar er hann engu að síður mikilvægur því hann er sérlega algengur hjá sjúklingum með hjarta- og æðasjúkdóma og margfaldar hættu á slæmri útkomu og kostnað meðferðar (1).
Á Íslandi hefur nýgengi og algengi lokastigsnýrnabilunar reyndar verið mun lægra en víðast hvar á Vesturlöndum en aukningin hefur engu að síður verið umtalsverð (mynd 1). Árlega hefja um 20 Íslendingar meðferð við nýrnabilun á lokastigi og var algengið 486 á milljón íbúa í árslok 2006 samanborið við til dæmis 700-800 á milljón íbúa á Norðurlöndum árið 2004 (2) og 1500 á milljón íbúa í Bandaríkjunum árið 2003 (3). Árið 2004 var talið að um 1,8 milljón sjúklingar í heiminum væru meðhöndlaðir vegna lokastigsnýrnabilunar og hefur þeim fjölgað um 6-7% árlega (4). Um 23% sjúklinga með lokastigsnýrnabilun hafa gengist undir ígræðslu á nýra en það er þó mismunandi milli landa og óvíða er hlutfallið hærra en hér þar sem 66% sjúklinga með lokastigsnýrnabilun voru með virkan nýragræðling í árslok 2006. Ígræðsla á nýra er kjörmeðferð við lokastigsnýrnabilun en hentar þó ekki öllum.
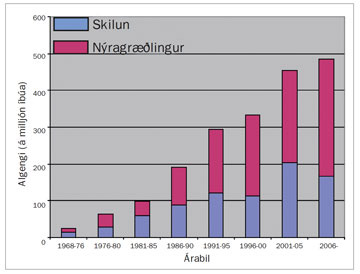
Mynd 1. Algengi lokastigsnýrnabilunar á Íslandi.
Meðalalgengi á hverju 5 ára tímabili frá 1968-2006. Súlan lengst til hægri sýnir algengi í árslok 2006 en þá voru 66% sjúklinga með starfandi nýragræðling en 34% í skilunarmeðferð.
Nýrnabilun hefur skert lífsgæði og minnkaðar lífslíkur í för með sér. Auk þess að vera þung byrði fyrir sjúklinga og fjölskyldur þeirra, hefur lokastigsnýrnabilun áhrif á samfélagið allt því meðferð hennar er mjög kostnaðarsöm þar sem hún krefst sérhæfðs starfsfólks, aðstöðu og tæknibúnaðar. Af framansögðu má vera ljóst að um umfangsmikið lýðheilsuvandamál er að ræða. Því tóku Alþjóðasamtök nýrnalækna (International Society of Nephrology) og Alþjóðasamtök nýrnafélaga (International Federation of Kidney Foundations) höndum saman og héldu upp á Alþjóðanýrnadaginn (World Kidney Day) á síðastliðnu ári í þeim tilgangi að vekja athygli og auka þekkingu almennings, forystumanna heilbrigðismála og heilbrigðisstofnana, og sjúklinga og fjölskyldna þeirra á mikilvægi nýrnasjúkdóma - að þeir séu algengir, alvarlegir og síðast en ekki síst að meðferðarúrræði séu fyrir hendi. Stefnt er að því að þessi dagur verði árviss viðburður og verður hann næst 8. mars 2007 www.worldkidneyday.org
Til að reyna að stemma stigu við sívaxandi fjölda sjúklinga með lokastigsnýrnabilun hefur áhugi manna í auknum mæli beinst að því að greina langvinnan nýrnasjúkdóm snemma og beita meðferð sem miðar að því að hindra framrás sjúkdómsins. Mikil gróska hefur verið í vísindarannsóknum á þessu sviði mörg undanfarin ár en nokkur vandamál hafa hamlað því starfi. Fyrst og fremst eru það óljósar skilgreiningar á langvinnum nýrnasjúkdómi sem hafa valdið erfiðleikum en einnig er nokkur óvissa í greiningu þar sem kreatínín í sermi er frekar ónákvæmur mælikvarði á nýrnastarfsemi (5) auk þess sem aðferðir sem notaðar eru við mælingu kreatíníns hafa ekki verið nægilega vel staðlaðar milli rannsóknarstofa (6). Síðustu ár hefur því verið mikil vakning í átt að því að skilgreina betur langvinnan nýrnasjúkdóm og leita nýrra aðferða til að meta nýrnastarfsemi ásamt því að staðla kreatínínmælingar. Örugg greining er forsenda þess að hægt sé að koma við meðferð er miðar að því að fyrirbyggja lokastigsnýrnabilun sem er sívaxandi baggi á samfélaginu.
Nýjar skilgreiningar langvinns nýrnasjúkdóms
Almennt er talið að gaukulsíunarhraði (GSH) sé besti mælikvarðinn á nýrnastarfsemi. Eðlilegur GSH er 90-120 ml/mín./1,73 m2. Í nýlegum leiðbeiningum frá Bandarísku nýrnasamtökunum (National Kidney Foundation) er lagt til að GSH verði hafður til grundvallar við mat á nýrnastarfsemi (7). Samkvæmt þessum leiðbeiningum er langvinnur nýrnasjúkdómur skilgreindur sem GSH undir 60 ml/mín./1,73 m2 og/eða merki um skemmdir í nýrum er greinast með þvag- eða myndgreiningarrannsóknum, til dæmis blóð- eða próteinmiga, í þrjá mánuði eða lengur. Langvinnum nýrnasjúkdómi er skipt í fimm stig eftir GSH (tafla I). Þannig er stig 1 eðlilegur GSH eða yfir 90 ml/mín./1,73 m2 en nýrnasjúkdómur greinist vegna merkja um nýrnaskemmdir við þvag- eða myndgreiningarrannsókn, til dæmis próteinmigu. Stigi 5 er náð þegar GSH er kominn niður fyrir 15 ml/mín./1,73 m2 en þá telst nýrnabilun komin á lokastig.
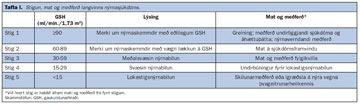
Mat á nýrnastarfsemi
Þó að mælt sé með að nota GSH til að greina og stiga langvinnan nýrnasjúkdóm, er bein mæling hans, til dæmis með mati á ísótópaúthreinsun (125I-joðþalamat eða 51Cr-EDTA), dýr og tímafrek og ekki vel fallin til nota í daglegu klínísku starfi. Einnig er mæling á kreatínínúthreinsun í sólarhringsþvagi óáreiðanleg þar sem skekkjur í framkvæmd þvagsöfnunar eru oft verulegar. Nýlegar rannsóknir benda til að jöfnur sem hægt er að nota til að reikna út GSH veiti jafnvel betri nálgun að raunverulegum GSH en mat á kreatínínúthreinsun (8, 9).
Kreatínín
Mæling á styrk kreatíníns í sermi hefur í gegnum tíðina verið notuð til að meta starfsemi nýrna. Kreatínín er amínósýruafleiða með massa 113 D. Það síast greiðlega í gauklum og seyting þess í nærpíplum er ekki ýkja mikil undir venjulegum kringumstæðum. Kreatínínúthreinsun í þvagi svipar því til GSH. Það er þó ýmsum vandkvæðum bundið að reiða sig á kreatínín þar sem aðrir þættir hafa áhrif á sermisþéttni þess. Má þar helst nefna vökvaástand einstaklingsins, vöðvamassa, aldur og kyn en einnig kjötneyslu og ýmis lyf, til dæmis trímetóprím (5). Þá er mæling kreatíníns í sermi ekki nægilega næm því það hækkar ekki að ráði fyrr en GSH hefur minnkað um meira en 50%.
Algengustu aðferðirnar til að mæla kreatínín í sermi hafa verið svokölluð Jaffé-aðferð og ensímaðferðir (6). Jaffé-aðferðin mælir einnig svonefnd kreatínínlíki (pseudocreatinines) og ofmetur því kreatínín um 10-20% hjá heilbrigðum einstaklingi. Ensímaðferðirnar mæla ekki þessi kreatínínlíki og ofmeta því ekki kreatínín í sermi. Viðmiðunarmörk ensímaðferðanna eru 50-90 µmól/l fyrir konur og 60-100 µmól/l fyrir karla samanborið við 60-100 µmól/l fyrir konur og 70-120 µmól/l í tilviki Jaffé-aðferðar.
Kreatínínjöfnur
Til að öðlast nákvæmara mat á GSH með mælingum kreatíníns í sermi hafa verið þróaðar jöfnur sem taka tillit til sumra framangreindra þátta. Mest hefur hin svonefnda Cockcroft-Gault- jafna verið notuð (tafla II) en hún spáir fyrir um kreatínínúthreinsun og innifelur auk kreatíníns, aldur, þyngd og kyn (10). Nýlega kom fram önnur jafna sem þróuð var út frá mælingum kreatíníns og 125I-joðþalamatúthreinsunar hjá 1628 einstaklingum með langvinnan nýrnasjúkdóm en þeir voru þátttakendur í bandarískri rannsókn er nefndist Modification of Diet in Renal Disease Study (MDRD) og var framkvæmd fyrir 15-20 árum. Þessi jafna innifelur fjórar breytur, kreatínín, aldur, kyn og kynþátt (11). Hún virðist vera heldur áreiðanlegri en Cockcroft-Gault-jafnan og hefur verið að ná fótfestu. Hún hefur þó þann ókost að vera flókin og lítt fallin til hugareiknings líkt og Cockcroft-Gault-jafnan. Það sem einkum takmarkar notkun beggja jafna er skortur á alþjóðlegri stöðlun kreatínínmælinga. Rannsóknir eru í gangi á gildi MDRD-jöfnunnar hjá öðrum kynþáttum en hvítum og svörtum, öldruðum einstaklingum, einstaklingum með mismunandi tegundir nýrnasjúkdóma og hjá heilbrigðum einstaklingum. Aðrar jöfnur hafa verið notaðar til að meta nýrnastarfsemi hjá börnum þar sem hvorki Cockcroft-Gault-jafnan né MDRD-jafnan hafa verið sannreyndar hjá þeim. Helstar má þar nefna Schwartz- (12) og Counahan-Barratt-jöfnur (9).

Eins og áður greinir er skortur á stöðlun kreatínínmælinga milli rannsóknastofa talinn eiga verulegan þátt í ónákvæmni reiknaðs GSH. Nú hefur verið hrint af stað alþjóðlegu átaki til að staðla kreatínínmælingar samkvæmt staðli sem mældur hefur verið með ákveðinni aðferð, massalitrófsgreiningu með ísótópaþynningu (Isotope Dilution Mass Spectrometry). Framleiðendur hvarfefna og mælitækja vinna nú að þessari stöðlun og er áætlað að þeirri vinnu ljúki á næsta ári. Slík stöðlun er ein af meginforsendum þess að rannsóknastofur geti farið að birta reiknaðan GSH samhliða niðurstöðum kreatínínmælinga (14).
Í sumum tilvikum er ástæða til að ætla að ekki sé hægt að reiða sig á kreatínín eða kreatínínjöfnur, til dæmis vegna óeðlilegs vöðvamassa, svo sem hjá vaxtarræktarfólki eða við vöðvarýrnun af ólíkum orsökum. Kann þá að vera ráðlegt að fá nákvæma mælingu á GSH með ísótóparannsókn.
Cystatín C
Þrátt fyrir þá framþróun sem hér hefur verið lýst er hægt að bæta um betur og enn er leitað að hentugri aðferð til að meta GSH. Síðustu ár hefur áhugi manna einkum beinst að cystatín C, litlu próteini (13 kD) sem framleitt er af öllum kjarnafrumum líkamans. Það síast greiðlega í gauklum og er brotið niður af frumum í nýrnapíplum. Cystatín C er því talið vænlegur kostur til að meta GSH og er talið vera betra en kreatínín í sermi eitt og sér (15). Hins vegar virðist mæling á cystatín C eða útreikningur á GSH sem byggist á cystatín C ekki hafa mikið umfram kreatínínjöfnur að bjóða (16). Mæling cystatín C er auk þess umtalvert dýrari og mælingaraðferðir hafa ekki verið staðlaðar þannig að sem stendur er ekki hægt að ráðleggja notkun þess í stað reiknaðs GSH sem byggist á kreatíníni.
Faraldsfræði langvinns nýrnasjúkdóms
Við upphaflegar rannsóknir á faraldsfræði langvinns nýrnasjúkdóms voru notaðar ýmsar aðferðir til að mæla kreatínín í sermi og mismunandi kreatíníngildi til að skilgreina sjúkdóminn og urðu niðurstöður því ærið misvísandi (17-20). Nýrri rannsóknir sem lagt hafa skilgreiningu Bandarísku nýrnasamtakanna frá árinu 2002 til grundvallar, sýna að tíðni langvinns nýrnasjúkdóms er talsvert há og er til að mynda um 11% í Bandaríkjunum (21). Hér á Íslandi var algengið um 7% meðal karla og 12% meðal kvenna samkvæmt nýlegri rannsókn sem byggði á gögnum frá Hjartavernd (22) og er það svipað og komið hefur fram í öðrum löndum (23-25). Athygli vekur að tíðni langvinns nýrnasjúkdóms er svipuð milli landa þó að tíðni lokastigsnýrnabilunar sé talsvert mismunandi (24). Bendir það til að framrás nýrnabilunar sé mismunandi meðal vestrænna þjóða en óljóst er hvernig á því stendur. Nauðsynlegt er þó að hafa hugfast að þessar rannsóknir hafa notað kreatínín í sermi og jöfnur sem byggja á því til að reikna út GSH og eru því háðar sömu annmörkum og kreatínínmælingarnar sjálfar. Nýleg rannsókn sem staðlaði niðurstöður kreatínínmælinga og kannaði algengi langvinns nýrnasjúkdóms og tíðni áhættuþátta fyrir lokastigsnýrnabilun í Noregi og Bandaríkjunum, sýndi samt svipaða tíðni langvinns nýrnasjúkdóms þótt algengi lokastigsnýrnabilunar sé mun meira vestanhafs. Höfundar hennar töldu að mismunandi dreifing áhættuþátta, meðal annars sykursýki og offitu, sem eru mun tíðari í Bandaríkjunum, gæti að minnsta kosti að hluta til útskýrt hvers vegna algengi lokastigsnýrnabilunar er meira þar (24). Orsakir langvinns nýrnasjúkdóms geta því verið mismunandi milli landa, til dæmis er sykursýkinýrnamein fátíð orsök hér á landi þar sem innan við 10% af sjúklingum með lokastigsnýrnabilun eru með sykursýki, en er allt að 40-50% annars staðar. Aðrar helstu orsakir langvinns nýrnasjúkdóms meðal fullorðinna eru háþrýstingur, æðakölkun, gauklabólga, millivefsbólga, stíflunýrnamein, og arfgengir sjúkdómar, svo sem arfgengur blöðrunýrnasjúkdómur með ríkjandi erfðamáta (17, 24).
Allar faraldsfræðirannsóknir hafa sýnt að algengi langvinns nýrnasjúkdóms eykst mjög með vaxandi aldri. Það er þekkt að nýrnastarfsemi hnignar með aldrinum og álitið er að GSH lækki að meðaltali um 1 ml/mín. á ári eftir að fullorðinsaldri er náð (26). Það þarf því ekki að koma á óvart að aldraðir séu áberandi í flokki þeirra sem eru með langvinnan nýrnasjúkdóm samkvæmt þessum nýju skilgreiningum. Rétt er því að fara varlega í að greina langvinnan nýrnasjúkdóm meðal aldraðra einstaklinga, einkum ef um væga minnkun á nýrnastarfsemi er að ræða og engin önnur skilmerki fyrir sjúkdómnum eru til staðar.
Afleiðingar langvinns nýrnasjúkdóms
Framrás yfir í lokastigsnýrnabilun er sú afleiðing langvinns nýrnasjúkdóms sem flestir óttast. Meðferð langvinns nýrnasjúkdóms beinist því einkum að því að seinka eða koma í veg fyrir hnignun nýrnastarfsemi. Á síðustu árum hefur fjöldi rannsókna sýnt að hægt er að hafa áhrif á framrás langvinns nýrnasjúkdóms með góðri blóðþrýstingsstjórnun, sérstaklega notkun hemla angíótensínummyndunarensíms og/eða angíótensín II-viðtækisblokka. Vísbendingar eru um að ávinningur sé af því að lækka blóðþrýsting meira en almennt hefur verið sýnt fram á hjá sjúklingum með háþrýsting eða niður fyrir 130/80, einkum ef próteinmiga umfram 1 g á dag er fyrir hendi (27). Mikilvægt er einnig að meðhöndla undirliggjandi orsakir vel. Má þar helst nefna góða sykurstjórnun hjá einstaklingum með sykursýki og skjóta meðferð stíflu í þvagvegum. Fylgikvillar nýrnabilunar, svo sem vökvasöfnun, háþrýstingur, blóðleysi og truflanir á kalsíum- og fosfatjafnvægi fara að koma fram þegar GSH er á bilinu 30-60 ml/mín./1,73 m2 (stig 3) og þarf að hyggja að meðferð þeirra á því stigi. Síðast en ekki síst þarf að huga að skömmtun lyfja sem eru útskilin um nýru.
Á margan hátt er aukin áhætta á hjarta- og æðasjúkdómum enn stærra vandamál en framrás yfir í lokastigsnýrnabilun meðal sjúklinga með langvinnan nýrnasjúkdóm. Athyglisvert er að það er allt að hundrað sinnum líklegra að þessir sjúklingar deyi úr hjarta- og æðasjúkdómum en að þeir fái lokastigsnýrnabilun (28) og fjölmargar rannsóknir benda til að bæði próteinmiga og skert nýrnastarfsemi séu sjálfstæðir áhættuþættir fyrir hjarta- og æðasjúkdóma (29-32). Enn fremur eru sjúklingar með lokastigsnýrnabilun í margfalt meiri hættu á að deyja úr hjarta- og æðasjúkdómum en jafnaldrar þeirra (mynd 2) (33). Því er afar þýðingarmikið að greina og meðhöndla langvinnan nýrnasjúkdóm snemma. Telja margir að með tímanlegri greiningu og meðferð megi stórlega minnka tíðni lokastigsnýrnabilunar og þannig draga úr sívaxandi útgjöldum vegna meðferðar hennar.
Greining langvinns nýrnasjúkdóms
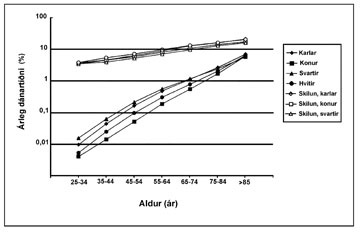
Mynd 2. Dánartíðni af völdum hjarta- og æðasjúkdóma í almennu þýði (lokuð tákn) og meðal skilunarsjúklinga (opin tákn).
Dánartíðni er sett fram á lógaritmakvarða. Eins og sjá má eru skilunarsjúklingar 10-1000 sinnum líklegri til að deyja árlega úr hjarta- og æðasjúkdómum en jafnaldrar þeirra.
Myndin er frá Levey AS, et al. Am J Kidney Dis 1998; 32: 853 (33) og hefur verið breytt lítillega. Hún er birt með góðfúslegu leyfi National Kidney Foundation.
Reiknaður GSH hefur verið að ryðja sér til rúms í klínísku starfi lækna austan hafs sem vestan og víða eru rannsóknarstofur farnar að gefa hann upp samhliða kreatíníngildum fyrir einstaklinga eldri en 18 ára. Það er fjögurra breytu MDRD-jafnan sem mestrar hylli nýtur því auk þess að vera eina jafnan sem hefur verið uppfærð fyrir staðlaðar kreatínínmælingar, eru upplýsingar um aldur og kyn sjúklings undartekningarlítið aðgengilegar fyrir rannsóknastofurnar. Fastanum 1,21 fyrir svartan kynþátt verður hins vegar læknir sjúklings að bæta við þegar við á. Reiknaður GSH er gefinn upp sem ml/mín./1,73 m2 líkamsyfirborðs. Útreikningur GSH er reyndar nokkuð ónákvæmur þegar GSH er hærri en 60 ml/mín./1,73 m2. Ástæða þess er meðal annars sú að stöðlunarskekkja við mælingu kreatíníns er hlutfallslega mest við efri viðmiðunarmörk þess (34). Auk þess var MDRD-jafnan upprunalega þróuð meðal einstaklinga með langvinnan nýrnasjúkdóm og því ef til vill ekki hægt að yfirfæra hana á heilbrigða einstaklinga (35). Þess vegna er ráðlegt að gefa eingöngu upp að GSH sé hærri en 60 ml/mín./1,73 m2 ef hann reiknast yfir þessum mörkum.
Fyrri hluta þessa árs mun rannsóknastofa í klínískri lífefnafræði á Landspítala fá vottun þess að aðferðin sem þar er notuð til mælinga á kreatíníni í sermi sé stöðluð samkvæmt nýjum alþjóðlegum leiðbeiningum. Samtímis því mun rannsóknastofan byrja að gefa upp reiknaðan GSH (samkvæmt MDRD-jöfnu) fyrir alla einstaklinga sem eru yfir 18 ára aldri, til viðbótar við kreatíníngildið. Vonast er til að þessi nýbreytni muni auðvelda starf lækna og gera greiningu og meðferð langvinns nýrnasjúkdóms markvissari. Reyndar finnst víða hugbúnaður til að nota við að reikna GSH og er auðvelt að nálgast forrit fyrir lófatölvur eða hægt er að finna slíka reiknivél á internetinu www.kidney.org/professionals/tools/ Þegar búið er að greina langvinnan nýrnasjúkdóm þarf að huga að orsök, öðrum mikilvægum sjúkdómum og áhættuþáttum, og stigi nýrnasjúkdómsins.
Ráðleggingar
Hin nýja skilgreining á langvinnum nýrnasjúkdómi og notkun reiknaðs GSH er mikið framfaraskref sem leiðir vonandi til þess að sjúkdómurinn greinist fyrr og að viðeigandi meðferð verði beitt í ríkari mæli en áður. Líklegt er að meðferð sem miðar að því að draga úr framrás langvinns nýrnasjúkdóms verði hafin fyrr og meðhöndlun fylgikvilla verði markvissari. Það er ekki síst vegna stóraukinnar áhættu á hjarta- og æðasjúkdómum sem meta ætti albúmín- eða próteinmigu og GSH, í raun ekki síður en blóðfitu eða blóðþrýsting. Forsenda þess að framangreind nálgun nýtist sem best er að læknar kynni sér vel nýjar skilgreiningar og ráðlagðar rannsóknir og meðferð við mismunandi stigum langvinns nýrnasjúkdóms. Gæti það gert heimilislæknum kleift að taka meiri þátt í meðferð slíkra sjúklinga sem hingað til hafa mestmegnis verið í umsjón nýrnalækna.
Hjá einstaklingum í aukinni hættu á að fá langvinnan nýrnasjúkdóm, til dæmis sjúklingum með háþrýsting eða sykursýki, ætti reglubundið að mæla kreatínín í sermi og gera þvagrannsókn. Hjá þeim sem greinast með langvinnan nýrnasjúkdóm er mikilvægt að greina undirliggjandi sjúkdóm og meðhöndla hann ef kostur er. Þær rannsóknir sem ráðlagt er að framkvæma eru þvagrannsókn (strimilpróf og smásjárskoðun), ómskoðun á nýrum, rafdráttur próteina í sermi og þvagi, og mæling þvagleifar í blöðru eftir þvaglát í völdum tilfellum. Frekari rannsóknir ráðast svo af niðurstöðum framangreindra rannsókna. Við greiningu er einnig rétt að hefja svokallaða nýrnaverndandi meðferð með angíótensínummyndunarensímshemli og/eða angíótensín II-viðtækisblokka sem og meðferð annarra áhættuþátta hjarta- og æðasjúkdóma. Er GSH fellur undir 60 ml/mín./1,73 m2 þarf að auki að hyggja að tilkomu fylgikvilla skertrar nýrnastarfsemi og meðhöndla þá, og þegar GSH fer niður fyrir 30 ml/mín./1,73 m2 þarf oft að skerpa á þeirri meðferð. Ráðlegt er að senda sjúkling til nýrnalæknis á þessu stigi því nauðsynlegt er að hann fái kynningu á meðferð lokastigsnýrnabilunar og að undirbúningur hennar sé hafinn tímanlega (36, 37).
Heimildir
1. Fried LF, Katz R, Sarnak MJ, Shlipak MG, Chaves PH, Jenny NS, et al. Kidney function as a predictor of noncardiovascular mortality. J Am Soc Nephrol 2005;16: 3728-35.
2. Anonymous. ERA-EDTA Registry 2004 Annual Report. ERA-EDTA Registry. Amsterdam, The Netherlands: Academic Medical Center, Department of Medical Informatics, 2006.
3. Anonymous. U.S. Renal Data System, USRDS 2003 Annual Data Report: Atlas of End-Stage Renal Disease in the United States. Bethesda, MD: National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases, 2003.
4. Grassmann A, Gioberge S, Moeller S, Brown G. ESRD patients in 2004: global overview of patient numbers, treatment modalities and associated trends. Nephrol Dial Transplant 2005; 20: 2587-93.
5. Perrone RD, Madias NE, Levey AS. Serum creatinine as an index of renal function: new insights into old concepts. Clin Chem 1992; 38:1933-53.
6. Myers GL, Miller WG, Coresh J, Fleming J, Greenberg N, Greene T, et al. Recommendations for improving serum creatinine measurement: a report from the Laboratory Working Group of the National Kidney Disease Education Program. Clin Chem 2006; 52: 5-18.
7. Anonymus. K/DOQI Clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis 2002; 39 Suppl 1:S1-S246.
8. Coresh J, Toto RD, Kirk KA, Whelton PK, Massry S, Jones C, et al. Creatinine clearance as a measure of GFR in screenees for the African-American Study of Kidney Disease and Hypertension pilot study. Am J Kidney Dis 1998; 32: 32-42.
9. Counahan R, Chantler C, Ghazali S, Kirkwood B, Rose F, Barratt TM. Estimation of glomerular filtration rate from plasma creatinine concentration in children. Arch Dis Child 1976; 51: 875-8.
10. Cockcroft DW, Gault MH. Prediction of creatinine clearance from serum creatinine. Nephron 1976; 16: 31-41.
11. Manjunath G, Sarnak MJ, Levey AS. Prediction equations to estimate glomerular filtration rate: an update. Curr Opin Nephrol Hypertens 2001; 10: 785-92.
12. Schwartz GJ, Brion LP, Spitzer A. The use of plasma creatinine concentration for estimating glomerular filtration rate in infants, children, and adolescents. Pediatr Clin North Am 1987; 34: 571-90.
13. Stromme JH, Rustad P, Steensland H, Theodorsen L, Urdal P. Reference intervals for eight enzymes in blood of adult females and males measured in accordance with the International Federation of Clinical Chemistry reference system at 37 degrees C: part of the Nordic Reference Interval Project. Scand J Clin Lab Invest 2004; 64: 371-84.
14. Levey AS, Coresh J, Greene T, Stevens LA, Zhang YL, Hendriksen S, et al. Using standardized serum creatinine values in the Modification of Diet in Renal Disease Study equation for estimating glomerular filtration rate. Ann Intern Med 2006; 145: 247-54.
15. Newman DJ, Thakkar H, Edwards RG, Wilkie M, White T, Grubb AO, et al. Serum cystatin C measured by automated immunoassay: a more sensitive marker of changes in GFR than serum creatinine. Kidney Int 1995; 47: 312-8.
16. Grubb A, Nyman U, Bjork J, Lindstrom V, Rippe B, Sterner G, et al. Simple cystatin C-based prediction equations for glomerular filtration rate compared with the Modification of Diet in Renal Disease prediction equation for adults and the Schwartz and the Counahan-Barratt prediction equations for children. Clin Chem 2005; 51: 1420-31.
17. Magnason RL, Indriðason OS, Sigvaldason H, Sigfússon N, Pálsson R. Prevalence and progression of CRF in Iceland: a population-based study. Am J Kidney Dis 2002; 40: 955-63.
18. Iseki K, Ikemiya Y, Fukiyama K. Risk factors of end-stage renal disease and serum creatinine in a community-based mass screening. Kidney Int 1997; 51: 850-4.
19. Culleton BF, Larson MG, Evans JC, Wilson PW, Barrett BJ, Parfrey PS, et al. Prevalence and correlates of elevated serum creatinine levels: the Framingham Heart Study. Arch Intern Med 1999; 159: 1785-90.
20. Jones CA, McQuillan GM, Kusek JW, Eberhardt MS, Herman WH, Coresh J, et al. Serum creatinine levels in the US population: Third National Health and Nutrition Examination Survey. Am J Kidney Dis 1998; 32: 992-9.
21. Coresh J, Astor BC, Greene T, Eknoyan G, Levey AS. Prevalence of chronic kidney disease and decreased kidney function in the adult US population: Third National Health and Nutrition Examination Survey. Am J Kidney Dis 2003; 41: 1-12.
22. Viktorsdóttir O, Pálsson R, Andrésdóttir MB, Aspelund T, Guðnason V, Indriðason OS. Prevalence of chronic kidney disease based on estimated glomerular filtration rate and proteinuria in Icelandic adults. Nephrol Dial Transplant 2005; 20: 1799-807.
23. Chadban SJ, Briganti EM, Kerr PG, Dunstan DW, Welborn TA, Zimmet PZ, et al. Prevalence of kidney damage in Australian adults: The AusDiab kidney study. J Am Soc Nephrol 2003; 14: S131-8.
24. Hallan SI, Coresh J, Astor BC, Asberg A, Powe NR, Romundstad S, et al. International comparison of the relationship of chronic kidney disease prevalence and ESRD risk. J Am Soc Nephrol 2006; 17: 2275-84.
25. Clase CM, Garg AX, Kiberd BA. Prevalence of low glomerular filtration rate in nondiabetic Americans: Third National Health and Nutrition Examination Survey (NHANES III). J Am Soc Nephrol 2002; 13: 1338-49.
26. Epstein M. Aging and the kidney. J Am Soc Nephrol 1996; 7: 1106-22.
27. Jafar TH, Stark PC, Schmid CH, Landa M, Maschio G, de Jong PE, et al. Progression of chronic kidney disease: the role of blood pressure control, proteinuria, and angiotensin-converting enzyme inhibition: a patient-level meta-analysis. Ann Intern Med 2003; 139: 244-52.
28. Keith DS, Nichols GA, Gullion CM, Brown JB, Smith DH. Longitudinal follow-up and outcomes among a population with chronic kidney disease in a large managed care organization. Arch Intern Med 2004; 164: 659-63.
29. Manjunath G, Tighiouart H, Ibrahim H, MacLeod B, Salem DN, Griffith JL, et al. Level of kidney function as a risk factor for atherosclerotic cardiovascular outcomes in the community. J Am Coll Cardiol 2003; 41: 47-55.
30. De Leeuw PW, Thijs L, Birkenhager WH, Voyaki SM, Efstratopoulos AD, Fagard RH, et al. Prognostic significance of renal function in elderly patients with isolated systolic hypertension: results from the Syst-Eur trial. J Am Soc Nephrol 2002; 13: 2213-22.
31. Irie F, Iso H, Sairenchi T, Fukasawa N, Yamagishi K, Ikehara S, et al. The relationships of proteinuria, serum creatinine, glomerular filtration rate with cardiovascular disease mortality in Japanese general population. Kidney Int 2006; 69: 1264-71.
32. Sarnak MJ, Levey AS, Schoolwerth AC, Coresh J, Culleton B, Hamm LL, et al. Kidney disease as a risk factor for development of cardiovascular disease: a statement from the American Heart Association Councils on Kidney in Cardiovascular Disease, High Blood Pressure Research, Clinical Cardiology, and Epidemiology and Prevention. Hypertension 2003; 42: 1050-65.
33. Levey AS, Beto JA, Coronado BE, Eknoyan G, Foley RN, Kasiske BL, et al. Controlling the epidemic of cardiovascular disease in chronic renal disease: what do we know? What do we need to learn? Where do we go from here? National Kidney Foundation Task Force on Cardiovascular Disease. Am J Kidney Dis 1998; 32: 853-906.
34. Coresh J, Astor BC, McQuillan G, Kusek J, Greene T, Van Lente F, et al. Calibration and random variation of the serum creatinine assay as critical elements of using equations to estimate glomerular filtration rate. Am J Kidney Dis 2002; 39: 920-9.
35. Lin J, Knight EL, Hogan ML, Singh AK. A comparison of prediction equations for estimating glomerular filtration rate in adults without kidney disease. J Am Soc Nephrol 2003; 14: 2573-80.
36. Kazmi WH, Obrador GT, Khan SS, Pereira BJ, Kausz AT. Late nephrology referral and mortality among patients with end-stage renal disease: a propensity score analysis. Nephrol Dial Transplant 2004; 19: 1808-14.
37. Jungers P, Massy ZA, Nguyen-Khoa T, Choukroun G, Robino C, Fakhouri F, et al. Longer duration of predialysis nephrological care is associated with improved long-term survival of dialysis patients. Nephrol Dial Transplant 2001; 16: 2357-64.
