05.tbl. 112. árg. 2026
Fræðigrein
Sjúkratilfelli. Óvenjuleg og viðráðanleg orsök beinmergsbilunar, tilfelli af blóðlækningadeild
Fyrirspurnum svarar Vilhjálmur Steingrímsson, vilhjalmur.steingrimsson@regionstockholm.se
Greinin barst 15. desember 2025, samþykkt til birtingar 19. febrúar 2026
Ágrip
Koparskortur er sjaldgæf og oft vangreind orsök blóðleysis, daufkyrningafæðar og taugakvilla. Í þessu tilfelli leitaði 47 ára karlmaður til læknis vegna þyngdartaps, þreytu og taugaeinkenna. Fyrstu niðurstöður rannsókna bentu til greiningar mergmisþroska þar sem blóðprufur sýndu blóðleysi og daufkyrningafæð. Ennfremur sýndi beinmergssýni frumuríkan merg með áberandi frymisbólum í forstigum mergfrumna. Í kjölfarið mældist alvarlegur koparskortur og hækkað sink í blóði og þvagi. Nánari saga leiddi í ljós langvarandi notkun á tannlími sem innihélt sink og koparskortur var afleiðing sinkofhleðslu. Einkennin gengu að mestu leyti til baka eftir koparuppbót og þegar notkun tannlímsins var hætt. Tilfellið undirstrikar mikilvægi þess að íhuga koparskort við óútskýrða beinmergsbilun.
Inngangur
Koparskortur er sjaldgæf orsök blóðleysis, daufkyrningafæðar og taugakvilla.1 Klínísk mynd getur verið ósértæk og líkst alvarlegum blóðsjúkdómum, þar á meðal mergmisþroska (myelodysplasia, MDS).2 Sinkeitrun er þekkt en oft vangreind orsök koparskorts og getur tengst notkun tannlíma sem innihalda sink.3 Snemmgreining er mikilvæg þar sem einkenni geta gengið algerlega til baka með viðeigandi meðferð. Hér lýsum við tilfelli manns með versnandi beinmergsbilun og taugaeinkenni þar sem undirliggjandi orsök reyndist óvænt en auðvelt að snúa henni við.
Sjúkratilfelli
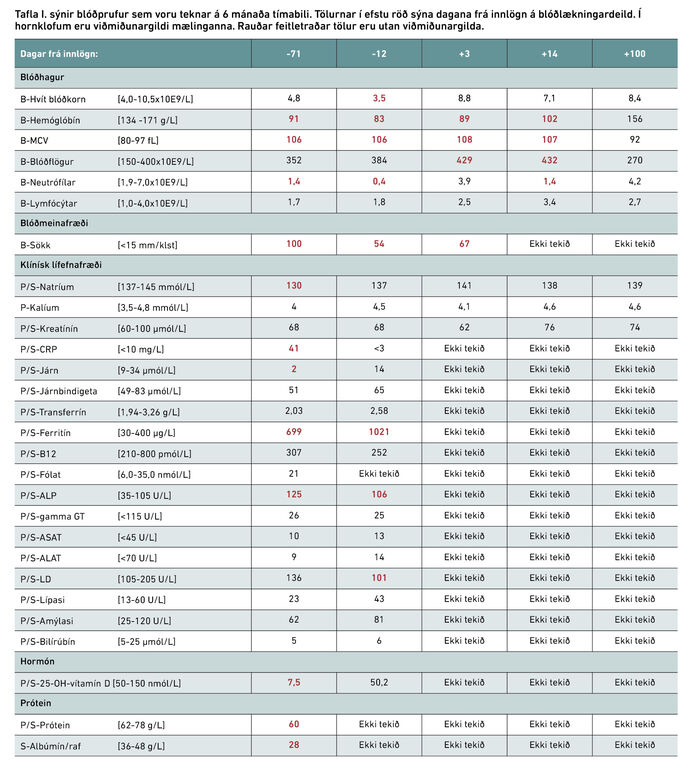
Áður hraustum 47 ára karlmanni var vísað til almennrar uppvinnslu á Landspítala vegna mikils þyngdartaps. Hann hafði lést um 25 kg á einu ári og vó 75 kg. Blóðprufur sýndu stórfrumublóðleysi (macrocytic anemia) og hækkað sökk en við kerfakönnun var til staðar þurr næturhósti, þreyta, kuldi í fótum og vægur dofi í tám. Hann hafði nýlega verið með hita en neitaði nætursvita. Hann var hraustur fyrir utan háþrýsting og tók við því metoprolol. Hann reykti og var með 20 pakkaár að baki og drakk nú áfengi í hófi en hafði drukkið meira áfengi fyrir veikindi. Fjölskyldusaga var ómarkverð. Við skoðun heyrðist væg önghljóð hægra megin í útöndun og öndunarhljóð voru fjarlægð. Einnig var lítið graftarkýli við endaþarm sem var langvarandi vandamál. Fyrstu blóðprufur sýndu væga til meðal blóðfrumufæð (pancytopenia, Hgb 91 g/L, MCV 106 fL, daufkyrningar 1,4x10E9/L, eitilfrumur 1,7x10E9/L), hátt sökk og alvarlegan D-vítamínskort auk markverðrar lækkunar á heildarpróteinum og albúmíni (sjá töflu I, dagur -71). Tölvusneiðmyndir voru pantaðar til skimunar fyrir krabbameini og voru ómarkverðar. Mótefnamæling (serology) var neikvæð með tilliti til HIV, lifrarbólgu B og lifrabólgu C. Grunur vaknaði um næringarskort og því var ákveðið að panta maga- og ristilspeglun sem voru ómarkverð en sýni frá maga leiddi í ljós langvinna bólgu af völdum Helicobacter pylori. Upprætingarmeðferð var því hafin í kjölfarið sem og uppbótarmeðferð við D-vítamínskorti.
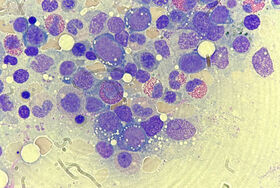
Tveim mánuðum síðar barst tilvísun á göngudeild blóðlækninga vegna versnandi einkenna. Nú var mikil þreyta og dagsyfja. Einnig var dofi kominn í hendur og hann gat ekki unnið vegna máttleysis. Blóðprufur sýndu versnun á stórfrumublóðleysi og alvarlega daufkyrningafæð (sjá töflu I, dagur –12). Á blóðlækningadeild vaknaði strax grunur um alvarlegan mergmisþroska eða jafnvel bráðahvítblæði. Því voru teknar ítarlegar blóðprufur og beinmergssýni við komu á dagdeild, auk þess sem sjúklingurinn var lagður inn vegna mikilla einkenna og alvarlegrar daufkyrningafæðar. Vegna gruns um næringarskort og óvenju ungs aldurs fyrir mergmisþroska var ákveðið að mæla einnig kopar í blóði. Mergrannsókn vakti grun um mergmisþroska en áberandi (og óvenjulegt) voru frymisbólur (vacuoles) í forstigum mergfrumna og rauðra blóðkorna (sjá mynd 1).
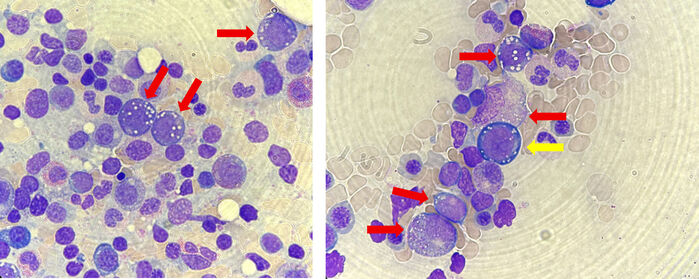
Mynd 1. Vinstri myndin sýnir þrjár frekar óþroskaðar mergfrumur (myelocytes) með frymisbólum (rauð ör). Hægri myndin sýnir frumrauðkorn (proerythroblast) fyrir miðju með frymisbólum (gul ör) ásamt fjórum mergfrumum á mismunandi þroskastigum með frymisbólum (rauð ör).
Járnkímfrumur (ring sideroblasts) var ekki að finna. Frumuflæðissjá sýndi verulega vinstri hneigð, rauðkyrningagnótt (eosinophilia) og mjög væga kímfrumuaukningu (excess blasts). Önnur uppvinnsla var ómarkverð (tölvusneiðmyndir, ræktanir, quantiFERON, glútenóþolsskimun). Þegar hér var komið við sögu var greiningin því talin mergmisþroski og reynd meðferð með filgrastim og -darbepoetinum alfa til að styðja við beinmerginn með tímabundnum bata (sjá töflu I, dagur 3).
Eftir sex daga uppvinnslu á blóðlækningadeild kom niðurstaða um að kopar í blóði var lækkaður (gildi: <50 µg/l, viðmiðunargildi: 560-1110 µg/l). Hafin var meðferð með átta mg kopar bisglycinate töflum (Dr. Mercola Copper Bisglycinate, 4 mg copper as copper bisglycinate tablets, dietary supplement) einu sinni á dag frá og með degi níu. Vegna taugaeinkenna var fengið mat taugalæknis og skoðun sýndi jafnvægisskerðingu við gang og talsverða truflun á stöðuskyni sem gat samrýmst koparskorti. MRI rannsókn sýndi engin merki um mænukvilla (myelopathy). Við ítarlega næringasögu þótti ónóg inntaka ólíkleg orsök koparskortsins. Fimm dögum eftir kopargjöf voru blóðgildi strax batnandi (sjá töflu I, dagur 14) en þá kom í ljós að sink gildi í blóði var hækkað (gildi: 1250 µg/l, viðmiðunargildi: 690-1170 µg/l). Það hafði verið mælt samkvæmt leiðbeiningum um uppvinnslu á koparskorti. Einnig var sinkmagn mælt í 24 tíma þvagsöfnun og reyndist það verulega hækkað (gildi: 2,79 mg/24klst, viðmiðunargildi: 0,15-0,8 mg/24klst). Gerðar höfðu verið litningarannsóknir á beinmerg með tilliti til mergmisþroska en þær sýndu engar litningabreytingar. Einnig útilokuðu erfðarannsóknir þekktar stökkbreytingar sem tengjast mergmisþroska.

Þá var aftur sest niður með sjúklingnum og tekin ítarlegri saga með tilliti til hækkunar á sinki en þá kom í ljós að hann hafði verið að nota Fixodent Complete Neutral tannlím (framleiðandi: Procter & Gamble, sjá mynd 2) fyrir falskar tennur en tannlímið innihélt sink og líklega hafði hann ekki fylgt notkunarleiðbeiningum sem skyldi. Hann var beðinn um að stöðva notkun tannlímsins.
Þremur mánuðum síðar kom hann aftur á göngudeild blóðlækninga í eftirlit. Blóðprufurnar voru orðnar eðlilegar (sjá töflu I, dagur 100) og líðan sjúklings mikið betri. Hann hafði þyngst á ný og gat unnið fullan vinnudag. Taugaeinkenni voru mikið batnandi en væg stöðuskynsbrenglun var enn til staðar. Ný koparmæling var innan viðmiðunarmarka og því var koparmeðferð hætt í kjölfarið. Við áframhaldandi eftirfylgd nokkrum mánuðum síðar mældust einnig eðlileg kopargildi.
Umræða
Blóðleysi, daufkyrningafæð og taugakvilli er þrenna (triad) sem hefur verið lýst í koparskorti.1 Einkennin geta því verið slappleiki og þreyta vegna blóðskorts og aukin áhætta á sýkingum vegna daufkyrningafæðar. Taugakvillar geta komið fram í mænu, úttaugum og í sjóntaug og meðal annars birst sem hreyfiglöp (ataxia), máttleysi, dofi í útlimum, minnkuð taugaviðbrögð, skert stöðuskyn og sjóntap.3 Taugaskaðinn getur orðið varanlegur.
Koparskortur er mjög sjaldgæfur en tilfellum hefur verið lýst áður.4,5 Kopar er nauðsynlegt snefilefni fyrir líkamann en ráðlagður dagskammtur landlæknis er um 900 µg fyrir fullorðin einstakling.6 Talið er að um fjórðungur nái ekki ráðlagðum dagskammti í Norður-Ameríku.7
Frásog kopars á sér stað fyrst og fremst í maganum og í skeifugörninni.3 Koparjónir eru teknar upp af Ctr1-próteininu sem vísar að iðraholi meltingarvegarins. Jónirnar eru síðan fluttar yfir í blóðrásina af ATP7A-próteininu.3 Sink hindrar -færslu kopars yfir í blóðrásina með því að auka tjáningu á próteini sem kallast málmþíónín (metallothionein). Próteinið klóbindur kopar og heldur því í frumum meltingarvegarins (sjá mynd 3). Kopar skilst síðan út með frumunum yfir í iðraholið (shedding).3
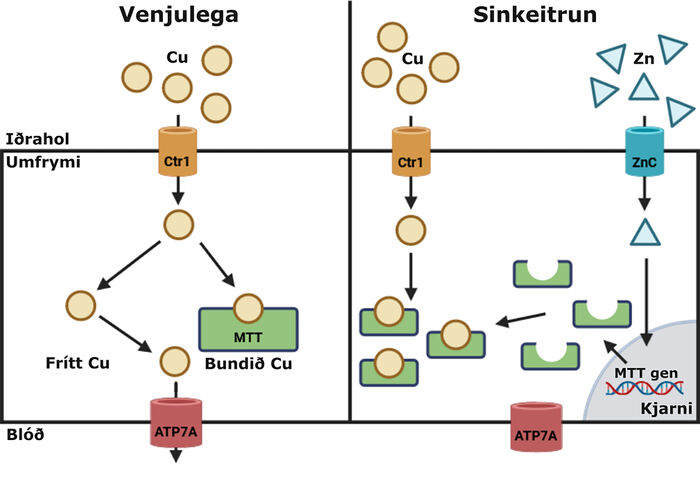
Mynd 3 sýnir hvernig frásogi á kopar er háttað undir venju-legum kringumstæðum og í sinkeitrun. Cu = Kopar, Zn = Sink, ZnC = Zinc channel, Ctr1 = High affinity copper uptake protein 1, MTT = Metallo-thionein, ATP7A = ATPase Copper Transporting Alpha. Mynd er byggð á sambærilegri mynd í heimild 23. Mynd búin til með Biorender og Inkscape.
Í okkar tilfelli hafði ástandið versnað mikið í kjölfar upprætingarmeðferðar á Helicobacter pylori en fræðilega séð geta prótónpumpuhemlar (proton pump inhibitors, PPI) dregið úr frásogi kopars.8 Frá meltingarveginum er kopar fluttur til lifrar bundinn við albúmín. Þaðan berst kopar til annarra líffæra að mestu leyti bundinn caeruloplasmíni.9
Blóðleysið í koparskorti er yfirleitt meðalfrumu (normocytic anemia) eða stórfrumu.3 Orsök blóðleysisins er ekki fullþekkt. Kopar er nauðsynlegur fyrir caeruloplasmín og hephaestín sem hvort um sig er mikilvægt í efnaskiptum járns. Bæði prótein taka þátt í flutningi á járni en í koparskorti safnast járn fyrir í lifrinni.3 Talið er að daufkyrningafæðin stafi af trufluðum þroska mergfrumna, skertri losun úr beinmerg og eyðingu þeirra.10 Afturskyggn rannsókn leiddi í ljós, öfugt við okkar tilfelli, að beinmergur í koparskorti er yfirleitt frumusnauður (hypocellular).11 Hinsvegar er einnig lýst tilfellum þar sem beinmergurinn verður frumuríkur (hypercellular)2 og minnir útlitið þá helst á mergmisþroska. Eins og í okkar tilfelli er oft að finna einkennandi frymisbólur í forstigum mergfrumna en einnig er hægt að sjá aukið járn í plasmafrumum.11 Þá hefur einnig verið lýst tilfelli þar sem sjúklingur var kominn í undirbúning fyrir beinmergsskipti áður en í ljós kom að koparskortur var undirliggjandi orsök beinmergsbilunarinnar.2
Orsökum koparskorts má gróflega skipta upp í fimm hluta: frásogsvandamál, erfðasjúkdóma, aðgerðir, næringaskort og sinkeitrun. Glútenóþol er algengasti frásogsvandinn sem getur leitt til koparskorts en tíðni hans meðal þeirra sem eru með glútenóþol er óþekkt.3,12 Menkes-sjúkdómur er X-tengdur víkjandi erfðasjúkdómur þar sem stökkbreyting í ATP7A-geninu veldur galla í samnefndu koparflutningspróteini. Sjúklingar með Menkes-sjúkdóm lifa yfirleitt ekki lengur en örfá ár.13 Ein algengasta ástæðan fyrir koparskorti er fyrri efnaskiptaaðgerð3 sem leiðir til minnkaðs frásogs á ýmsum jónum, þar með talið koparjónum. Í þessum tilvikum getur tekið áratugi fyrir einkenni að myndast.14 Langvarandi næring í æð getur valdið koparskorti, sérstaklega hjá einstaklingum þar sem snefilefnauppbót hefur verið stöðvuð, til dæmis vegna gallstasa.11,15,16 Algengasta ástæðan fyrir sinkeitrun er notkun tannlíma sem innihalda sink.3 Lyfja- og matvælastofnun Bandaríkjanna gaf út tilkynningu árið 2011 þar sem varað var við notkun tannlíma sem innihéldu sink17 og var hættan talin mest ef notað var mikið magn af tannlími í langan tíma, gervitennur pössuðu illa eða notkunarleiðbeiningum ekki fylgt. Merkingum á tannvörum er oft ábótavant en sumir framleiðendur framleiða nú tannlím án sinks og tilgreina það sérstaklega á umbúðunum.18 Í tilfellinu okkar hafði sjúklingurinn notað Fixodent Complete Neutral tannlím (sjá mynd 2) til lengri tíma. Samkvæmt framleiðanda er meðalfrásog af sinki í gegnum munnslímhúð um tvö mg á dag en efri neyslumörk eru um 25 mg á dag.6,19
Greining á koparskorti byggist fyrst og fremst á mælingu kopars í blóði. Hjá sjúklingum með koparskort þar sem taugaeinkenni eru komin fram er kopar í blóði yfirleitt lækkaður,20 sem gerir því hefðbundna koparmælingu í blóði góða rannsókn í slíkum tilfellum. Mælingin endurspeglar heildarmagn kopars í blóði, það er bæði kopar bundinn við caeruloplasmín og óbundinn kopar. Ef grunur vaknar um sinkeitrun ætti að mæla sink í blóði og/eða í 24 tíma þvagútskilnaði.21 Við grun um koparskort ætti einnig mæla B12, enda getur B12-skortur fylgt (til dæmis eftir aðgerðir á maga)20 og birtingarmyndin getur verið svipuð.5 Einnig ætti að skima fyrir glútenóþoli og mikilvægt að fá segulómskoðun til að útiloka mænukvilla þegar taugaeinkenni eru til staðar.21
Engar rannsóknir hafa verið gerðar til að ákvarða viðeigandi skammta, gjafaleið eða tímalengd koparuppbótarmeðferðar. Þar sem oft er þörf á langtímauppbót með kopar, er gjöf á kopar í æð ekki ákjósanlegur kostur og yfirleitt ekki nauðsynleg. Stundum er byrjað á kopargjöf í æð og síðan skipt yfir í kopartöflur. Upphafsskammtur kopars um munn getur verið allt frá 2 til 8 mg á dag í viku þar sem lækkað er um 2 mg vikulega í fjórar vikur ef byrjað er á hærri skammti.21,22 Viðhaldskammtar ákvarðast af blóðgildum í reglulegu eftirliti. Gjöf á kopar í æð er viðeigandi ef um er ræða koparskort vegna frásogsvanda en þá er algengt að byrja á 2 mg í æð einu sinni á dag í fimm daga.21,22 Ef um er að ræða sinkeitrun þá þarf að komast að undirliggjandi ástæðu og leiðrétta hana.
Kopargjöf kemur yfirleitt í veg fyrir frekari taugakvilla en batinn er breytilegur og sumir sjúklingar hafa því miður langvarandi taugaeinkenni. Hins vegar svarar beinmergurinn yfirleitt meðferð fljótt og að fullu. Tilfellið okkar lýsir óvenjulegri en viðráðanlegri orsök beinmergsbilunar og taugakvilla hjá tiltölulega ungum einstaklingi. Mikilvægt er því að hafa koparskort í huga þar sem saga, skoðun og niðurstöður hefðbundinna rannsókna gefa tilefni til.
Heimildir
1. Wazir SM, Ghobrial I. Copper deficiency, a new triad: anemia, leucopenia, and myeloneuropathy. J Community Hosp Intern Med Perspect. 2017:2;7(4):265–8.
2. Gregg XT, Reddy V, Prchal JT. Copper deficiency masquerading as myelodysplastic syndrome. Blood. 2002:15;100(4):1493–5.
3. Jaiser SR, Winston GP. Copper deficiency myelopathy. J Neurol. 2010:16;257(6):869–81.
4. Moon N, Aryan M, Westerveld D, et al. Clinical Manifestations of Copper Deficiency: A Case Report and Review of the Literature. Nutrition in Clinical Practice. 2021:9;36(5):1080–5
5. Kumar N, Gross JB, Ahlskog JE. Copper deficiency myelopathy produces a clinical picture like subacute combined degeneration. Neurology. 2004:13;63(1):33–9.
6. Embætti landlæknis. island.is. 2024. Næring - ráðleggingar embættis landlæknis. https://island.is/naering-radleggingar-landlaeknis – júlí 2025.
7. Klevay LM. Is the Western diet adequate in copper? Journal of Trace Elements in Medicine and Biology. 2011;25(4):204–12.
8. Plantone D, Renna R, Primiano G, et al. PPIs as possible risk factor for copper deficiency myelopathy. J Neurol Sci [Internet]. 2015:15;349(1):258–9.
9. Linder MC. Ceruloplasmin and other copper binding components of blood plasma and their functions: an update. Metallomics. 2016;8(9):887–905.
10. Percival SS. Neutropenia Caused by Copper Deficiency: Possible Mechanisms of Action. Nutr Rev. 2009:27;53(3):59–66.
11. Halfdanarson TR, Kumar N, Li C, et al. Hematological manifestations of copper deficiency: a retrospective review. Eur J Haematol. 2008:13;80(6):523–31.
12. Halfdanarson TR, Kumar N, Hogan WJ, et al. Copper Deficiency in Celiac Disease. J Clin Gastroenterol. 2009;43(2):162–4.
13. Tümer Z, Møller LB. Menkes disease. Eur J Hum Genet. 2010;18(5):511–8.
14. Kumar N, Ahlskog JE, Gross JB. Acquired hypocupremia after gastric surgery. Clinical Gastroenterology and Hepatology. 2004;2(12):1074–9.
15. Fuhrman MP, Herrmann V, Masidonski P, et al. Pancytopenia after removal of copper from total parenteral nutrition. JPEN J Parenter Enteral Nutr. 2000;24(6):361–6.
16. Shike M. Copper in parenteral nutrition. Gastroenterology. 2009;137(5 Suppl):S13-7.
17. U.S. Food and Drug Administration. Letter of Notice and Recommended Action to Denture Adhesive Manufacturers [Internet]. 2011. https://www.fda.gov/medical-devices/dental-devices/denture-adhesives – júlí 2025
18. GSK. GSK. 2010. GSK Consumer Healthcare warns consumers of potential health risks associated with long-term excessive use of zinc-containing denture adhesives. https://www.gsk.com/en-gb/media/press-releases/gsk-consumer-healthcare-warns-consumers-of-potential-health-risks-associated-with-long-term-excessive-use-of-zinc-containing-denture-adhesives/ – júlí 2025
19. Procter & Gamble. Frequently Asked Questions about Fixodent Denture Adhesive. DentureLiving.com [Internet]. https://www.dentureliving.com/en-us/faq – júlí 2025
20. Kumar N, Ahlskog JE, Klein CJ, et al. Imaging features of copper deficiency myelopathy: a study of 25 cases. Neuroradiology. 2006;48(2):78–83.
21. Kumar N. UpToDate. Copper deficiency myeloneuropathy. https://www.uptodate.com/contents/copper-deficiency-myeloneuropathy – ágúst 2025
22. Osadchyi V, Van Antwerp SN, Vredenburgh J. Zinc-Induced Copper Deficiency Myeloneuropathy Masquerading as Paraneoplastic Syndrome: A Case Report. Cureus. 2025;17(4):e82995.
23. Pitton Rissardo J, Fornari Caprara A. Copper deficiency myelopathy secondary to parenteral zinc supplementation during chronic dialysis. Neurol Asia. 2019:1;24:79–82.