04. tbl. 112. árg. 2026
Fræðigrein
Rannsókn. Árangur hlutabrottnáms á vélinda við vélindakrabbameini á Íslandi
Fyrirspurnum svarar Bjarni Geir Viðarsson, bjarnigv@landspitali.is
Greinin barst 15. nóvember 2025, samþykkt til birtingar 5. mars 2026.
Ágrip
Inngangur
Vélindakrabbamein er sjöunda algengasta dánarorsök af völdum krabbameina á heimsvísu. Meðferð í læknanlegum tilgangi er aðeins veitt sjúklingum með staðbundinn sjúkdóm og felur oftast í sér hlutabrottnám á vélinda með eða án krabbameinslyfja- og/eða geislameðferðar fyrir aðgerð. Markmið þessarar rannsóknar var að lýsa bakgrunnsþáttum og kanna afdrif sjúklinga sem gengust undir hlutabrottnám á vélinda vegna vélindakrabbameins á Íslandi.
Efniviður og aðferðir
Rannsóknin var afturskyggn ferilrannsókn á öllum sjúklingum sem greindust á Íslandi með staðbundið vélindakrabbamein á árunum 2015-2020 og gengust undir hlutabrottnám. Helstu þættir til skoðunar voru fylgikvillar, endurkoma krabbameinsins og fimm ára lifun. Fylgikvillar voru flokkaðir eftir Clavien-Dindo flokkunarkerfinu og notuð var lýsandi tölfræði. Endurkoma var áætluð með andlát án endurkomu krabbameins sem samkeppandi atburð, og lifun metin með Kaplan-Meier greiningu.
Niðurstöður
Alls voru 33 sjúklingar sem gengust undir hlutabrottnám á vélinda. Miðgildi aldurs var 66 ár og voru karlmenn meirihluti sjúklinga (76%). Flestir sjúklingar fengu krabbameinslyfja- og/eða geislameðferð fyrir aðgerðina (94%). Clavien-Dindo flokkar >3a komu fram hjá 45% sjúklinga. Af þeim var samgötunarleki algengasti fylgikvillinn og greindist í 30% tilfella. Enginn sjúklingur lést innan 30 daga frá aðgerð en tveir (6%) létust innan 90 daga. Fimm ára lifun var 44% og sjúkdómsfrí lifun 30% eftir fimm ár. Uppsafnað nýgengi á endurkomu krabbameinsins var 21% eftir eitt ár en 55% eftir fimm ár.
Ályktun
Árangur hlutabrottnáms á vélinda á Íslandi er að mestu leyti sambærilegur við erlend þýði, en tíðni samgötunarleka er þó hærri hérlendis. Þrátt fyrir það reyndist snemmkomin dánartíðni lág og langtímalifun sambærileg því sem sést á Norðurlöndunum.
Inngangur
Vélindakrabbamein er sjöunda algengasta dánarorsökin af völdum krabbameina og fer nýgengi þess vaxandi á heimsvísu.1-3 Á Íslandi nær vélindakrabbamein einungis til 1-2% krabbameinsgreininga og er meðalaldur um 72 ár við greiningu.4 Tvær megingerðir vélindakrabbameina eru kirtilþekjukrabbamein (adenocarcinoma) og flöguþekjukrabbamein (squamous cell carcinoma), en af þeim er kirtilþekjukrabbamein algengara hjá vestrænum þjóðum og hefur almennt betri horfur.1,5
Þrátt fyrir að lifun sjúklinga með vélindakrabbamein hafi batnað á síðustu tveimur áratugum, eru horfurnar enn slæmar þar sem einkenni koma oft seint fram, jafnvel þó sjúkdómurinn hafi dreift sér.6 Um helmingur sjúklinga hefur fjarmeinvörp við greiningu og er klínísk stigun sjúkdóms mikilvægur þáttur þegar kemur að meðferðarvali og mati á horfum.7 Enn í dag er læknandi meðferð aðeins hægt að veita þeim sem greinast með staðbundinn sjúkdóm. Hlutabrottnám á vélinda er helsta læknandi meðferðin og er oftast veitt samhliða krabbameinslyfja- og/eða geislameðferð fyrir aðgerðina (neoadjuvant).8 Aðgerðin er umfangsmikil og henni fylgir áhætta á alvarlegum fylgikvillum, því leggjast sjúklingar almennt inn á gjörgæslu- eða hágæsludeild til eftirlits í kjölfar aðgerða.9,10 Í völdum tilvikum, þar sem æxlið er bundið við slímhúð eða grunnt í undirslímu (submucosa), er hægt að fjarlægja meinið með vélindaspeglun.11
Helstu snemmkomnu fylgikvillarnir eftir hlutabrottnám á vélinda eru leki á samgötun (anastomotic leak), nýtilkomið gáttatif og lungnabólga.12 Áður fyrr var brottnámið fyrst og fremst framkvæmt í opinni aðgerð en síðastliðna tvo áratugi hefur aðgerðum í holsjá, kviðsjá eða þjarka fjölgað verulega. Algengasta aðgerðartegundin er svokölluð Ivor-Lewis-aðgerð, en þar er æxlið fjarlægt með kviðarhols- og brjóstholsskurðaðgerð.13
Á síðustu áratugum hefur langtímaárangur eftir skurðaðgerðir á vélinda farið batnandi.8,13 Það má helst rekja til framfara í meðferð og betra vals á sjúklingum vegna snemmgreininga og nákvæmari klínískrar TNM-stigunar fyrir aðgerð, meðal annars með tilkomu jáeindaskanna. Þeir sjúklingatengdu þættir sem eru sjálfstæðir áhættuþættir fyrir verri lifun eftir hlutabrottnám eru meðal annars hærri aldur, karlkyn, aukin sjúkdómsbyrði, vannæring og reykingar.14
Endurkoma tengist jafnframt verri lifun en allt að 52% sjúklinga fá endurkomu eftir hlutabrottnám.15 Hærri pT og/eða pN stig eru einnig sterkir forspárþættir fyrir endurkomu og þar með verri horfum.16-19
Fyrri samantekt, unnin sem lokaverkefni bakkalárgráðu, fjallaði um sjúklinga með vélindakrabbamein.20 Sú rannsókn tók til allra sjúklinga sem greindust með vélindakrabbamein á árunum 2012–2019, bæði þeirra sem gengust undir aðgerð og þeirra sem gerðu það ekki. Engin ritrýnd rannsókn hefur hingað til lýst afdrifum sjúklinga sem gengist hafa undir skurðaðgerð við vélindakrabbameini á Íslandi. Meginmarkmið þessarar rannsóknar var því að meta árangur meðferðar hjá þeim sjúklingum sem gangast undir hlutabrottnám á vélinda vegna vélindakrabbameins hérlendis með sérstaka áherslu á snemmkomna fylgikvilla, endurkomu krabbameins og langtímalifun. Til viðbótar var markmiðið að lýsa bakgrunns- og meðferðartengdum þáttum hjá þessum sjúklingahópi.
Efniviður og aðferðir
Rannsóknarsnið og leyfi
Rannsóknin var afturskyggn ferilrannsókn á sjúklingum á Landspítala sem greindust með vélindakrabbamein og höfðu ábendingu fyrir hlutabrottnámi á vélinda árin 2015-2020. Tilskilin leyfi voru fengin frá Vísindasiðanefnd (VSN-22-115), Vísindarannsóknarnefnd Landspítala og Krabbameinsskrá Íslands.
Rannsóknarþýðið
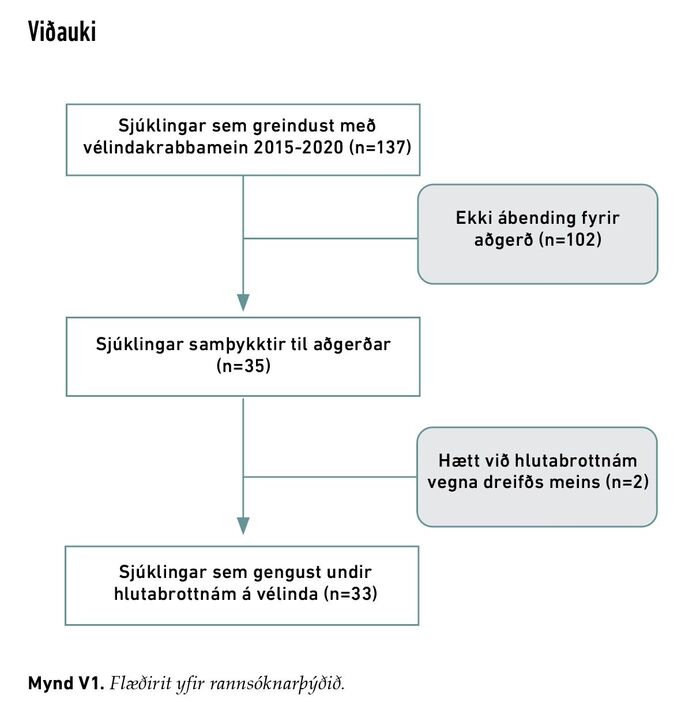
Upplýsingar um alla sjúklinga sem greindust með vélindakrabbamein (ICD-10: C15.0–C15.9) og krabbamein á maga- og vélindamótum (ICD-10: 16.0, Siewert-flokkun I, II eða óviss staðsetning á maga- og vélindamótum) á Íslandi frá 1. janúar 2015 til 31. desember 2020 voru fengnar úr Krabbameinsskrá Íslands. Krabbamein í maga- og vélindamótum eru flokkuð með vélindakrabbameini vegna sambærilegrar stigunar og meðferðar.21 Alls greindust 137 sjúklingar með vélindakrabbamein á tímabilinu og voru 35 (25,5%) af þeim sem áttu að gangast undir hlutabrottnám á vélinda frá 23. mars 2015 til 19. apríl 2021. Í tveimur tilfellum var hætt við hlutabrottnámið þar sem dreift mein fannst í upphafi aðgerðar, sem ekki hafði greinst við uppvinnslu, og því ekki um að ræða skurðtækan sjúkdóm. Lokaþýðið samanstóð því af 33 sjúklingum með vélindakrabbamein sem undirgengust hlutabrottnám á vélinda. Í viðauka má sjá flæðirit yfir rannsóknarþýðið (mynd V1).
Breytur og gagnasöfnun
Gögn voru fengin úr rafrænu sjúkraskrárkerfi Landspítala og Krabbameinsskrár. Breytur fyrir aðgerð samanstóðu af bakgrunnsþáttum sjúklinga, þar á meðal lýðfræðilegum upplýsingum, reykingasögu, sjúkdómsbyrði, klínískri stigun sjúkdómsins (cTNM) og hvort sjúklingur fékk krabbameinslyfja- og/eða geislameðferð fyrir aðgerðina (neoadjuvant). Aðgerðartengdar breytur voru aðgerðartækni, tegund aðgerðar, staðsetningu samgötunar og fjölda eitla sem fjarlægðir voru. Eftir aðgerð voru upplýsingar um meinafræðilega stigun sjúkdómsins (pTNM), fylgikvilla, lengd sjúkrahúslegu, endurinnlagnir, endurkomu krabbameins og lifun skráðar.

Þá fylgikvilla sem voru skoðaðir sérstaklega má sjá í töflu II. Samgötunarleki þurfti að vera staðfestur klínískt og með myndgreiningu. Meiriháttar sogæðaleki var skilgreindur sem þörf á aftöppun sogæðavökva >7 daga. Bráður nýrnaskaði eftir aðgerð var skilgreindur eftir KDIGO-leiðbeiningunum, annaðhvort sem meira en 50% hækkun frá kreatínínmælingu fyrir aðgerð eða hækkun um ≥26 umól/l. Nýtilkomið gáttatif var skilgreint sem gáttatif eða gáttaflökt staðfest með hjartalínuriti og án fyrri sögu. Greining á lungnabólgu nefnd í læknisnótum ásamt „nýjum íferðum“ á myndgreiningu var notuð til að bera kennsl á þá breytu. Loftbrjóst og fleiðruvökvi voru skráð sem fylgikvilli ef þörf var á inngripi með brjóstholskera. Öndunarbilun eftir aðgerð var skilgreind sem endurtekin barkaþræðing (unplanned reintubation) eða síðkomin fjarlæging barkarennu (delayed extubation, ≥48 klst) eftir aðgerð, sem tengdist ekki enduraðgerð. Eftirfylgni snemmkominna fylgikvilla voru 30 dagar og voru þeir flokkaðir eftir alvarleika með Clavien--Dindo-flokkunarkerfinu.22 Flokkur 1 segir til um öll frávik frá eðlilegu bataferli eftir aðgerð, til dæmis óráð án lyfjameðferðar, vökvi í æð, notkun ógleðilyfja eða þvagræsilyfja, og þörf á verkjameðferð með aðstoð sérhæfðs verkjateymis. Flokkur 2 eru fylgikvillar sem krefjast lyfjameðferðar umfram það sem er notað við flokk 1, til dæmis blóðgjöf, næring í æð og sýklalyf. Flokkur 3 eru fylgikvillar sem krefjast inngrips með aðgerð eða speglun, annaðhvort í staðdeyfingu (3a) eða svæfingu (3b). Flokkur 4 samanstendur af lífshættulegum fylgikvillum, með bilun í einu (4a) eða fleirum (4b) líffærakerfum, sem krefjast gjörgæslumeðferðar. Dánartíðni innan 30 daga frá aðgerð var skráð sem flokkur 5.
Heildarlifun var skilgreind sem tími frá vélindaaðgerð til andláts af hvaða orsök sem er. Sjúkdómsfrí lifun var skilgreind sem tími frá aðgerð til fyrstu staðfestu endurkomu krabbameins eða andláts af hvaða orsök sem er. Upplýsingar um lifun og endurkomu voru skráðar í gagnagrunninn til júlí 2025.
Tölfræðiúrvinnsla
Tölfræðiúrvinnsla var framkvæmd með R (útgáfu 4.4.1) og RStudio (útgáfu 2024.09.0). Lýsandi tölfræði var notuð til að meta rannsóknarþýðið í heild. Flokkabreytur eru birtar sem fjöldi og hlutfall (%), en samfelldar breytur sem miðgildi og fjórðungaspönn (fs). Wilcoxon Signed-Rank Test var notað til þess að meta misræmi milli cTNM- og pTNM-stigunar. Í kjölfar þess að tíðni samgötunarleka reyndist hærri í niðurstöðum en búist var við var gerð leitandi greining (explorative analysis) á hópum með og án samgötunarleka. Mann Whitney U tölfræðipróf var notað til að bera saman tölulegar breytur milli hópa með og án samgötunarleka og Fisher´s exact próf fyrir flokkabreytur. Tölfræðileg marktækni miðaðist við p<0,05, en áhrifastærð með Cohen´s d (standardized mean difference, SMD) var notuð til að meta mun á áhættuþáttum milli hópa. Heildarlifun og sjúkdómsfrí lifun voru metnar með Kaplan-Meier aðferðinni. Endurkoma krabbameins var reiknuð sem uppsafnað nýgengi (cumulative incidence) þar sem dánartíðni var tekin með sem samkeppandi atburður (competing event).
Niðurstöður
Bakgrunns- og meðferðartengdir þættir fyrir aðgerð
Alls gengust 33 sjúklingar undir hlutabrottnám á vélinda eftir að hafa greinst með vélindakrabbamein á árunum 2015-2020. Tafla I sýnir bakgrunnsþætti sjúklinga, æxliseiginleika, meðferð fyrir aðgerð og aðgerðartengda þætti. Miðgildi aldurs var 66 ár (spönn: 44–78) og í meirihluta voru karlmenn (76%). Krabbameinin reyndust í flestum tilvikum vera kirtilmyndandi (73%) og í 82% tilvika var æxlið staðsett í neðri hluta vélindans. Þá höfðu 14 (42%) sjúklingar American Society of Anesthesiologist (ASA) flokkun ≥3 fyrir aðgerð.
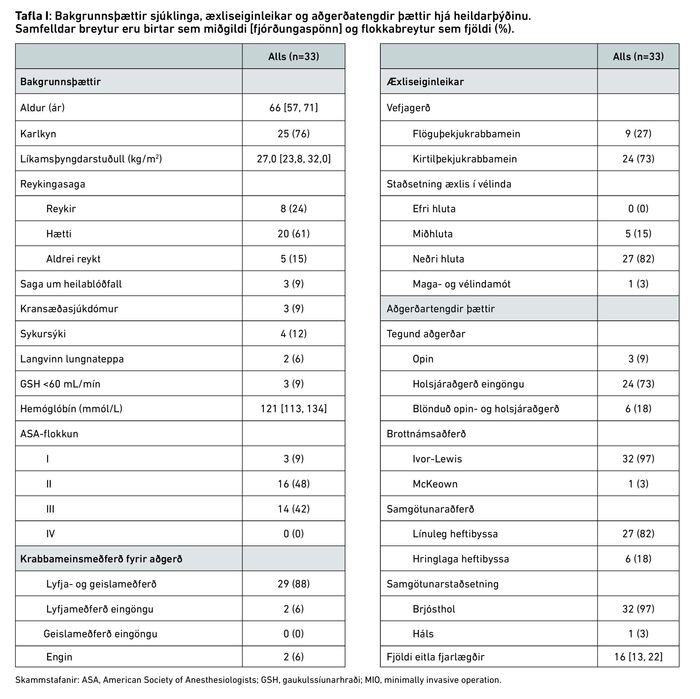
Ivor-Lewis-aðferðin, sem felur í sér samgötun í brjóstholi milli maga og vélinda, var framkvæmd í 97% tilvika og algengasta aðgerðartæknin var kviðsjár- og brjóstholsspeglun eingöngu (70%) þar sem aðgerðin er framkvæmd í gegnum minni skurði (minimally invasive) í staðinn fyrir opna aðgerð á kviðar- og brjóstholi. Flestir sjúklingar fengu krabbameins-lyfja- og/eða geislameðferð fyrir aðgerðina (n=31, 94%), en tveir þeirra afþökkuðu geislameðferð og fengu því einungis krabbameinslyfjameðferð (tafla I).
Stigun sjúkdóms fyrir og eftir aðgerð
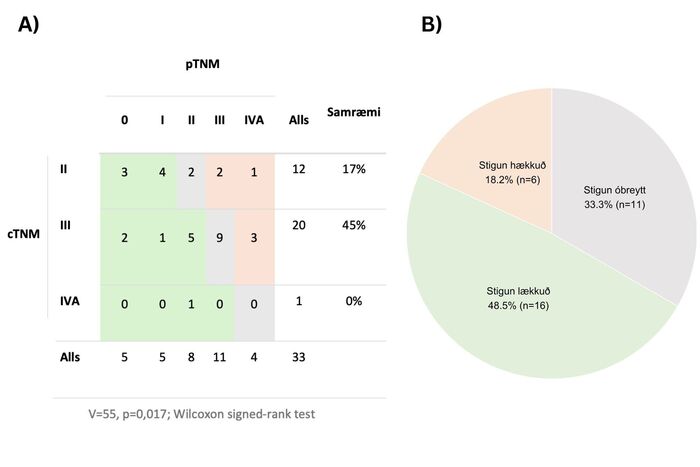
Fyrir aðgerðina voru flestir sjúklingar með cTNM-stigun III (61%) og II (36%), en aðeins einn á stigi IV-A (3%) og enginn á stigi I. Eftir aðgerð voru 48% sjúklinga með lægri pTNM-stigun heldur en cTNM-stigun fyrir aðgerðina, 18% með hærri stigun og í tæplega þriðjungi tilfella var stigun óbreytt (33%) (mynd 1B). Sjá má samræmi milli cTNM- og pTNM-stigunar eftir aðgerð á mynd 1A. Ekki náðist róttækt brottnám hjá sex sjúklingum (18%), en hjá þeim hafði krabbameinið vaxið út í úthjúp (adventitia) vélindans. Þeir sjúklingar sem voru með hærri stigun eftir aðgerð voru með hærri flokkun svæðiseitla (cN<pN). Flokkun frumæxlisins fyrir og eftir aðgerð (cT og pT) reyndist hins vegar misjöfn.
Snemmkomnir fylgikvillar
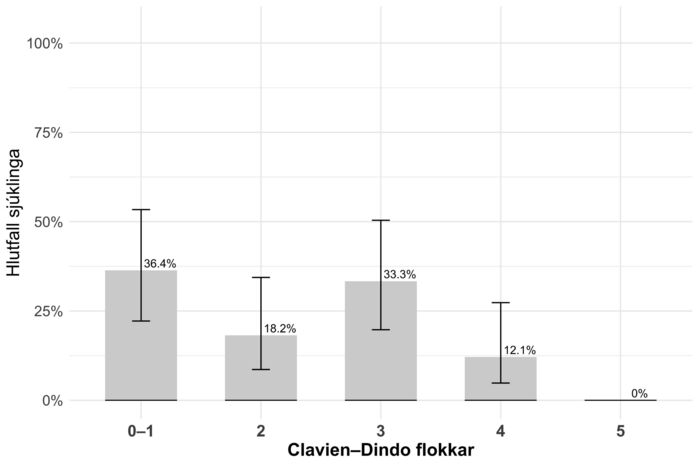
Af heildarþýðinu voru 12 (36%) án fylgikvilla eða með minni háttar frávik eftir aðgerð (Clavien-Dindo 0-1) (mynd 2). Alls fékk 21 (64%) sjúklingur fylgikvilla sem flokkuðust undir Clavien-Dindo ≥2. Meðal þeirra voru sex (18%) í flokki 2 (minni háttar fylgikvillar sem krefjast lyfjameðferðar), fjórir (12%) í flokki 3a (inngrip án svæfingar) og sjö (21%) í flokki 3b (inngrip í svæfingu). Fjórir sjúklingar fengu lífshættulega fylgikvilla; einn í flokki 4a (3%) og þrír í flokki 4b (9%). Enginn sjúklingur lést innan 30 daga frá aðgerð (flokkur 5) en tveir (6%) innan 90 daga.
Samgötunarleki var algengasti fylgikvillinn og greindist í kjölfar 30% aðgerða (tafla II). Hann var meðhöndlaður með stoðneti hjá sjö sjúklingum en hjá þremur þurfti enduraðgerð. Öndunarbilun kom fram hjá þremur (9%), en aðrir meiri háttar fylgikvillar komu sjaldnar fram. Algengustu minni háttar fylgikvillar voru lungnabólga (15%) og nýtilkomið gáttatif (9%). Miðgildi [fs] dvalar á gjörgæslu eftir aðgerð var 1 dagur [1–3] og miðgildi sjúkrahúslegu eftir aðgerð voru 16 dagar [8–31].
Lifun og endurkoma krabbameins
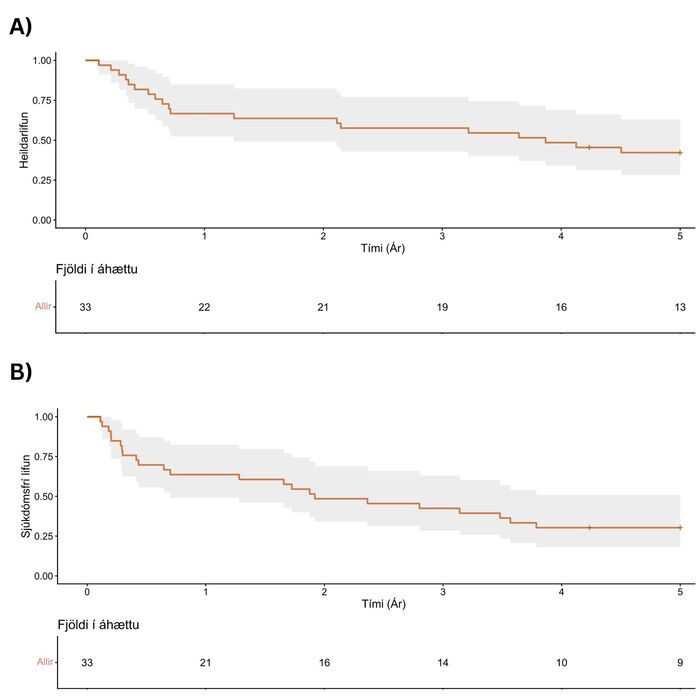
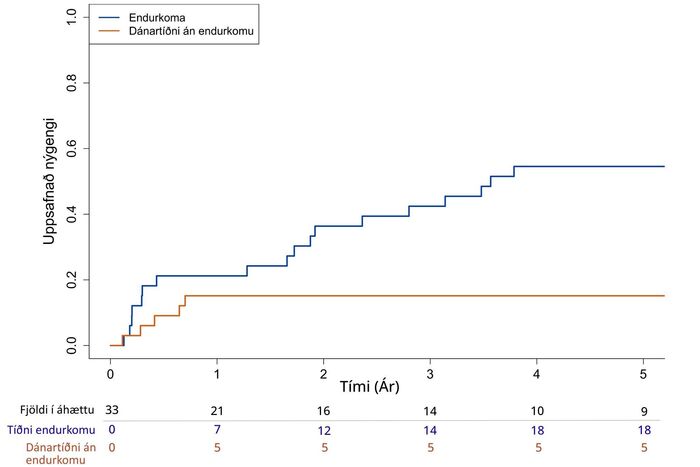
Heildarlifun (95% öryggisbil) var 70% (56%-89%) eftir eitt ár og 44% (30%-65%) eftir fimm ár (mynd 3A). Af þeim 19 sjúklingum sem létust á fyrstu fimm árunum eftir aðgerð voru flestir (n=15, 80%) sem létust af krabbameinstengdri orsök, vegna endurkomu krabbameinsins. Sjúkdómsfrí lifun (95% öryggisbil) var 64% (49%-82%) eftir eitt ár og 30% (18%-51%) eftir fimm ár (mynd 3B). Miðgildi [fs] eftirfylgdartíma fyrir lifun voru 3,9 ár [0,6-5,8] og fyrir sjúkdómsfría lifun voru það 1,7 ár [0,30 – 3,0]. Uppsafnað nýgengi á endurkomu krabbameinsins var 21% eftir eitt ár en 55% eftir fimm ár (mynd 4).
Leitandi greining á samanburði sjúklinga með og án samgötunarleka
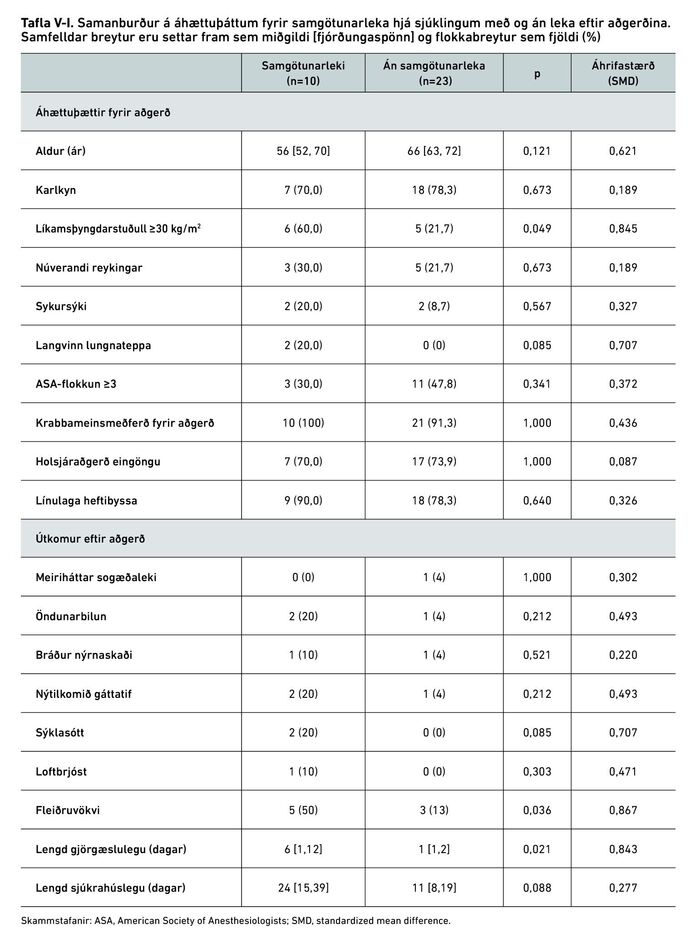
Tafla V-I sýnir mun á áhættuþáttum og útkomum einstaklinga með og án samgötunarleka. Hlutfall sjúklinga í offitu var marktækt hærra í hópi þeirra sem fengu samgötunarleka (60%, sbr. 22%, p=0,049, SMD=0,85). Miðgildi [fs] aldurs var 10 árum lægra í hópnum sem fékk leka (56 [52-70], sbr. 66 [63, 72], p=0,121, SMD=0,621) og tíðni langvinnrar lungnateppu hærri (20%, sbr. 0%, p=0,085, SMD=0,707), en munurinn var þó ekki marktækur. Hvað varðar fylgikvilla var Clavien-Dindo flokkur ≥3b algengari í hópnum með leka (70%, sbr. 17%, p=0,006) þar sem samgötunarleki er ávallt flokkaður í Clavien-Dindo >2, nema fylgikvillinn sé meðhöndlaður án inngrips, sem var ekki raunin hér. Meðferð fleiðruvökva var einnig marktækt hærri hjá einstaklingum með samgötunarleka. Miðgildi dvalartíma á gjörgæslu (6 dagar, sbr. 1 dagur, p=0,021) og lengd sjúkrahúslegu í heild sinni (24 dagar, sbr. 11 dagar, p=0,088) var lengri meðal þeirra sem fengu samgötunarleka, þótt seinni samanburðurinn hafi ekki náð tölfræðilegri marktækni. Tíðni óvæntrar enduraðgerðar og sýklasóttar var einnig hærri í hópnum með samgötunarleka, en þó var munurinn ekki tölfræðilega marktækur. Aðrir áhættuþættir eða fylgikvillar sýndu áhrifastærð undir 0,50 milli hópa.
Umræða
Þessi rannsókn er sú fyrsta sem einblínir sérstaklega á sjúklinga sem hlutu meðferð með hlutabrottnámi á vélinda í íslensku þýði og veitir ítarlega lýsingu á bakgrunnsþáttum og afdrifum þeirra eftir aðgerð. Þessi rannsókn sýndi að langtímalifun hérlendis í kjölfar hlutabrottnáms á vélinda vegna vélindakrabbameins er 44%, en sömu niðurstöður sáust í Svíþjóð fyrir sama tímabil.8 Þrátt fyrir ásættanlega langtímaniðurstöðu fékk tæplega helmingur sjúklinga fylgikvilla af flokki Clavien-Dindo ≥3a (45%).
Á Íslandi eru fáar skurðaðgerðir við vélindakrabbameini framkvæmdar á hverju ári. Þrátt fyrir það er mikilvægt að slík þjónusta sé til staðar innan lands, til að tryggja að sjúklingar með staðbundið vélindakrabbamein geti fengið meðferð án þess að þurfa að sækja hana erlendis. Jafnframt hefur slík þjónusta mikilvægt gildi fyrir bráðaþjónustu eins og við vélindarof sem oft krefst tafarlausrar meðferðar og í einstaka tilfellum hlutabrottnáms á vélinda. Í afturskyggnri rannsókn á vélindaaðgerðum við Brigham and Women´s Hospital í Bandaríkjunum reyndist ekki vera munur á dánartíðni sjúklinga sem undirgengust aðgerð hjá skurðlæknum með <7 aðgerðir/ári (low volume) og þeirra með meira magn aðgerða (high volume).23 Hins vegar var tíðni fylgikvilla aðeins hærri hjá skurðlæknum með færri aðgerðir. Bandaríska þýðið var sambærilegt þýðinu í þessari rannsókn hvað varðar bakgrunnsþætti, fyrir utan að hérlendis var hærri tíðni krabbameinsmeðferða fyrir aðgerð (80%, sbr. 94%) og hærri cTNM-stigun.23 Hvað varðar fylgikvilla, þá var tíðni nýtilkomins gáttatifs og meiriháttar sogæðaleka lægri í okkar rannsókn samanborið við bandarísku rannsóknina. Aftur á móti var tíðni bráðs nýrnaskaða, aftöppunar á fleiðruvökva, blóðsýklasóttar og samgötunarleka hærri hérlendis.23
Í erlendum rannsóknum hefur hlutfall samgötunarleka verið allt upp að 49% en algengast er að hlutfallið sé á bilinu 5–25%.24 Ekki er ljóst hvað veldur hærri lekatíðni hér á landi (30%). Þrátt fyrir þessa niðurstöðu nær rannsóknin til aðgerða fram til apríl 2021 og því er ekki hægt að fullyrða hvort tíðni leka hafi breyst á síðustu árum. Kviðsjáraðgerðir voru einnig að ryðja sér til rúms hérlendis á rannsóknartímabilinu. Því er möguleiki að skurðlæknarnir hafi enn verið snemma í lærdómskúrfunni (early learning phase) þegar kom að framkvæmd hlutabrottnáms á vélinda í kviðsjá þar sem aðgerðin er tæknilega flókin og krefst mikillar reynslu.25 Þar að auki getur fámennur sjúklingahópur valdið talsverðum breytileika í niðurstöðum. Leitandi greining á okkar þýði sýndi að sjúklingar með líkamsþyngdarstuðul >30kg/m2 voru líklegri til að þróa með sér samgötunarleka, en offita er þekktur áhættuþáttur fyrir þeim fylgikvilla.26 Jafnframt tengdist samgötunarleki hærri tíðni aftöppunar á fleiðruvökva, en hærri tíðni aftöppunar hérlendis miðað við önnur þýði gæti skýrst af hærri lekatíðni þar sem samgötunarleki er áhættuþáttur fyrir aukinn fleiðruvökva.23,27 Með því að minnka tíðni samgötunarleka væri mögulega hægt að minnka áhættu á öðrum fylgikvillum og þar með stytta legutíma.
Í fjölsetrarannsókn sem náði til 24 stofnana með mikla reynslu af vélindaaðgerðum (high volume centers), var tíðni fylgikvilla metin samkvæmt Clavien-Dindo flokkunarkerfinu eins og í þessari rannsókn.9 Í samanburði við okkar niðurstöður voru fylgikvillar í flokki 2 sambærilegir (18%, sbr. 20%). Tíðni fylgikvilla sem kröfðust inngrips var hærri í okkar þýði, bæði flokkur 3 (33%, sbr. 21%) og flokkur 4 (12%, sbr. 8%), sem sennilega skýrist af hærra hlutfalli samgötunarleka. Þrátt fyrir það var snemmkomin dánartíðni, flokkur 5, lægri í okkar þýði (0%, sbr. 3%).
Í þessari rannsókn var sjúkdómsfrí lifun 30% og uppsafnað nýgengi endurkomu krabbameins 55% eftir fimm ár. Þessar niðurstöður endurspegla að endurkoma eftir hlutabrottnám á vélinda er algeng þrátt fyrir að meðferð hafi verið veitt í læknandi tilgangi. Í stórri fjölsetrarannsókn í Evrópu sem tók til 4.719 sjúklinga var sjúkdómsfrí lifun eftir fimm ár 41% sem er aðeins hærra en í okkar rannsókn.28 Einnig sýndi evrópska rannsóknin að 56% sjúklinga fengu endurkomu krabbameins, sambærilegt við okkar niðurstöður, en miðgildi eftirfylgdartíma fyrir sjúkdómsfría lifun var þó styttri í okkar rannsókn (1,7 ár, sbr. 2,9 ár í evrópsku rannsókninni) sem gæti haft áhrif á þann samanburð. Þýðin voru að mestu sambærileg með tilliti til þekktra áhættuþátta fyrir endurkomu og lifun en þrátt fyrir mun á sjúkdómsfrírri lifun í okkar þýði samanborið við evrópsku rannsóknina (30%, sbr. 41%) ber að túlka þennan mun með varúð þar sem þýðið er lítið og munurinn gæti samsvarað fáum sjúklingum. Niðurstaða evrópsku rannsóknarinnar fellur þó innan 95% öryggisbils okkar (18%-51%), en samanburðurinn gefur engu að síður tilefni til frekari athugunar í stærra þýði.
Marktækur munur var á stigun sjúkdómsins fyrir og eftir aðgerð (p = 0,017). Tæplega helmingur sjúklinga var með lægri pTNM-stigun eftir aðgerð miðað við cTNM fyrir aðgerðina. Þetta má sennilega að mestu leyti skýra með áhrifum krabbameinslyfja- og geislameðferðar. Hins vegar voru 18% tilfella með hærri pTNM-stigun miðað við cTNM, vegna fleiri jákvæðra eitla sem greindust eftir aðgerð. Þetta gæti orsakast af ófullnægjandi meðferðarsvörun og hröðum vexti æxlisins í sumum tilvikum. Einnig geta eitlar haft smásæ meinvörp (micrometastases) sem sjást ekki nema á vefjafræðisýni og því virst eðlilegir á myndgreiningu. Niðurstöðurnar endurspegla vel þekktar takmarkanir cTNM-stigunar fyrir aðgerð og misræmi á cTNM og pTNM,29,30 þrátt fyrir stigun með jáeindaskanna, holsjárómskoðun (endoscopic ultrasound, EUS) og berkjuspeglun. Því er mikilvægt að túlka cTNM-niðurstöður með varúð þegar komið er að skurðaðgerðinni.
Styrkleikar og veikleikar
Styrkleikar rannsóknarinnar eru að hún byggir á þýði sem nær til heillar þjóðar og þar sem skráning krabbameina er lögbundin á Íslandi eykur það gæði gagnanna og nákvæmni skráningarinnar. Aðgerðirnar voru að mestu leyti einsleitar, sem lágmarkar breytileika í meðferð vegna mismunandi aðgerðartækni. Helsti veikleiki rannsóknarinnar er fámennur sjúklingahópur sem takmarkar tölfræðilegt afl og möguleika til að greina marktæk tengsl milli breyta. Einnig vantaði upplýsingar um mikilvæga áhættuþætti, svo sem næringarástand, en þær upplýsingar er sjaldan að finna í sjúkraskrám þessara sjúklinga.
Árangur hlutabrottnáms á Íslandi er ásættanlegur með 30-daga dánartíðni lægri eða sambærilega því sem sést í erlendum þýðum og sambærilega langtímalifun og í Svíþjóð. Tíðni samgötunarleka reyndist þó ívið hærri en víða annars staðar.8,9,23,31 Það virtist ekki hafa áhrif á snemmkomna dánartíðni, sem gæti endurspeglað skilvirka greiningu og meðhöndlun fylgikvillans. Þessar niðurstöður undirstrika mikilvægi frekari rannsókna á samgötunarleka í íslensku þýði, til að bæta áhættumat fylgikvillans fyrir aðgerð sem og að styðja sjúklinga betur í upplýstri ákvarðanatöku. Niðurstöður þessarar rannsóknar gætu þannig nýst sem grunnur að áframhaldandi rannsóknum og mögulega stuðlað að breytingum á meðferð vélindakrabbameins á Landspítala.
Þakkir
Þakkir fær Flensborgarskólinn í Hafnarfirði fyrir styrk úr Fræðslusjóð Jóns Þórarinssonar.
Mynd 1. A) Tafla sem sýnir mun milli klínískrar (cTNM) og meinafræðistigunnar (pTNM). B) Hlutfall sjúklinga þar sem stigun lækkaði, var óbreytt eða hækkaði eftir aðgerð.
Mynd 2. Hlutfall sjúklinga í hverjum Clavien-Dindo flokki með 95% öryggisbili. Ef sjúklingur fékk fylgikvilla sem tilheyrðu fleiri en einum flokki, var aðeins hæsti flokkurinn tekinn til greina.
Mynd 3. Kaplan-Meier graf sem sýnir A) heildarlifun og B) sjúkdómsfría lifun, allra sjúklinga sem undirgengust hlutabrottnám á vélinda.
Mynd 4. Graf sem sýnir uppsafnað nýgengi á endurkomu vélindakrabbameins og dánartíðni án endurkomu (samkeppandi atburður) eftir aðgerð. Taflan neðst á myndinni sýnir fjölda í áhættu árlega, uppsafnaðan fjölda atburða fyrir endurkomu og andlát án endurkomu.
Mynd V1. Flæðirit yfir rannsóknarþýðið.
Heimildir
| 1. Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2024;74(3):229-263. https://doi.org/10.3322/caac.21834 PMid:38572751 | ||||
| 2. Deboever N, Jones CM, Yamashita K, er al. Advances in diagnosis and management of cancer of the esophagus. BMJ 2024;385:e074962. https://doi.org/10.1136/bmj-2023-074962 PMid:38830686 | ||||
| 3. DiSiena M, Perelman A, Birk J, et al. Esophageal Cancer: An Updated Review. South Med J 2021;114(3):161-168. https://doi.org/10.14423/SMJ.0000000000001226 PMid:33655310 | ||||
| 4. Krabbameinsskrá. Vélindakrabbamein. (https://www.krabb.is/krabbamein/tolfraedi/krabbamein-og-gaedaskraning). - september 2025. | ||||
| 5. Matz M, Valkov M, Sekerija M, et al. Worldwide trends in esophageal cancer survival, by sub-site, morphology, and sex: an analysis of 696,974 adults diagnosed in 60 countries during 2000-2014 (CONCORD-3). Cancer Commun (Lond) 2023;43(9):963-980. https://doi.org/10.1002/cac2.12457 PMid:37488785 PMCid:PMC10508138 | ||||
| 6. Griffin SM, Jones R, Kamarajah SK, et al. Evolution of Esophagectomy for Cancer Over 30 Years: Changes in Presentation, Management and Outcomes. Ann Surg Oncol 2021;28(6):3011-3022. https://doi.org/10.1245/s10434-020-09200-3 PMid:33073345 PMCid:PMC8119401 | ||||
| 7. Jamel S, Tukanova K, Markar S. Detection and management of oligometastatic disease in oesophageal cancer and identification of prognostic factors: A systematic review. World J Gastrointest Oncol 2019;11(9):741-749. https://doi.org/10.4251/wjgo.v11.i9.741 PMid:31558978 PMCid:PMC6755111 | ||||
| 8. Lundberg E, Mattsson F, Gottlieb-Vedi E, et al. Time Trends in Survival After Surgery for Esophageal Cancer in a National Population-Based Study in Sweden. Ann Surg Oncol 2025;32(5):3167-3174. https://doi.org/10.1245/s10434-025-17007-3 PMid:39962004 PMCid:PMC11976786 | ||||
| 9. Low DE, Kuppusamy MK, Alderson D, et al. Benchmarking Complications Associated with Esophagectomy. Ann Surg 2019;269(2):291-298. https://doi.org/10.1097/SLA.0000000000002611 PMid:29206677 | ||||
| 10. Sahm E, Olutola O, Ata A, et al. Society of Asian Academic Surgeons When Is Intensive Care Unit Admission Needed After an Esophagectomy? J Surg Res 2024;300:109-116. https://doi.org/10.1016/j.jss.2024.04.067 PMid:38810525 | ||||
| 11. Noordzij IC, Curvers WL, Schoon EJ. Endoscopic resection for early esophageal carcinoma. J Thorac Dis 2019;11(Suppl 5):S713-S722. https://doi.org/10.21037/jtd.2019.03.19 PMid:31080649 PMCid:PMC6503291 | ||||
| 12. Edmondson J, Hunter J, Bakis G, O'Connor A, et al. Understanding Post-Esophagectomy Complications and Their Management: The Early Complications. Journal of Clinical Medicine 2023;12(24). https://doi.org/10.3390/jcm12247622 PMid:38137691 PMCid:PMC10743498 | ||||
| 13. Bolger JC, Donohoe CL, Lowery M, et al. Advances in the curative management of oesophageal cancer. Br J Cancer 2022;126(5):706-717. https://doi.org/10.1038/s41416-021-01485-9 PMid:34675397 PMCid:PMC8528946 | ||||
| 14. Kamarajah SK, Marson EJ, Zhou DY, et al. Meta-analysis of prognostic factors of overall survival in patients undergoing oesophagectomy for oesophageal cancer. Diseases of the Esophagus 2020;33(11). https://doi.org/10.1093/dote/doaa038 PMid:32448903 | ||||
| 15. Kang M, Kim W, Kang CH, et al. The Prognostic Value of Oligo-Recurrence Following Esophagectomy for Esophageal Cancer. J Chest Surg 2023;56(6):403-411. https://doi.org/10.5090/jcs.23.050 PMid:37696781 PMCid:PMC10625960 | ||||
| 16. Kalff MC, Henckens SPG, Voeten DM, et al. Recurrent Disease After Esophageal Cancer Surgery: A Substudy of The Dutch Nationwide Ivory Study. Ann Surg 2022;276(5):806-813. https://doi.org/10.1097/SLA.0000000000005638 PMid:35880759 | ||||
| 17. Mariette C, Balon JM, Piessen G, et al. Pattern of recurrence following complete resection of esophageal carcinoma and factors predictive of recurrent disease. Cancer 2003;97(7):1616-23. https://doi.org/10.1002/cncr.11228 PMid:12655517 | ||||
| 18. Hu SY, Gao HJ, Jiang ZH, et al. A Recurrence Predictive Model for Node-negative Esophageal Squamous Cell Carcinoma After Upfront Esophagectomy. Semin Thorac Cardiovasc Surg 2024;36(1):102-111. https://doi.org/10.1053/j.semtcvs.2022.08.016 PMid:36089122 | ||||
| 19. Lee PC, Mirza FM, Port JL, et al. Predictors of recurrence and disease-free survival in patients with completely resected esophageal carcinoma. J Thorac Cardiovasc Surg 2011;141(5):1196-206. https://doi.org/10.1016/j.jtcvs.2011.01.053 PMid:21397267 | ||||
| 20. Lárusson ED. Gæðaskráning vélindakrabbameina á Íslandi 2012-2019. Samanburður milli tímabila og við gæðaskráningu í Svíþjóð. Læknadeild. Skemman: Háskóli Íslands; 2020:86. | ||||
| 21. Rice TW, Ishwaran H, Ferguson MK, et al. Cancer of the Esophagus and Esophagogastric Junction: An Eighth Edition Staging Primer. J Thorac Oncol 2017;12(1):36-42. https://doi.org/10.1016/j.jtho.2016.10.016 PMid:27810391 PMCid:PMC5591443 | ||||
| 22. Dindo D, Demartines N, Clavien PA. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Ann Surg 2004;240(2):205-13. https://doi.org/10.1097/01.sla.0000133083.54934.ae PMid:15273542 PMCid:PMC1360123 | ||||
| 23. Dolan D, White A, Lee DN, et al. Short and Long-term Outcomes Among High-Volume vs Low-Volume Esophagectomy Surgeons at a High-Volume Center. Semin Thorac Cardiovasc Surg 2022;34(4):1340-1350. https://doi.org/10.1053/j.semtcvs.2021.09.007 PMid:34560249 | ||||
| 24. Kamarajah SK, Lin A, Tharmaraja T, et al. Risk factors and outcomes associated with anastomotic leaks following esophagectomy: a systematic review and meta-analysis. Dis Esophagus 2020;33(3). https://doi.org/10.1093/dote/doz089 PMid:31957798 | ||||
| 25. Ozawa S, Koyanagi K, Ninomiya Y, et al. Postoperative complications of minimally invasive esophagectomy for esophageal cancer. Ann Gastroenterol Surg 2020;4(2):126-134. https://doi.org/10.1002/ags3.12315 PMid:32258977 PMCid:PMC7105848 | ||||
| 26. Axtell AL, Angeles C, McCarthy DP, et al. Anastomotic Leak After Esophagectomy: Analysis of the STS General Thoracic Surgery Database. Ann Thorac Surg 2025;119(4):796-804. https://doi.org/10.1016/j.athoracsur.2024.12.019 PMid:39864771 | ||||
| 27. Gao C, Xu G, Wang C, Wang D. Evaluation of preoperative risk factors and postoperative indicators for anastomotic leak of minimally invasive McKeown esophagectomy: a single-center retrospective analysis. J Cardiothorac Surg 2019;14(1):46. https://doi.org/10.1186/s13019-019-0864-4 PMid:30819240 PMCid:PMC6394086 | ||||
| 28. Gujjuri RR, Clarke JM, Elliott JA, et al. Predicting long-term survival and time-to-recurrence after esophagectomy in patients with esophageal cancer - Development and validation of a multivariate prediction model. Ann Surg 2023;277(6):971-978. https://doi.org/10.1097/SLA.0000000000005538 PMid:37193219 PMCid:PMC7614526 | ||||
| 29. Capovilla G, Moletta L, Pierobon ES, et al. Optimal Treatment of cT2N0 Esophageal Carcinoma: Is Upfront Surgery Really the Way? Ann Surg Oncol 2021;28(13):8387-8397. https://doi.org/10.1245/s10434-021-10194-9 PMid:34142286 | ||||
| 30. Kollatos C, Johansson J, Hermansson M. 513 What factors influence the accuracy of clinical staging of esophageal- and gastric cancer in sweden? A national register study. Diseases of the Esophagus 2021;34(Supplement_1). https://doi.org/10.1093/dote/doab052.513 | ||||
| 31. Bailey SH, Bull DA, Harpole DH, et al. Outcomes after esophagectomy: a ten-year prospective cohort. Ann Thorac Surg 2003;75(1):217-22; discussion 222. https://doi.org/10.1016/S0003-4975(02)04368-0 PMid:12537219 | ||||