10. tbl. 95. árg. 2009
Fræðigrein
Flöguþekjukrabbamein á höfuð- og hálssvæði
Ágrip
Flöguþekjukrabbamein á höfuð- og hálssvæði eru nokkuð algeng og tengist tilurð þeirra sterklega reykingum og áfengisneyslu. Aðrir áhættuþættir eru sýkingar af völdum human papillomavirus. Meðferð þessara æxla kallar á samstarf margra sérgreina eigi góður árangur að nást. Í gegnum tíðina hafa skurðaðgerðir og geislameðferð verið meginstoð meðferðar en á síðastliðnum áratug hefur samtvinnuð geisla- og lyfjameðferð leikið æ stærra hlutverk, sérstaklega gegn sjúkdómi á hærra stigi. Eigi greining sér stað á lægri stigum sjúkdómsins eru horfur tiltölulega góðar. Útbreiddur sjúkdómur hefur slæmar horfur og hafa framfarir í meðferð á því stigi verið takmarkaðar. Á síðari árum hafa orðið umtalsverðar breytingar á meðferð þessara æxla og eru þær framfarir hvatinn að þessari grein.
Faraldsfræði
Krabbamein á höfuð- og hálssvæði eru nokkuð algeng og er yfirgnæfandi meirihluti þeirra af flöguþekjugerð (FÞKHH).1 Meðalaldur við greiningu er um 60 ár og karlar eru þrisvar til fjórum sinnum líklegri til að greinast með FÞKHH en konur. Hærra nýgengi hjá körlum má sennilega rekja til þess að þeir eru líklegri til að reykja og nota áfengi í óhófi. Á árunum 2001-2005 var árlegt nýgengi krabbameins í barkakýli 2,2/100.000 hjá íslenskum körlum en 0,7/100.000 hjá íslenskum konum. Krabbamein í vör og munnholi voru nokkru algengari eða 4,4/100.000 hjá körlum en 2,0/100.000 hjá konum. Búist er við meira en 47.500 nýjum tilfellum í Bandaríkjunum árið 2008 og reikna má með að meira en 11.200 látist af völdum sjúkdómsins.2 Í Evrópu var áætlað að allt að 130.000 ný tilfelli hefðu greinst árið 2006 og um væri að ræða 7% allra greinda krabbameina.3 Á heimsvísu var talið að meira en 477.000 tilfelli af FÞKHH yrðu greind í körlum en 167.000 í konum.4 Það má því sjá að þetta er umfangsmikið vandamál á heimsvísu þó að tilfellin hérlendis séu frekar fá.
Áhættuþættir
Tóbaksreykingar og áfengisneysla eru talin skýra verulegan hluta allra tilfella FÞKHH og hefur verið áætlað að áhættan sé allt að fertugföld ef saman fara verulegar reykingar og óhófleg neysla áfengis.5 Tengsl við reykingar eru mun sterkari en tengslin við áfengisneyslu og áhættan er mest ef reykingar og áfengisneysla fara saman.6 Áfengisneysla ein sér virðist einnig vera sjálfsstæður áhættuþáttur en ekki eins afgerandi og reykingar. Munn- og neftóbaksnotkun hefur einnig verið tengd FÞKHH en tengsl reyklauss tóbaks við krabbamein virðast veigaminni en tengsl reyktóbaks.7 Léleg tannhirða er einnig álitin áhættuþáttur. Sjúklingum með sögu um FÞKHH er hættara við endurteknum krabbameinum á höfuð- og hálssvæði ásamt öðrum illkynja sjúkdómum tengdum sömu áhættuþáttum, sérstaklega lungnakrabbameini og vélindakrabbameini og endurspeglar það víðtæk krabbameinsvaldandi áhrif tóbaksreyks á slímhúðir loft- og meltingarvegar (field cancerization).8, 9 Á undanförnum árum hefur komið í ljós að sýkingar af völdum human papillomavirus (HPV), sérstaklega sermigerð (serotype) 16 og 18 eru sterkur áhættuþáttur FÞKHH og sennilega skýringin í mörgum þeim tilfella þar sem reykingum og áfengisdrykkju er ekki til að dreifa.10, 11 Svo virðist sem HPV tengdum FÞKHH fari fjölgandi og þau kunni að hafa betri horfur en þau æxli sem ekki tengjast HPV.12, 13 HPV-sýkingar virðast vera sérstaklega tengdar krabbameinum í munnholi og koki en síður í barkakýli.11
Einkenni
Sjúklingar með FÞKHH leita til læknis vegna ýmissa einkenna og ræður staðsetning og útbreiðsla meinsins þar mestu. Krabbamein í munnholi koma oftast fram sem sár sem gróa ekki eða fyrirferð. Verkir eru algengir og geta bent til þess að meinið sé vaxið inn í taugar. Einnig geta þau haft áhrif á hreyfingu tungu með kyngingarerfiðleikum og þá um leið áhrif á næringarinntöku með tilheyrandi þyngdartapi. Séu meinin vaxin inn í kjálkabein geta lausar tennur eða verkir í tönnum verið vandamál, sem og dofi í dreifingu fimmtu heilataugar. Krabbamein í munnkoki hafa oftast kyngingarerfiðleika í för með sér og verki og ekki er óalgengt að sjúklingar hafi fengið nokkra sýklalyfjakúra vegna hálsbólgu áður en meinið uppgötvast. Aukinheldur getur meinið uppgötvast við uppvinnslu á hnúti á hálsi. Krabbamein í barkakýli hafa mjög mismunandi einkenni en mestu skiptir staðsetning innan barkakýlis. Æxli í ofanraddglufu (supraglottis) geta orðið stór áður en þau fara að hafa áhrif á öndun eða kyngingu og þar sem sogæðakerfið þar er ríkulegt eru eitlameinvörp algeng. Hins vegar eru mein á raddböndum oft greind snemma þar sem sjúklingur er með hæsi vegna breytinga á eiginleikum raddbandsins eða í lengra gengnum meinum út af festingu raddbands vegna ífarandi vaxtar. Krabbamein í nefholi geta orðið stór án þess að sjúklingurinn fái veruleg einkenni. Vökvi í miðeyra án skýringar í fullorðnu fólki getur gefið til kynna æxli í nefkoki en algengasta einkenni þess æxlis er hnútur á hálsi. Við mat á FÞKHH á alltaf að gera ítarlega heilataugaskoðun þar sem krabbamein geta vaxið með taugum að höfuðkúpubotni og inn í heilabú.
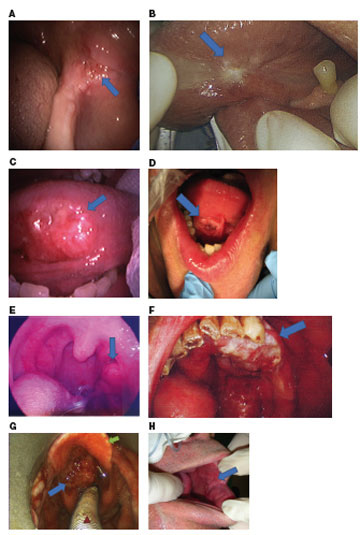
Mynd 1. Klínískar myndir af flöguþekjukrabbameinum á höfði og hálsi af ýmsum stigum. A. T1 æxli (blá ör) í munnholi fyrir aftan endajaxl (trigonum retromolare). B. T1 krabbamein á hlið tungu (blá ör). C. T2 krabbamein á hlið tungu (blá ör). D. T2 æxli í fram munnbotni (blá ör). E. T3 hálskirtilskrabbamein (blá ör). F. T3 æxli í munnholi, efri kjálka (blá ör). G. T3 ofanraddglufukrabbamein (blá ör), barkalok (græn ör), leysibarkaslanga (rauður örvaoddur). H. T2 krabbamein í munnholi (blá ör).
Eins og að framan greinir eru verkir, kyngingartruflanir, hæsi, þyngdartap, öndunarerfiðleikar og langvarandi sár einkenni sem alltaf ætti að rannsaka nánar hjá fullorðnum, sérstaklega reykingamönnum. Mynd 1 sýnir myndir af æxlum af mismunandi stigum á höfuð- og hálssvæði.
Greining
Greining FÞKHH er jafnan nokkuð einföld, sérstaklega ef auðvelt er að ná sýni frá æxlinu. Sýnataka er algert grundvallaratriði í greiningu krabbameins. Sjúklingar með FÞKHH þurfa nánast alltaf að undirgangast stífa barkakýlis-, vélinda- og barkaspeglun í svæfingu sem í 4-14% tilfella leiðir í ljós annað krabbamein14, 15 en einnig til að kanna nánar útbreiðslu meinsins og eru þá stundum tekin stigunarsýni aðlægt, sérstaklega þegar skurðaðgerð er fyrirhuguð. Stöku sinnum greinast sjúklingar með áberandi hálseitlameinvörp án þess að upphafsæxli finnist (cancer of unknown primary). Tilkoma jáeindasneiðmyndarannsókna (PET/CT) hefur hjálpað til við greiningu á óþekktu frumæxli þar sem í um 40-50% tilfella sést upptaka við myndgreininguna16, 17 sem hjálpar til við hnitmiðaða sýnatöku í svæfingu. Af þeim æxlum þar sem upphafsæxlið finnst ekki við fyrstu leit, reynast um 80% vera í tungurót (base of tongue) eða hálskirtli þegar leitað er með nákvæmari aðferðum.17
Tölvusneiðmyndarrannsókn (TS) eða segulómskoðun (SÓ) með skuggaefni eru hjálplegar rannsóknarleiðir við mat á eitlum á hálssvæði og útbreiðslu frummeinsins. TS er þó ódýrari og fljótlegri og er mun meira notuð en SÓ sem fyrsta rannsókn (mynd 2).
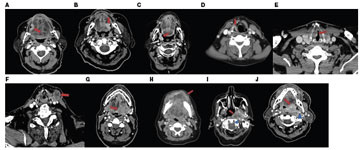
Mynd 2. Sneiðmyndir af flöguþekjukrabbameinum á höfði og hálsi af ýmsum stigum. A. T1 tunguæxli (rauð ör). B. T3 tunguæxli (rauð ör). C. T2 hálskirtilsæxli (rauð ör). D. T2 barkakýliskoksæxli (rauð ör). E. T2 hægra raddbandsæxli (rauð ör). F. Eitlameinvarp á hálsi (rauð ör). G. T4a tungurótaræxli (rauð ör). H. T4a fremra munnbotnsæxli sem er búið að éta sig í gegnum kjálkann (rauð ör). I. T4b nefkoksæxli (rauð ör) sem hefur vafið sig í kringum innri hálsslagæð (blár örvaroddur). J. T4b munnkoksæxli (rauð ör) sem hefur vafið sig í kringum innri hálsslagæð (blár örvaroddur).
Í um 10% tilfella nýgreindra FÞKHH finnast krabbamein í lungum (frummein og/eða mein-vörp) og líkurnar á því aukast eftir því sem stig frummeinsins er hærra.18 Staðsetning (munnkok, barkakýliskok, ofanraddglufa) er áhættuþáttur fyrir lungnameinvörp ásamt jákvæðum hálseitlum (N2/3).18 TS er sennilega besta rannsóknin til að útiloka lungnameinvörp. Finnist lungnameinvörp er meðferð nánast einungis líknandi, það er meðhöndla einkenni og fyrirbyggja fylgikvilla krabbameinsins. Líknandi meðferð getur þó falið í sér víðtæka skurðaðgerð með enduruppbyggingu, sérstaklega ef verkir eru miklir.
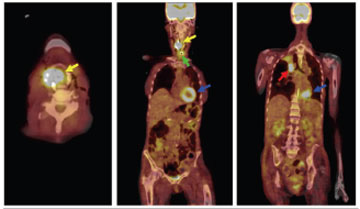
Mynd 3. 68 ára stórreykingakona sem var endurtekið lögð inn vegna andþyngsla og talin hafa versnandi langvinnan lungnateppusjúkdóm. Hún reyndist hafa stórt óþroskað flöguþekjuæxli í barkakýli. JS-rannsókn gerð til stigunar sýndi staðsetningu æxlisins vel (gular örvar), engin merki um eitlameinvörp en staðsetningu tracheostomiu (græn ör). Rannsóknin sýndi einnig æxli í hægra lunga (rauð ör) sem reyndist upprunnið frá berkju hægra efra lungnablaðs og talið var annað frumæxli (second primary tumor). Einnig má sjá vinstri slegil hjartans vel á þessari JS-mynd (blá ör).
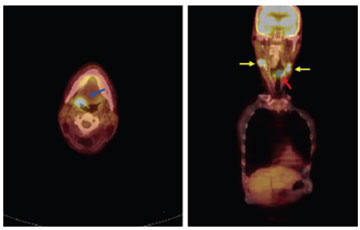
Mynd 4. Sextugur stórreykingamaður með vaxandi hnút vinstra megin á hálsi. JS sýnir upptöku í hálseitlum beggja vegna sem samrýmist meinvörpum (gular örvar). Einnig er að finna upptöku í hálskirtli hægra megin sem teygir sig yfir á tungurótina (blá ör). Auk þess var að finna upptöku í barkakýliskoki sem samrýmdist öðru frumæxli (rauð ör).
Á síðari árum hafa jáeindasneiðmyndarannsóknir (JS) verið notaðar í auknum mæli við stigun og eftirfylgni krabbameina á höfuð- og hálssvæði (myndir 3 og 4).19 Tæknin er sérlega hentug til þess að meta hvort sjúkdómurinn er staðbundinn eða útbreiddur. Í sumum tilfellum greinir JS fjarmeinvörp eða annað æxli og þannig getur rannsóknin hlíft sjúklingnum við því að gangast undir erfiða staðbundna meðferð sem ólíkleg væri til að lengja líf eða bæta lífsgæði.20 Einnig hafa JS verið notaðar til mats á meðferðarárangri, sérstaklega eftir lyfja- og geislameðferð. Ef JS er gerð þremur mánuðum eftir lok meðferðar og sýnir enga upptöku í frummeini eða hálseitlum ásamt eðlilegri líkamsskoðun er óhætt að fylgjast með sjúklingnum og framkvæma ekki eitlaúrnám.21 JS hefur einnig sýnt notagildi við ákvörðun og undirbúning geislameðferðar.22
Stigun
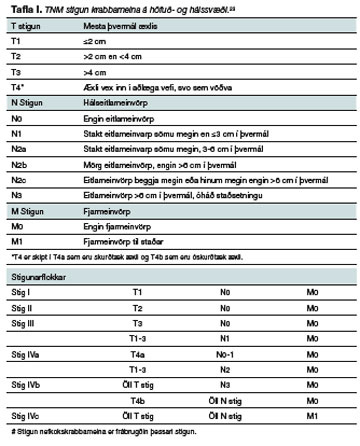
Stigun krabbameina á höfuð- og hálssvæði er flókin og endurspeglar flókna líffærafræði svæðisins. Núverandi stigunarkerfi er kennt við American Joint Committee on Cancer (AJCC) og styðst við svokallað TNM-kerfi (tafla I).23 Í þessu kerfi ákvarðast T-stigun af stærð og útbreiðslu upprunalega æxlisins og N-stigun af því hvort eitlameinvörp eru á hálsi. Mikilvægt er að greina hálseitlameinvörp því þau spá fyrir um horfur. Að jafnaði lækka lífslíkur um 50% ef eitlameinvörp greinast á hálsi.24 M-stig æxlisins ræðst af því hvort það hefur dreift sér til fjarlægra líffæra eða eitla utan höfuð- og hálssvæðis. Stigun FÞKHH er mismunandi eftir staðsetningu frumæxlis og til nánari glöggvunar á þessu vísast í vef bandarísku krabbameinsstofnunarinnar (National Cancer Institute), www.cancer.gov. Við stigun FÞKHH eru skörp skil á skiptingu svæða efri öndunar- og meltingarvegar (mynd 5). Til að auðvelda umræðu og fyrirbyggja rugling er hentugt að skipta eitlastöðvum á hálsi í fimm svæði eftir því hvar á hálsinum þær eru (mynd 6).
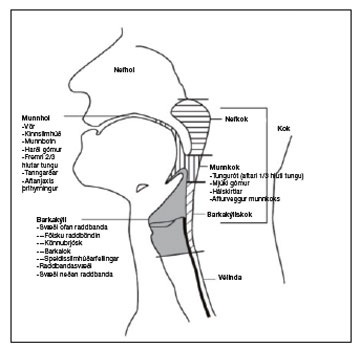
Mynd 5. Skipting höfuð- og hálssvæðis með tilliti til stigunar.
Munnhol er skilgreint frá vörum til fremri slímhúðarfellingar hálskirtils sem og að mótum mjúka og harða góms og inniheldur einnig fremri 2/3 hluta tungu. Frekari undirstaðir (subsites) innan munnhols hafa síðan sérstaka nálgun hvað meðferð varðar (tunga, munnbotn, harði gómur, kinnslímhúð, varir, aftanjaxls þríhyrningur (retromolar trigone) og tanngarðar (alveolar ridges). Munnkok inniheldur mjúka góminn, aftari 1/3 tungu, hálskirtil og afturvegg munnkoksins. Það nær niður að mótum barkaloks (epiglottis) og tungubotns. Barkakýliskok er skilgreint frá mótum barkaloks og tungubotns (vallecula) niður að neðri hluta hringbrjósksins (cartilago cricoidei) og inniheldur peruskotið (piriform fossa), afturhringbrjóskssvæðið og hliðar/afturveggi. Barkakýli er skipt í þrjú svæði: ofan raddbanda, raddbönd og neðan raddbanda (supraglottis, glottis, subglottis). Svæðið ofan raddbanda inniheldur barkalok, speldisslímhúðarfellingar (aryepiglottic folds), könnubrjósk og fölsku raddböndin. Raddbönd eru skilgreind frá neðri hluta fölsku raddbandanna og ná 1 cm niður fyrir þau. Svæðið neðan raddbanda nær frá mörkum raddbanda að neðri hluta hringbrjósks. Nefkok nær frá koknösum (choanae posteriores) að afturvegg og neðri mörk eru efra yfirborð mjúka gómsins.
Birt með leyfi CMPMedica. Úr: Cancer Management: A Multidisciplinary Approach, 11th edition 2008. Pazdur R, Wagman L, Camphausen K, et al (Ritstj.), Kafli 4. Öll réttindi áskilin.
Almennt um meðferð FÞKHH
Meðferð FÞKHH krefst náinnar samvinnu sérfræðinga, háls-, nef og eyrnaskurðlækna og krabbameinslækna. Einnig skipta lýtalæknar og talmeinafræðingar miklu í meðferð þessara sjúklinga. Meðferðarúrræði eru rædd á sameiginlegum fundum með röntgenlæknum og meinafræðingum þar sem farið er yfir rannsóknarniðurstöður og meðferðaráætlun ákveðin í kjöl-farið. Fundir af þessu tagi (tumor board) hafa áhrif á meðferð sjúklinga.25 Hér er stuttlega fjallað um mismunandi meðferðarmöguleika, svo sem skurðaðgerðir, geislameðferð og lyfjameðferð og síðan um ákveðin krabbamein innan efri öndunar- og loftvegar þar sem meðferð er oft sérlega flókin. Með vissu millibili gefa bæði evrópsk og bandarísk samtök út leiðbeiningar um meðferð FÞKHH og má nálgast á netinu og í tímaritum.26-29
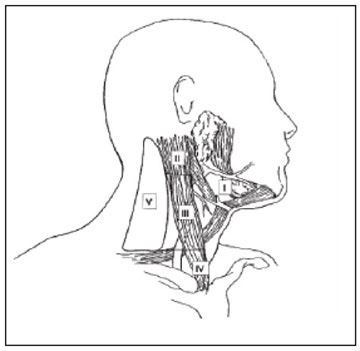
Mynd 6. Eitlastöðvar hálsins.
Birt með leyfi CMPMedica. Úr: Cancer Management: A Multidisciplinary Approach, 11th edition 2008. Pazdur R, Wagman L, Camphausen K, et al (Ritstj.), Kafli 4. Öll réttindi áskilin.
Skurðaðgerð
Skurðaðgerðir og geislameðferð hafa verið meginmeðferðarleiðir við FÞKHH. Pendúllinn hefur hins vegar sveiflast í átt að frummeðferð með geislum með eða án lyfjameðferðar, sérstaklega í meðferð munnkoks-, nefkoks-, barkakýlis- og barkakýliskokskrabbameina. Misjafnt er milli landa og sjúkrahúsa hvort menn beita meira skurðaðgerð eða geislameðferð og fer eftir ráðandi sérþekkingu á hverjum stað. Skurðaðgerðir eru enn mikið brúkaðar við meðferð á krabbameini í munnholi þar sem fylgikvillar geislameðferðar eru talsverðir miðað við skurðaðgerð, sem og við minni krabbameinum (T1 og T2) þar sem leysiaðgerð er oft framkvæmd ein og sér. Ef meinið er vaxið inn í brjósk eða bein er skurðaðgerð líklegri til lækningar en geislameðferð. Skurðaðgerð er einnig notuð sem björgunaraðgerð (salvage) fyrir mein sem koma aftur eða standast frumgeislameðferð með eða án lyfjameðferðar. Meginmarkmið skurðaðgerðar er að sneiða meinið burt með nægjanlegum skurðbrúnum (1-2 cm) í þrívídd sem og stigun eitla (N0) eða meðferð eitla (N+) með eitlaúrnámi á hálsi (neck dissection).
Meðhöndlun eitla á hálsi er viðfangsefni í stöðugri endurskoðun, sérstaklega með tilliti til hversu víðtækt eitlaúrnám er nauðsynlegt. Róttækt hálseitlaúrnám* var staðalaðgerð lengi vel en nú er áherslan meiri á sértækt eitlaúrnám (selective neck dissection) þar sem eitlar sem eru líklegastir til að innihalda krabbamein í N0¥ tilfellum eru fjarlægðir.30 Ef hálsinn er N+ er núorðið beitt MRM (modified radical neck dissection)# og einungis þeir líffærahlutar sem krabbameinið er vaxið inn í, ef nokkrir, eru teknir.
Nýjar leiðir til enduruppbyggingar með fríum vefflutningi hafa einnig breytt skurðaðgerðum þar sem hægt er að gera mjög víðtækar aðgerðir með enduruppbyggingu sem leiðir til tiltölulega góðrar starfsgetu með tilliti til raddar og kyngingar.
Eftir að leysigeislatæknin kom fram í lækningaskyni hefur CO2 leysirinn verið mjög nytsamt tæki til meðhöndlunar á krabbameinum, sérstaklega í barkakýli, sem og annarra meina á höfuð- og hálssvæði. Leysiskurðaðgerð er sérstaklega hentug fyrir minni æxli en sumir hafa einnig náð góðum árangri með lengra gengin æxli.31, 32 Leysiskurðaðgerðir hafa jafnframt verið notaðar við endurkomu æxlis eftir geislameðferð með góðum árangri.33 Nýverið kom fram tækni sem gerir það að verkum að hægt er að leiða geislann um þráð (Omniguide®) sem á eftir að auðvelda notkun á þessu þrönga svæði.34
Geislameðferð með eða án lyfjameðferðar
Meðferð á staðbundnum krabbameinum:
Í mörgum tilfellum er geislameðferð ein og sér jafnlíkleg til árangurs og skurðaðgerð en val á meðferð fer eftir staðsetningu æxlis, hugsanlegum fylgikvillum og óskum sjúklings. Lyfjameðferð virðist bæta litlu við geisla í meðferð staðbundinna meina á lágu stigi. Geislameðferð hefur þann kost að hægt er að lækna staðbundin mein án þess að fjarlægja líffærið og slík meðferð veldur sjaldnar sjáanlegum lýtum eða truflun á starfsemi líffærisins en skurðaðgerð.35 Geislameðferð er gjarnan gefin fimm daga vikunnar í sjö vikur þar sem heildargeislaskammturinn er nálægt 70 gray (Gy). Ýmsar nýjungar í geislameðferð, svo sem fleiri en ein meðferð á dag (hyperfractionation) virðast hafa bætt lífslíkur sjúklinga lítillega en slíkum meðferðum er þó óvíða beitt þar sem bráðar aukaverkanir eru meiri og þær krefjast gjarnan sértæks búnaðar og fleira starfsfólks. Geislameðferð eftir skurðaðgerð á hálsi í N+ tilfellum dregur úr líkum á staðbundinni endurkomu meinsins og bætir lifun.36
Meðferð á langt gengnum krabbameinum án meinvarpa:
Ef mein eru staðbundin en þó langt gengin er yfirleitt þörf á geislameðferð ásamt krabbameinslyfjameðferð. Rannsóknir hafa sýnt að samhliða meðferð með geislum og krabbameinslyfjum (geislalyfjameðferð, concurrent chemoradiation therapy) er líklegri til árangurs en geislameðferð ein sér eða lyfjameðferð gefin fyrir eða eftir geislameðferð (sequential therapy).37 Horfur sjúklinga sem gengist hafa undir geislameðferð hafa batnað á síðustu áratugum og vera má að skýringin sé aukin notkun samhliða lyfjameðferðar. Ávinningurinn af samhliða geislalyfjameðferð er um 8% betri fimm ára lifun umfram það sem áunnið er með geislameðferð einni saman.37 Samhliða meðferð virðist þó ekki draga mikið úr hættunni á fjarmeinvörpum og slík meðferð hefur í för með sér umtalsvert alvarlegri aukaverkanir en geislameðferð ein sér. Ef ekki er talið að sjúklingur þoli hefðbundna geislalyfjameðferð má annaðhvort nota geislameðferð eða geislameðferð ásamt cetuximab sem er mótefni gegn vaxtarviðtökum á yfirborði æxlisfrumnanna (epidermal growth factor). Sé cetuximab bætt við geislameðferð má bæta árangur meðferðarinnar án þess að auka fylgikvillana svo marktækt sé.38 Þrátt fyrir að geislalyfjameðferð með cetuximab lofi góðu er cisplatín enn kjörlyf ásamt geislameðferð í þeim sjúklingum er þola slíka meðferð. En meðferðin er flestum sjúklingum afar strembin, jafnvel þeim sem annars eru við góða heilsu. Ef æxli er skurðtækt virðist samhliða geislalyfjameðferð eftir skurðaðgerð (adjuvant meðferð) gagnast í völdum tilfellum og dregur slík meðferð úr líkum á endurkomu sjúkdómsins og bætir hugsanlega lífslíkur.39 Ávinningurinn af slíkri eftirmeðferð virðist þó fyrst og fremst bundinn við þá sjúklinga sem reynast hafa jákvæðar skurðbrúnir að aðgerð lokinni eða eitlameinvörp sem ná út fyrir eitilinn sjálfan og inn í aðlæga vefi.40 Barkaskurður (tracheotomy) til að tryggja loftveg og öndun ásamt magaraufun (gastrostomy) til að viðhalda næringarástandi sjúklingsins getur verið nauðsynleg á meðan meðferð stendur þar sem kynging er þá oft verulega skert og getur í sumum tilvikum skaðast varanlega.
Lengi hefur verið vitað að kröftug krabbameinslyfjameðferð í upphafi meðferðar áður en lagt er út í skurðaðgerð eða geislameðferð, getur minnkað stærð æxlisins og hugsanlega bætt horfur.41 Þessi meðferð telst þó ekki enn vera kjörmeðferð en á vel við í völdum tilfellum ef mein eru langt gengin en staðbundin. Bráðir fylgikvillar geislameðferðar og sérstaklega geislalyfjameðferðar eru umtalsverðir. Nær allir sjúklingar verða fyrir verulegum slímhúðarskaða (mucositis) sem yfirleitt veldur verulegum verkjum og skertri inntöku næringar. Undantekningarlítið þurfa sjúklingar sterk verkjalyf meðan á meðferð stendur og fyrstu vikurnar eftir að meðferð lýkur.
Lyfjameðferð
Lyfjameðferð hefur hlutverk í meðferð útbreidds sjúkdóms og má búast við svörun í 20-40% sjúklinga en svörunin varir yfirleitt ekki lengur en 2-4 mánuði.42 Þau lyf sem einkum eru notuð eru cisplatín, karbóplatín, 5-flúoroúracíl (5-FU), capecitabín, metótrexat, paclítaxel og dócetaxel. Þessi lyf má ýmist gefa ein eða í samsetningum. Þótt samsetningar lyfja, svo sem cisplatíns og 5-FU, séu áhrifaríkar er óljóst hvort þær bæta marktækt lifun sjúklinga.43 Allt að 13% sjúklinga með langt gengið krabbamein svara cetuximab og í allt að 56% sjúklinga tekst að halda aftur af sjúkdómnum um nokkurra mánaða skeið.44 Einn kostur við cetuximab er að lyfið þolist mun betur en hefðbundin frumudrepandi krabbameinslyf og er því sérlega hentugt í öldruðum sjúklingum og sjúklingum sem hafa önnur vandamál sem hamla notkun frumudrepandi lyfja. Tvö önnur lyf sem hamla starfsemi EGFR, erlotinib og gefitinib, hafa einnig sýnt nokkra virkni í meðferð útbreidds sjúkdóms. Nýlega var birt rannsókn sem styður notkun cetuximab sé það gefið ásamt og samhliða frumudrepandi lyfjameðferð með platínulyfjum og 5-FU og virtist cetuximab bæta lifun sjúklinga miðað við frumudrepandi lyfjameðferð eingöngu.45 Lyfið er þó enn sem komið er afar dýrt en mögulega má finna ákveðna undirhópa sjúklinga þar sem meðferð þessi er líkleg til árangurs.
Meðferð ákveðinna gerða flöguþekjukrabbameina á höfuð- og hálssvæði
Krabbamein í munnholi (oral cavity):
Í flestum tilvikum er skurðaðgerð kjörmeðferð við krabbameini í munnholi. Geislameðferð hefur líklega svipuð áhrif með tilliti til lækningar á krabbameininu en hefur hærri tíðni fylgikvilla, sérstaklega geislunarbeindrep (osteoradionecrosis).46 Horfur þessara sjúklinga fara mikið eftir stigi sjúkdómsins (tafla I). Enduruppbygging eftir krabbameinsaðgerðir á þessu svæði hefur gert stærri aðgerðir mögulegar með góðri endurhæfingu raddar og kyngingar.
Krabbamein í munnkoki (oropharynx):
Meðferð þessara æxla á öllum stigum hefur færst að verulegu leyti yfir í geislameðferð með eða án lyfjameðferðar. Skurðaðgerðir eru geymdar fyrir endurkomu æxla þó enn séu læknar sem beita skurðaðgerðum við þessum æxlum með jafngóðum árangri og geislun. Æxli á lágu stigi (T1-T2, N0-N1) hafa tiltölulega góðar horfur þar sem 5 ára lifun er 70-80%.47 Ef æxlin eru langt gengin en samt staðbundin (T3-T4, N2-N3) er geislalyfjameðferð talin kjörmeðferð. Fimm ára lifun fyrir stig III er 50% og stig IV er 30%.23 Í völdum tilfellum má beita skurðaðgerð að geislalyfjameðferð lokinni hafi svörun við meðferð verið ófullkomin og æxlið enn talið skurðtækt.42
Krabbamein í barkakýliskoki (hypopharynx):
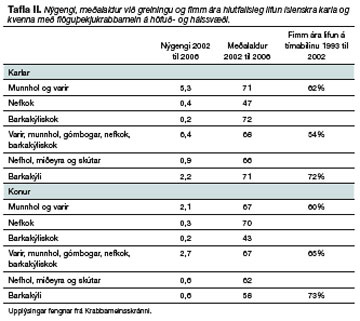
Þessi æxli eru yfirleitt langt gengin við greiningu með ífarandi æxlisvexti og hálseitlameinvörpum.42 Ástæðan er að einkenni smárra æxla á þessum stað eru lítil sem engin. Horfur eru slæmar þar sem 5 ára lifun allra æxla er um 30%.48 Tafla II sýnir fimm ára lifun þessara æxla á Íslandi. Hefðbundin meðferð er annaðhvort skurðaðgerð með geislameðferð eða geislalyfjameðferð að aðgerð lokinni eða geislalyfjameðferð eingöngu.49
Krabbamein í barkakýli (larynx):
Meðferð æxla í barkakýli hefur breyst talsvert á síðastliðnum áratugum en nú gangast flestir sjúklinganna undir geislameðferð. Markmið meðferðar á þessum æxlum er að viðhalda starfandi barkakýli og raddböndum og þar með eðlilegri rödd ásamt því að veita læknandi meðferð.50 Starfhæfni barkakýlisins með tilliti til raddar, öndunar og kyngingar verður að meta til að geta ráðlagt viðeigandi meðferð. Geislun er ólíkleg til að bæta kyngingu sé hún á annað borð orðin slæm og er frekar líkleg til að gera hana verri, sérstaklega ef lyfjameðferð er beitt líka. Ef sjúklingur með langt gengið krabbamein kýs geislameðferð þarf að huga að loftvegi áður en meðferð hefst og þurfa sumir sjúklinganna barkaskurð. Æxli á lágu stigi má meðhöndla með geislameðferð eingöngu eða takmarkaðri skurðaðgerð. Skurðaðgerðir eru mismunandi eftir því hvar í barkakýlinu meinið er og hversu útbreitt það er, brottnám barkakýlis er oft beitt en leysigeislaskurðaðgerð í barkakýlisspeglun er æ algengari. Meðhöndla þarf eitla í ofanraddglufuæxlum í öllum tilvikum með eitlaúrnámi eða geislun og fer það að mestu eftir frummeðferð hvor meðferðin er notuð. Lengra gengin æxli (T stig IIB til IV) geta verið meðhöndluð með skurðaðgerð eða geislalyfjameðferð. Oftar er þó meðhöndlað með geislalyfjameðferð.50 Sýnt hefur verið fram á að geislalyfjameðferð er jafnlíkleg til lækningar og skurðaðgerð en þess utan er slík meðferð líklegri til að viðhalda starfhæfu barkakýli.51, 52 Í sumum tilvikum svara sjúklingar ekki geislalyfjameðferð en þá er jafnan beitt barkakýlisbrottnámi. Slík aðgerð er einnig nauðsynleg ef krabbamein í barkakýli kemur aftur eftir að sjúklingur hefur gengist undir geislameðferð. Þær hafa þó gjarnan hærri fylgikvilla í för með sér, svo sem kokhúðarsamgang (pharyngocutaneous fistula), þá sérstaklega ef lyfjameðferð hefur verið beitt aukalega.53
Krabbamein í nefkoki (nasopharynx):
Þessi krabbamein eru um margt ólík hinum algengari FÞKHH en gjarnan er sjúkdómurinn langt gengin með útbreiddum eitlameinvörpum við greiningu.54 Nefkokskrabbamein eru frekar sjaldgæf á Vesturlöndum en mun algengari í Austurlöndum fjær, sérstaklega í Kína og tengist tilurð þeirra þar sterklega sýkingum af völdum Epstein-Barr veirunnar. Hornsteinn meðferðar nefkokskrabbameina er geislameðferð en á síðasta áratug hefur verið sýnt fram á að geislalyfjameðferð bætir horfur umtalsvert.55
Hálseitlameinvörp af óþekktum uppruna:
Í 2-5% af öllum tilfellum af FÞKHH er engan upphafsstað að finna þrátt fyrir ítarlega skoðun.56 Jáeindasneiðmyndarannsónir geta verið gagnlegar í þessum hópi sjúklinga.57 Uppvinnslan miðar að því að finna frumæxlið með ítarlegri skoðun í svæfingu með barkakýlisspeglun og sýnatöku frá tungurót og hálskirtlatöku en í um 80% tilfella er frummeinið þar ef það finnst.17 Hefðbundin meðferð þessara sjúklinga var fyrst og fremst skurðaðgerð með eitlabrottnámi en nú er geislameðferð eða geislalyfjameðferð einnig beitt og er þá geislað á nefkok, munnkok og eitla í afturkoki (retropharynx)58 og á eitlastöðvar á hálsi.
Enduruppbygging eftir krabbameinsaðgerðir
Vefjaenduruppbygging eftir skurðaðgerðir á höfuð- og hálssvæði hefur þróast mikið undanfarin ár og áratugi.59-63
Starfhæfni og áferð þess vefjar sem settur er í staðinn þarf að parast við þann sem tekinn var í burtu, sem dæmi ef bein er tekið er settur beinflipi í staðinn. Ávallt skyldi hafa í huga að það eru til margar leiðir að sama marki en góð regla er að velja þá leið sem er einföldust og öruggust fyrir sjúklinginn.
Eftirfylgd að meðferð lokinni
Sjúklingar sem gengist hafa undir meðferð við FÞKHH þurfa nána eftirfylgd. Markmið hennar er annars vegar að fylgjast með mögulegri endurkomu sjúkdómsins og annarra æxla í efri loftvegi og hins vegar að líta eftir fylgikvillum meðferðarinnar. Mælt er með sameiginlegu eftirliti háls-, nef- og eyrnaskurðlæknis og krabbameinslæknis á 2-4 mánaða fresti fyrstu tvö árin og síðan 4-6 mánaða fresti næstu þrjú ár. Þegar liðin eru fimm ár frá greiningu er sennilega nægilegt að fylgjast með þessum sjúklingum á árs fresti. Ekki er ljóst hvert er ákjósanlegt hlutverk myndgreiningarrannsókna að meðferð lokinni en rannsóknir benda til að JS-rannsókn þremur mánuðum eftir lok meðferðar og síðan ári eftir meðferð geti hjálpað til við að útiloka að æxlið hafi tekið sig upp á ný (neikvætt forspárgildi nálægt 100%).21 Á þeim stöðum þar sem ekki er möguleiki á að gera JS-rannsókn ætti að minnsta kosti framkvæma TS-rannsókn 4-6 mánuðum eftir að meðferð lýkur og síðan þegar einkenni og skoðun gefa tilefni til. Geislameðferð á höfuð- og hálssvæði getur valdið margvíslegum síðkomnum fylgikvillum og skerðingu lífsgæða.64 Þar má nefna skerta munnvatnsframleiðslu sem getur leitt til verulegra tannskemmda, vanstarfsemi á skjaldkirtli ef geislameðferð var beitt á háls-inn, drep í kjálkabeini og bandvefsmyndun á hálssvæði. Margir þessara sjúklinga líða fyrir næringarskort að meðferð lokinni og oft eru verulegar kyngingartruflanir sem geta leitt til ásvelginga. Í sumum tilfellum er þörf á langtímanotkun magaraufunar til næringar. Mikil hjálp fylgir aðstoð næringarfræðinga og talmeinafræðinga meðan á meðferð stendur og eftir að meðferð lýkur.
Niðurlag
Flöguþekjukrabbamein á höfuð- og hálssvæði (FÞKHH) eru krabbamein sem sterklega tengjast reykingum og neyslu áfengis. Einnig virðist sem nokkur hluti þessara krabbameina tengist sýkingu af völdum human papillomavirus (HPV), sérstaklega í þeim sem aldrei hafa reykt. Greining þessara meina er venjulega fengin með ítarlegri skoðun sérfræðings í háls-, nef- og eyrnasjúkdómum. Myndgreiningarrannsóknir skipa meginhlutverk í greiningu og stigun sjúkdóms en á síðari árum hafa jáeindasneiðmyndir rutt sér til rúms í auknum mæli sem ein meginstoð greiningar og uppvinnslu. Meðferð FÞKHH er flókin og mikilvægt er að meðferðarsérfræðingar vinni náið saman að meðferð hvers og eins sjúklings. Hefðbundið teymi sérfræðinga samanstendur af háls-, nef- og eyrnalæknum með reynslu í krabbameinsaðgerðum, krabbameinslæknum og myndgreiningarsérfræðingum. Einnig skipa talmeinafræðingar verulega stóran sess í meðferð á FÞKHH. Skurðaðgerð er enn kjörmeðferð við mörgum krabbameinum af lágu stigi en samtvinnuð meðferð með geislum og krabbameinslyfjum er notuð gegn flestum lengra gengnum meinum. Í mörgum tilfellum má komast af án skurðaðgerðar en slíkt er einkar heppilegt við æxli á raddböndum eða í barkakýli þar sem oft reynist mögulegt að lækna sjúklinginn án þess að þurfi að fjarlægja barkakýlið. Að meðferð lokinni þurfa þessir sjúklingar á náinni eftirfylgd að halda til stuðnings vegna bráðra og síðkominna aukaverkana meðferðarinnar og mögulegri endurkomu meinsins.
Þakkir
Íslensku krabbameinsskránni eru færðar þakkir fyrir að láta í té íslenskar tölur um nýgengi og lifun sjúklinga með flöguþekjukrabbamein á höfuð- og hálssvæði.
Heimildir
1. Barnes L, Eveson JW, Reichart P, Sidransky D. World Health Organization Classification of Tumours: Pathology and Genetics of Head and Neck Tumours. Lyon: IARC Press; 2005.
2. Jemal A, Siegel R, Ward E, et al. Cancer statistics, 2008. CA Cancer J Clin 2008; 58: 71-96.
3. Ferlay J, Autier P, Boniol M, Heanue M, Colombet M, Boyle P. Estimates of the cancer incidence and mortality in Europe in 2006. Ann Oncol 2007; 18: 581-92.
4. Kamangar F, Dores GM, Anderson WF. Patterns of cancer incidence, mortality, and prevalence across five continents: defining priorities to reduce cancer disparities in different geographic regions of the world. J Clin Oncol 2006; 24: 2137-50.
5. Goldenberg D, Lee J, Koch WM, et al. Habitual risk factors for head and neck cancer. Otolaryngol Head Neck Surg 2004; 131: 986-93.
6. Pelucchi C, Gallus S, Garavello W, Bosetti C, La Vecchia C. Alcohol and tobacco use, and cancer risk for upper aerodigestive tract and liver. Eur J Cancer Prev 2008; 17: 340-44.
7. Boffetta P, Hecht S, Gray N, Gupta P, Straif K. Smokeless tobacco and cancer. Lancet Oncol 2008; 9: 667-75.
8. Brown LM, McCarron P, Freedman DM. New Malignancies Following Cancer of the Buccal Cavity and Pharynx. In: Curtis RE, Freedman DM, Ron E, et al., eds. New Malignancies Among Cancer Survivors: SEER Cancer Registries, 1973-2000. Bethesda, MD: National Cancer Institute, NIH Publ. No. 05-5302.; 2006: 15-57.
9. Caporaso NE, Dodd KW, Tucker MA. New Malignancies Following Cancer of the Respiratory Tract. In: Curtis RE, Freedman DM, Ron E, et al., eds. New Malignancies Among Cancer Survivors: SEER Cancer Registries, 1973-2000. Bethesda, MD: National Cancer Institute, NIH Publ. No. 05-5302.; 2006: 145-79.
10. D'Souza G, Kreimer AR, Viscidi R, et al. Case-control study of human papillomavirus and oropharyngeal cancer. N Engl J Med 2007; 356: 1944-56.
11. Kreimer AR, Clifford GM, Boyle P, Franceschi S. Human papillomavirus types in head and neck squamous cell carcinomas worldwide: a systematic review. Cancer Epidemiol Biomarkers Prev 2005; 14: 467-75.
12. Chaturvedi AK, Engels EA, Anderson WF, Gillison ML. Incidence trends for human papillomavirus-related and -unrelated oral squamous cell carcinomas in the United States. J Clin Oncol 2008; 26: 612-9.
13. Fakhry C, Westra WH, Li S, et al. Improved survival of patients with human papillomavirus-positive head and neck squamous cell carcinoma in a prospective clinical trial. J Natl Cancer Inst 2008; 100: 261-9.
14. Hujala K, Sipila J, Grenman R. Panendoscopy and synchronous second primary tumors in head and neck cancer patients. Eur Arch Otorhinolaryngol 2005; 262: 17-20.
15. Haughey BH, Gates GA, Arfken CL, Harvey J. Meta-analysis of second malignant tumors in head and neck cancer: the case for an endoscopic screening protocol. Ann Otol Rhinol Laryngol 1992; 101: 105-12.
16. Roh JL, Kim JS, Lee JH, et al. Utility of combined (18)F-fluorodeoxyglucose-positron emission tomography and computed tomography in patients with cervical metastases from unknown primary tumors. Oral Oncol 2008.
17. Mendenhall WM, Mancuso AA, Amdur RJ, Stringer SP, Villaret DB, Cassisi NJ. Squamous cell carcinoma metastatic to the neck from an unknown head and neck primary site. Am J Otolaryngol 2001; 22: 261-7.
18. Loh KS, Brown DH, Baker JT, Gilbert RW, Gullane PJ, Irish JC. A rational approach to pulmonary screening in newly diagnosed head and neck cancer. Head Neck 2005; 27: 990-4.
19. Garcia C, Flamen P. Role of positron emission tomography in the management of head and neck cancer in the molecular therapy era. Curr Opin Oncol 2008; 20: 275-9.
20. Scott AM, Gunawardana DH, Bartholomeusz D, Ramshaw JE, Lin P. PET changes management and improves prognostic stratification in patients with head and neck cancer: results of a multicenter prospective study. J Nucl Med 2008; 49: 1593-600.
21. Yao M, Smith RB, Graham MM, et al. The role of FDG PET in management of neck metastasis from head-and-neck cancer after definitive radiation treatment. Int J Radiat Oncol Biol Phys 2005; 63: 991-9.
22. Wong RJ. Current status of FDG-PET for head and neck cancer. J Surg Oncol 2008; 97: 649-52.
23. Greene FL, Page DL, Fleming ID, et al. AJCC Cancer Staging Manual. Springer, New York 2002.
24. Grandi C, Alloisio M, Moglia D, et al. Prognostic significance of lymphatic spread in head and neck carcinomas: therapeutic implications. Head Neck Surg 1985; 8: 67-73.
25. Westin T, Stalfors J. Tumour boards/multidisciplinary head and neck cancer meetings: are they of value to patients, treating staff or a political additional drain on healthcare resources? Curr Opin Otolaryngol Head Neck Surg 2008; 16: 103-7.
26. Pivot X, Felip E. Squamous cell carcinoma of the head and neck: ESMO clinical Recommendations for diagnosis, treatment and follow-up. Ann Oncol 2008;19 Suppl 2:ii79-80.
27. NCCN Practice Guidelines in Oncology: Head and Neck Cancers (www.nccn.org/professionals/physician_gls/PDF/head-and-neck.pdf).
28. Diagnosis and management of head and neck cancer. A national clinical guideline. Scottish Intercollegiate Guidelines Network. Edinburgh (www.sign.ac.uk/pdf/sign90.pdf); 2006.
29. ESMO Clinical Recommendations. Squamous cell carcinoma of the head and neck. http://annonc.oxfordjournals.org/cgi/content/full/20/suppl_4/iv121.2009.
30. Ferlito A, Rinaldo A, Silver CE, et al. Neck dissection: then and now. Auris Nasus Larynx 2006; 33: 365-74.
31. Martin A, Jackel MC, Christiansen H, Mahmoodzada M, Kron M, Steiner W. Organ preserving transoral laser microsurgery for cancer of the hypopharynx. Laryngoscope 2008; 118: 398-402.
32. Hinni ML, Salassa JR, Grant DG, et al. Transoral laser microsurgery for advanced laryngeal cancer. Arch Otolaryngol Head Neck Surg 2007; 133: 1198-204.
33. Steiner W, Vogt P, Ambrosch P, Kron M. Transoral carbon dioxide laser microsurgery for recurrent glottic carcinoma after radiotherapy. Head Neck 2004; 26: 477-84.
34. Jacobson AS, Woo P, Shapshay SM. Emerging technology: flexible CO2 laser WaveGuide. Otolaryngol Head Neck Surg 2006; 135: 469-70.
35. Argiris A, Karamouzis MV, Raben D, Ferris RL. Head and neck cancer. Lancet 2008; 371: 1695-709.
36. Kao J, Lavaf A, Teng MS, Huang D, Genden EM. Adjuvant radiotherapy and survival for patients with node-positive head and neck cancer: an analysis by primary site and nodal stage. Int J Radiat Oncol Biol Phys 2008; 71: 362-70.
37. Pignon JP, le Maitre A, Bourhis J. Meta-Analyses of Chemotherapy in Head and Neck Cancer (MACH-NC): an update. Int J Radiat Oncol Biol Phys 2007; 69:S112-114.
38. Bonner JA, Harari PM, Giralt J, et al. Radiotherapy plus cetuximab for squamous-cell carcinoma of the head and neck. N Engl J Med 2006; 354: 567-78.
39. Winquist E, Oliver T, Gilbert R. Postoperative chemo-radiotherapy for advanced squamous cell carcinoma of the head and neck: a systematic review with meta-analysis. Head Neck 2007; 29: 38-46.
40. Bernier J, Cooper JS, Pajak TF, et al. Defining risk levels in locally advanced head and neck cancers: a comparative analysis of concurrent postoperative radiation plus chemotherapy trials of the EORTC (#22931) and RTOG (# 9501). Head Neck 2005; 27: 843-50.
41. Cruz JJ, Ocana A, Navarro M, Barco ED, Fonseca E. New options in the treatment of locally advanced head and neck cancer: role for induction chemotherapy. Cancer Treat Rev 2008; 34: 268-74.
42. Marur S, Forastiere AA. Head and neck cancer: changing epidemiology, diagnosis, and treatment. Mayo Clin Proc 2008; 83: 489-501.
43. Choong N, Vokes E. Expanding role of the medical oncologist in the management of head and neck cancer. CA Cancer J Clin 2008; 58: 32-53.
44. Vermorken JB, Herbst RS, Leon X, Amellal N, Baselga J. Overview of the efficacy of cetuximab in recurrent and/or metastatic squamous cell carcinoma of the head and neck in patients who previously failed platinum-based therapies. Cancer 2008; 112: 2710-9.
45. Vermorken JB, Mesia R, Rivera F, et al. Platinum-based chemotherapy plus cetuximab in head and neck cancer. N Engl J Med 2008; 359: 1116-27.
46. Jereczek-Fossa BA, Orecchia R. Radiotherapy-induced mandibular bone complications. Cancer Treat Rev 2002; 28: 65-74.
47. Makitie AA, Pukkila M, Laranne J, et al. Oropharyngeal carcinoma and its treatment in Finland between 1995-1999: a nationwide study. Eur Arch Otorhinolaryngol 2006; 263: 139-43.
48. Hoffman HT, Karnell LH, Shah JP, et al. Hypopharyngeal cancer patient care evaluation. Laryngoscope 1997; 107: 1005-17.
49. Lefebvre JL, Chevalier D, Luboinski B, Kirkpatrick A, Collette L, Sahmoud T. Larynx preservation in pyriform sinus cancer: preliminary results of a European Organization for Research and Treatment of Cancer phase III trial. EORTC Head and Neck Cancer Cooperative Group. J Natl Cancer Inst 1996; 88: 890-9.
50. Pfister DG, Laurie SA, Weinstein GS, et al. American Society of Clinical Oncology clinical practice guideline for the use of larynx-preservation strategies in the treatment of laryngeal cancer. J Clin Oncol 2006; 24: 3693-704.
51. Induction chemotherapy plus radiation compared with surgery plus radiation in patients with advanced laryngeal cancer. The Department of Veterans Affairs Laryngeal Cancer Study Group. N Engl J Med 1991; 324: 1685-90.
52. Forastiere AA, Goepfert H, Maor M, et al. Concurrent chemotherapy and radiotherapy for organ preservation in advanced laryngeal cancer. N Engl J Med 2003; 349: 2091-8.
53. Ganly I, Patel S, Matsuo J, et al. Postoperative complications of salvage total laryngectomy. Cancer 2005; 103: 2073-81.
54. Wei WI, Sham JS. Nasopharyngeal carcinoma. Lancet 2005; 365: 2041-54.
55. Baujat B, Audry H, Bourhis J, et al. Chemotherapy in locally advanced nasopharyngeal carcinoma: an individual patient data meta-analysis of eight randomized trials and 1753 patients. Int J Radiat Oncol Biol Phys 2006; 64: 47-56.
56. Mahoney EJ, Spiegel JH. Evaluation and management of malignant cervical lymphadenopathy with an unknown primary tumor. Otolaryngol Clin North Am 2005; 38: 87-97, viii-ix.
57. Rusthoven KE, Koshy M, Paulino AC. The role of fluorodeoxyglucose positron emission tomography in cervical lymph node metastases from an unknown primary tumor. Cancer 2004; 101: 2641-9.
58. Beldi D, Jereczek-Fossa BA, D'Onofrio A, et al. Role of radiotherapy in the treatment of cervical lymph node metastases from an unknown primary site: retrospective analysis of 113 patients. Int J Radiat Oncol Biol Phys 2007; 69: 1051-8.
59. Dalgorf D, Higgins K. Reconstruction of the midface and maxilla. Curr Opin Otolaryngol Head Neck Surg 2008; 16: 303-11.
60. Okay DJ, Genden E, Buchbinder D, Urken M. Prosthodontic guidelines for surgical reconstruction of the maxilla: a classification system of defects. J Prosthet Dent 2001; 86: 352-63.
61. Bokhari WA, Wang SJ. Tongue reconstruction: recent advances. Curr Opin Otolaryngol Head Neck Surg 2007; 15: 202-7.
62. Hurvitz KA, Kobayashi M, Evans GR. Current options in head and neck reconstruction. Plast Reconstr Surg 2006; 118:122e-133e.
63. Gilbert RW, Neligan PC. Microsurgical laryngotracheal reconstruction. Clin Plast Surg 2005; 32: 293-301, v.
64. Martino R, Ringash J. Evaluation of Quality of Life and Organ Function in Head and Neck Squamous Cell Carcinoma. Hematol Oncol Clin North Am 2008; 22: 1239-56.
