12. tbl. 94. árg. 2008
Fræðigrein
Umlykjandi lífhimnuhersli - tvö tilfelli og yfirlit yfir sjúkdóminn
Ágrip
Umlykjandi lífhimnuhersli (encapsulating peritoneal sclerosis) er alvarlegur fylgikvilli kviðskilunar. Nýgengi þess fer vaxandi á heimsvísu. Talið er að langtímanotkun ólífvænna skilvökva sé helsti orsakavaldurinn en sjúkdómurinn greinist oft eftir bráða lífhimnubólgu. Horfur hafa batnað með notkun lyfja og þróun skurðaðgerðar.
Hér á landi hefur umlykjandi lífhimnuhersli greinst hjá tveimur af 124 kviðskilunarsjúklingum. Samanlagt nýgengi er þannig 1,6% sem er svipað og annars staðar. Sjúkrasaga sjúklinganna tveggja var lík; þeir veiktust báðir í kjölfar bráðrar lífhimnubólgu, svöruðu sykursterameðferð vel í bráðafasa sjúkdómsins en þurftu síðar á skurðaðgerð að halda þar sem smágirnið var frílagt (enterolysis). Aðgerð heppnaðist vel í báðum tilvikum.
Bakgrunnur
Kviðskilun var fyrst reynd sem meðferð við nýrnabilun árið 1923.1 Hún varð þó ekki sjálfsagður valkostur sem meðferð við nýrnabilun á lokastigi fyrr en rúmum fimmtíu árum síðar. Það gerðist eftir að Popovich og félagar birtu reynslu sína af nýju formi kviðskilunar sem gerði sjúklingum kleift að sjá sjálfir um meðferðina í heimahúsum.2 Hún fólst í því að skipt var um skilvökva 4-5 sinnum á sólarhring í gegnum kviðlegg. Meðferðin var nefnd continuous ambulatory peritoneal dialysis en á íslensku hefur hún verið kölluð kviðskilun með pokaskiptum. Þá er vísað til þess að skilvökvinn kemur í plastpokum í magni sem hentar fyrir eina áfyllingu, oftast tveir lítrar. Nú orðið geta sjúklingar valið milli pokaskipta og meðferðar að næturlagi með aðstoð sjálfvirkrar vélar sem skiptir um skilvökva með reglulegu millibili (automated peritoneal dialysis).
Skilvökvi er hafður í kviðarholi sjúklings, allan sólarhringinn í tilviki pokaskipta en tæplega hálfan sólarhringinn í tilviki næturvélar. Allir skilvökvar innihalda hæfilegt magn salta og búfferefna en eru að öðru leyti mismunandi eins og fram kemur í töflu I. Efni ferðast undan þéttnihalla milli háræðablóðs og skilvökva þannig að hinn nýrnabilaði losnar við úrgangsefni og sölt [skilun (dialysis)]. Há glúkósaþéttni í skilvökva veldur osmótískum þrýstingsmun á milli blóðs og skilvökva. Því flyst vökvi úr blóði í skilvökva þannig að hinn nýrnabilaði safnar síður á sig vökva [vökvabrottnám (ultrafiltration)].
Þrátt fyrir mikla þróunarvinnu eru allir skilvökvar að einhverju leyti ólífvænir (bioincompatible) og á það bæði við um þá vökva sem notaðir eru á nýrnadeild Landspítala (tafla I)3 og vökva annarra framleiðenda. Mestum áhyggjum veldur hin háa glúkósaþéttni en ekki hefur tekist að finna hentugt efni sem gæti að öllu leyti komið í stað glúkósa. Henni fylgir hár osmótískur þrýstingur, skaðleg niðurbrotsefni sem myndast við dauðhreinsun skilvökvans (glucose degradation products = GDP) og glúkósaskotin eggjahvítuefni í lífhimnu (advanced glucose end products = AGE).4, 5 GDP og AGE hvetja framleiðslu efna sem örva bólgu (cytokines), bandvefsmyndun (transforming growth factor beta) og nýæðamyndun (vascular endothelial growth factor).6 Þessir þættir geta að miklu leyti skýrt þær breytingar sem verða á lífhimnu kviðskilunarsjúklinga með tímanum; iðraþekjufrumur (mesothelium) losna, bandvefur eykst og nýæðamyndun eykst.7 Með vaxandi fjölda smáæða eykst gegndræpi lífhimnu og osmótískur þrýstingsmunur milli blóðs og skilvökva eyðist hratt.8 Þá minnkar vökvaflæði úr blóði í skilvökva og sjúklingurinn fær bjúg. Vökvavandamál af þessum toga (ultrafiltration failure) eru algeng ástæða þess að kviðskilun er hætt.9 Sjúklingar eru mjög misnæmir fyrir þessari þróun en til að fylgjast með henni er gegndræpi lífhimnu metið með einföldu prófi af og til.
Helstu fylgikvillar kviðskilunar eru ofangreind vökvavandamál, bráð lífhimnubólga og afleiðingar aukins þrýstings í kviðarholi, til dæmis haulmyndun. Umlykjandi lífhimnuhersli (encapsulating peritoneal sclerosis) er hins vegar alvarlegasti fylgikvilli þeirrar ólífvænu meðferðar sem kviðskilun hlýtur að teljast. Í þessari grein er sagt frá þeim tveimur sjúklingum sem greinst hafa hér á landi með umlykjandi lífhimnuhersli, rakið það sem vitað er um algengi, orsakir, greiningu og meðferð sjúkdómsins og rædd þýðing hans fyrir meðferð nýrnabilunar á lokastigi.
Tilfellin
Tilfelli 1
Sjúklingur er karlmaður fæddur 1943, með lokastigsnýrnabilun á grunni IgA-nýrnameins. Hann fékk nýragræðling úr látnum gjafa 1987. Græðlingurinn bilaði vegna endurkomu IgA-nýrnameins og var næturkviðskilun með aðstoð vélar hafin í október 1998. Notaðir voru skilvökvarnir Dianeal® og Extraneal® (sjá töflu I). Í byrjun var erfitt að eiga við yfirvökvun og háþrýsting. Þau vandamál leystust eftir að nýragræðlingurinn var fjarlægður en hins vegar varð skilunin þá ónóg. Því var meðferðinni breytt í pokaskipti. Eftir það gekk vel með bæði skilun og vökvabrottnám. Við upphaf kviðskilunar kom í ljós að lífhimnan var mjög gegndræp en heldur hafði dregið úr þeim eiginleika við mat í september 2005. Lífhimnubólga af völdum Staphylococcus aureus var meðhöndluð í febrúar 2005 með góðum árangri. Sams konar sýking greindist í febrúar 2006 en í það skipti dugði sýklalyfjameðferð ekki til. Sjúklingur var enn fárveikur eftir mánaðarlanga meðferð með ýmsum sýklalyfjum, snemmbúið brottnám kviðleggs og fjölda neikvæðra ræktana úr skilvökva og blóði. Hann hafði háan hita og kviðverki, gat ekki nærst og CRP var hækkað (hæst 328 mg/L). Sneiðmynd af kviðarholi sýndi þykkveggja, samanlóðað smágirni. Grunur lék á umlykjandi lífhimnuhersli og sykursterameðferð (prednisólón 1 mg/kg) var hafin í apríl. Svörunin var dramatísk; innan fárra daga varð sjúklingur hita- og verkjalaus og innan tveggja vikna lækkaði CRP niður í 30 mg/L. Sjúklingur fékk blóðskilun, nærðist og þyngdist. Smám saman var dregið úr prednisólónskammti og þeirri meðferð hætt eftir hálft ár. Sumarið 2006 bar á vægum kviðverkjum, um haustið fór sjúklingur að fá garnastífluköst og í byrjun desember var hann háður næringu í æð. Um miðjan desember var gerð opin kviðarholsaðgerð. Í ljós kom að verulega þykknuð lífhimna þakti kviðarholið og garnirnar voru umluktar bandvefshjúp (mynd 1). Lífhimnusýni sýndi umtalsverða þykknun á lífhimnu með þéttum, frumufátækum bandvef (mynd 2). Garnirnar voru losaðar með því að skræla bandvefsherslið utan af þeim í fimm klukkustunda langri aðgerð. Engir fylgikvillar voru eftir aðgerðina og sjúklingur var fljótur að jafna sig. Hann var settur á tamoxifen 20 mg á dag eftir aðgerð og er enn á þeirri meðferð. 22 mánuðum eftir aðgerð eru engin merki þess að sjúkdómurinn hafi tekið sig upp að nýju.
Tilfelli 2
Sjúklingur er karlmaður, fæddur 1982. Haustið 2004 greindist hjá honum langt gengin nýrnabilun sem reyndist vera á grunni IgA-nýrnameins. Í nóvember sama ár var kviðskilunarmeðferð með pokaskiptum hafin og skilvökvarnir Physioneal® og Extraneal® notaðir. Við upphaf þeirrar meðferðar var lífhimnan fremur gegndræp en þó var aldrei erfitt að ná vökva af sjúklingi. Gegndræpi lífhimnu var ekki metið aftur. Í júní 2007 kom gat á ytri enda kviðskilunarleggsins. Upp úr því fékk sjúklingur lífhimnubólgu í fyrsta sinn. Síðan tók hvert lífhimnubólgutilvikið við af öðru og alls urðu þau fjögur á þremur mánuðum. Úr skilvökva ræktuðust í réttri tímaröð: kóagúlasaneikvæður Staphylococcus, Corynebacterium tegund, Bacillus tegund og Corynebacterium tegund. Sjúklingur var meðhöndlaður með sýklalyfjum samkvæmt ræktunarniðurstöðum og skilvökvaræktanir urðu neikvæðar á milli. Þegar sjúklingur fékk sína fjórðu lífhimnubólgu í september 2007 var gripið til þess ráðs að skipta um kviðlegg og var blóðskilun hafin í bið eftir gróanda kviðsára. Fyrir aðgerð var sjúklingur slappur og hafði væga kviðverki en eftir aðgerð versnuðu þessi einkenni mjög. Tveimur vikum eftir aðgerð fékk hann garnastíflu. Þá var kviðleggurinn fjarlægður í kviðsjáraðgerð sem leiddi í ljós mikla samvexti og samanlóðaðar garnir. Vefjasýni sýndi verulega þykknun á lífhimnu með frumufátækum bandvef. Sykursterameðferð (prednisólon 0,5 mg/kg) var hafin með ágætum árangri; garnir fóru í gang og CRP lækkaði úr 166 mg/L í 12 mg/L á tveim vikum. Þrem mánuðum síðar fór sjúklingur aftur að fá versnandi garna-stífluköst. Í byrjun janúar 2008 var því gerð aðgerð svipuð þeirri sem lýst er í fyrra tilfellinu. Eftir það linnti verkjum og sjúklingur fór að nærast. Hann var settur á tamoxífen 20 mg á dag og haldið var áfram að lækka prednisólónskammtinn. Tveimur mánuðum eftir aðgerð fékk sjúklingur nýragræðling frá móður sinni.
Yfirlit
Tíðni
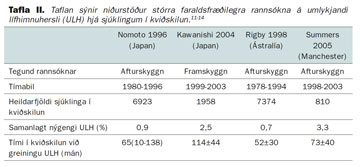
Árið 1980 greindist umlykjandi lífhimnuhersli í fyrsta sinn hjá kviðskilunarsjúklingi.10 Tafla II sýnir niðurstöður stærstu faraldsfræðilegra rannsókna sem gerðar hafa verið á sjúkdómnum.11-14 Í framskyggnri japanskri rannsókn var nýgengið 0% eftir 3 ár í kviðskilun, 0,7% eftir 5 ár, 5,9% eftir 10 ár og 17,2 % eftir meira en 15 ár.11 Í ástralskri rannsókn var árlegt nýgengi 0,19% á árunum 1980-1989 og 0,44% á árunum 1990-1994.13 Nýgengið jókst með meðferðarlengd og var þannig 6,4% eftir 5 ár og 19,4% eftir 8 ár.13 Rannsóknir gefa þannig skýra mynd af nýgengi sem eykst með tímanum í tvennum skilningi, það er að segja frá ári til árs og með meðferðarlengd.15
Umlykjandi lífhimnuhersli greinist oft mánuðum og jafnvel árum eftir að kviðskilun er hætt og þá oftast hjá nýraþegum. Í mörgum greinum er ekki minnst á hlut nýraþega en í japönsku rannsókninni voru þeir meirihluti tilfella.11
Orsakir
Umlykjandi lífhimnuhersli kemur fyrir hjá öðrum en kviðskilunarsjúklingum og stundum finnst engin orsök.16 Í gagnasöfnum er umfjöllun um slík tilfelli hverfandi miðað við þau sem tengjast kviðskilun. Í árdaga kviðskilunar með pokaskiptum mátti rekja flest tilfellin til asetats í skilvökva og/eða klórhexídíns í sótthreinsunarvökva.17, 18 Á níunda áratugnum var notkun þessara efna bönnuð á kviðskilunardeildum og skýrir því ekki þau tilfelli sem greinst hafa síðustu 15-20 árin. Ekki er loku fyrir það skotið að einhver þeirra efna sem nú er stundum bætt í skilvökva (til dæmis sýklalyf og heparín) geti haft skaðvænleg áhrif á lífhimnuna. Aldur, kyn og grunnsjúkdómur í nýrum virðast ekki hafa þýðingu.11
Kviðskilun sem slík veldur breytingum á lífhimnu sem leiða til aukins gegndræpis eins og fyrr greinir.19 Mikill meirihluti sjúklinga með umlykjandi lífhimnuhersli hefur haft mjög gegndræpa lífhimnu fyrir greiningu.20 Tími í kviðskilun er besti forspárþáttur umlykjandi lífhimnuherslis.21 Þessi atriði styðja þá kenningu að myndun umlykjandi lífhimnuherslis sé í raun fyrirsjáanleg þróun hjá sjúklingi í kviðskilun til langs tíma. Svonefnd second hit-kenning gerir hins vegar ráð fyrir að einhver annar þáttur en áfallalaus kviðskilun útleysi sjúkdóminn eða flýti fyrir þróun hans og er þar helst litið til lífhimnubólgu og nýraígræðslu.15, 22, 23

Mynd 1. Myndin sýnir þykka lífhimnu sem myndar hjúp utan um garnirnar.
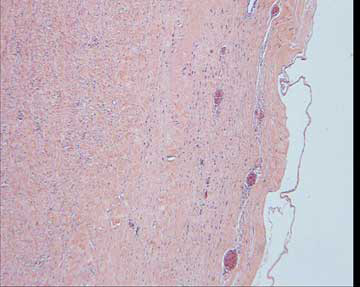
Mynd 2. Á myndinni sést lífhimnusýni. Iðraþekjan er horfin en eftir stendur þykkt, frumufátækt bandvefslag.
Í framskyggnu japönsku rannsókninni greindist umlykjandi lífhimnuhersli í kjölfar lífhimnubólgu hjá 25% sjúklinga en í áströlsku rannsókninni hjá 40%.11, 13 Margir sjúklingar mynda ekki umlykjandi lífhimnuhersli þrátt fyrir endurtekna lífhimnubólgu og margir með þekkt umlykjandi lífhimnuhersli hafa aldrei fengið lífhimnubólgu.21 Þannig virðist lífhimnubólga skipta máli fyrir þróun umlykjandi lífhimnuherslis hjá hluta sjúklinga. Tengslin gætu skýrst af bólgusvörun og fibrínútfellingum sem fylgja sýkingum.13
Óljóst er hvers vegna umlykjandi lífhimnuhersli greinist eftir að kviðskilunarmeðferð hefur verið stöðvuð. Stór hluti þeirra sjúklinga sem hætta í kviðskilun hafa mjög gegndræpa lífhimnu og eru þannig í aukinni áhættu.9 Hjá slíkum sjúklingum gæti sjúkdómsferlið einfaldlega hafa verið vel á veg komið þegar kviðskilun var stöðvuð. Auk þess gæti verið skaðlegt að hætta þeirri skolun sem af kviðskilun hlýst.21 Langflestir nýraþegar fá meðferð með kalsíneurínblokka til að koma í veg fyrir höfnun en þau lyf ýta undir bandvefsmyndun.24, 25
Erfðaþættir gætu ráðið því hversu hætt sjúklingum er við umlykjandi lífhimnuhersli. Í því tilliti er helst horft til gena sem kóða fyrir prótínum sem hafa áhrif á bólgu og bandvefsmyndun. Í lítilli rannsókn fannst munur á erfðabreytileika gens sem kóðar fyrir AGE-viðtaka milli kviðskilunarsjúklinga með og án umlykjandi lífhimnuherslis.26
Að lokum má nefna að sú eitrun sem fylgir nýrnabilun gæti komið við sögu. Stór rannsókn sýndi að bandvefslag lífhimnunnar var að meðaltali 50 µm hjá hraustu fólki, 150 µm hjá blóðskilunarsjúklingum og 270 µm hjá kviðskilunarsjúklingum.27
Einkenni og greining
Meirihluti sjúklinga fær hægt vaxandi einkenni. Helstu einkenni stafa af garnastíflu sem kemur oftast í köstum til að byrja með en getur orðið stöðug. Sjúklingarnir fá svæsna kviðverki, ógleði og uppköst og næringarástand versnar. Við skoðun eru garnahljóðin léleg og oft þreifast fyrirferð í kviðnum. Oft sést aukning á bráðafasaprótínum (til dæmis CRP) í sermi við upphaf einkenna.
Síðustu ár hafa birst lýsingar á bráðasjúkdómi sem kemur oftast í kjölfar lífhimnubólgu.28-33 Í þessum tilvikum eru sjúklingarnir jafnan fárveikir með háan hita og mikla aukningu á bráðafasapró-tínum í sermi. Ekki er vitað hversu stór hluti þeirra sem greinast með umlykjandi lífhimnuhersli í tengslum við lífhimnubólgu veikjast á þennan hátt en um mikinn minnihluta virðist vera að ræða.
Grunur vaknar oftast vegna einkenna. Staðfesting fæst með myndgreiningarrannsókn eða kviðarholsaðgerð. Á sneiðmynd sjást kalkanir og þykkveggja, samanlóðaðar garnalykkjur.34 Mælt er með sneiðmynd til greiningar en ómskoðun má nota til að fylgjast með þykkt garnaveggja hjá kviðskilunarsjúklingum.35 Við kviðarholsaðgerð kemur í ljós þykk, brúnleit lífhimna sem líkist leðri. Hún þekur kviðarholið að innan og myndar hjúp sem þrengir að görnum. Við smásjárskoðun á lífhimnusýni sést þykknuð lífhimna með misþykku frumufátæku bandvefslagi. Bólgufrumuíferð í vefnum er yfirleitt mjög lítt áberandi. Smáæðar eru misáberandi eftir svæðum.
Meðferð og horfur
Við greiningu umlykjandi lífhimnuherslis er kviðleggur fjarlægður og kviðskilun hætt. Verkjalyfjameðferð og næringu í æð er beitt eins og þurfa þykir. Ein og sér hafa þessi úrræði þó lítil áhrif á gang sjúkdómsins sem nánast alltaf leiddi til dauða áður fyrr. Þótt sjúkdómurinn sé sjaldgæfur og ekki til neinar slembaðar meðferðarrannsóknir er augljóst að horfur hafa batnað verulega við notkun lyfja og þróun skurðaðgerðar.
Sykursterar hafa bjargað lífum í svæsnum bráðatilfellum.28,33 Menn telja þá einnig gera gagn við hægari sjúkdómsgangi og er því mælt með sykursterum í þeim einu meðferðarleiðbeiningum sem til eru.21 Nákvæmar leiðbeiningar varðandi skammtastærð og meðferðarlengd liggja ekki fyrir en menn hafa trú á að meðferðin hjálpi mest snemma í ferlinu.21 Önnur ónæmisbælandi lyf hafa verið reynd í litlum mæli, til dæmis azatíóprín og mýkófenílat mófetíl.36, 37 Tamoxífen hefur gefið góða raun við aftanskinutrefjun (retroperitoneal fibrosis) og var þess vegna upphaflega reynt við umlykjandi lífhimnuhersli.38 Meðferð einstakra tilfella eða lítilla hópa bendir til gagnsemi en þó verður að athuga að stundum hafa sykursterar verið gefnir samtímis.39-42
Lengst af var talið að forðast ætti skurðaðgerðir við umlykjandi lífhimnuhersli enda dóu flestir af völdum lífhimnubólgu eftir aðgerð.43 Þetta breyttist eftir að þróuð var aðgerð sem byggist á að skræla bandvefspokann varlega utan af görnunum og losa samvexti44 og birtur árangur 112 slíkra aðgerða hjá 86 sjúklingum.44 Dánartíðni eftir aðgerð var 5,8% en aðrir hlutu bata að einhverju eða öllu leyti. Tæplega fjórðungur sjúklinga fékk þó sjúkdóminn aftur eftir 15 mánuði að meðaltali og þurfti að fara í eina eða fleiri enduraðgerðir.44 Þeir sem þurftu að fara í enduraðgerð höfðu samkvæmt smásjárskoðun fleiri smáæðar í lífhimnu en hinir. Var það eini marktæki forspárþáttur endurkomu sem höfundar fundu.44
Fyrirbyggjandi aðgerðir
Best væri að fyrirbyggja umlykjandi lífhimnuhersli. Leiðbeiningar um fyrirbyggjandi aðgerðir hafa nýlega verið birtar þó lítið sé um hágæðarannsóknir á sjúkdómnum.21 Samkvæmt leiðbeiningunum á að nota þá veikustu glúkósalausn sem hægt er án þess að sjúklingur safni á sig vökva. Áhersla er lögð á að leita leiða til að koma í veg fyrir lífhimnubólgu. Óhætt er talið að beita kviðskilun án varúðarráðstafana í fimm ár ef ekki koma upp sérstök vandamál svo sem vökvasöfnun (þá er rétt að meta lífhimnugegndræpi) eða einkenni umlykjandi lífhimnubólgu (þá er rétt að rannsaka). Eftir fimm ára meðferð er mælt með að meta lífhimnugegndræpi tvisvar á ári. Ef gegndræpi eykst eða sjúklingur fær endurtekna lífhimnubólgu þykir á öllum stigum rétt að fylgjast mjög nákvæmlega með sjúklingi og jafnvel stöðva kviðskilun.
Á Landspítala er farið eftir þessum leiðbeiningum nema hvað byrjað er fyrr að meta lífhimnugegndræpi.
Umræða
Alls hafa 124 sjúklingar verið í kviðskilun á Íslandi frá upphafi (1985-2008). Tveir sjúklingar hafa greinst með umlykjandi lífhimnuhersli og er samanlagt nýgengi sjúkdómsins því 1,6% sem er svipað og annars staðar. Ekki hafa birst tíðnitölur frá hinum Norðurlöndunum.
Fyrri sjúklingur okkar er sá sem lengst hefur verið í kviðskilun hér á landi (88 mánuði) og sá seinni hafði verið alllengi í kviðskilun (34 mánuði). Aukið gegndræpi lífhimnu var þekkt í báðum tilfellum. Sjúklingarnir voru því báðir í áhættuhópi og báðir fengu umlykjandi lífhimnuhersli í kjölfar lífhimnubólgu. Fyrri sjúklingurinn fékk svæsinn bráðasjúkdóm upp úr vel meðhöndlaðri lífhimnubólgu. Hann var hætt kominn en svaraði sykursterameðferð vel. Seinni sjúklingurinn fékk sjúkdóminn upp úr endurtekinni lífhimnubólgu en allur gangur var heldur vægari en í fyrra tilfellinu. Sjúkdómurinn greindist án tafar hjá seinni sjúklingnum, sennilega vegna reynslunnar af þeim fyrri. Aðgerð heppnaðist mjög vel í báðum tilvikum. Svo langt er liðið frá aðgerð fyrri sjúklingsins að líklegt má telja að hann sé að fullu læknaður. Eftirfylgnin er hins vegar stutt hjá seinni sjúklingnum.
Vaxandi nýgengi umlykjandi lífhimnuherslis er áhyggjuefni. Líklegustu skýringuna telja flestir vera fjölgun sjúklinga sem hafa verið lengi í kviðskilun. Samt sem áður undrast margir þróunina því að síðasta áratuginn hafa kviðskilunarvökvar tekið talsverðum framförum. Rannsóknir á frumum og tilraunadýrum benda til að þeir séu nú lífvænni.45 Þó glúkósi sé enn uppistaðan í flestum skilvökvum fær meirihluti kviðskilunarsjúklinga í hinum vestræna heimi endurbættan og líklega skaðminni glúkósavökva. Glúkósinn er geymdur í afmörkuðu hólfi með lágu sýrustigi sem leiðir til minni myndunar á GDP við dauðhreinsun. Fyrir notkun er glúkósanum blandað við afganginn af vökvanum sem inniheldur bíkarbónat. Útkoman er skilvökvi með sama sýrustig og mannslíkaminn og lága GDP-þéttni. Áfram er þó glúkósaþéttnin há og osmótíski þrýstingurinn sömuleiðis (tafla I). Íkódextrín og há þéttni amínósýra eru uppistöður annarra vökva sem notaðir hafa verið til að draga úr glúkósanotkun en hvort tveggja er lífhimnunni framandi og hugsanlega skaðlegt.46 Þannig eru allir skilvökvar í notkun líklega að einhverju leyti ólífvænir.
Búast má við framförum. Stöðugt er unnið að endurbótum á skilvökvum. Stórar fjölþjóðlegar rannsóknir eru hafnar til leitar að áhættuþáttum og söfnunar á lífsýnum fyrir erfðafræðiathuganir.47 Hugsanlega má nýta sér lyf sem beint er gegn ýmsum þáttum í ferlum bólgu-, bandvefs- og nýæðamyndunar.48 Jafnvel má hugsa sér ígræðslu iðraþekjufruma en þær framleiða ýmis efni sem eru lífhimnunni nauðsynleg.49
Þrátt fyrir endurbætta skilvökva vex nýgengi umlykjandi lífhimnuherslis og hætta er á að sjúkdómurinn þróist eða haldi áfram að þróast eftir að kviðskilun hefur verið stöðvuð. Lyfjameðferð og skurðaðgerð hafa þó stórbætt horfur þeirra sjúklinga sem greinast með sjúkdóminn og líkur eru á að í framtíðinni fjölgi meðferðarvalkostum og að hugsanlega verði hægt að vinsa úr þá sjúklinga sem eru í mestri hættu. Trúlega eru einn eða tveir áratugir þangað til í ljós kemur hvort umlykjandi lífhimnuhersli skerði notkunarmöguleika kviðskilunar að ráði. Sú spurning brennur á þeim sem sinna sjúklingum með nýrnabilun á lokastigi því ekki er um marga meðferðarmöguleika að ræða.
Heimildir
1. Heusser H, Werder H. Untersuchungen über Peritonealdialyse. Muench Med Wochenschr 70(2) 1923; 70: 1478-80.
2. Popovich RP, Moncrief JW, Nolph KD, Ghods AJ, Twardowski ZJ, Pyle WK. Continuous ambulatory peritoneal dialysis. Ann Intern Med 1978; 88: 449.
3. www.fass.se/október 2008
4. Inagi R, Miyata T, Yamamoto T, et al. Glucose degradation product methylglyoxal enhances the production of vascular endothelial growth factor in peritoneal cells: role in the functional and morphological alterations of peritoneal membranes in peritoneal dialysis. FEBS lett 1999; 463: 260-4.
5. Nakamura S, Niwa T. Advanced glycation end-products and peritoneal sclerosis. Semin Nephrol 2004; 24: 502-5.
6. Ha H, Cha MK, Choi HN, Lee HB. Effects of peritoneal dialysis solutions on the secretion of growth factors and extra cellular matrix proteins by human peritoneal mesothelial cells. Perit Dial Int 2002; 22: 171-7.
7. Devuyst O, Topley N, Williams JD. Morphological and functional changes in the dialysed peritoneal cavity: impact of more biocompatible changes. Nephrol Dial Transplant 2002; 17: 12-5.
8. Numata M, Nakayama M, Nimura S, Kawakami M, Lindholm B, Kawaguchi Y. Association between an increased surface area of peritoneal microvessels and a high peritoneal solute transport rate. Perit Dial Int 2003; 23; 116-22.
9. Churchill DN, Thorpe KE, Nolph KD. Increased peritoneal membrane transport is associated with decreased patient and technique survival for continuous peritoneal dialysis patients. The Canada-USA (CANUSA) Peritoneal Dialysis Study Group. J Am Soc Nephrol 1998; 9: 1285-92.
10. Gandhi VC, Humayan HM, Ing JS, et al. Sclerosing thickening of the peritoneal membrane in maintenance peritoneal dialysis patients. Arch Intern Med 1980; 140: 1201-3.
11. Kawanishi H, Kawaguchi Y, Fukui H, et al. Encapsulating peritoneal sclerosis in Japan: a prospective, controlled, multicenter study. Am J Kidney Dis 2004; 44: 729-37.
12. Nomoto Y, Kawaguchi Y, Kubo H, et al. Sclerosing encapsulating peritonitis in patients undergoing continuous ambulatory peritoneal dialysis: a report of the Japanese Sclerosing Encapsulating Peritonitis Study Group. Am J Kidney Dis 1996; 28: 420-7.
13. Rigby RJ, Hawley CM. Sclerosing peritonitis: the experience in Australia. Nephrol Dial Transplant 1998; 13: 154-9.
14. Summers AM, Clancy MJ, Syed F, et al. Single-center experience of encapsulating peritoneal dialysis for end-stage renal failure. Kidney Int 2005; 68: 2381-8.
15. Korte MR, Yo M, Betjes MGH, et al. Increasing incidence of severe encapsulating peritoneal sclerosis after kidney transplantation. Nephrol Dial Transplant 2007; 22: 2412-4.
16. Xu P, Chen LH, Li YM. Idiopathic sclerosing encapsulating peritonitis (or abdominal cocoon): a report of 5 cases. World J Gastroenterol 2007; 13: 3649-51.
17. Rottembourg J, Gahl GM, Poignet JL, et al. Severe abdominal complications in patients undergoing continuous ambulatory peritoneal dialysis. Proceedings of the Europian Dialysis and Transplantation Assocociation 1983; 20: 236-42.
18. Junor BJR, Briggs JD, Forewell MA, Dobbie JW, Henderson I. Sclerosing peritonitis ? the controbution of chlorhexidine in alcohol. Peritoneal Dialysis Bulletin 1985; 5: 101-4.
19. Gillerot G, Devuyst O. Molecular mechanisms modifying the peritoneal membrane exposed to peritoneal dialysis. Clin Nephrol 2003; 60: 106.
20. Yamamoto R, Nakayama M, Hasegawa T, et al. High-transport membrane is a risk factor for encapsulating peritoneal sclerosis developing after long-term continuous ambulatory pertoneal dialysis treatment. Adv Perit Dial 2002; 18: 131-4.
21. Kawaguchi Y, Saito A, Kawanishi H, et al. Recommendations on the management of encapsulating peritoneal sclerosis in Japan, 2005: diagnosis, predictive markers, treatment, and preventive measures. Perit Dial Int 2005; 25; S83-S95.
22. Saito A. Peritoneal dialysis in Japan: the issue of encapsulating peritoneal sclerosis and future challenges. Perit Dial Int 1999; 2005: 25(suppl 4): S77-82.
23. Arnadottir M, Alm P, Simonsen S, Rippe B. Skleroserande peritonit - en sällsynt men allvarlig komplikation vid peritonealdialys. Läkartidningen 1992; 89: 3665-8.
24. Maluccio M, Sharma V, Lagman M, et al. Tacrolimus enhances transforming growth factor beta 1 expression and promotes tumor progression. Transplantation 2003; 76: 597-602.
25. Khanna A, Plummer M, Bromberek C, Bresnahan B, Hariharan S. Expression of TGF-beta and fibrogenic genes in transplant recipients with tacrolimus and cyclosporine nephrotoxicity. Kidney Int 2002; 62: 2257-64.
26. Numata M, Nakayama M, Hosoya T, et al. Possible pathologic involvement of receptor for advanced glycation end products (RAGE) for development of encapsulating peritoneal sclerosis in Japanese CADP patients. Clin Nephrol 2004, 62: 455-60
27. Williams JD, Craig KJ, Topley N, et al. Morphologic changes in the peritoneal membrane of patients with renal disease. J Am Soc Nephrol 2002; 13: 470-9.
28. Courtney AE, Doherty CC. Fulminant sclerosing peritonitis immediately following acute bacterial peritonitis. Nephrol Dial Transplant 2006; 21: 532-4.
29. Courtney AE, Doherty CC. Single-center experience of encapsulating peritoneal sclerosis in patients on peritoneal dialysis for end-stage renal failure. Kidney Int 2006; 69: 1094.
30. Rajani R, Smyth J, Koffman CG, Abbs I, Goldsmith DJ. Differential effect of sirolimus vs prednisolone in the treatment of sclerosing encapsulating peritonitis. Nephrol Dial Transplant 2002; 17: 2278-80.
31. Evrenkaya TR, Atasou EM, Unver S, Basekim C, Baloglu H, Tulbek MY. Corticosteroid and tamoxifen therapy in sclerosing encapsulating peritonitis in a patient on continuous ambulatory peritoneal dialysis. Nephrol Dial Transplant 2004; 19: 2423-4.
32. Michael C, Hufnagel G, Niang A, et al. Sclerosing peritonitis. Nephrologie 2001; 22: 141-8.
33. Mori Y, Matsuo S, Sutoh H, Toriyama T, Kawahara H, Hotta N. A case of a dialysis patient with sclerosing peritonitis successfully treated with corticosteroid therapy alone. Am J Kidney Dis 1997; 30: 275-8.
34. Georg C, Al-Zwae K, Nair S, Cast JEI. Computed tomography appearances of sclerosing encapsulating peritonitis. Clin Radiol 2007; 61: 732-7.
35. Duman S, Ozbek SS, Gunay ES, et al. What does peritoneal thickness in peritoneal dialysis patients tell us? Advances in peritoneal dialysis 2007; 23: 28-33.
36. Wong CF, Beshir S, Khalil A, Pai R, Ahmad R. Successful treatment of encapsulating peritoneal sclerosis with azathioprine and prednisolone. !!!!
37. Lafrance JP, Létourneau I, Ouimet D, et al. Successful treatment of encapsulating peritoneal sclerosis with immunosuppressive therapy. Am J Kidney Dis 2008; 51: E7-10.
38. Moroni G, Gallelli B, Banfi G, Sandri S, Messa P, Ponticelli C. Long-term outcome of idiopathic retroperitoneal fibrosis treated with surgical and/or medical approaches. Nephrol Dial Transplant 2006; 21: 2485-90.
39. Wong CF. Clinical experience with tamoxifen in encapsulating peritoneal sclerosis. Perit Dial Int 2006; 26; 183-4.
40. del Peso G, Bajo AM, Gil F, et al. Clinical experience with tamoxifen in peritoneal syndromes. Adv Perit Dial 2003; 19: 32-5.
41. Moustafellos P, Hadjanastassiou V, Roy D, Velzzeboes NE. Tamoxifen therapy in encapsulating sclerosing peritonitis in patients after kidney transplantation. Transplant Proc 2006; 38: 2913-4.
42. Kawanishi H, Kawaguchi Y. Prevalence and therapeutic outcome of sclerosing encapsulating peritonitis (EPS) ? a multicenter study in Japan. Jin To Toseki 2000; 49: 225-8.
43. Kawanishi H, Watanabe H, Moriishi M, Tsuchiya S. Successful surgical management of encapsulating peritoneal sclerosis. Perit Dial Int 2005; 25: S39-S47.
44. Kawanishi H, Moriishi M, Tsuchiya S. Experience of 100 surgical cases of encapsulating peritoneal sclerosis: investigation of recurrent cases after surgery. Advances in Perit Dial 2007; 22: 60-4.
45. Holmes CJ, Faict D. Peritoneal dialysis solution biocompatibility: definitions and evaluation strategies. Kidney Int 2003; 64 (Suppl 88): S50-56.
46. Chan TM, Yung S. Studying the effects of new peritoneal dialysis solutions on the peritoneum. Perit Dial Int 2007; 27(Suppl 2):
47. Summers AM, Brenchley PEC. An international encapsulating peritoneal sclerosis registry and DNA bank: why we need one. Perit Dial Int 2006; 26: 559-63.
48. Io H, Hamada C, Ro Y, Ito Y, Hirahara I, Tomino Y. Morphological changes of peritoneum and expression of VEGF in encapsulated peritoneal sclerosis rat models. Kidney Int 2004; 65: 1927-36.
49. Hekking LH, Harvey VS, Havenith CE, van den Born J, et al. Mesothelial cell transplantation in models of acute inflammation and chronic peritoneal dialysis. Perit Dial Int 2003; 23: 323-30.