Áhrif Pentavac- og MMR-bólusetningar á þarma ungbarna
ÁgripTilgangur: Að meta hvort MMR-bólusetning (measles, mumps and rubella) valdi þarmabólgu hjá íslenskum börnum. Rannsóknin var ekki hönnuð til að svara spurningunni hvort MMR-bólusetning valdi einhverfu.
Aðferðir: Rannsökuð voru 109/20 börn fyrir bólusetningu og tveim, fjórum og 12-18 vikum eftir bólusetningu með Pentavac- og MMR-bóluefnum. Athugað var hvort merki væri um þarmabólgu með því að mæla kalprotectín í hægðasýni.
Niðurstöður: Hvorugt bóluefnið var tengt nokkurri marktækri breytingu á þéttni kalprotectíns í hægðum og kom ekkert fram sem benti til þarmabólgu.
Ályktun: Þar sem þessi rannsókn hefur sýnt að MMR-bólusetningin tengist ekki þarmabólgu þá mælir það gegn tilgátunni um að MMR tengist einhverfu í gegnum bólgu í þörmum.
Inngangur
Gagnsemi bólusetningar ungbarna við mislingum, hettusótt og rauðum hundum (MMR) er hafið yfir allan vafa en hér á landi hefur verið bólusett við þessum sjúkdómum með samsettu bóluefni (MMR) síðan 1989. Það er því mikil reynsla komin á þessa framkvæmd og aukaverkanir eru fáar og flestar meinlausar. Náttúruleg sýking af þessum farsóttum veldur hins vegar miklum veikindum og oft heilsutjóni og jafnvel dauða. Sérstaklega eru mislingar skæðir.
Á seinustu árum hafa komið fram tilgátur um að MMR-bólusetning geti leitt til þarmabólgu með leka á þörmum. Skaðleg efni komist þannig út í blóðið og truflað þroska heilann á viðkvæmu stigi og það síðar komið fram sem einhverfa.
Það er þekkt að börn með einhverfu hafa mörg hver eitlabólgur í kviðarholi og ristilbólgur. Hefur þetta ástand verið kallað einhverfuþarmabólga og fylgja henni margvísleg einkenni frá meltingarfærum. Rannsóknir á þessum sjúkdómi hafa allar verið gerðar mörgum árum eftir bólusetningu með MMR (1, 2). Orsök og meingerð einhverfuþarmabólgu er hins vegar umdeild (3) og enn fremur er hlutverk þarmanna óljóst í þróun sjúkdóma í taugakerfi sem geta komið fram sem einhverfa eða þroskaraskanir (4, 5).
Ein tilgátan um meingerð einhverfu þarmabólgu er þannig að bólusetning gegn mislingum, hettusótt og rauðum hundum (MMR) veki ekki mótefnasvar hjá ónæmiskerfinu (3). Vírusinn í mislingabóluefninu nái að setjast að til langframa í eitlavef í þörmum og leiði það til ónæmissvars sem komi fram í hnútum eða stækkun á eitlum í þörmum og þarmabólgu. Þarmabólga leiðir aftur til leka í þörmum sem leyfir frásog á efnum sem eru skaðleg fyrir taugakerfið, sérstaklega á viðkvæmum tíma fyrir þróun heilans í kringum 18 mánuða aldur. Afleiðingin geti verið seinkun eða truflun á þroska sem kemur fram í margvíslegum einkennum, meðal annars einhverfu (3). Sumt í þessum tilgátum er ekki hægt að rannsaka beint í börnum af augljósum ástæðum. Meginþáttur tilgátunnar er hins vegar sá að þarmabólga komi fram fljótlega eftir bólusetningu með MMR. Þetta er hægt að rannsaka þar sem nú eru til nokkur næm og sértæk próf til að meta þarmabólgu hjá börnum. Eitt slíkt próf er mæling á kalprotectíni í hægðum sem gefur nákvæma vísbendingu um bólgu í þörmum (6). Bólusetning á Íslandi fer fram á heilsugæslustöðvum og er þátttaka nálægt 100%. Pentavac (Pasteur Mérieux) bólusetning (gegn barnaveiki, stífkrampa, kíghósta og mænuveiki ásamt Hemophilus influenza týpu B) er gefin við þriggja, fimm og 12 mánaða aldur og MMR (Priorix, Smithkline Beecham) bólusetning við 18 mánaða aldur. Við könnuðum merki um þarmabólgu með kalprotectínaðferðinni fyrir og eftir Pentavac-bólusetningu og fyrir og eftir MMR-bólusetningu í hópi barna.
Tilgangur: Að meta hvort MMR-bólusetning valdi þarmabólgu hjá íslenskum börnum. Rannsóknin var ekki hönnuð til að svara spurningunni hvort MMR-bólusetning valdi einhverfu sem er mjög fátíð. Til þess þarf mun fleiri þátttakendur og lengra eftirlit en framkvæmt var í þessari rannsókn.
Þátttakendur og aðferðir
Eitthundrað og níu börn sem komu til bólusetningar á Miðstöð heilsuverndar barna á Barónsstíg eða á Heilbrigðisstofnun Suðurnesja í Reykjanesbæ tóku þátt í rannsókninni. Hópurinn var valinn þannig að haft var samband við foreldra allra barna sem áttu að mæta á ákveðnu tímabili í ungbarnavernd og þeim boðin þátttaka í rannsókninni. Framkvæmd, eðli og tilgangur rannsóknarinnar var skýrður út fyrir foreldrum. Mikill meirihluti þeirra sem haft var samband við var fús að taka þátt í rannsókninni. Útilokunarskilmerki fyrir þátttöku voru þau sömu og tilgreind eru af framleiðendum bóluefnisins (7). Börnin voru rannsökuð með því að fá hægðasýni og var mælt í því kalprotectín (Calprest, Calprotech Ltd., London, UK) fyrir Pentavac (við 12 mánaða aldur) og fyrir MMR (við 18 mánaða aldur) bólusetningu og tveim, fjórum og 12-18 vikum síðar (8). Aðferðin sem notuð var við kalprotectínmælingu í þessari rannsókn er frábrugðin þeim sem áður hefur verið greint frá (6, 9-11) og skilur þar mest á milli mismunandi aðferða við upplausn og úrdrátt efnanna úr hægðasýninu. Enn fremur er minna hægðasýni notað í okkar rannsókn heldur en í fyrri rannsóknum (200 mg í stað 5 gr). Calprest aðferðin gefur kalprotectíngildi sem eru um það bil fimm sinnum hærri en fyrri aðferð (13) og hefur aukið næmi (14) til að greina þarmabólgu. Kalprotectín er 36 kDa prótein sem bindur kalk og zink og er um 60% af próteinum í frymi hvítfrumna (neutrophyla). Það brotnar ekki niður í meltingarvegi og þolir vel geymslu við stofuhita. Ef bólga er í þörmum eða þarmavegg þá safnast hvítfrumur á þau svæði, brotna niður og skiljast út í hægðum. Eldri aðferðir til að greina bólgu í þörmum byggðust á geislamerkingu hvítfrumna með technesium og síðan var notað skann til að staðsetja hvar frumurnar söfnuðust saman. Mæling á kalprotectíni í hægðum er mun nákvæmari og auk þess auðveldari eftir að sýnt var fram á að hægðasöfnun er ekki nauðsynleg heldur dugði eitt 200 gr sýni. Aðferðin er mjög næm til að greina bólgu í þörmum bæði hjá börnum og fullorðnum en hún er ekki sértæk hvað varðar orsakir bólgunnar og hún gefur engar upplýsingar um hvar bólgan er í meltingarvegi (6, 9-11). Rannsóknin var gerð samkvæmt leyfi siðanefndar Landspítala Hringbraut, siðanefndar Miðstöðvar Heilsuverndar barna við Barónsstíg, siðanefndar Heilbrigðisstofnunar Suðurnesja, Reykjanesbæ, Persónuverndar og Vísindasiðanefndar. Staðtölulegur munur var prófaður með Wilcoxon's "ranked sums test" og pöruðu student t prófi.
Niðurstöður
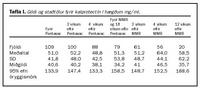
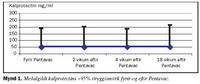
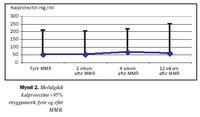
Tafla I sýnir helstu gildi og staðtölur fyrir kalprotectín í hægðum mg/ml hjá börnunum sem tóku þátt í tilrauninni. Það er enginn staðtölulegur munur á neinum tímapunkti (p>0,25) hvorki fyrir né eftir Pentavac-bólusetningu eða fyrir MMR-bólusetningu og tveimur, fjórum og 12-18 vikum á eftir. Alls byrjuðu 109 börn í tilrauninni og 56 skiluðu sýnum fjórum vikum eftir MMR-bólusetningu. Auk þess skiluðu 20 börn sýnum 12 vikum eftir MMR. Ástæða fyrir lítilli þátttöku við 12 vikna skoðun var mun minni áhugi foreldra en í upphafi rannsóknar og erfiðara var að fá sýni. Mynd 1 og 2 sýnir sömu gildi og í töflunni, það er miðgildi +95% öryggismörk fyrir og eftir bólusetningu með Pentavac og MMR en taflan sýnir fleiri staðtölur.
Umræða
Náttúruleg mislingasýking leggst mjög á eitlavef þarmanna og getur valdið svæsnum niðurgangi, eitlabólgu og þarmabólgu, einkum neðst í mjógirni. Þessi klíníska mynd líkist stundum Crohn's sjúkdómi (15, 16). Því hefur verið haldið fram að mislingavírus komi við sögu í meingerð Crohn's sjúkdóms (17-20) og enn fremur öðrum sjúkdómum, eins og mænusiggi (multiblesclerosis) (21). Þessi tilgáta er umdeild. Það hefur hins vegar vakið mikla athygli og áhuga að því hefur verið haldið fram að mislingabóluefni sem er búið til úr lifandi veikluðum vírus og gefið í þeim tilgangi að valda vægum sjúkdómi sem gefur varanlegt ónæmi geti jafnframt leitt til þarmabólgu sem aftur stuðli að myndun einhverfu (1, 2). Þessi möguleiki hefur bæði mikla klíníska þýðingu og einnig verulegar lagalegar afleiðingar og hugmyndin endurvekur gamlan ágreining um hlutverk þarmanna í sjúkdómum í taugakerfi.
Tilgátan um að MMR-bólusetning leiði til þarmabólgu og einhverfu var sett fram til að reyna að skýra algengi þarmabólgu hjá börnum með einhverfu og einkenni frá taugakerfi (1) og hugsanlegt tímalegt samband milli MMR-bólusetningar og einhverfu (3). Aðalatriðið í þessari tilgátu er að veiklaður mislingavírus í bóluefninu geti valdið langvarandi þarmabólgum sem leiði til frásogs á efnum sem skaði taugakerfið og geti hugsanlega truflað eðlilegan þroska heilans (22-24). Þessi tilgáta er studd nokkrum rökum þar sem óeðlileg þarmastarfsemi hefur fundist hjá einhverfum börnum og þar í einnig bólga og leki í görn (25-27) en þetta hefur eingöngu verið rannsakað mörgum árum eftir bólusetningu með MMR. Þarmabólga hefur enn fremur fundist við skoðun á vefjasýnum (1, 2), einkum í ristli, en mjög sjaldan hefur bólgu verið lýst í mjógirni. Þetta er ekki umdeilt heldur aðeins hlutverk og áhrif mislingabólusetningar í tilurð þessarar bólgu fyrst eftir bólusetningu og síðan síðbúin áhrif á þroska heilans. Í okkar rannsókn var sérstaklega skoðaður sá möguleiki hvort MMR-bólusetning leiddi til klínískrar eða leyndrar þarmabólgu í ungbörnum eftir bólusetningu og var notað til þess mjög næm aðferð sem búið er að prófa vel hjá fullorðnum (6, 12, 28) og í börnum (29, 30). Það er áhugavert að kalprotectín í hægðum hjá ungbörnum breytist mikið á fyrsta aldursári, það er hátt á fyrstu mánuðum en fer síðan lækkandi. Þessi breyting stafar sennilega af því að þá er að ávinnast ónæmi (oral immune tolerance) gegn fastri fæðu. Okkar rannsókn byrjar við 12 mánaða aldur og þá er þessi breyting að mestu gengin yfir en tíminn sem okkar rannsókn beinist að er eftir MMR-bólusetningu sem er gefin við 18 mánaða aldur. Á þessum tíma er kalprotectín stöðugt og lítill breytileiki milli einstaklinga (31, 32).
Kalprotectínþéttni í hægðasýnum fyrir bólusetningu í okkar rannsókn var sambærileg við það sem áður hefur verið lýst í heilbrigðum börnum. Rannsóknin sýndi hvorki merki um að Pentavac- né MMR-bólusetning framkallaði þarmabólgu í neinu barnanna tveim, fjórum og 12-18 vikum eftir bólusetningu. Á þessum tíma er ónæmissvar í hámarki og á að gefa varanlegt ónæmi. Þetta er í miklu ósamræmi við það sem gerist eftir náttúrulega sýkingu með mænusótt og mislingum en báðir þessir sjúkdómar geta gefið mikil einkenni frá meltingarfærum og mikla bólgu (15, 16). Niðurstöður okkar benda ekki til að MMR-bóluefnið valdi bólgu í þörmum hjá heilbrigðum börnum og mælir það eindregið gegn tilgátunni um að MMR-bólusetning veki upp þarmabólgu sem aftur leiði til einhverfu. Þetta útilokar hins vegar ekki þann möguleika að bólusetningin geti haft óæskileg áhrif á viðkvæm börn með óeðlilegt ónæmiskerfi eða hjá börnum sem hafa upplag fyrir sjálfsofnæmissjúkdóma. Ef þetta er tilfellið þá er það ekki bólusetningin sjálf sem veldur þessu svari heldur upplag einstaklingsins og það mundi þá einnig koma fram og jafnvel enn frekar ef um náttúrulega sýkingu af mislingum væri að ræða. Því hefur enn fremur verið haldið fram að samsett MMR-bóluefni stuðli frekar að þarmabólgu heldur en ef bóluefnin eru gefin ein og sér og ekki á sama tíma. Þar sem niðurstöður okkar sýna að samsett MMR-bóluefni veldur ekki þarmabólgu er ekki ástæða til að gefa bóluefnin hvort í sínu lagi eða á ólíkum tíma.
Þakkir
Rannsóknina styrktu Vísindasjóður Landspítala Hringbraut og Wyeth Lederle.
Heimildir
1. Wakefield AJ, Murch SH, Anthony A, Linnell J, Casson DM, Malik K, et al. Ileal-lymphoid-nodular hyperplacia, non-specific colitis, and pervasive developmental disorder in children. Lancet 1998; 351: 637-41.
2. Wakefield AJ, Anthony A, Murch SH, Thomson M, Montgomery SM, Davies S, et al. Enterocolitis in children with developmental disorders. Am J Gastroenterol 2000; 95: 2285-95.
3. Halsey NA, Hyman SL. Measles-mumps-rubella vaccine and autistic spectrum disorder: report from the new challenges in childhood immunizations conference convened in Oak Brook, Illinois, June 12-13, 2000. Pediatrics 2001; 107: E84.
4. Dohan FC. Coeliac disease and schizophrenia. Lancet 1970; i: 897-8.
5. Wood NC, Hamilton I, Axon ATR, Khan SA, Quirke P, Mindham RH, et al. Abnormal intestinal permeability. An aetiological factor in chronic psychiatric disorders? Br J Psychiatr 1987; 150: 853-6.
6. Tibble J, Teahon K, Thjodleifsson B, Roseth A, Sigthorsson G, Bridger S, et al. A simple method for assessing intestinal inflammation in Crohn's disease. Gut 2000; 47: 506-13.
7. Bjarnason I, Macpherson AJM, Hollander D. Intestinal permeability: An overview. Gastroenterology 1995; 108: 1566-81.
8. Ball LK, Ball R, Douglas Pratt R. An Assessment of Thimerosal Use in Childhood Vaccines. Pediatrics 2001; 107: 1147-54.
9. Tibble J, Sigthorsson G, Fagerhol M, Bjarnason I. Surrogate markers of intestinal inflammation a repredictive for relapse in patients with inflammatory bowel disease. Gastroenterology 2000; 119: 15-22.
10. Roseth A, Teahon K, Rihani H, Sigthorsson G, Macpherson A, Price AB, et al. A new method for assessing intestinal inflammation in man. Lancet 1997; Submitted.
11. Roseth AG, Fagerhol MK, Aadland E, Schjonsby H. Assessment of the neutrophil dominating calprotectin in feces. A methodologic study. Scand J Gastroenterol 1992; 27: 793-8.
12. Roseth AG, Schmidt PN, Fagerhol MK. Correlation between faecal excretion of Indium-111-labelled granulocytes and Calprotectin, a granulocyte marker protein, in patients with inflammatory bowel disease. Scand J Gastroenterol 1999; 34: 50-4.
13. Brandsnes TH, Dale S, Holtlund J, Skuibina E, Schionsby H, Johne B. Improved assay for fecal claprotectin. Clin Chim Acta 2000; 292: 41-54.
14. Johne B, Kronborg O, Ton HJ, Kristinsson J, Fuglerod D. A new calprotect in test for colorectal neoplasia. Clinical results and comparison with previous method. A Scand J Gastroenterol 2001; 36: 291-6.
15. Assad F. Measles: Summary of worldwide impact. Rev Infect Dis 1983; 5: 452-9.
16. Gershon A. Measles (Rubeola). In: Harrison's Principles of Internal Medicine, 14 edition. Fauci AS, Braunwald E, Isselbacher KJ, Wilson JD, Martin JB, Kasper DL, Hauser SL, Longo DL (eds). McGraw-Hill, NewYork. 1998: 1123-5.
17. Ghosh S, Armitage E, Wilson D, Minor PD, Afzal MA. Detection of persistent measles virus infection in Crohn's disease: current status of experimental work. Gut 2001; 48: 748-52.
18. Wakefield AJ, Pittilo RM, Sim R, Cosby SL, Stephenson JR, Dhillon AP, et al. Evidence of persistent measles virus infection in Crohn's disease. J Med Virol 1993; 39: 345-53.
19. Wakefield AJ, Ekbom A, Dhillon AP, Pittilo RM, Pounder RE. Crohn's disease: pathogenesis and persistent measles virus infection. Gastroenterology 1995; 108: 911-6.
20. Montgomery SM, Morris DL, Pounder RE, Wakefield AJ. Paramyxovirus infections in childhood and subsequent inflammatory bowel disease. Gastroenterology 1999; 116: 796-803.
21. Summers BA, Appel MJ. Aspects of canine distemper virus and measles virus encephalomyelitis. Neuropathol Appl Neurobiol 1994; 6: 525-34.
22. Reichelt WH, Stensrud J-EM, Reichelt KL. Peptide excretion in celiac disease. J Paed Gastroenterol Nutrt 1998; 26: 305-9.
23. Sun Z, Cade JR. A peptide found in schizophrenia and autism causes behavioral changes in rats. Autism 1999; 3: 85-95.
24. Friedman DI, Amidon GL. Oral absorption of peptides: influence of pH and inhibitors on the intestinal hydrolysis of Leu-Enkephalin and analogues. Pharmaceutical Res 1991; 8: 93-7.
25. D'Eufemia P, Celli M, Finocchiaro R, Pacifico L, Viozzi L, Zaccagnini M, et al. Abnormal intestinal permeability in children with autism. Acta Paediatr 1996; 85: 1076-9.
26. Horvath K, Papdimitriou JC, Rabsztyn A, Drachenberg C, Tildon JT. Gastrointestinal abnormalities in children with autistic disorder. J Paediatr 1999; 135: 559-63.
27. Anthony A, Bjarnason I, Sigthorsson G, Montgomery SM, Murch SH, Thompson M, et al. Faecal calprotect in levels correlate with acute inflammation in autistic enterocolitis. Gut 2000; 46 (supplII): A3.
28. Tibble J, Sigthorsson G, Foster R, Scott D, Roseth A, Bjarnason I. Faecal calprotectin: A simple method for the diagnosis of NSAID-induced enteropathy. Gut 1999; 45: 362-6.
29. Bunn SK, Bisset WM, Main MJ, Gray ES, Olson S, Golden BE. Fecal calprotectin: validation as a noninvasive measure of bowel inflammaiton in childhood inflammatory bowel disease. J Pediatr Gastroenterol Nutr 2001; 33: 14-22.
30. Bunn SK, Bisset WM, Main MJ, Golden BE. Fecal calprotectin as a measure of disease activity in childhood inflammatory bowel disease. J Pediatr Gastroenterol Nutr 2001; 32: 171-7.
31. Rugtveit J, Fagerhol MK. Age Dependent Variations in Fecal Calprotect in Concentrations in Children. J Pediatr Gastroenterol Nut, 2002; 34: 323-4.
32. Golden B, Bunn S, M Main. Age-Dependent Variations in Fecal Calprotectin Concentrations in Children. J Pediatr Gastroenterol Nut, 2002; 34: 324-5.
Effect of Pentavac and MMR vaccination on the intestine
| English Summary |
| Þjóðleifsson B, Davíðsdóttir K, Agnarsson Ú, Theodórs A, Gunnarsdóttir A, Möller E, Jónsdóttir A, Sigþórsson G, Kjeld M, Bjarnason I Effect of Pentavac and MMR vaccination on the intestine Læknablaðið 2002; 88: 491-4 Objective: The safety of infant vaccination has been questioned in recent years. In particular it has been suggested that the measles, mumps and rubella (MMR) vaccination leads to brain damage manifesting as autism consequent to the development of an "enterocolitis" in the immediate post-vaccination period. Aim: To assess if MMR vaccination is associated with sub-clinical intestinal inflammation which is central to the autistic "enterocolitis" theory. The study was not designed to test directly the association of autism to MMR vaccination. Material and methods: We studied 109/20 infants, before and two and four weeks after immunization with Pentavac and MMR vaccines, for the presence of intestinal inflammation (faecal calprotectin). Results: Neither vaccination was associated with any significant increase in faecal calprotectin concentrations. Conclusions: The failure of the MMR vaccination to cause an intestinal inflammatory response provides evidence against the proposed gut-brain interaction that is central to the autistic "enterocolitis" hypothesis. Keywords: Intestinal inflammation, MMR vaccination, Pentavac vaccination, autism. Correspondance: Bjarni Þjóðleifsson, bjarnit@landspitali.is |