Fræðigreinar
Yfirlitsgrein Gáttatif Meðferðarkostir við aldamót
Ágrip
Gáttatif er vaxandi vandamál og er búist við að nýgengi þess muni aukast verulega á næstu áratugum. Gáttatif getur komið fram við ólíkar aðstæður, hjá þeim sem hafa hjartasjúkdóm sem og hjá þeim sem hafa eðlilegt hjarta. Orsakir gáttatifs geta verið margvíslegar. Gáttatif getur valdið verulegum einkennum, þar með talið hjartabilun, hjartsláttaróþægindum og heilablóðfalli. Dánartíðni sjúklinga með gáttatif er aukin. Að undanförnu hafa komið fram ýmsir nýir möguleikar í meðferð þessa sjúkdóms. Blóðþynningarmeðferð dregur verulega úr hættu á heilablóðfalli. Ný lyf við hjartsláttartruflunum hafa mörg hver reynst vel, bæði við að venda sjúklingum yfir í sínustakt og til að viðhalda sínustakti. Þá hafa komið fram ýmsar nýjungar við rafvendingu á gáttatifi. Brennslumeðferð við þessum sjúkdómi fer vaxandi og gæti á næstu árum orðið mikilvægur valkostur í meðferð gáttatifs.Í þessari grein er fjallað um ný lyf í meðferð gáttatifs, nýjungar við rafvendingu og brennslumeðferð.
English Summary |
| Guðmundsdóttir IJ, Arnar DO Atrial fibrillation: therapeutic options at the turn of the century Læknablaðið 2000; 86: 841-7 Atrial fibrillation is an increasing health care problem and the incidence of this arrhythmia is expected to increase substantially in the next two decades. Atrial fibrillation can be seen in patients with structural heart disease as well as those who have a normal heart. A variety of underlying mechanisms can lead to atrial fibrillation, including parasympathetic stimulation causing vagal atrial fibrillation. Complications of atrial fibrillation include congestive heart failure and stroke. Atrial fibrillation is an independent risk factor for increased mortality. In recent years a number of new treatment options have emerged. Anticoagulation decreases the risk of stroke and new antiarrhythmic drugs have been developed which increase the likelihood of conversion to and subsequent maintenance of sinus rhythm. In addition there have been advances in the approach to electrical cardioversion. Radiofrequency ablation therapy is a promising option in the treatment of atrial fibrillation and could be increasingly utilized in the near future. This paper focuses on advances in the therapy of atrial fibrillation, including new pharmacological agents, radiofrequency ablation and electrical cardioversion. Key words: atrial fibrillation, therapy, review. Correspondence: Davíð O. Arnar. E-mail: davidar@rsp.is |
Inngangur
Gáttatif er algengasta viðvarandi hjartsláttartruflunin. Talið er að yfir 4% þeirra sem komnir eru yfir sextugt hafi fengið að minnsta kosti eitt tilvik gáttatifs (1). Nýgengi gáttatifs er að aukast og helst það í hendur við fjölgun þeirra sem ná háum aldri og bætta lifun sjúklinga með kransæðasjúkdóma og hjartabilun. Því er spáð að nýgengi þessarar takttruflunar muni aukast um allt að 60% á næstu tveimur áratugum (2). Algengast er að gáttatif komi fram hjá sjúklingum með hjartasjúkdóm, oftast kransæðasjúkdóm eða háþrýsting (3). Ef gáttatif er til staðar án greinanlegs hjartasjúkdóms, er talað um stakt (lone) gáttatif. Stakt gáttatif sést gjarnan hjá yngra fólki en nýlegar rannsóknir benda til að tengsl geti verið milli þess og offitu (4). Einnig benda athuganir til þess að stakt gáttatif geti stundum verið arfgengt, þó það eigi líklega einungis við minnihluta þeirra sem hafa stakt gáttatif (5).
Ekki er óalgengt að gáttatif komi í köstum (paroxysmal atrial fibrillation), en sjúklingar hafa þá eðlilegan sínustakt á milli. Gáttatif kallast viðvarandi (chronic) ef það hefur staðið samfellt lengur en í sex mánuði.
Nýlega var sýnt fram á að margir sjúklingar sem fengu gáttatif í köstum fengu kast milli miðnættis og sex á morgnana, en færri fyrri hluta dags (6). Þetta er andstætt því sem þekkt er með tímasetningu kransæðastíflu, þar sem upphaf einkenna er oftast fyrripart dags. Gáttatifsköst koma þannig fyrir hjá hluta sjúklinga að nóttu til og einnig hefur verið lýst að gáttatif geti komið eftir máltíð, en þetta eru einmitt aðstæður þar sem að vagal örvun er í hámarki. Gáttatif sem kemur gjarnan við þessar aðstæður hefur því verið nefnt vagal gáttatif (7). Jafnframt er það vel þekkt að köst af gáttatifi geta byrjað við álag eða áreynslu. Bæði örvandi og letjandi hlutar ósjálfráða taugakerfisins geta þannig ýtt undir gáttatif (8). Þannig virðist gáttatif hafa ýmsar undirtegundir og getur verið mikilvægt að hafa það í huga þegar tekin er ákvörðun um val meðferðar.
Einkenni
Sjúklingar með gáttatif geta verið einkennalausir en algengara er að þeir finni fyrir hjartsláttaróþægindum, skertu úthaldi eða jafnvel hjartabilunareinkennum. Gáttatif þolist sérstaklega illa hjá sjúklingum með hjartabilun. Gáttasamdráttur tapast og skiptir það oft miklu máli hjá þeim sem hafa skerta starfsemi vinstra slegils.
Fyllitími vinstra slegils styttist hjá þeim sem hafa hraða sleglasvörun og það getur einnig leitt til hjartabilunareinkenna. Einnig veldur sú óregla sem verður á sleglataktinum ein og sér líkast til minnkun á útfalli hjartans (9). Ef sleglasvörun í gáttatifi er hröð getur það stuðlað að hjartabilun hjá þeim sem höfðu eðlilegan slegil fyrir (tachycardia-induced cardiomyopathy) (10). Þessi tegund hjartabilunar getur oft gengið til baka að fullu ef dregið er úr hraða sleglasvörunar. Mikilvægt er að hafa þetta í huga við mat á sjúklingum með gáttatif sem hafa skerta starfsemi vinstri slegils, sér í lagi þeim sem ekki hafa fyrri sögu um hjartasjúkdóma.
Blóðþynning
Við gáttatif verður rafvirkni í gáttum óskipulögð og gáttasamdráttur skerðist. Þetta stuðlar að stasa á blóði og segamyndun, sérstaklega í eyra vinstri gáttar. Áhættan á segareki getur verið allt að fimmfalt hærri hjá þeim sem hafa gáttatif heldur en hjá þeim sem eru í sínustakti (11). Hjá þeim sem hafa hjartalokusjúkdóm í kjölfar gigtsóttar, sérstaklega míturlokusjúkdóm, getur áhættan á segareki verið allt að sautjánföld (11). Vegna hættu á segareki hjá sjúklingum með gáttatif er mælt með blóðþynningu með warfaríni hjá þeim sem eru í mestri hættu á slíku. Notkun blóðþynningarlyfja hjá sjúklingum með gáttatif hefur verið mikið rannsökuð á síðasta áratugi og áður verið gerð ítarleg skil í Læknablaðinu (12).
Samsett gögn úr fimm rannsóknum á gagnsemi blóðþynningar hjá sjúklingum með gáttatif, sem ekki tengdist hjartalokusjúkdómi, sýndu að árleg tíðni heilablóðfalls var 4,5% hjá sjúklingum með gáttatif sem fengu lyfleysu, en 1,4% hjá sjúklingum sem fengu warfarínblóðþynningu þar sem stefnt var að INR (International Normalized Ratio) gildi milli 2,0 og 3,0 (13). Þannig stuðlaði blóðþynningarmeðferð að 68% lækkun á tíðni heilablóðfalls. Jafnframt kom í ljós að tíðni meiriháttar blæðinga hjá hópnum sem fékk virkt lyf var 1,3% á ári á móti 1,0% hjá lyfleysuhópnum og var sá munur ekki marktækur. Ný grein þar sem teknar eru saman niðurstöður 16 rannsókna staðfestir enn frekar gagnsemi blóðþynningar hjá sjúklingum með gáttatif (14).
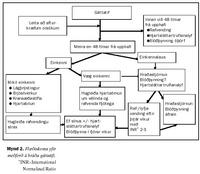
En þurfa allir sjúklingar með gáttatif blóðþynningarmeðferð? Svo er líkast til ekki. Ítarlegri skoðun á ofangreindum samsettum gögnum sýndi að hægt var að spá fyrir um hverjir væru í mestri hættu á segareki (tafla I) (13). Þeir sem hafa einn eða fleiri af eftirtöldum klínískum áhættuþáttum: háþrýsting, sykursýki, sögu um heilaáfall eða tímabundna blóðþurrð í heila og aldur yfir 65 ára eru í aukinni hættu. Jafnframt hafa rannsóknir gefið til kynna að skertur samdráttur í vinstri slegli og stækkuð vinstri gátt (yfir 5,0 cm), hvoru tveggja metið með ómskoðun, séu áhættuþættir fyrir segareki. Sumir vilja einnig telja hjartavöðvasjúkdóm með ósamstæðri þykknun á sleglaskipt til áhættuþátta fyrir segareki hjá sjúklingum með gáttatif. Þeir sem hafa einhvern af ofangreindum áhættuþáttum ættu því tvímælalaust að vera á warfarínblóðþynningu, þar sem stefnt er að INR gildi 2,0-3,0, ef frábending er ekki til staðar. Ítrekað skal að þeir sem hafa gáttatif og lokusjúkdóm í kjölfar gigtsóttar eiga að vera á blóðþynningarmeðferð.
Aspirín eitt og sér eða aspirín með lágskammta warfaríni er ekki jafn árangursrík meðferð og warfarínmeðferð þar sem stefnt er að INR gildi milli 2,0 og 3,0, aspirín meðferð dregur úr áhættu á heilablóðfalli um 22% (13). Ekki er þörf á að nota aspirín til viðbótar við warfarín nema ef kransæðasjúkdómur er einnig til staðar. Ef algjör frábending er fyrir notkun warfaríns ætti að hugleiða notkun aspiríns.
Áhætta á segareki hjá þeim sem hafa engan af ofangreindum áhættuþáttum er aðeins um 1% á ári (13). Hjá þeim hópi dugir aspirín eitt og sér eða jafnvel engin blóðþynningarmeðferð. Rétt er að taka fram að áhættan á segareki hjá þeim sem hafa gáttatif sem kemur í köstum er sú sama og hjá þeim sem hafa viðvarandi gáttatif.
Lyfjameðferð
Tveir meginvalkostir standa til boða við meðferð gáttatifs; annars vegar að endurheimta sínustakt í því markmiði að bæta hemódýnamískt ástand sjúklings, forðast viðvarandi gáttatif og ef til vill draga úr hættu á segareki. Hins vegar að reyna ekki að venda gáttatifi heldur stjórna sleglahraðanum og blóðþynna sjúkling til að draga úr áhættu á segareki. Seinni kosturinn kemur sérstaklega til greina hjá þeim sjúklingum sem eru einkennalausir eða hafa væg einkenni. Hvor aðferðin er valin fer talsvert eftir einkennum sjúklings en óvíst er hvort annar meðferðarkosturinn sé betri en hinn með tilliti til lifunar. AFFIRM rannsóknin, sem er nú er í gangi í Bandaríkjunum, ber þessa tvo meðferðarkosti saman og er áætlað er að henni ljúki á næstu tveimur árum.Sé sú leið valin að reyna að koma sjúklingi í sínustakt eru tvær aðferðir mögulegar. Annars vegar rafvending og hins vegar vending með lyfjum sem virka á hjartsláttartruflanir. Rafvending sem gerð er í stuttri svæfingu hefur frumárangur á bilinu 75-95% (15,16). Hætta á segareki samfara rafvendingu getur verið á bilinu 5-7% (17). Blóðþynning virðist draga verulega úr þessari hættu. Blóðþynning í kringum rafvendingar er ekki jafn vel rannsökuð og blóðþynning hjá sjúklingum með langvinnt gáttatif. Flestar rannsóknir á þessu hafa verið afturskyggnar og óslembaðar (17,18). Þrátt fyrir að ekki séu til góðar upplýsingar um æskilega tímalengd blóðþynningar í kringum rafvendingu er nú mælt með fullri warfarínblóðþynningu í þrjár vikur fyrir og fjórar vikur eftir árangursríka rafvendingu (19). Samkvæmt nýlegri rannsókn þar sem stuðst var við hjartaómun um vélinda leystust tæplega 90% sega í vinstri gátt upp eftir þriggja vikna blóðþynningarmeðferð (20). Þetta virðist styðja tímalengd meðferðar í þrjár vikur fyrir rafvendingu. Einnig er þekkt að þrátt fyrir að rafvirkni í gáttum lagist við vendingu, þá geta liðið allt að fjórar vikur uns samdráttur í gáttum er orðinn eðlilegur á ný (21). Þetta er talið stafa af tímabundnum hjartavöðvasjúkdómi í gáttum (atrial cardiomyopathy) sem er tilkominn vegna hraða óreglunnar. Hlutverk annarra blóðþynningarlyfja, svo sem smá-heparína í tengslum við rafvendingu er óþekkt. Heparíngjöf í skamman tíma, í 24-48 tíma í kringum rafvendingu, er ekki fullnægjandi og getur áhættan á segareki í slíkum tilfellum verið allt að 5,3% (22).
Vegna þeirrar staðreyndar að einungis um 50% sjúklinga haldast í sínustakti í 12 mánuði eftir rafvendingu er líklegt að lengri blóðþynning en fjórar vikur eftir árangursríka rafvendingu sé ráðleg, að minnsta kosti fyrir valda sjúklinga. Hefur tilhneigingin reyndar verið í þá átt að halda áfram með blóðþynningu lengur en fjórar vikur hjá flestum sjúklingum með gáttatif vegna hættu á endurkomu óreglunnar.
Gáttatifi sem varað hefur skemur en 48 klukkustundir er óhætt að venda með lyfjum eða rafmagni án nokkurrar blóðþynningar fyrir eða á eftir. Áhættan á segareki hjá þeim hópi er innan við 1% (23).
Hvað varðar lyf til vendingar á gáttatifi yfir í sínustakt standa ýmsir möguleikar til boða. Lyf eins og sótalól (Sotacor®), prókaínamíð (Pronestyl®) eða dísópýramíð (Durbis®) eru gjarnan notuð til að reyna að koma aftur á sínustakti. Kínidín var töluvert notað áður, en hefur lítið fram yfir prókaínamíð eða dísópýramíð og veldur talsverðum aukaverkunum frá meltingarvegi. Lyf eins og flekainíð (Tambocor®) eða própafenón (Rytmonorm®) hafa einnig gefist vel hjá sjúklingum sem hafa ekki hjartasjúkdóma. Amíódarón (Cordarone®) hefur fram til þessa ekki verið talið gott til að venda gáttatifi yfir í sínustakt en er hins vegar mjög gagnlegt lyf til að halda sjúklingum í sínustakti (24).
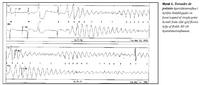
Íbútilíð er nýtt lyf við hjartsláttartruflunum af flokki III. Sýnt hefur verið að 35% sjúklinga í gáttatifi venda yfir í sínustakt á fyrstu klukkustund eftir gjöf lyfsins í æð (25). Einnig getur íbútilíð dregið úr orkuþörf við rafvendingu. Meginaukaverkun við gjöf lyfsins er torsades de pointes sleglahraðtaktur sem kemur fram hjá allt að 7% sjúklinga og þarfnast rafvendingar hjá 2-3% (mynd 1) (25).
Tvö ný lyf af þriðja flokki lyfja við hjartsláttartruflunum, azimilíð og dófetilíð, hafa verið í þróun og nokkrar rannsóknir á þeim verið kynntar þar sem virkni þeirra gegn gáttatifi hefur verið skoðuð. Dófetilíð virðist bæði vera gagnlegt við að venda fólki úr gáttatifi og að viðhalda sínustakti (26). Helsta aukaverkun lyfsins er að það getur innleitt torsades de pointes eins og flest lyf af þriðja flokki. DIAMOND rannsóknin benti hins vegar til að lyfið hefði ekki áhrif á lifun fólks með hjartabilun eða eftir hjartadrep (26). Virðast frumniðurstöður rannsókna á þessum lyfjum í meðferð gáttatifs lofa góðu, að minnsta kosti enn sem komið er. Í þróun er einnig nýtt lyf, drónedarón sem er joðlaus afleiða amíódaróns. Það virðist hafa marga af eiginleikum amíódaróns án eitrunaráhrifa þess á líffæri, til dæmis lungu, lifur og skjaldkirtil. Í framtíðinni gæti þetta lyf orðið valkostur við meðferð á gáttatifi og í gangi er rannsókn á gagnsemi þess undir þeim kringumstæðum.
Þrátt fyrir að frumárangur af vendingu gáttatifs sé nokkuð góður er stundum erfiðara að halda sjúklingi í sínustakti til lengri tíma. Ef ekki eru gefin nein lyf við hjartsláttaróreglu eftir vendingu haldast einungis um 25% sjúklinga í sínustakti eftir 12 mánuði. Ef notuð eru lyf við hjartsláttartruflunum hækkar hlutfallið í um 50%, þó heldur betri árangurs megi vænta ef amíódarón er notað (24).
Ákvörðun um hvaða lyf við hjartsláttartruflunum skuli nota til að halda sjúklingi í sínustakti tekur gjarnan mið af hjartasjúkdómi og fjölda tilvika af gáttatifi sem viðkomandi hefur fengið. Einnig verður að taka mið af því hvaða lyf hafa áður verið reynd. Ef sjúklingur hefur eðlilegt hjarta og aðeins fengið gáttatif einu sinni kemur til greina að fylgjast með honum án þess að nota lyf við hjartsláttaróreglu. Ef ákvörðun er tekin um að nota lyf hjá sjúklingum án hjartasjúkdóms koma til greina lyf af flokki 1C, 1A eða lyf eins og sótalól. Hjá sjúklingum sem hafa kransæðasjúkdóm og hafa fengið kransæðastíflu eru lyf eins og sótalól og amíódarón góður valkostur. Hjá sjúklingum með hjartabilun og skertan vinstri slegil er amíódarón líkast til fyrsti og eini valkosturinn sem stendur. Hins vegar er mögulegt að lyf eins og dófetilíð gætu í framtíðinni hentað þessum sjúklingahópi (26). Hjá þeim sem hafa þykknun á hjartavöðva eru lyf af flokki 1C eða 1A kostir, en forðast skyldi lyf af þriðja flokki sem lengja QT bil, þar sem að þeir sem hafa hjartavöðvaþykknun hafa gjarnan lengda hrifspennu fyrir og lenging QT bils ýtir undir hættu á torsades de pointes. Ef um svokallað vagal gáttatif er að ræða kemur til greina að nota lyf eins og dýsópýramíð sem hefur vagólýtísk áhrif eða jafnvel með gangráði þannig að sjúklingur fái síður hægatakt sem ýtt gæti undir að gáttatif byrji. Lyfjameðferð sem hægir á hjartslætti á því ekki við ef sjúklingur hafur vagal gáttatif.
Töluverð umræða hefur verið undanfarið um hvort óhætt sé að byrja með lyf við hjartsláttartruflunum utan sjúkrahúss hjá völdum sjúklingum. Öllum lyfjum við hjartsláttartruflunum fylgir hætta á versnandi eða nýjum takttruflunum (pro-arrhythmia) (27,28). Mest er áhættan gjarnan í upphafi meðferðar og því hefur tilhneigingin verið sú að hafa sjúkling á sjúkrahúsi og í hjartarafsjá í 48 til 72 klukkustundir eftir að meðferð er hafin. Þegar ákvörðun er tekin um hvort byrja eigi með lyf innan eða utan sjúkrahúss þarf meðal annars að taka tillit til eftirfarandi þátta: meðfylgjandi hjartasjúkdóma, sögu um leiðslutruflanir, lengd QT bils, mæligilda á söltum í blóði, hvort sjúklingur er í sínustakti eða með gáttatif þegar byrjað er á lyfinu og hvaða lyf er verið að nota. Þannig skyldi alltaf leggja sjúkling inn á sjúkrahús þegar fyrirhugað er að byrja með hjartsláttartruflanalyf ef hann hefur kransæðasjúkdóm eða skertan samdrátt í vinstri slegli. Einnig skyldi varast að byrja með þau lyf sem geta lengt QT bil utan sjúkrahúss hjá þeim sem hafa QT bil lengra en 420 msek. Varasamt getur verið að byrja með lyf utan sjúkrahúss ef sjúklingur er í gáttatifi vegna þess að, ef sínustaktur kemst á, getur komið í ljós vanstarfsemi á sínushnút og verulegur hægataktur getur fylgt í kjölfarið. Lyf af flokki 1C eru eingöngu notuð hjá þeim sem hafa eðlilegt hjarta. Mismunandi er hversu mikið sjúklingar eru rannsakaðir áður en þeir teljast vera með eðlilegt hjarta. Hjá yngra fólki er líkast til nóg að gera ómskoðun, en hjá fólki sem komið er á þann aldur að geta haft kransæðasjúkdóm er gjarnan einnig framkvæmt áreynslupróf. Hjá völdum sjúklingum er líklega óhætt að byrja með flest lyf utan sjúkrahúss, en þó eru þeir sem leggjast eindregið gegn því að lyf af flokki 1A séu gefin án þess að sjúklingur sé í rafsjá í að minnsta kosti 48 klukkustundir.
Ef ekki tekst að koma sjúklingi í sínustakt verður oftast að beita lyfjameðferð til að stjórna sleglasvörun í gáttatifi. Ýmis lyf koma þá til greina: betablokkar, kalsíumblokkar, dígoxín og jafnvel amíódarón. Oft þarf að nota fleiri en eitt lyf til að ná nægilegum árangri, en í slíkum tilfellum skyldi fara varlega, sérstaklega ef blandað er saman verapamíli og betablokkurum. Aðrar aðferðir til að stjórna sleglasvörun eru meðal annars brennsla á A-V hnút, með eða án ísetningar gangráðs. Rétt er að benda á að ef sjúklingur er í langvinnu gáttatifi er yfirleitt tilgangslaust að halda áfram með hjartsláttartruflanalyf þar sem ávinningur af slíku er lítill, en hætta á því að takttruflun versni og jafnvel geti ný komið upp.
Hlutverk hjartaómunar um
vélinda í meðferð gáttatifs
Þegar segar myndast hjá sjúklingum með gáttatif er algengast að þeir séu staðsettir í eyra vinstri gáttar. Segar í vinstra gáttareyra eru oft illsjáanlegir með ómun um brjóstvegg, en vélindaómun er hins vegar mjög næm til að greina slíkt. Sýnt hefur verið fram á að ef segi í gátt er útilokaður með vélindaómun er hættulítið að rafvenda sjúklingi strax án þriggja vikna blóðþynningar (29). Auk þess að flýta fyrir vendingu þá getur þetta dregið úr blæðingarhættu með því að stytta þann tíma sem sjúklingur þarf að vera á blóðþynningu og dregið úr kostnaði vegna blóðþynningarlyfja og eftirlits. Ef þessari aðferð er beitt er þó nauðsynlegt að blóðþynna sjúklinga í að minnnsta kosti fjórar vikur eftir vendingu vegna þess að dæmi eru um að segarek hafi orðið eftir vendingu þrátt fyrir að enginn blóðsegi hafi sést á vélindaómun fyrir vendingu (30). Gáttatif veldur hjartavöðvasjúkdómi (cardiomyopathy) í gáttum og eftir vendingu tekur það gáttirnar allt að fjórar vikur að ná aftur eðlilegum samdrætti. Þessar aðstæður geta ýtt undir myndun blóðsega ef sjúklingur er ekki á blóðþynningu. Tengsl eru á milli þess hversu lengi gáttatif hefur staðið fyrir vendingu og þess tíma sem það tekur gáttirnar að ná fullri samdráttarhæfni á ný (20).Í gangi er stór samanburðarrannsókn á vendingu með aðstoð vélindaómunar og vendingu með hefðbundinni blóðþynningu (það er í þrjár vikur fyrir og fjórar vikur eftir rafvendingu). Þessi rannsókn kallast ACUTE rannsóknin og hafa niðurstöður forkönnunar (pilot study) verið birtar (31). Sjúklingum var slembiraðað í tvo hópa, annars vegar hóp þar sem gerð var vélindaómun og ef ekki sást blóðsegi var framkvæmd rafvending strax. Því var síðan fylgt eftir með fjögurra vikna blóðþynningu. Ef segi sást á vélindaómun voru sjúklingar settir á blóðþynningu og rafvent síðar. Í hinum hópnum voru sjúklingar blóðþynntir á hefðbundinn hátt. Niðurstöður leiddu í ljós að rafvending, snemma eftir að vélindaómun hafði útilokað blóðsega í gáttum, var bæði örugg og fýsileg aðferð. Kom í ljós að rafvending var gerð að minnsta kosti 4,7 vikum síðar ef notuð var hefðbundin aðferð. Hins vegar er ekki fullljóst á þessu stigi hvaða sjúklingum hentar best rafvending með vélindaómunaraðferðinni. Í fljótu bragði virðist að þessi aðferð henti best þeim sem veruleg einkenni hafa af gáttatifi og geti því tæpast beðið eftir vendingu og jafnframt þeim sem ekki er treyst í langtíma blóðþynningu. Lokaniðurstöður ACUTE rannsóknarinnar, sem enn er í gangi, gætu þó varpað nánara ljósi á hvaða sjúklingahópi henti best þessi aðferð.
Nýjungar í meðferð gáttatifs
Þó meirihluti sjúklinga hrökkvi í sínustakt við rafvendingu um brjóstvegg, gagnast slíkt ekki öllum. Þeim, sem ekki hrökkva í sínustakt, standa nokkrir kostir til boða. Reyna má formeðferð með íbútilíði sem þá er gefið yfir 10 mínútur og rafvending reynd aftur. Í nýlega birtri rannsókn fóru allir í sínustakt, eftir að hafa fengið íbútilíð og rafstuð, sem ekki höfðu svarað rafstuði einu (32). Þá má reyna endurtekið rafstuð með verulegum þrýstingi á spaða til að minnka viðnám (33). Einnig má reyna rafvendingu með rafskautum sem lögð eru til hjartans tímabundið í gegnum eina af stærri bláæðunum. Rafskautin eru síðan tengd við ytri rafstuðsgjafa (34). Nýir rafstuðsgjafar þar sem rafstuðið er tvífasa (biphasic) hafa sýnt betri árangur af rafvendingu um brjóstvegg en hefðbundnar einfasa rafstuðgjafar og gætu orðið til að auka enn frekar frumárangur rafvendingar um brjóstvegg (35). Þessar aðferðir eru valkostur fyrir þá sem þola gáttatif illa en ekki hafa svarað hefðbundinni ytri rafvendingu.Undanfarin ár hefur verið í þróun ígrætt gáttarafstuðstæki (atrial defibrillator) sem er sérhannað til meðferðar á gáttatifi. Þessi tækni er hliðstæð ígræddum hjartarafstuðstækjum sem nú eru gjarnan notuð við takttruflunum frá sleglum. Leiðslur til að gefa rafstuð eru settar niður í hægri gátt og í kransstokk (sinus coronarius) auk þess sem sett er gangráðsleiðsla í hægri slegil. Sjálfu boxinu er síðan komið fyrir undir húð á brjósti, líkt og með gangráð. Þessi tæki geta gefið rafstuð sem er allt að 6 Joule. Þau hafa reynst mjög árangursrík í að venda gáttatifi yfir í sínustakt og í nýlegri rannsókn var árangurinn 96% (36). Þá voru engin tilfelli þar sem sleglatakttruflanir framkölluðust við rafstuðið. Slíkt ígrætt hjartarafstuðstæki gæti verið gagnlegt sjúklingum sem endurtekið fá gáttatif sem veldur þeim verulegum einkennum. Þó er ekki fullljóst hvaða hlutverki þessi tæki munu gegna í meðferð gáttatifs í framtíðinni. Ekki er þó ólíklegt að þau muni þróast á þann veg að framleidd verði ígrædd hjartarafstuðstæki sem geti rafvent bæði gátta- og sleglatakttruflunum.
Ábendingar fyrir gangráðsmeðferð hjá sjúklingum með gáttatif hafa í gegnum tíðina verið tachy/brady syndrome, gáttatif þar sem sleglasvörun er mjög hæg og eftir brennslu á A-V hnút. Hins vegar hefur einnig komið í ljós að sjúklingum sem fá gangráð vegna sjúks sínushnúts er hættara við gáttatifi ef að eingöngu er settur inn gangráður með sleglaleiðslu, heldur en ef settur er inn gangráður þar sem hægri gátt er örvuð (37). Þannig virðist gangráður sem örvar gáttir mögulega geta komið í veg fyrir gáttatif síðar. Gæti þetta meðal annars stafað af því að gangráður getur dregið úr leiðslutöf í gáttum og einnig minnkað líkur á aukaslögum frá gáttum sem geta átt þátt í að framkalla gáttatif. Nýlegar tilraunir með sérstakri gangráðstækni þar sem settar eru inn tvær gáttaleiðslur hafa einnig gefist vel til að viðhalda sínustakti hjá sjúklingum með gáttatif sem ekki hafa svarað lyfjameðferð (38). Þessar rannsóknir hafa fram til þessa hins vegar aðeins náð til fárra sjúklinga, en niðurstöðurnar hafa vakið athygli. Einnig hafa verið gerðar tilraunir með sértækar gangráðsstillingar til að draga úr aukaslögum frá gáttum sem stundum eru forverar gáttatifs.
Brennslumeðferð (radiofrequency ablation) er nú beitt í vaxandi mæli við gáttatifi. Ýmsum afbrigðum hennar er beitt í þessum tilgangi en í megindráttum er um að ræða fjórar mismunandi leiðir; brennslu á A-V hnút, brennslu á aukaleiðnibraut, brennslu við lungnabláæð og loks svonefnd maze aðgerð, með brennslu gegnum legg (catheter maze).
Brennslu á A-V hnút er beitt til þess að ná betri stjórn á sleglahraða hjá sjúklingum með gáttatif. Í flestum slíkum tilfellum þarf að setja inn gangráð með sleglaleiðslu. Þó er mögulegt að gera hlutabrennslu á A-V hnút þannig að leiðni um hann er torvelduð, en reynt er að forðast algert rof á A-V hnútnum. Þessi aðferð hefur gefist vel á nokkrum sjúkrahúsum en ekki náð verulegri útbreiðslu. Gáttatif kemur stundum í kjölfar annarra ofansleglatakttruflana (supraventricular tachycardiu) sem stafa af aukaleiðslubandi í hjarta. Slíkt er algengara hjá yngra fólki og stundum orsök gáttatifs sem kemur í köstum. Í slíkum tilfellum getur brennsla á aukaleiðslubandinu hindrað frekari köst af gáttatifi.
Enn einn mögulegur orsakaþáttur gáttatifs í köstum er aukaslög sem eiga upptök sín á mótum vinstri gáttar og lungnabláæða. Hefur þetta fundist sér í lagi hjá yngri sjúklingum sem hafa ekki hjartasjúkdóm. Nýleg rannsókn sýndi fram á það að brennsla á því svæði þar sem þessi aukaslög áttu uppruna sinn var mjög árangursrík til að koma í veg fyrir frekari tilvik gáttatifs (39). Þannig reyndust 28 af 38 sjúklingum með tíð köst af gáttatifi, sem fengu slíka meðferð, vera lausir við hjartsláttaróregluna á þeim tæpu 12 mánuðum sem þeim var fylgt eftir. Óvíst er hins vegar með langtímaárangur. Ekki er vitað hvort þessi aðferð gagnist sjúklingum með langvinnt gáttatif eða þeim sem hafa gáttatif samfara hjartasjúkdómi. Talsvert vandasamt getur verið að brenna í vinstri gátt. Uppruni þessara aukaslaga er gjarnan í gáttarvef sem getur stundum teygt sig langt inn í lungnabláæðar og í slíkum tilfellum er hætta á að valda lokun á bláæðinni með brennslunni. Erfitt getur verið að finna bláæðarnar og getur slík brennsluaðgerð tekið langan tíma. Hætta er einnig á rofi í vinstri gátt en veggir hennar eru fremur þunnir. Í þróun eru brennsluleggir sem miða að því að gera brennsluna auðveldari og áhættuminni og þannig gæti notkun þessarar aðferðar við meðferð gáttatifs aukist á næstu árum.
Svokölluð maze skurðaðgerð, sem var þróuð af Cox og samverkamönnum hans hefur stundum verið notuð hjá sjúklingum með gáttatif (40). Í þeirri aðgerð eru bæði hægri og vinstri gáttareyru skorin af og lungnabláæðar til vinstri gáttar eru raflífeðlisfræðilega einangraðar. Síðan eru gerðir skurðir í báðar gáttir sem miða að því að viðhalda leiðni frá sínushnút niður í A-V hnút, en draga úr möguleikum gáttanna til að valda nauðsynlegum fjölda hringsóls (multiple reentrant waveforms) sem er nauðsynlegt til að gáttatif viðhaldist. Þessi aðgerð þykir talsvert inngrip, en hefur gefið góða raun hjá völdum hópi sjúklinga þar sem hefðbundin meðferð hefur ekki dugað.
Á allra síðustu árum hafa þróast aðferðir þar sem reynt hefur verið að búa til hliðstæðar línur og gerðar eru í maze skurðaðgerð með brennsluaðferðum (40). Í slíkum tilfellum er reynt að brenna bæði í hægri og vinstri gátt. Þessi meðferð er enn á tilraunastigi, en í fyrstu reyndist talsvert erfitt með hefðbundnum brennsluleggjum að brenna línur í gáttunum. Leiddi það til mjög langra aðgerða þar sem bæði sjúklingurinn og læknirinn urðu fyrir talsverðri geislun og einnig var hætta á að segi myndaðist í vinstri gátt við endurteknar brennslur sem gat valdið heilablóðfalli (40). Þróun á nýjum brennsluleggjum hefur hins vegar aukið bjartsýni á að slík meðferð gæti orðið valkostur í náinni framtíð hjá sjúklingum með gáttatif.
Samantekt
Því er spáð að nýgengi gáttatifs muni aukast á næstu áratugum. Á sama tíma eru meðferðarmöguleikar gáttatifs að verða fjölbreyttari. Ný lyf við hjartsláttartruflunum sem miða að því að viðahalda sínustakti eru í sjónmáli og blóðþynningarmeðferð getur dregið verulega úr áhættu á heilablóðfalli. Nýjar aðferðir við rafvendingu, lyfjavendingu og brennslumeðferð á gáttatifi eru í stöðugri þróun og eiga að öllum líkindum eftir að verða fýsilegur kostur í meðferð gáttatifs á næstu árum. Viðhorf til gáttatifs hefur einnig breyst á þann veg að farið er á líta meira á gáttatif sem langvinnan sjúkdóm. Meðferðin beinist í ríkara mæli að því að halda sjúkdómnum og einkennum niðri fremur en að lækna hann.Heimildir
1. Cairns JA, Connolly SJ. Nonrheumatic atrial fibrillation: risk of stroke and role of antithrombotic therapy. Circulation 1991; 84: 469-81.2. Go AS, Hylek EM, Philips KA, Henault LE, Selby JV, Singer DE. Prevalence of atrial fibrillation, national implications for management and stroke prevention: the anticoagulation and risk factors for atrial fibrillation (ATRIA) study [abstract]. Circulation 1999; 100: I-397.
3. Arnar DO, Danielsen R. Factors predicting maintenance of sinus rhythm after direct current cardioversion of atrial fibrillation and flutter. Cardiology 1996; 87: 181-8.
4. Murphy MT, Grimm RA, Lauer MS, Klein AL, Lin SS, Chung MK, et al. Obesity: a powerful correlate of lone atrial fibrillation independent of blood pressure [abstract]. Circulation 1999; 100, I-824.
5. Brugada R, Tapscott T, Czermuszewics GZ, Manan AJ, Iglesias A, Mont L, et al. Identification of a genetic locus for familial atrial fibrillation. N Engl J Med 1997; 336: 905-11.
6. Yamashita T, Murukawa Y, Sezaki K, Inoue M, Hayami M, Shuzui Y, et al. Circadian variation of paroxysmal atrial fibrillation. Circulation 1997; 96: 1537-41.
7. Coumel P. Autonomic influences in atrial fibrillation. J Cardiovasc Electrophysiol 1996; 7: 999-1007.
8. Martins JB, Arnar DO. Assessment of the role of the autonomic nervous system in tachycardias. In: Zipes DP, Jalife J, eds. Cardiac Electrophysiology: from cell to bedside. Philadelphia: WB Saunders; 1999: 828-34.
9. Clark DM, Plumb VJ, Epstein AE, Kay GN. Hemodynamic effects of an irregular sequence of ventricular cycle lengths during atrial fibrillation. J Am Coll Cardiol 1997; 30: 1039-45.
10. Packer DL, Bardy GH, Worley SJ, Samitu MS, Cobb FR, Coleman RE, et al. Tachycardia induced cardiomyopathy: a reversible form of left ventricular dysfunction. Am J Cardiol 1986; 57: 563-70.
11. Wolf PA, Dauber TR, Thomas HE Jr, Kannell WB. Epidemiologic assesment of chronic atrial fibrillation. The Framingham Study. Neurology 1978; 28: 973-7.
12. Arnar DO, Danielsen R. Gáttatif og blóðþynning. Læknablaðið 1992; 78: 419-22.
13. Atrial fibrillation investigators group. Risk factors for stroke and efficacy of antithrombotic therapy in atrial fibrillation: analysis of pooled data from five randomized controlled trials. Arch Intern Med 1992; 116: 6-12.
14. Hart RG, Benavente O, McBride R, Pearce LA. Antithrombotic therapy to prevent stroke in patients with atrial fibrillation: A meta-analysis. Ann Intern Med 1999; 131: 492-501.
15. Arnar DO, Danielsen R. Frumárangur af rafvendingu vegna hjartsláttartruflana frá gáttum. Læknablaðið 1992; 78: 87-93.
16. Kerber RE. Transthoracic cardioversion of atrial fibrillation and flutter: standar techniques and new advances. Am J Cardiol 1996; 78/Suppl 8A: 22-6.
17. Bjerkelund CJ, Orning OM. The efficacy of anticoagulation in preventing embolism related to DC electrical cardioversion of atrial fibrillation. Am J Cardiol 1969; 23: 208-15.
18. Arnold AZ, Mick MJ, Mazurek MP, Loop FD, Trohman RG. Role of prophylactic anticoagulation for direct current cardioversion in patients with atrial fibrillation or atrial flutter. J Am Coll Cardiol 1992; 19: 851-5.
19. Laupacis A, Alberts G, Dalen JE, Dunn MI, Jacobson AK, Singer DE. Antithrombotic therapy in atrial fibrillation. Chest 1998; 114/Suppl: 579S-589S.
20. Collins LJ, Silverman DI, Douglas PS, Manning WJ. Cardioversion of nonrheumatic atrial fibrillation: reduced thromboembolic complications with 4 weeks of precardioversion anticoagulation are related to atrial thrombus resolution. Circulation 1995; 92: 156-9.
21. Manning WJ, Silverman DI, Katz SA, Riley MF, Come PC, Doherty RM, et al. Impaired left atrial mechanical function after cardioversion: relation to duration of atrial fibrillation. J Am Coll Cardiol 1994; 23: 1535-40.
22. Arnar DO, Danielsen R. Short term heparin versus coumadin anticoagulation prior to electroconversion of atrial arrhythmias [abstract]. XIV Nordic Congress of Cardiology, Aarhus, June 2-4, 1993.
23. Weigner MJ, Caulfield TA, Danias PG, Silverman DI, Manning WJ. Risk for clinical thromboembolism associated with conversion to sinus rhythm in patients with atrial fibrillation lasting less than 48 hours. Ann Intern Med 1997; 126: 615-20.
24. Roy D, Talajic M, Dorian P, Connolly S, Eisenberg MJ, Green M, et al. Amiodarone to prevent recurrence of atrial fibrillation. N Engl J Med 2000; 342: 913-20.
25. Stambler BS, Wood MA, Ellenbogen KA, Perry KT, Wakefield LK, VanderLugt JT, et al. Efficacy and safety of repeated intravenous doses of ibutilide for conversion of atrial flutter or fibrillation. Circulation 1996; 94: 1613-21.
26. Torp-Pedersen C, Möller M, Bloch-Thomsen PE, Kober L, Sandoe E, Egstrup K, et al. Dofetilide in patients with congestive heart failure and left ventricular dysfunction. N Engl J Med 1999; 341: 857-65.
27. Prystowsky EW. Proarrhythmia during drug tratment of supraventricular taschycardia: paradoxical risk of sinus rhythm for sudden death. Am J Cardiol 1996; 78: 35-41.
28. Velebit V, Podrid P, Lown B, Cohen BH, Graboys TB. Aggrevation and provocation of ventricular arrhythmias by antiarrhythmic drugs. Circulation 1982; 65: 886-94.
29. Manning WJ, Silverman DI, Gordon SPF, Krumholz HM, Douglas P. Cardioversion from atrial fibrillation without prolonged anticoagulation with use of transesophageal echocardiography to exclude the presence of atrial thrombi. N Engl J Med 1993; 328: 750-5.
30. Black IW, Fatken D, Sagar KB, Khandheria BK, Leung DY, Galloway JM, et al. Exclusion of atrial thrombus by transesophageal echocardiography does not preclude embolism after cardioversion of atrial fibrillation. Circulation 1994; 89: 2509-13.
31. Klein AL, Grimm RA, Black IW , Leung DY, Chung MK, Vaughn S, et al. Cardioversion guided by transesophageal echocardiography. The ACUTE pilot study. Ann Intern Med 1997; 126: 200-9.
32. Oral H, Souza JJ, Michaud GF, Knight B, Goyal R, Strickberger A, et al. Facilitating transthoracic cardioversion of atrial fibrillation with ibutilide pretreatment. N Engl J Med 1999; 340: 1849-54.
33. De Bruyn VH, Park TH, Botteron GW, Faddis MN, Baker BM, Guerrero PA, et al. Pressure assisted cardioversion for atrial fibrillation [abstract]. Circulation 1998; 98: I-102.
34. Levy S, Ricard P, Guenuoun M, Yapo F, Trigano J, Mansouri C, et al. Low energy cardioversion of spontaneous atrial fibrillation. Immediate and long term results. Circulation 1997; 96: 253-9.
35. Mittal S, Ayati S, Stein KM, Markowitz SM, Slotwiner SJ, Scheiner MA, et al. Effect of transthoracic impedance on cardioversion efficacy: Rectilinear biphasic versus sine wave monophasic shocks for transthoracic cardioversion of atrial fibrillation [abstract]. Circulation 1999, 100: I-721.
36. Wellens HJJ, Lau C-P, Luederitz B, Akhtar M, Waldo A, Camm AJ, et al. Atrioverter: an implantable device for the treatment of atrial fibrillation. Circulation 1998; 98: 1651-6.
37. Sutton R, Kenny RA. The natural history of sick sinus syndrome. PACE 1986; 9: 1110-4.
38. Saksena S, Prakash A, Hill M, Krol RB, Munsit AN, Matthew PP. Prevention of recurrent atrial fibrillation with chronic dual site atrial pacing. J Am Coll Cardiol 1996; 28: 687-94.
39. Haissaguerre M, Jais P, Shah DC, Takahashi A, Hocini M, Quiniou G, et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med 1998; 339: 659-66.
40. Cox JC, Boineau JP, Schussler RB, Kater KM, Lappas DG. Five year experience with the maze procedure for atrial fibrillation. Ann Thor Surg 1993; 56: 814-23.
41. Haissaguerre M, Jais P Shah DC, Clementy J. Catheter ablation for atrial fibrillation: clinical electrophysiolgy of linear lesions. In: Zipes DP, Jalife J, eds. Cardiac Electrophysiology: from cell to bedside. Philadelphia: WB Saunders; 1999: 994-1008.