01. tbl. 94. árg. 2008
Fræðigrein
Veirulyf gegn inflúensu og leiðbeiningar um notkun þeirra í heimsfaraldri
The use of anti-viral agents in pandemic influenza, Icelandic guidelines
Ágrip
Vinna við gerð viðbragðsáætlana vegna heimsfaraldurs inflúensu stendur nú sem hæst hér á landi sem í öðrum löndum. Lyfjameðferð gegn inflúensu mun gegna mikilvægu hlutverki í þessum áætlunum og hefur það markmið að draga úr alvarlegum afleiðingum heimsfaraldurs og hefta útbreiðslu hans.
Í þessari yfirlitsgrein er fjallað um þau veirulyf sem líkleg eru til að skila árangri við meðferð á alvarlegri inflúensu og leiðbeiningar gefnar um notkun þeirra. Mikilvægt er að sátt verði um leiðbeiningar um notkun veirulyfjanna svo hægt verði að tryggja bestu nýtingu þeirra birgða sem til verða í landinu.
Inngangur
Á 20. öld hafa þrír heimsfaraldrar inflúensu geisað í heiminum og var spánska veikin 1918 þeirra skæðust en talið er að í löndum þar sem hún gekk hafi um helmingur íbúa sýkst og um 50 milljónir látist (1). Ef næsti heimsfaraldur inflúensu líkist spönsku veikinni má ætla að hér á landi geti um 150.000 manns sýkst, um 100.000 veikst alvarlega og allt að 6000 látist ef ekkert verður að gert (2-4). Svo skæður faraldur myndi valda gríðarlegu álagi á heilbrigðisþjónustuna og miklum þjóðfélagslegum skaða.
Því er brýnt að skipuleggja og leggja mat á aðgerðir sem heft geta útbreiðslu inflúensunnar.
Veirulyf munu gegna mjög þýðingarmiklu hlutverki í heimsfaraldri bæði við meðhöndlun veikra einstaklinga og til að fyrirbyggja sýkingu. Hér er gerð grein fyrir þeim veirulyfjum sem mestar vonir eru bundnar við þegar heimsfaraldur ríður yfir og leiðbeiningar gefnar um notkun þeirra. Þar eð engin reynsla er af notkun lyfjanna í heimsfaraldri þá byggja leiðbeiningarnar að mestu á rannsóknum og reynslu af notkun þeirra í árlegri inflúensu og þeirri reynslu sem fengist hefur við notkun þeirra hjá sjúklingum sem sýkst hafa af H5N1-stofni inflúensuveirunnar.
Veirulyf gegn inflúensuveirum
Um þessar mundir eru þrír flokkar veirulyfja á markaði sem eru virk gegn inflúensuveirum en það eru núkleósíð/núkleótíð lyf en í þeim flokki er ríbavírín, M2-hemlar, en í þeim flokki eru amantadín og rímantadín og loks neuramínídasa (NA) hemlar. Frekari rannsóknir þurfa að fara fram á núkleósíð/núkleótíð lyfjum hjá mönnum áður en hægt verður að mæla með almennri notkun þeirra við inflúensu (5, 6). M2-hemlar munu ekki gegna þýðingarmiklu hlutverki í heimsfaraldri inflúensu vegna hárrar tíðni á myndun ónæmis (7-10) og algengra aukaverkana (7, 11). Í þessari grein verður því einungis gerð grein fyrir NA-hemlum og notkun þeirra.
NA (neuramínídasa) hemlar
Tvö lyf í þessum flokki, oseltamivír (Tamiflu®) og zanamivír (Relenza®) hafa verið á markaði frá því um 2000 en þau koma í veg fyrir að inflúensuveiran losni frá sýktum frumum og eru virk gegn A og B stofnum veirunnar (12, 13).
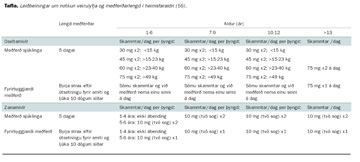
Oseltamivír er til bæði í töflu- og mixtúruformi og er ætlað einstaklingum eins árs og eldri. Meðferðar- og fyrirbyggjandi skammta má sjá í meðfylgjandi töflu.
Zanamivír er einungis til sem innöndunarduft og er ætlað þeim sem eru fimm ára og eldri. Engar rannsóknir hafa borið saman virkni þessara lyfja en lyfleysurannsóknir benda til að hún sé mjög svipuð bæði hvað varðar meðferð sýktra einstaklinga og fyrirbyggjandi notkun (12).
Árangur meðferðar sýktra einstaklinga með NA-hemlum í árlegri inflúensu
Oseltamivír hjá þeim sem eru eldri en eins árs og zanamivír hjá eldri en fimm ára eru virk í meðferð við inflúensu (14). Þau stytta lengd veikinda um einn til tvo sólarhringa og draga verulega úr einkennum (15-18). Virkni lyfjanna til að koma í veg fyrir alvarlegar afleiðingar sýkingarinnar er óljósari (14, 19, 20) en þó virðist oseltamivír koma í veg fyrir alvarlega lungnabólgu og dregur úr sjúkrahússinnlögnum (16). Bestur árangur næst ef meðferð hefst innan 12 klukkustunda frá upphafi einkenna en árangur er vafasamur ef meðferðin hefst >48 klukkustunda eftir að einkenni koma fram (21-23). Meðferð sem hefst snemma dregur verulega úr veirumagni í öndunarvegi sjúklinga og minnkar þannig líkur á smiti en styttir hins vegar ekki þann tíma sem sjúklingur er smitandi (15, 24, 25). Ýmislegt bendir til að lyfin séu einnig virk hjá ónæmisbældum einstaklingum og dragi úr alvöru sýkingarinnar (26, 27).
Árangur fyrirbyggjandi meðferðar með NA-hemlum í árlegri inflúensu.
Oseltamivír og zanamivír koma í veg fyrir staðfesta inflúensu hjá 70-90% heilbrigðra (12, 28, 29) en fyrirbyggjandi virkni hjá ónæmisbældum einstaklingum hefur ekki verið fyllilega rannsökuð (30).
Í heimsfaraldri verður lögð áhersla á að gefa fjölskyldumeðlimum veikra einstaklinga fyrirbyggjandi meðferð. Fjórar rannsóknir hafa verið birtar um árangur fyrirbyggjandi notkunar oseltamivírs og zanamivírs á heimilum þar sem inflúensa hafði greinst (31-35). Helstu niðurstöður þeirra eru:
- Virkni (efficacy) 10 daga fyrirbyggjandi meðferðar með oseltamivíri var 81-91% ef litið er á virkni til að fyrirbyggja veikindi en 48-63% til að koma í veg fyrir sýkingu með eða án einkenna. Þetta þýðir í raun að hluti þeirra sem fékk fyrirbyggjandi meðferð í 10 daga fékk einkennalausa sýkingu með fjórfaldri hækkun mótefna gegn inflúensuveirunni sem væntanlega verndaði gegn frekari sýkingu (33-35).
- Virkni 10 daga fyrirbyggjandi meðferðar með zanamivíri var 75% þegar horft var á virkni til að hindra veikindi en 60% til að koma í veg fyrir sýkingu (31, 32, 35).
- Líkur á smiti minnkuðu um 19% þegar sjúklingar voru meðhöndlaðir með zanamivíri en 80% við meðhöndlun með oseltamivíri (35). Þessar niðurstöður benda til að sjúklingar með inflúensu smiti síður ef þeir eru meðhöndlaðir með oseltamivíri heldur en zanamivíri.
Árangur meðferðar með NA-hemlum gegn H5N1-stofni inflúensuveiru
Bæði oseltamivír og zanamivír hafa sýnt góða virkni í tilraunaglösum gegn öllum stofnum H5N1 (36, 37) en oseltamivír ónæmum stofnum hefur þó verið lýst hjá nokkrum sjúklingum á oseltamivír meðferð (38).
Engar staðlaðar rannsóknir hafa verið gerðar á virkni NA hemla hjá einstaklingum sem sýkst hafa af H5N1-stofni inflúensuveirunnar né heldur árangri lyfjanna til að koma í veg fyrir smit. Meðferð með oseltamivíri hefur verið lýst hjá 25 veikum einstaklingum af völdum H5N1 (39). Af þeim létust 19 og virtist árangur meðferðarinnar því vera lítill. Hins vegar hófst meðferðin seint og ekki fyrr en sjúklingarnir voru orðnir alvarlega veikir. Virkni oseltamivírs verður því tæpast metin af þessum upplýsingum.
Lítil reynsla er af notkun zanamivírs við sýkingu af völdum H5N1. Sýnt hefur verið fram á að lyfið er virkt gegn öllum stofnum veirunnar inni á rannsóknarstofu og einnig þeim stofnum sem eru með minnkað næmi fyrir oseltamivíri (38).
Ónæmi árlegrar inflúensu fyrir NA-hemlum
Ónæmi fyrir oseltamivíri hefur verið lýst hjá um 1% fullorðinna og 5% barna sem meðhöndluð voru með oseltamivíri í árlegri inflúensu (24, 40). Hærra ónæmi fyrir oseltamivíri hefur verið lýst í Japan og í einni rannsókn greindist ónæmi hjá 16-18% barna (41, 42). Þessar niðurstöður benda til að ónæmi sjáist oftar hjá börnum sem meðhöndluð eru með oseltamivíri heldur en fullorðnum.
Dýratilraunir benda til að oseltamivír-ónæmar inflúensuveirur smitist síður milli einstaklinga og valdi vægari einkennum en næmar veirur (43, 44). Þetta vekur vonir um að þótt ónæmi fyrir oseltamivíri yrði útbreitt í heimsfaraldri þá myndi það ekki hafa alvarlegar afleiðingar í för með sér. Allar oseltamivír ónæmar veirur hafa reynst næmar fyrir zanamivíri (38, 45, 46).
Ónæmi fyrir zanamivíri hefur ekki verið lýst hjá einstaklingum með inflúensu en hefur verið lýst hjá ónæmisbældum einstaklingi með inflúensu sem hafði verið meðhöndlaður í 10 daga (46). Því er hugsanlegt að ónæmi sé líklegra að myndast fyrir oseltamivíri en zanamivíri. Hins vegar sýna niðurstöðurnar að ónæmi fyrir NA-hemlum getur myndast við mikla notkun lyfjanna. Þar sem allar oseltamivír-ónæmar veirur eru næmar fyrir zanamivíri er ljóst að í heimsfaraldri er nauðsynlegt að birgðir af báðum lyfjum þurfa að vera tiltækar.
Ónæmi H5N1-inflúensuveiru fyrir NA-hemlum
Ónæmi H5N1-inflúensuveiru fyrir oseltamivíri hefur verið lýst hjá nokkrum sjúklingum í Víetnam sem höfðu verið meðhöndlaðir með lyfinu (38). Sömu veirustofnar voru hins vegar næmir fyrir zanamivíri (38). Lítil reynsla er af notkun zanamivírs hjá sjúklingum sem sýktir eru af H5N1 og ónæmi ekki verið lýst.
Aukaverkanir NA-hemla
Aukaverkanir oseltamivírs eru sjaldgæfar og ekki alvarlegar. Algengustu aukaverkanirnar eru ógleði og uppköst sem geta sést hjá allt að 10% einstaklinga (15, 47, 48) en til að draga úr þeim hefur verið mælt með að gefa lyfið ekki á fastandi maga (21). Í seinni tíð hefur nokkur umræða farið fram um hvort notkun oseltamivírs geti tengst ruglástandi hjá börnum. Engin óyggjandi orsakatengsl virðast vera á milli oseltamivír-notkunar og þessara einkenna (49, 50). Heilbrigðisyfirvöld víða um heim hafa hvatt heilbrigðisstarfsmenn til að fylgjast vel með og tilkynna möguleg tengsl lyfsins við ofangreind einkenni.
Aukaverkanir af völdum zanamivírs eru sjaldséðar en þó hefur slæmum astmaeinkennum verið lýst hjá einstaklingum með undirliggjandi lungnasjúkdóma (51, 52).
Leiðbeiningar um notkun veirulyfja við sýkingu af völdum H5N1-stofns inflúensuveiru
Inflúensa af stofni H5N1 hefur greinst í fuglum, einkum í Suðaustur-Asíu frá 1997. Frá 2003 hafa sýkingarnar verið mjög skæðar í hænsnfuglum og valdið miklum búsifjum, einkum í Suðaustur-Asíu, og hafa á seinni árum borist til annarra heimsálfa. Þó H5N1-stofn veirunnar sé bráðsmitandi og alvarlegur í fuglum er sjaldgæft að hann berist frá fuglum í menn og smit milli manna hefur einungis verið staðfest í örfáum tilfellum (53). Í júní 2007 höfðu greinst rúmlega 300 einstaklingar í heiminum með sýkingu af völdum H5N1. Flestir þeirra voru búsettir í Suðaustur-Asíu, voru yngri en 20 ára og yfir 50% höfðu látist (39, 54).
Sérfræðihópur á vegum Alþjóðaheilbrigðismálastofnunarinnar hefur gefið út leiðbeiningar um notkun veirulyfja til að meðhöndla og fyrirbyggja sýkingar af völdum H5N1 (55) og einnig hefur samstarfsnefnd sóttvarnalæknis, Landbúnaðarstofnunar, Umhverfisstofnunar og Vinnueftirlitsins gefið út leiðbeiningar til starfsmanna alifuglabúa um varnaraðgerðir gegn fuglaflensu (56, 57).
Leiðbeiningar sérfræðihóps Alþjóðaheilbrigðis-málastofnunarinnar eru eftirfarandi (55, 57):
- Meðferð hjá sjúklingum með fuglainflúensu á að hefja eins fljótt og auðið er eftir að einkenni koma í ljós og helst innan 48 klukkustunda.
- 0seltamivír gefið í hefðbundnum skömmtum tvisvar á dag í að minnsta kosti fimm daga (sjá töflu), eða
- Zanamivír gefið í hefðbundnum skömmtum tvisvar á dag í að minnsta kosti fimm daga (sjá töflu)
- Fyrirbyggjandi meðferð. Leiðbeiningar um fyrirbyggjandi meðferð eru hins vegar óljósar. Taka verður tillit til þess hversu náið samneyti hins heilbrigða einstaklings var við hinn sýkta (mann eða dýr) og einnig hversu góðar varnaraðgerðir voru viðhafðar þegar samneytið átti sér stað.
Mælt er með fyrirbyggjandi meðferð hjá einstaklingum sem haft hafa náið samneyti við sýktan einstakling/dýr eða unnið með H5N1-inflúensuveiru á rannsóknarstofu þar sem hlífðarbúnaður var ekki notaður.
Með nánu samneyti er átt við:
a. Tengsl við menn: Náin tengsl (innan eins metra) við einstakling sem er með mögulega eða staðfesta sýkingu af völdum H5N1 (58, 59).
b. Tengsl við hænsni eða villta fugla: Vinna við slátrun eða förgun sýktra fugla eða handleikið sýktan fugl án hlífðarbúnaðar.
Fyrirbyggjandi meðferð skal hefja eins fljótt og auðið er eftir að samneytið átti sér stað. Varðandi nánari leiðbeiningar er vísað í greinargerð sérfræðihópsins (55, 57) og leiðbeiningar sóttvarnalæknis, Landbúnaðarstofnunar, Umhverfisstofnunar og Vinnueftirlitsins (56).
Viðbragðsáætlanir vegna heimsfaraldurs inflúensu
Í áætlunum flestra þjóða vegna heimsfaraldurs inflúensu er gert ráð fyrir umfangi faraldurs sem svipar til spönsku veikinnar 1918. Í þeim faraldri sýktust um 50% allra einstaklinga og 2,5-5% hinna sýktu létust (2).
Undir forystu sóttvarnalæknis og ríkislögreglustjóra hefur um nokkurt skeið verið unnið að gerð viðbragðsáætlana á Íslandi sem mikilvægt er að hrinda í framkvæmd í byrjun faraldurs. Hluti þeirrar vinnu beinist að því að tryggja nægar birgðir veirulyfja þegar heimsfaraldur ríður yfir því þau munu gegna mjög þýðingarmiklu hlutverki við að draga úr smiti og í meðferð veikra einstaklinga.
Viðbragðsáætlanir vegna heimsfaraldurs inflúensu hafa fjögur meginmarkmið:
- Draga úr smiti og halda í lágmarki fjölda þeirra einstaklinga sem sýkjast?
- Hægja á faraldri þannig að sem fæstir einstaklingar séu veikir á hverjum tíma. Þannig minnkar álag á heilbrigðisþjónustuna og alla innviði samfélagsins, og tími vinnst til að koma bóluefni á markað gegn hinum nýja stofni inflúensuveirunnar.
- Lækna og líkna sjúkum
- Viðhalda innviðum samfélagsins
Í byrjun árs 2007 hafði hið opinbera keypt um 100.000 meðferðarskammta (meðferð fyrir 100.000 einstaklinga í fimm daga) af oseltamivíri og zanamivíri en stefnt er að því að auka þær birgðir í 150.000 skammta. Sóttvarnalæknir ber ábyrgð á þessum birgðum fyrir hönd hins opinbera, stjórnar dreifingu þeirra og gefur út notkunarleiðbeiningar.
Líklegt má telja að ýmis fyrirtæki og einstaklingar muni safna að sér birgðum veirulyfja þegar heimsfaraldur verður í aðsigi þó ekki sé mælt með slíku. Mikilvægt er að allar stærri birgðir hér á landi verði opinberlega skráðar, þeim ávísað af læknum samkvæmt leiðbeiningum sem hér eru birtar og notkun þeirra skráð. Að öðrum kosti verða lyfin notuð ómarkvisst, líklegt að skortur komi upp og ónæmi aukist.
Ferguson og félagar hafa gert stærðfræðilíkan um áætlaðan árangur oseltamivírs og zanamivírs í heimsfaraldri inflúensu í Bretlandi og Bandaríkjunum (60, 61). Þar er gert ráð fyrir að um helmingur íbúa sýkist, um 30% þurfi meðferð vegna veikinda og að fyrirbyggjandi meðferð verði gefin fjölskyldumeðlimum hinna sýktu í 10 daga. Niðurstöður benda til að slík notkun geti dregið úr tíðni sýkinga um 50% en þó því aðeins að meðferð hjá sýktum einstaklingum hefjist innan sólarhrings frá byrjun veikinda og fyrirbyggjandi meðferð hefjist innan sólarhrings frá upphafi samneytis við veikan einstakling. Við raunverulegar aðstæður verður einnig gripið til margvíslegra annarra samfélagslegra aðgerða sem miða að því að hefta útbreiðslu faraldursins og er vonast til að það muni í heild sinni skila umtalsverðum árangri (60).
Á Íslandi er áætlað að dreifing og notkun oseltamivírs og zanamivírs verði eftirfarandi:
- Lyfjunum verður dreift til sóttvarnalækna umdæma og svæða, og til apóteka Landspítala og Sjúkrahússins á Akureyri seint á hættustigi eða snemma á neyðarstigi samkvæmt ákvörðun sóttvarnalæknis.
Samkvæmt reglugerð nr. 834/2007 er Íslandi skipt upp í átta sóttvarnaumdæmi. Í hverju sóttvarnaumdæmi er einn yfirlæknir heilsugæslustöðvar skipaður sóttvarnalæknir umdæmisins af heilbrigðis- og tryggingamálaráðherra og er hann ábyrgur fyrir sóttvörnum í sínu umdæmi undir stjórn sóttvarnalæknis. Tilnefna má fleiri sóttvarnalækna í hverju umdæmi og nefnast þeir sóttvarnalæknar svæða og starfa undir stjórn sóttvarnalæknis umdæmisins.
- Sóttvarnalæknar umdæma og svæða tryggja örugga geymslu lyfjanna og sjá um dreifingu þeirra til heilsugæslustöðva í umdæminu. Þeir sjá um að koma leiðbeiningum um notkun til lækna og annars heilbrigðisstarfsfólks.
- Heilsugæslulæknar sjá um að koma lyfjum til sjúklinga, skrá notkun þeirra og að notkun þeirra verði samkvæmt leiðbeiningum sóttvarnalæknis.
- Á Landspítala bera smitsjúkdómalæknar ábyrgð á notkun lyfjanna.
Leiðbeiningar sóttvarnalæknis um notkun veirulyfja í heimsfaraldri
Rétt er að árétta að einungis læknar geta ávísað veirulyfjum til sjúklinga hvort sem þau eru gefin veikum einstaklingum eða í fyrirbyggjandi skyni.
1. Notkun hjá veikum einstaklingum.
Mikilvægt er að meðferð veikra einstaklinga með veirulyfjum hefjist eins fljótt og hægt er eftir að veikindi koma í ljós því þá er mesta von um árangur. Stefna ber að því að meðferð hefjist á fyrsta sólarhring veikinda en ólíklegt er að hún skili árangri ef hún hefst >48 klukkustundum eftir að veikindi hófust og því vafasamt að hefja meðferð í slíkum tilfellum. Meðferðarlengd mun í flestum tilfellum verða að minnsta kosti fimm dagar.
- Oseltamivír er skammtað samkvæmt meðfylgjandi töflu.
- Zanamivír er gefið eldri en fimm ára eða þeim sem geta sogað lyfið að sér samkvæmt meðfylgjandi töflu.
Mælt er með notkun oseltamivírs hjá sjúklingum sem grunaðir eru um sýkingar í öðrum líffærakerfum en öndunarvegi. Zanamivír verkar staðbundið á yfirborði öndunarvegar og dreifist því lítið um líkamann. Rannsóknir benda einnig til að oseltamivír dragi meira úr smithæfni veirunnar heldur en zanamivír (35).
2. Fyrirbyggjandi notkun.
Gert er ráð fyrir að meðgöngutími sýkingarinnar sé tveir til þrír dagar og að sýktur einstaklingur sé smitandi frá einum sólarhring áður en einkenni koma í ljós í allt að sjö til 10 daga. ?
Þar sem meðferð sjúklinga með oseltamivíri eða zanamivíri dregur verulega úr líkum á smiti (sérstaklega oseltamivír) (15, 24, 35) má halda því fram að ekki sé alltaf þörf á fyrirbyggjandi meðferð hjá einstaklingum sem komast í nána snertingu (innan við einn metra) við sjúklinga sem eru á fullri veirulyfjameðferð. Auk þess draga aðrar varnaraðgerðir eins og góður handþvottur, notkun sloppa, gríma, hanska og gleraugna verulega úr líkum á smiti og minnka þannig þörfina á veirulyfjum (58, 59).
Lyfjameðferð heilbrigðra sem munu komast eða hafa komist í mikla nálægð við sýkta einstaklinga verður að byggjast á mati þeirra lækna sem ávísa lyfjunum. Við það mat þarf að taka tillit til eftirfarandi:
- Hversu miklar líkur eru á því að sjúklingurinn sé með inflúensu?
- Hversu skæður er faraldurinn og hversu miklar líkur eru á alvarlegum veikindum ef einstaklingurinn sýkist?
- Er sjúklingur á fullri veirulyfjameðferð?
- Hversu góðar varnaraðgerðir voru (verða) viðhafðar þegar samneytið átti sér stað?
- Hversu lengi var (verður) einstaklingurinn útsettur fyrir smiti? Náið samneyti í langan tíma eykur líkur á smiti.
- Líkur á aukaverkunum við fyrirbyggjandi notkun.
- Hefur einstaklingurinn verið bólusettur með bóluefni gegn heimsfaraldri
Læknar geta því mælt með eftirfarandi fyrirbyggjandi notkun:
a. Engin fyrirbyggjandi meðferð verður gefin en full meðferð hafin strax (innan 48 klukkustunda og helst innan 24 klukkustunda) eftir að viðkomandi sýnir merki um sýkingu. Þar sem birgðir veirulyfja eru takmarkaðar má færa fyrir því rök að slík notkun tryggi bestu nýtingu lyfjanna en þó með þeirri hættu að fjöldi sjúklinga geti orðið verulegur og sumir hugsanlega orðið alvarlega veikir. Ef faraldurinn verður hins vegar ekki skæður er skynsamlegt að nota lyfin á þennan hátt vegna aukaverkana lyfjanna sem sést geta við langvarandi fyrirbyggjandi notkun. Þeir sem bólusettir hafa verið gegn heimsfaraldri eiga ekki að fá fyrirbyggjandi veirulyf nema sýnt hafi verið fram á að bóluefnið veiti litla vörn.
b. Fyrirbyggjandi meðferð verður hafin eins fljótt og auðið er eftir að einstaklingur hefur komist í mikla nálægð við sjúkling (innan við eins metra fjarlægð) og gefin í 10 daga. Verði heilbrigður einstaklingur á fyrirbyggjandi meðferð veikur skal hann settur á fulla meðferð. Vert er að benda á að þeir sem eru á fyrirbyggjandi meðferð fá oft einkennalausa sýkingu og geta því hugsanlega verið varðir gegn frekari sýkingu eftir að fyrirbyggjandi meðferð líkur (35). Ef sá sem verið hefur á fyrirbyggjandi meðferð kemst aftur í nána snertingu við sjúkling með inflúensu skal hann ekki settur á fyrirbyggjandi meðferð en full meðferð hafin ef einkenni um sýkingu koma fram. Notkun á þennan hátt tryggir næstbestu nýtingu veirulyfjanna.
c. Fyrirbyggjandi meðferð verður gefin heilbrigðum einstaklingi áður en hann kemst í mikla nálægð við þá sem eru sýktir. Meðferð verður gefin í að minnsta kosti 10 daga eftir síðasta samneyti við sjúkling og að hámarki í sex vikur. Útbreidd notkun lyfjanna á þennan hátt er hins vegar óhagkvæm og þau munu nýtast fáum.
Í grófum dráttum má skipta þeim sem þurfa fyrirbyggjandi lyfjameðferð í þrjá hópa:
1. Fjölskyldumeðlimir veikra
Samkvæmt viðbragðsáætlun verður leitast við að meðhöndla sýkt fólk heima svo lengi sem ástand þeirra leyfir. Heimilið ásamt fjölskyldumeðlimum verður einangrað í 10 daga, hinn veiki settur á veirulyfjameðferð eins fljótt og auðið er en meðferð einkennalausra fjölskyldumeðlima ákveðin samkvæmt liðum a eða b hér að ofan.
2. Heilbrigðisstarfsfólk
Dregið verður úr smithættu á heilbrigðisstofnunum með því að gera heilbrigðisstarfsfólki sem vinnur með sýkta einstaklinga skylt að nota sérstakan hlífðarbúnað og fylgja ýmsum öðrum sóttvarnaráðstöfunum. Auk þess verða sjúklingar með inflúensu settir á veirulyfjameðferð sem dregur verulega úr líkum á smiti. Hætta á sýkingu hjá heilbrigðisstarfólki minnkar því verulega og því hægt að bjóða meðferð samkvæmt liðum a, b eða c.
3. Löggæslulið, björgunarsveitir
Leitast verður við að hafa eins fáa í vinnu við að flytja og annast sjúka eins og kostur er. Rík áhersla verður lögð á notkun hlífðarbúnaðar, að leiðbeiningum um sóttvarnir verði fylgt og veirulyf verði boðin samkvæmt liðum a eða b.
4. Aðrir
Ekki verður ástæða til að setja þá sem ekki hafa verið í mikilli nálægð við sýkta einstaklinga á fyrirbyggjandi meðferð. Aðeins eftir að samneyti hefur átt sér stað og líkur á smiti eru miklar verður ástæða til að hefja fyrirbyggjandi meðferð.
Almenningur verður hvattur til fylgja leiðbeiningum sem miða að því að draga úr smithættu.
Lokaorð
Næsti heimsfaraldur inflúensu getur valdið miklu mannfalli og gríðarlegum þjóðfélagslegum skaða ef ekki verður brugðist við á réttan hátt. Í viðbragðsáætlunum vegna heimsfaraldurs er gert ráð fyrir að veirulyf muni gegna þýðingarmiklu hlutverki. Þar sem birgðir veirulyfja hér á landi eru takmarkaðar er ljóst að leiðbeiningar um notkun lyfjanna verða að vera skýrar og markvissar til að þau nýtist sem best og ónæmislíkum verði haldið í lágmarki.
Það er von höfunda að sátt skapist um leiðbeiningar þær sem hér eru birtar og læknar ávísi veirulyfjunum á ábyrgan hátt þegar til heimsfaraldurs kemur. Aðeins á þann hátt verður hægt að draga úr skaðlegum áhrifum inflúensunnar.
Þakkir
Sigurði B. Þorsteinssyni og Magnúsi Gottfreðssyni yfirlæknum eru þakkaðar góðar ábendingar.
Heimildir
1. Potter CW. A history of influenza. J Appl Microbiol 2001; 91: 572-9.
2. Johnson NP, Mueller J. Updating the accounts: global mortality of the 1918-1920 Spanish? influenza pandemic. Bull Hist Med 2002; 76: 105-15.
3. Thoroddsen ÞJ. Innflúenzan fyrrum og nú. Læknablaðið 1919; 5: 74-9.
4. Heilbrigðisskýrslur 1918.
5. Smee DF, Wandersee MK, Wong MH, Bailey KW, Sidwell RW. Treatment of mannan-enhanced influenza B virus infections in mice with oseltamivir, ribavirin and viramidine. Antivir Chem Chemother 2004; 15: 261-8.
6. Sidwell RW, Bailey KW, Wong MH, Barnard DL, Smee DF. In vitro and in vivo influenza virus-inhibitory effects of viramidine. Antiviral Res 2005; 68: 10-7.
7. Hayden FG. Perspectives on antiviral use during pandemic influenza. Philos Trans R Soc Lond B Biol Sci 2001; 356: 1877-84.
8. Hayden FG. Antiviral resistance in influenza viruses--implications for management and pandemic response. N Engl J Med 2006; 354: 785-8.
9. Hayden F. G AF, Amantadine, rimantadine and related agents. Antimicrobial therapy and vaccines. 1999, Baltimore MD: Williams and Wilkins: in: Yu V, Meigan T, Barriere S. 1344-65.
10. Hurt AC, Selleck P, Komadina N, Shaw R, Brown L, Barr IG. Susceptibility of highly pathogenic A(H5N1) avian influenza viruses to the neuraminidase inhibitors and adamantanes. Antiviral Res 2007; 73: 228-31.
11. Hayden FG, Aoki FY, Amantadine, rimantadine and related agents. Antimicrobial therapy and vaccines, ed. V.L.Yu TCMSLB, 1999 Baltimore: Williams and Wilkins. 1344-65.
12. Hayden FG, Pavia AT. Antiviral management of seasonal and pandemic influenza. J Infect Dis 2006; 194 Suppl 2: S119-26.
13. Kim CU, Chen X, Mendel DB. Neuraminidase inhibitors as anti-influenza virus agents. Antivir Chem Chemother 1999; 10: 141-54.
14. Jefferson T, Demicheli V, Rivetti D, Jones M, Di Pietrantonj C, Rivetti A. Antivirals for influenza in healthy adults: systematic review. Lancet 2006; 367: 303-13.
15. Treanor JJ, Hayden FG, Vrooman PS, et al. Efficacy and safety of the oral neuraminidase inhibitor oseltamivir in treating acute influenza: a randomized controlled trial. US Oral Neuraminidase Study Group. JAMA 2000; 283: 1016-24.
16. Kaiser L, Wat C, Mills T, Mahoney P, Ward P, Hayden F. Impact of oseltamivir treatment on influenza-related lower respiratory tract complications and hospitalizations. Arch Intern Med 2003; 163: 1667-72.
17. Monto AS, Webster A, Keene O. Randomized, placebo-controlled studies of inhaled zanamivir in the treatment of influenza A and B: pooled efficacy analysis. J Antimicrob Chemother 1999; 44 Suppl B: 23-9.
18. Kaiser L, Keene ON, Hammond JM, Elliott M, Hayden FG. Impact of zanamivir on antibiotic use for respiratory events following acute influenza in adolescents and adults. Arch Intern Med 2000; 160: 3234-40.
19. Monto AS, Robinson DP, Herlocher ML, Hinson JM, Jr., Elliott MJ, Crisp A. Zanamivir in the prevention of influenza among healthy adults: a randomized controlled trial. JAMA 1999; 282: 31-5.
20. Puhakka T, Lehti H, Vainionpaa R, et al. Zanamivir: a significant reduction in viral load during treatment in military conscripts with influenza. Scand J Infect Dis 2003; 35: 52-8.
21. Aoki FY, Macleod MD, Paggiaro P, et al. Early administration of oral oseltamivir increases the benefits of influenza treatment. J Antimicrob Chemother 2003; 51: 123-9.
22. Hayden FG, Treanor JJ, Betts RF, Lobo M, Esinhart JD, Hussey EK. Safety and efficacy of the neuraminidase inhibitor GG167 in experimental human influenza. JAMA 1996; 275: 295-9.
23. Hayden FG, Osterhaus AD, Treanor JJ, et al. Efficacy and safety of the neuraminidase inhibitor zanamivir in the treatment of influenzavirus infections. GG167 Influenza Study Group. N Engl J Med 1997; 337: 874-80.
24. Whitley RJ, Hayden FG, Reisinger KS, et al. Oral oseltamivir treatment of influenza in children. Pediatr Infect Dis J 2001; 20: 127-33.
25. Sato M, Hosoya M, Kato K, Suzuki H. Viral shedding in children with influenza virus infections treated with neuraminidase inhibitors. Pediatr Infect Dis J 2005; 24: 931-2.
26. Bowles SK, Lee W, Simor AE, et al. Use of oseltamivir during influenza outbreaks in Ontario nursing homes, 1999-2000. J Am Geriatr Soc 2002; 50: 608-16.
27. Nordstrom BL, Sung I, Suter P, Szneke P. Risk of pneumonia and other complications of influenza-like illness in patients treated with oseltamivir. Curr Med Res Opin 2005; 21: 761-8.
28. Cooper NJ, Sutton AJ, Abrams KR, Wailoo A, Turner D, Nicholson KG. Effectiveness of neuraminidase inhibitors in treatment and prevention of influenza A and B: systematic review and meta-analyses of randomised controlled trials. BMJ 2003; 326: 1235.
29. Turner D, Wailoo A, Nicholson K, Cooper N, Sutton A, Abrams K. Systematic review and economic decision modelling for the prevention and treatment of influenza A and B. Health Technol Assess 2003; 7: iii-iv, xi-xiii, 1-170.
30. Chik KW, Li CK, Chan PK, et al. Oseltamivir prophylaxis during the influenza season in a paediatric cancer centre: prospective observational study. Hong Kong Med J 2004; 10: 103-6.
31. Hayden FG, Gubareva LV, Monto AS, et al. Inhaled zanamivir for the prevention of influenza in families. Zanamivir Family Study Group. N Engl J Med 2000; 343: 1282-9.
32. Monto AS, Pichichero ME, Blanckenberg SJ, et al. Zanamivir prophylaxis: an effective strategy for the prevention of influenza types A and B within households. J Infect Dis 2002; 186: 1582-8.
33. Hayden FG, Belshe R, Villanueva C, et al. Management of influenza in households: a prospective, randomized comparison of oseltamivir treatment with or without postexposure prophylaxis. J Infect Dis 2004; 189: 440-9.
34. Welliver R, Monto AS, Carewicz O, et al. Effectiveness of oseltamivir in preventing influenza in household contacts: a randomized controlled trial. JAMA 2001; 285: 748-54.
35. Halloran ME, Hayden FG, Yang Y, Longini IM, Jr., Monto AS. Antiviral effects on influenza viral transmission and pathogenicity: observations from household-based trials. Am J Epidemiol 2007; 165: 212-21.
36. Organization CSaIR, CSIRO based drug effective against bird flu. www.csiro.au/
37. Trampuz A, Prabhu RM, Smith TF, Baddour LM. Avian influenza: a new pandemic threat?(erratum appears in Mayo Clin Proc 2004; 79: 833). Mayo Clinic Proceedings 2004; 79: 523-30; quiz 30.
38. de Jong MD, Tran TT, Truong HK, et al. Oseltamivir resistance during treatment of influenza A (H5N1) infection. N Engl J Med 2005; 353: 2667-72.
39. Beigel JH, Farrar J, Han AM, et al. Avian influenza A (H5N1) infection in humans. N Engl J Med 2005; 353: 1374-85.
40. Roberts NA. Treatment of influenza with neuraminidase inhibitors: virological implications. Philosophical transactions of the Royal Society of London 2001; 356: 1895-7.
41. Kiso M, Mitamura K, Sakai-Tagawa Y, et al. Resistant influenza A viruses in children treated with oseltamivir: descriptive study. Lancet 2004; 364: 759-65.
42. Ward P, Small I, Smith J, Suter P, Dutkowski R. Oseltamivir (Tamiflu) and its potential for use in the event of an influenza pandemic. J Antimicrob Chemother 2005; 55 Suppl 1: i5-i21.
43. Ives JA, Carr JA, Mendel DB, et al. The H274Y mutation in the influenza A/H1N1 neuraminidase active site following oseltamivir phosphate treatment leave virus severely compromised both in vitro and in vivo. Antiviral Res 2002; 55: 307-17.
44. Le QM, Kiso M, Someya K, et al. Avian flu: isolation of drug-resistant H5N1 virus. Nature 2005; 437: 1108.
45. Mishin VP, Hayden FG, Gubareva LV. Susceptibilities of antiviral-resistant influenza viruses to novel neuraminidase inhibitors. Antimicrob Agents Chemother 2005; 49: 4515-20.
46. Wetherall NT, Trivedi T, Zeller J, et al. Evaluation of neuraminidase enzyme assays using different substrates to measure susceptibility of influenza virus clinical isolates to neuraminidase inhibitors: report of the neuraminidase inhibitor susceptibility network. J Clin Microbiol 2003; 41: 742-50.
47. Dutkowski R, Thakrar B, Froehlich E, Suter P, Oo C, Ward P. Safety and pharmacology of oseltamivir in clinical use. Drug safety 2003; 26: 787-801.
48. Nicholson KG, Aoki FY, Osterhaus AD, et al. Efficacy and safety of oseltamivir in treatment of acute influenza: a randomised controlled trial. Neuraminidase Inhibitor Flu Treatment Investigator Group. Lancet 2000; 355: 1845-50.
49. Oseltamivir: cutaneous and neurological adverse effects in children. Prescrire international 2006; 15: 182-3.
50. Okumura A, Kubota T, Kato T, Morishima T. Oseltamivir and delirious behavior in children with influenza. Pediatr Infect Dis J 2006; 25: 572.
51. Henney JE. From the food and drug administration: revised labeling for zanamivir. 2000; 284: 1234.
52. Cooper NJ, Sutton AJ, Abrams KR, Wailoo A, Turner D, Nicholson KG. Effectiveness of neuraminidase inhibitors in treatment and prevention of influenza A and B: systematic review and meta-analyses of randomised controlled trials. BMJ 2003; 326: 1235.
53. www.who.int/csr/disease/avian_influenza/timeline2007_06_21.pdf.
54. www.who.int/csr/disease/avian_influenza/country/en/
55. Schunemann HJ, Hill SR, Kakad M, et al. WHO Rapid Advice Guidelines for pharmacological management of sporadic human infection with avian influenza A (H5N1) virus. Lancet Infect Dis 2007; 7: 21-31.
56. Leiðbeiningar til starfsmanna á alifuglabúum og þeirra sem sjá um förgun fugla og annarra dýra sem sýkt eru af skæðri fuglainflúensu. (www.landlaeknir.is/lisalib/getfile.aspx?itemid=3024.
57. www.who.int/csr/disease/avian_influenza/guidelines/clinicalmanage07/en/index.html.
58. Tang JW, Li Y, Eames I, Chan PK, Ridgway GL. Factors involved in the aerosol transmission of infection and control of ventilation in healthcare premises. J Hosp Infect 2006; 64: 100-14.
59. www.pandemicflu.gov/plan/healthcare/maskguidancehc.html.
60. Ferguson NM, Cummings DA, Fraser C, Cajka JC, Cooley PC, Burke DS. Strategies for mitigating an influenza pandemic. Nature 2006; 442: 448-52.
61. Ferguson NM, Cummings DA, Cauchemez S, et al. Strategies for containing an emerging influenza pandemic in Southeast Asia. Nature 2005; 437: 209-14.
