Fræðigreinar
Leit að stökkbreytingum í stjórnunargeni sem ákvarðar þroska fitufrumna hjá íslenskum börnum með offitu
Ágrip
Inngangur: Talið er að holdafar fólks megi að hluta rekja til erfðabreytileika. Erfiðlega hefur þó gengið að einangra þau gen sem hlut eiga að máli. PPARg2 (peroxisome proliferator activated receptor g2) er umritunarþáttur af fjölskyldu kjarnahormónaviðtaka. Talið er að hann gegni lykilhlutverki við þroska og sérhæfingu fitufrumna. Nýlega var lýst stökkbreytingunni Pro115Gln í geni PPARg2 og sýnt fram á marktæk orsakatengsl hennar við alvarlega offitu. Ekki er vitað hve algeng þessi stökkbreyting í raun og veru er eða hvort hana er að finna hjá öllum þjóðum. Markmið rannsóknarinnar er að kanna hvort þessa stökkbreytingu sé að finna meðal íslenskra barna með alvarlega offitu.Efniviður og aðferðir: Í rannsókninni tóku þátt 35 einstaklingar á aldrinum 4-18 ára sem fengið höfðu greininguna offita. Einnig gáfu átta aðstandendur, á aldrinum 19-41 árs, sýni. Skilyrði var að offita hefði verið vandamál frá barnæsku. Notast var við hugtakið líkamsþyngdarstuðull (body mass index, BMI) til þess að lýsa svipgerð viðfanga. Þátttakendur höfðu líkamsþyngdarstuðul á bilinu: 28,0-52,2 kg/m2.
DNA var einangrað úr hvítum blóðkornum. Beitt var fjölliðunarhvarfi (PCR, polymerase chain reaction) til að magna upp 131 bp bút sem inniheldur umrætt svæði. Afurðin var melt með skerðiensíminu Hinc II og skoðuð á geli, merkt með ethidíum brómíði. Til að leita að öðrum stökkbreytingum á þessum sama 131 basaparabút var hann magnaður upp með fjölliðunarhvarfi sem fyrr og svo beitt á hann ensími sem greinir stökkbreytingar (enzymatic mutation detection, EMD). Að lokum voru DNA bútar þeirra einstaklinga sem gáfu vísbendingar með EMD raðgreindir með aðferð Sangers.
Niðurstöður: Pro115Gln stökkbreytingin fannst ekki eftir meltingu með Hinc II. Grunur vaknaði um basabreytingar hjá þremur einstaklingum með EMD en með raðgreiningu tókst ekki að staðfesta þessar breytingar.
Ályktanir: Stökkbreytingin Pro115Gln eða aðrar basabreytingar á svipuðu svæði í PPARg2 umritunarþættinum virðist ekki vera orsakaþáttur snemmkominnar alvarlegrar offitu hjá íslenskum börnum.
English Summary |
| Ágústsson TÞ, Hákonarson H, Ólafsson Í, Hjaltadóttir G, Þórsson ÁV A mutation detection in a transcription factor for adipocyte development in children with severe obesity Læknablaðið 2001; 87: 119-24 Objective: A substantial proportion of human obesity may be explained by genetic variability. Researchers have tried to identify the important genes in obesity with little sucsess. PPARg2 (peroxisome proliferator activated receptor g 2) is a transcription factor of the nuclear hormone receptor superfamily. It plays a key role in the developement and differentiation of adipocytes. Recently the mutation Pro115Gln in the PPARg2 gene was identified and shown to have a significant correlation with severe obesity. The actual prevalence and distribution of this mutation is not known. The aim of this study was to look for this mutation among Icelandic children suffering from severe obesity. Material and methods: Thirty-five children and adolescents, aged 4-18, who have been diagnosed with severe obesity participated in the study. Eight parents and siblings aged 19-41 also participated. All study subjects had been obese since early childhood. Body mass index (BMI) was used to describe the phenotype of the subjects. The participants had a BMI of 28.0 to 52.2 kg/m2. Genomic DNA was extracted from leucocytes. A 131 bp segment was amplified using polymerase chain reaction. The amplified product was digested with the restriction enzyme Hinc II, resolved on agarose gel and visualized under ultraviolet illumination after staining with ethidium bromide. To examine other mutations on the same 131 bp segment enzymatic mutation detection (EMD) was used. Finally the segments giving variable results using EMD were sequenced using the classic Sanger´s method. Results: The mutation Pro115Gln was not found in any of the specimens after analysis of the restriction fragment length polymorphism. The results of EMD indicated mutations or polymorphisms in three of the subjects but DNA sequencing failed to confirm these results. Conclusions: The mutation Pro115Gln or other genetic alternations within the exon examined do not appear to have a significant role in severe early - onset obesity in Icelandic children. Key words: obesity, mutation, PPARg, peadiatrics, endocrinology. Correspondence: Hákon Hákonarson. E-mail: hakonh@landspitali.is and Ísleifur Ólafsson. E-mail: isleifur@landspitali.is |
Inngangur
Offita er talin algengasta heilsufarsvandamál fólks í hinum vestræna heimi. Talið er að um þriðjungur allra Bandaríkjamanna þjáist af offitu og offita er talin önnur algengasta dánarorsök af viðráðanlegum orsökum þar í landi (1-3).Offitu má skilgreina sem óvenjumikla söfnun þríglýseríða í fitufrumur. Við skilgreiningu á offitu er oft notast við hugtakið líkamsþyngdarstuðull (LÞS) (body mass index, BMI) sem er þyngd viðkomandi einstaklings deilt með hæð hans í öðru veldi (kg/m2). Þessa stærð er auðvelt að mæla og reikna út og hefur hún reynst hafa sæmilega fylgni við nákvæmari fitumælingar og er því hjálpleg við læknisfræðilega skilgreiningu á offitu (4). Meðalgildi líkamsþyngdarstuðuls bandarískra karla er um 25 kg/m2. Talið er að æskilegast sé að gildið sé á bilinu 23 til 25 kg/m2 (5). Sýnt hefur verið fram á að ef líkamsþyngdarstuðull fer yfir 28 kg/m2 megi búast við þrisvar til fjórum sinnum meiri hættu á sjúkdómum á borð við heilablóðfall, blóðþurrðarsjúkdóma í hjarta og sykursýki af gerð II heldur en hjá eðlilegum einstaklingum (6). Offita í barnæsku er ennfremur talin auka hættu á sjúkdómum þegar komið er fram á fullorðinsár, óháð því hvort breyting verði á holdafari (7).
Margt bendir til að ýmsir erfðaþættir ráði að miklu leyti hve miklum fituvef viðkomandi safnar á sig (8-12). Til þess að einstaklingur haldi sömu þyngd þarf að vera nákvæmt jafnvægi á milli fæðuinntöku og orkunotkunar. Ekki er að fullu vitað hvernig þessu jafnvægi er stjórnað en fjöldi kenninga hefur verið settur fram (13-21). Fjöldi rannsókna hefur einnig verið framkvæmdur til að áætla að hve miklu leyti offita er erfður eiginleiki meðal manna. Tvíburarannsóknir hafa sýnt fram á erfðastuðla á bilinu 0,4-0,98 og verður það að teljast nokkuð afgerandi vísbending um að töluverðan hluta offitu megi rekja til erfðabreytileika (22-25). Ljóst er að erfðir ráða miklu um breytileika í líkamsþyngdarstuðli, fitudreifingu og fleiri eiginleika því tengda. Erfiðlega hefur gengið að finna erfðaþætti sem geta skýrt þetta í mönnum. Hins vegar hefur tekist að einangra nokkur gen í músum og rottum þar sem gallar valda alvarlegri offitu. Einna þekktast þessara gena er ob genið í músum. Afurð gensins er eggjahvítuefnið leptín. Samsvarandi gen í mönnum er LEP genið (26). Ef mýs eru arfhreinar fyrir stökkbreytingu í þessu geni (ob/ob) verða þær sjúklega feitar ásamt því að blóðsykur hækkar (26). Aðeins örfá dæmi um slíkar stökkbreytingar hafa fundist í mönnum með offitu. (27,28).
Þau gen sem helst hafa verið skoðuð með offitu í huga tengjast flest hver stjórnun á fæðuinntöku, orkunotkun og öðrum efnaskiptaferlum. Nýlega var lýst stökkbreytingum í genum sem við koma sérhæfingu fitufrumna og fitusöfnun og hafa bein tengsl við offitu. Má þar nefna PPARg (peroxisome proliferator activated receptors) genin sem eru umritunarþættir sem bindast og svara hormónum (29-31). Nýlega tókst að staðsetja PPARg genin á 25 bandi p armsins á litningi 3 (3p25) (31-33). Hvað varðar þroska og sérhæfingu fitufrumna hefur mikilvægi PPARg2 gensins orðið augljóst, en genið gegnir lykilhlutverki við umritun ýmissa gena sem einkennandi geta talist fyrir fitufrumur (29,34-41). Nýlega var lýst stökkbreytingunni Pro115Gln í geni PPARg2 og sýnt fram á marktæk orsakatengsl við offitu en talið er að hún hafi einmitt þau áhrif að koma í veg fyrir fosfórýleringu sem leiðir til aukinnar starfsemi umritunarþáttarins (42). Ekki er vitað hve algeng þessi stökkbreyting er í raun og veru eða hvort hana er að finna hjá öllum þjóðum. Því hefur verið haldið fram að offitu, sem fram kemur á barnsaldri, megi fremur rekja til erfða en síðkomnari tilfelli (43). Markmið rannsóknarinnar er að kanna hvort stökkbreytinguna Pro115Gln, og aðrar stökkbreytingar á svipuðu svæði PPARg2, er að finna meðal of feitra íslenskra barna.
Efniviður og aðferðir
Úrtak: Haft var samband við 48 einstaklinga sem hafa verið í meðferð hjá innkirtlasérfræðingi barna á Sjúkrahúsi Reykjavíkur. Um var að ræða einstaklinga sem fengið höfðu greininguna offita (obesitas) og höfðu líkamsþyngdarstuðul yfir 28 kg/m2. Upplýsingabréf voru send til aðstandenda og í kjölfarið haft samband símleiðis. Þátttöku í rannsókninni samþykktu 38 og skrifuðu allir undir upplýst samþykki. Einnig gáfu átta aðstandendur sýni. Við sýnatöku skrifuðu þátttakendur undir upplýst samþykki til þátttöku. Áður en rannsóknarvinna hófst hafði vísindasiðanefnd Sjúkrahúss Reykjavíkur fallist á fyrirkomulag hennar. Hugtakið líkamsþyngdarstuðull var notað til að lýsa svipgerð einstaklinganna. Þátttakendur höfðu líkamsþyngdarstuðul á bilinu 28,0 til 52,2 kg/m2. Meðaltal alls hópsins var 35 kg/m2 og gefur sú tala nokkuð góða mynd af hópnum sem heild. Aldur var á bilinu fjögurra til 41 árs. Meðalaldur var um 19 ár en langflestir voru á aldrinum 10 til 20 ára. Kynjaskipting þátttakenda var nokkuð jöfn: 23 konur (53%) og 20 karlar (47%).
Aðferðir: Teknir voru 10 ml af heilblóði til DNA einangrunar og 10 ml af sermi sem geymt var til hormónamælinga. DNA var einangrað úr heilblóðinu með prótínasa K meltingu og hefðbundinni etanólútfellingu .
Fyrst var leitað sérstaklega að Pro115Gln stökkbreytingunni. 131 basapara DNA bútur sem inniheldur viðkomandi stökkbreytingu var magnaður upp með fjölliðunarhvarfi (polymerase chain reaction). Við hvörfin voru notaðir þreifararnir (Pharmacia Biotech)
: 5´TGCAATCAAAGTGGAGCCTGCATGTC3´ og : 5´CAGAAGCTTTATCTCCACAGAC3´.
Fjölliðunarhvarfið hófst á eðlissviptingu (denaturation) við 95°C í fimm mínútur svo voru endurteknir 39 hringir sem samanstóðu af: eðlissviptingu (94°C í 30 sekúndur), temprun (annealing) (61°C í 30 sekúndur) og lengingu (extension) (72°C í 30 sekúndur). Eftir hringina 39 tók við lenging við 72°C í eina mínútu. + þreifarinn er breyttur þar sem sett er inn G í stað C þremur bösum fyrir ofan umrædda stökkbreytingu. Þetta er gert til þess að mynda skerðiset fyrir skerðiensímið Hinc II (Pharmacia Biotech) ef stökkbreytingin er fyrir hendi (mynd 1).
Ef stökkbreytingin er fyrir hendi klippir Hinc II 131 basaparabútinn, sem magnaður var upp, í tvo búta sem eru 26 bp annars vegar og 105 bp hins vegar. Fjölliðunarhvarfsafurðin var melt með átta einingum af Hinc II skerðiensíminu við 37°C í um einn og hálfan klukkutíma og svo rafdregin á 4% agarósageli í 1% TBE búffer, merkt með ethidíum brómíði og skoðuð í útfjólubláu ljósi. Ef einstaklingur reynist arfhreinn fyrir umrædda stökkbreytingu koma fram tvö bönd (26bp+105bp) en ef hann er arfblendinn koma fram þrjú bönd (26bp+105bp+131bp). Hins vegar ef viðkomandi er arfhreinn án stökkbreytingar kemur aðeins fram eitt 131 bp band. Til stærðargreiningar á þeim böndum sem fram komu var notast við fX - 174 - RF DNA Hae III meltiafurð (Pharmacia Biothech). Ferlið var tvítekið fyrir hvert sýni.
Til að leita að öðrum basabreytingum á þessum sama 131 bp bút var beitt ensími sem greinir stökkbreytingar (enzymatic mutation detection, EMD(TM)). Notað var PASSPORT Mutation Scanning Kit (Amersham Pharmacia Biotech AB). Búturinn var magnaður upp með fjölliðunarhvarfi með sömu þreifurum og áður en bætt inn geislamerktu adenósíni, [a-33P]ATP. Einnig var magnaður upp bútur úr heilbrigðum einstaklingi (villigerð) með sömu aðferðum. Fjölliðunarhvarfið hófst sem fyrr á eðlissviptingu við 95°C í fimm mínútur. Að því búnu var eftirfarandi hringur endurtekinn 35 sinnum: eðlissvipting (94°C í 30 sekúndur), temprun (61°C í 30 sekúndur) og lenging (72°C í eina mínútu). Að lokum var lengt í eina mínútu við 72°C. Að því búnu voru myndaðir heteródímerar úr villigerðinni og þeim einstaklingum sem rannsaka á. Var þetta gert með því að blanda saman fjölliðunarhvarfsafurðum þátttakanda og villigerðar ásamt blendingslausn (hybridization buffer). Að því loknu voru blöndurnar hitaðar við 100°C í fimm mínútur og svo hafðar við stofuhita í um 10 mínútur. Síðan var afurðin melt með skerðiensíminu T4 endonucleasa VII við 37°C í um tvær klukkustundir. Skerðiensímið þekkir og klýfur heteródímerinn þar sem mispörun eða lykkjumyndun verður. Alltaf er einhver ósértæk melting fyrir hendi en ef um basabreytingar er að ræða á meltingin að verða meiri og sérhæfðari. Meltir bútarnir eru svo rafdregnir á 6% raðgreiningargeli í 0,5% TBE búffer. Gelið var flutt yfir á filterpappír og lagt í röntgenhirslu og filman svo framkölluð eftir tvo sólarhringa. Ferlið var tvítekið fyrir hvert sýni
Til að kanna nánar þá einstaklinga sem gefið höfðu grunsamleg svör með EMD var erfðaefni þeirra á þessu svæði að lokum raðgreint. Fyrst voru 131 basapara bútarnir einangraðir úr agarósageli og síðan raðgreindur með aðferð Sangers. Til þess var notast við: Thermo Sequenase(TM) cycle sequencing kit (Amersham).
Niðurstöður
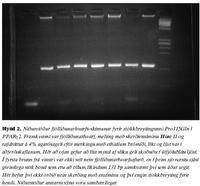
Til að leita sérstaklega að stökkbreytingunni Pro115Gln var notast við skimun byggða á meltingu með skerðiensími, eins og lýst er í aðferðakaflanum. Við skoðun á agarósagelum þar sem fjölliðunarhvarfsafurðin, melt með Hinc II, hafði verið rafdregin sást aðeins eitt band í öllum tilvikum. Staðsetning þessa bands kom heim og saman við 131 basapara lengd ef miðað er við það merkigen sem notað var (mynd 2). Stökkbreytingin Pro115Gln fannst því ekki hjá neinum þeirra 43 einstaklinga sem skoðaðir voru. Ferlið var tvítekið fyrir hvert sýni og voru niðurstöður eins í öllum tilvikum Til að leita að öðrum basabreytingum á þessum sama 131 bp bút var beitt EMD(TM), eins og lýst er í aðferðakaflanum. Þegar niðurstöður EMD(TM) voru skoðaðar komu í ljós nokkuð afgerandi jákvæðar niðurstöður hjá þremur einstaklingum og nokkuð veikari vísbendingar hjá fimm til viðbótar (mynd 3).
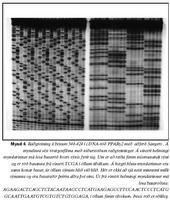
Þau bönd sem fram komu voru svipuð í öllum þremur tilfellum og bentu til basabreytingar um miðbik bútsins. Í hinum fimm tilfellunum var um að ræða mun óræðnara misræmi við niðurstöður annarra einstaklinga.
Til þess að skoða betur þær vísbendingar sem fram komu við EMD var afurð þeirra einstaklinga raðgreind með aðferð Sangers. Í öllum tilfellum voru basaraðir eðlilegar (mynd 4).
Umræða
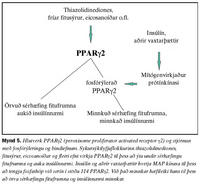
Offita stafar bæði af umhverfis- og erfðaþáttum sem stýra orkuinntöku og fitusöfnun. Mikil orkusöfnun leiðir hvoru tveggja til stækkunar á fitufrumum (hypertrophy) og fjölgunar þeirra (hyperplasia) (1). Fyrirrennarar fitufrumna eru lítt sérhæfðir og líkjast helst bandvefsfrumum (fibroblasts) í myndgerð sinni. Virkjun umritunarþáttarins PPARg2 er talin skipta miklu máli við sérhæfingu þessara frumna yfir í fitufrumur (adipocyte) (35,37). Eins og drepið var á í inngangi er stjórnun PPARg2 í raun tvíþætt. Í fyrsta lagi byggist hún á tengingu ýmissa efna og vaxtarþátta svo sem: frírra fitusýra, eicosanoíða og sykursýkilyfja af flokki thiazolidienodiones. Í öðru lagi er virkni stýrt með fosfórýleringu (38-41) (mynd 5).Virkni umritunarþáttarins PPARg2 minnkar við tengingu fosfathóps við serín í stöðu 114 (40,41). Stökkbreyting á því svæði gæti því komið í veg fyrir fosfórýleringu og þannig valdið of mikilli starfsemi. Í rannsókninni var leitað að stökkbreytingum á þessu svæði sem hugsanlega tengjast offitu (42).
Enginn þeirra 43 einstaklinga sem athugaðir voru höfðu Pro115Gln stökkbreytinguna. Því má álykta sem svo að þessi ákveðna stökkbreyting eigi ekki marktækan þátt í tilurð snemmkominnar offitu hjá Íslendingum. Ristow og félagar lýstu nýlega stökkbreytingunni hjá fjórum Þjóðverjum með alvarlega offitu (líkamsþyngdarstuðul 37,9-47,3) (42). Ekki fannst fylgni milli stökkbreytingarinnar og sykursýki eða blóðfitubrenglana og var jafnvel talið að um nýja undirtegund offitu væri að ræða. Í rannsókn Ristows og félaga var erfðaefni 121 offitusjúklings og 237 einstaklinga af eðlilegri þyngd athugað. Stökkbreytingin var fyrir hendi í um 3% þeirra offitusjúklinga sem skoðaðir voru en í um 1% allra þátttakenda (42). Ekki er vitað hve algeng þessi stökkbreyting í raun og veru er eða hvort hana er að finna annars staðar í heiminum. Vel gæti hugsast að hún sé aðeins til á afmörkuðum svæðum í Evrópu en hafi ekki komið fram hér á landi. Í rannsókn Ristows og félaga var ekki tekið tillit til hvort offitan hefði verið vandamál allt frá barnæsku. Líklegt verður að teljast að offita sem fram kemur á barnsaldri eigi fremur rætur sínar að rekja til erfðaþátta en offita sem fram kemur á fullorðinsárum (43). Því má ætla að gallar á þessu ákveðna svæði PPARg2 leiki enn síður hlutverk í erfðri offitu meðal Íslendinga.
Ef til vill má telja til annmarka að jákvætt viðmið við Hinc II meltingu vantaði. Betra hefði verið að sjá í raun og veru hvernig stökkbreyttur einstaklingur lítur út og þá hvort meltingin hafi í öllum tilvikum heppnast. Þó verður að minnast þess að öll sýni voru skoðuð á fleiri vegu til leitar að stökkbreytingum og eflaust hefðu komið fram jákvæð svör þar ef stökkbreyting hefði verið fyrir hendi.
Nokkuð bar á falsk-jákvæðum niðurstöðum í niðurstöðum EMD(TM). Sem skimunaraðferð fyrir stökkbreytingum er EMD(TM) þekkt fyrir mikið næmi en heldur lítið sértæki. Í nokkrum tilfellum kom fram þó nokkur ósértæk mögnun við PCR. Hugsanlegt er að hún hafi verið meiri í einstökum sýnum og á einhvern hátt átt þátt í þessum svörunum. Með hliðsjón af þessu voru umræddir erfðaefnisbútar raðgreindir til frekari greiningar.
Tengsl PPARg2 og offitu eru sterk. Sú stökkbreytingaleit sem var gerð í þessari rannsókn beindist aðeins að afar litlum hluta gens PPARg2. Það er því verðugt verkefni að skoða fleiri svæði þess með þetta ákveðna vandamál í huga. Yen og félagar fundu nýlega erfðabreytileika þar sem alanín kemur í stað prólíns í stöðu 12 PPARg2 (44). Ekki er vitað hvaða hlutverki þetta svæði PPARg2 gegnir(44), en Deeb og félögum tókst að sýna fram á tengsl þessa erfðabreytileika við: minni virkni viðtækisins, lægri líkamsþyngdarstuðul og aukið insúlínnæmi(45).
Í þessari rannsókn var leitað að stökkbreytingunni Pro115Gln og öðrum basabreytingum á svipuðu svæði PPARg2. Skoðaðir voru 43 einstaklingar sem hafa átt við offituvandamál að stríða frá barnæsku. Ekki var að finna neitt óeðlilegt í erfðaefni þessara sjúklinga á þessu afmarkaða svæði PPARg2. Því má álykta að breytileiki á umræddu svæði PPARg2 sé ekki orsakavaldur offitu hjá íslenskum börnum.
Þakkir
Sérstakar þakkir fær starfsfólk rannsóknadeildar Sjúkrahúss Reykjavíkur og aðstoðar- og deildarlæknar barnadeildar Sjúkrahúss Reykjavíkur fyrir aðstoð við sýnatökur.Heimildir
1. Rosenbaum M, Leibel RL, Hirsch J. Obesity. N Engl J Med 1997; 337: 396-407.2. Kuczmarski RJ, Flegal KM, Campell SM, Johnson CL. Increasing prevalence of overweight among US adults: the National Healt and Nutrition Examination Surveys, 1960 to 1991. JAMA 1994; 272: 205-11.
3. McGinnis JM, Foege WH. Actual causes of death in the United States. JAMA 1993; 270: 2207-12.
4. Bouchard C, ed. Genetics of obesity Boca Rohan, ELA. Washington USA: CRC Press; 1994.
5. Willett WC, Dietz WH, Colditz GA. Guidelines for healthy weight. N Engl J Med 1999; 341: 427-34.
6. Van Itallie TB. Health implications of overweight and obesity in the United States. Ann Intern Med 1985; 103: 983-8.
7. Must A, Jacquis PF, Dalla GE, Bajerna CJ, Dietz WA. Long term morbitity and mortality of overweight adolescents: a follow up of the Harvard Growth study of 1922 to 1935. N Engl J Med 1992; 327: 1350-5.
8. Danfoth E Jr, Burger A. The role of thyroid hormones in the control of energy expenditure. Clin Endocrinol Metab 1984; 13: 581-95.
9. Weigle DS, Sande KJ, Iverius PH, Monsen ER, Brunzell JD. Weight loss leads to a marked decrease in nonresting energy expenditure in ambulatory human subjects. Metabolism 1988; 37: 930-6.
10. Leibel RL, Hirsch J. Diminished energy requirements in reduced-obese patients. Metabolism 1984; 33: 164-70.
11. Wadden TA. Treatment of obesity by moderate and severe caloric restriction. results of clinical research trials. Ann Intern Med 1993; 229: 188-93.
12. Rosenbaum M, Leibel RL. Pathophysiology of childhood obesity. Adv Pediatr 1988; 35: 73-137.
13. Steffens AB, Strubbe JH, Balkan B, Scheuring JW. Neuroendocrine mechanisms involved in regulation of body weight, food intake and metabolism. Neurosci Biobehav Rev 1990; 14: 305-13.
14. Flier JS. The adipocyte: storage depot or node on the energy information superhighway? Cell 1995; 80: 15-8.
15. Friedman MI, Tordoff MG, Ramirez I. Intergrated metabolic control of food intake. Brain Res Bull 1986; 17: 855-9.
16. Geary N. Role of gut peptides in meal regulation. In: Weston LA, Savage LM, eds. Obesity: advances in understanding and treatment. Southborough, Mass: International Business Communications; 1996: 2.1.1.-2.1.34.
17. Figlewicz DP, Schwartz MW, Seeley RJ, Chavez M, Baskin DG, Woods SC, et al. Endocrine regulation of food intake and body weight. J Lab Clin Med 1996; 127: 328-32.
18. Rohner-Jeanrenaud F. A neuroendocrine reappraisal of the dual-centre hypothesis: its implications for obesity and insulin resistance. Int J Obes Relat Metab Disord 1995; 19: 517-53.
19. Leibel RL, Berry EM, Hirsch J. Metabolic and hemodynamic responces to endogenous and exogenous catecholamines in formerly obese subjects. Am J Physiol 1991; 260: R785-R791.
20. Landsberg L, Young JB. The role of the sympathoadrenal system in modulating energy expenditure. Clin Endocrinol Metab 1984; 13: 475-99.
21. Aarone LJ, Mackintosh R, Rosenbaum M, Leibel RL, Hirsch J. Autonomic nervous system activity and energy expenditure during weight gain and weight loss. Am J Physiol 1995; 269: R222-R225.
22. Bodurtha JN, Mosteller M, Hewitt JK, Nance WE, Eaves LJ, Moskowitz WB, et al. Genetic analysis of anthropometric measures in 11-year-old twins: The Medical College of Viginia Twin Study. Pediatr Res 1990; 28: 1-4.
23. Börjeson M. The aetiology of obesity in children. Acta Paediatr Scand 1976; 65: 279-87.
24. Brook CG, Huntley RMC, Slack J. Influence of heredity and environment in determination of skinfold thickness in children. BMJ 1975; 28: 719-21.
25. Fabsitz RR, Carmelli D, Hewitt JK. Evidence for independent genetic influences on obesity in middle age. Int J Obes 1992; 16: 657-66.
26. Zhang Y, Proenca R, Maffei M, Barone M, Leopold L, Friedman JM. Poitional cloning of the mouse obese gene and its human homologue [erratum, Nature 1995; 374: 479]. Nature 1994; 372: 425-32.
27. Considine RV, Considine EL, Williams CJ, Nyce MR, Magosin SA, Bauer TL, et al. Evidence against either a premature stop codon or the absence of obese gene mRNA in human obesity. J Clin Invest 1995; 95: 2986-8.
28. Considine RV, Considine EL, Williams CJ, Nyce MR, Zhang P, Opentanova I, et al. Mutation screening and identification of a sequence variation in the human ob gene coding region. Biochem Biophys Res Commun 1996; 220: 735-9.
29. Tontonoz P, Erding H, Graves RA, Budavari AI, Spiegelman BM. mPPARg2: tissue specific regulator of an adipocyte enhancer. Genes Dev 1994; 8: 1224-34.
30. Zhu Y, Qi C, Korenberg JR, Chen XN, Noya D, Sambasiva Rao M, et al. Proc Natl Acad Sci USA 1995; 92: 7921-5
31. Greene ME, Blumberg B, McBride OW, Yi HF, Kronpuist K, Kwan K, et al. Isolation of the human peroxisome proliferator activated receptor gamma cDNA: expression in hematopoietic cells and chromosomal mapping. Gen Expr 1995; 4: 281-99.
32. Beamer BA, Negri C, Yen C-J, Gavrilova O, Rumberger JM, Durcan MJ, et al. Chromosomal localization and partial genomic structure of the human peroxisome proliferator activated receptor gamma (hPPAR-gamma) gene. Biochem Biophys Res Commun 1997; 233: 756-9.
33. Fajas L, Auboeuf D, Raspe E, Schoonjans K, Lefebvre AM, Saladin R, et al. The organization, promoter analysis and expression of the human PPARg gene. J Biol Chem 1997; 272: 18779-89
34. Elbrecht A, Chen Y, Cullinan CA, Hayes N, Leibowitz MD, Moller DE, et al. Molecular cloning, expression and characterization of human peroxisome proliferator activated receptors gamma-1 and gamma-2. Biochem Biophys Res Commun 1996; 224: 431-7.
35. Spiegelman BM, Flier JS. Adipogenesis: rounding out the big picture. Cell 1996; 87: 377-9.
36. Latruffe N, Vamecq J. Peroxisome proliferators and peroxisome proliferator activated receptors (PPARs) as regulators of lipid metabolism. Biochimie 1997; 79: 81-94.
37. Tontonoz P, Hu E, Spiegelman BM. Stimulation of adipogenesis in fibroblasts by PPARg2, a lipid-activated trascription factor. Cell 1994; 79: 1147-56.
38. Lehmann JM, Moore LB, Smith-Oliver TA, Wilkinson WO, Willson TM, Kliewer SA. An antidiabetic thiazolidinedione is a high affinty ligand for peroxisome proliferator-activated receptor gamma (PPARg). J Biol Chem 1995; 270: 12953-6.
39. Kliewer SA, Lenhard JM, Willson TM, Patel I, Morris DC, Lehmann JM. A prostaglandin J2 metabolite binds peroxisome proliferator activated receptor g and promotes adipocyte differentiation. Cell 1995; 83: 813-9.
40. Hu E, Kim JB, Sarraf P, Spiegelman BM. Inhibition of adipogenesis through MAP kinase-mediated phosphorylation of PPARg. Science 1996; 274: 2100-3.
41. Adams M, Reginato MJ, Shao DL, Lazar MA, Chatterjee VK. Transcriptional activation by peroxisome proliferator - activated receptor gamma is inhibitated by phoshorylation at a consensus mitogen-activated protein kinase site. J Biol Chem 1997; 272: 5128-32.
42. Ristow M, Müller-Wieland D, Pfeiffer A, Krone W, Kahn CR. Obesity associated with a mutation in a genetic regulator of adipocyte differentiation. N Eng J Med 1998; 339; 953-9.
43. Stunkard AJ, Sorensen TI, Hanis C, Teasdale TW, Chakraborty R, Schull WJ, et al. An adoption study of human obesity. N Engl J Med 1986; 314: 193-8.
44. Yen CJ, Beamer BA, Negri C, Silver K, Brown KA, Yarnall DP, et al. Molecular scanning of the human peroxisome proliferator activated receptor gamma gene in diabetic Caucasians: identifications of a Pro12Ala PPARg2 missense mutation. Biochem Biophys Res Commun 1997; 241: 270-4.
45. Deeb SS, Fajas L, Nemoto M, Pihlajamaki J, Mykkanen L, Kuusisto J, et al. A Pro12ala substitution in PPARg2 associated with decreased receptor activity, lower body mass index and improved insulin sensitivity. Nature Genet 1998; 20: 284-7.