05. tbl. 94. árg. 2008
Fræðigrein
Smásæ ristilbólga - yfirlit
Ágrip
Hugtakið smásæ ristilbólga er samnefnari fyrir tvo sjúkdóma; bandvefsristilbólgu og eitilfrumu-ristilbólgu. Við ristilspeglun er slímhúðin eðlileg en greining fæst með sýnatöku á ristilslímhúð. Meinafræðilega einkennist bandvefsristilbólga einkum af þykknuðu kollagenlagi undir yfirborðsþekju slímhúðar ristilsins en eitilfrumuristilbólga af eitilfrumuíferð í yfirborðsþekju, kirtilþekju og eiginþynnu slímhúðar án aukningar á kollageni í ristilslímhúðinni. Þó að sjúkdómarnir tveir hafi nokkuð aðgreinanlegt meinafræðilegt mynstur er megineinkenni þeirra beggja langvinnur vatnskenndur niðurgangur án blóðs. Smásæ ristilbólga er talin orsaka um 4-13% langvinns niðurgangs en algengi hennar er mun hærra meðal eldra fólks. Nýgengi bandvefsristilbólgu og eitilfrumuristilbólgu hefur farið mjög hækkandi á síðustu árum. Steralyf eru áhrifaríkustu lyfin við smásærri ristilbólgu og búdesóníð er mest rannsakaða og best staðfesta meðferðin. Tilgangur þessarar yfirlitsgreinar er að kynna tvo tiltölulega nýja sjúkdóma sem eru ein algengasta ástæða langvinns niðurgangs, sérstaklega meðal eldra fólks.
Inngangur
Smásæ ristilbólga (microscopic colitis, MC) er ástæða langvinns niðurgangs í um 4-13% tilfella (1). Algengið er mun hærra meðal eldra fólks (>60 ára) (1). Smásæ ristilbólga er samnefnari fyrir tvo sjúkdóma; bandvefsristilbólgu (collagenous colitis, CC) og eitilfrumuristilbólgu (lymphocytic colitis, LC). Þótt sjúkdómarnir hafi nokkuð aðgreinanleg meinafræðileg mynstur er megineinkenni beggja langvinnur vatnskenndur niðurgangur án blóðs. Sjúkdómarnir koma aðallega fram hjá eldra fólki, einkum konum (2). Við ristilspeglun er slímhúðin yfirleitt eðlileg og greining fæst eingöngu með sýnatöku úr ristilslímhúð. Við smásjárskoðun sést ristilbólga með ákveðnum meinafræðiskilmerkjum. Meinafræðilega einkennist bandvefsristilbólga af þykknuðu kollagenlagi undir yfirborðsþekju slímhúðar ristilsins (3, 9) en eitilfrumuristilbólga af eitilfrumuíferð í yfir-borðsþekju, kirtilþekju og eiginþynnu slímhúðar án aukningar á kollageni í ristilslímhúðinni (5, 10). Því hefur verið haldið fram að sameiginleg orsök sé fyrir sjúkdómunum tveimur og vegna mjög áþekkrar klínískrar myndar hefur hugtakið "watery diarrhea-colitis syndrome" verið sett fram (7-8). En þrátt fyrir sömu einkenni er margt sem bendir til þess að þetta séu tveir sjúkdómar eins og rætt verður hér að neðan.
Bandvefsristilbólgu var fyrst lýst árið 1976 en eitilfrumuristilbólgu árið 1989 (9-10). Síðan þá hefur fjöldi rannsókna birst um sjúkdómana tvo sem styrkt hefur fræðilega tilurð þeirra. Smásæ ristilbólga hefur verið nokkuð rannsökuð í Bandaríkjunum og Evrópu og meðal annars á Íslandi en ekki hefur verið skrifað um smásæja ristilbólgu á íslensku svo höfundar viti til. Tilgangurinn með þessari yfirlitsgrein er að kynna tvo tiltölulega nýja sjúkdóma (CC og LC) sem eru ein algengasta ástæða langvinns niðurgangs, sérstaklega meðal eldra fólks.
Faraldsfræði
Smásæ ristilbólga var áður sjaldgæf en er nú allalgeng orsök langvinns niðurgangs, ekki síst hjá eldra fólki, einkum á Vesturlöndum. Hún er talin orsaka á bilinu 4-13% langvinns niðurgangs en hlutfallslegt algengi hennar er mun hærra meðal eldra fólks (2). Nýgengi CC og LC hefur farið mjög hækkandi á síðustu árum eins og sést vel í faraldsfræðilegum rannsóknum frá Örebro í Svíþjóð og Olmstead-sýslu í Minnesóta þar sem nýgengið hefur verið kannað reglulega frá árunum 1984-85 þar til nú (11). Hækkaði nýgengi LC í Olmstead-sýslu úr 0,5 á hverja 100.000 íbúa á ári á tímabilinu 1985-88 upp í 12,9 á tímabilinu 1997-2001 sem er hæsta nýgengi sem hefur verið birt (12). Í Svíþjóð jókst nýgengi CC frá 0,8 á hverja 100.000 íbúa á ári tímabilið 1984-1988 í 6,1 tímabilið 1996-1998 (1, 4). Nýgengi MC mælist í sumum löndum nú hærra en nýgengi sáraristilbólgu og Crohns sjúkdóms (1, 11). En eins og með marga aðra sjúkdóma er óvíst hvort um raunverulega aukningu nýgengis sé að ræða eða aukna vitund um sjúkdóminn og betri greiningu.
Ekki eru til miklar heimildir um faraldsfræði MC þegar kemur að heilum þjóðum en rannsókn sem gerð var á Íslandi og náði til alls landsins sýndi nýgengi sem er með því hæsta sem mælst hefur, þrátt fyrir að ströng meinafræðileg skilmerki væru notuð til greiningar (13). Fyrrgreind rannsókn náði yfir alla sem greindust með MC yfir fimm ára tímabil, frá 1995-1999. Í rannsókninni greindust 125 manns með MC, þar af 71 með CC og 54 með LC. Meðaltalsnýgengi CC var 5.2 og LC 4.0 á hverja 100.000 íbúa á ári. Þetta er eina rannsóknin á smásærri ristilbólgu svo vitað sé sem tekur til heillar þjóðar.
Báðir sjúkdómarnir eru algengari í konum en körlum. CC hefur mælst allt að 15 sinnum algengari í konum en körlum en að meðaltali er hann um 4-5 sinnum algengari (2). Minni kynjamunur er í LC og hafa sumar rannsóknir ekki sýnt fram á neinn kynjamun. Að meðaltali er LC þó um 2-3 sinnum algengari í konum en körlum (14).
Algengi beggja sjúkdóma eykst með hækkandi aldri. Meðalaldur sjúkdómanna tveggja er í flestum rannsóknum milli 60-70 ár (2). Í íslensku rannsókninni var meðalaldur fyrir CC 66 ár og fyrir LC 69 ár, en það er heldur hærri aldur en aðrar rannsóknir hafa sýnt. Báðir sjúkdómar hafa greinst í börnum en það er þó afar sjaldgæft (15).
Meinafræði
Greining á smásærri ristilbólgu byggir á útliti sýna frá ristilslímhúð við smásjárskoðun (2), enda er meðal skilgreiningaratriða bæði bandvefsristilbólgu og eitilfrumuristilbólgu að slímhúð ristilsins sé innan eðlilegra marka þegar hún er skoðuð með berum augum eða í gegnum speglunartæki.

Mynd 1. Bandvefsristilbólga (CC). Hvíta örin bendir á verulega þykknað lag kollagens undir yfirborðsþekju slímhúðar. Svarta örin sýnir hrörnaða yfirborðsþekju sem losnað hefur frá undirliggjandi vef. (Stækkun er x300)
Smásjárgreining bandvefsristilbólgu (mynd 1) byggist á því að veruleg þykknun komi fram á grunnhimnu (basement membrane) svæði undir yfirborðsþekju slímhúðar. Þannig kemur fram bandvefsþykknun (kollagen-útfellingar) á grunnhimnusvæði sem nemur að minnsta kosti 10 microna þykkt, en í sumum tilvikum er skilgreiningin miðuð við 15 microna þykkt. Jafnframt hefur fjölgað bólgufrumum í eiginþynnu slímhúðar, einkum eitilfrumum og plasmafrumum. Yfirborðsþekja slímhúðar getur verið innan eðlilegra marka en gjarnan koma fram hrörnunarbreytingar í yfirborðsþekju með losi þekju frá undirliggjandi eiginþynnu eða grunnhimnu og byrjandi yfirborðs sármyndun (16-18).
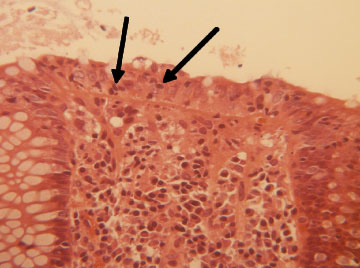
Mynd 2. Eitilfrumuristilbólga (LC). Örvarnar á myndinni benda á eitilfrumur (litlu dökku kjarnarnir) innan um yfirborðsþekjufrumur. (Stækkun er x500)
Smásjárgreining eitilfrumuristilbólgu (mynd 2) byggir að hluta til á svipuðu útliti og sést í bandvefsristilbólgu. Þar kemur fram aukning bólgufrumna í eiginþynnu, einkum eitilfrumna og plasmafrumna en minna af kleyfkirndum bólgufrumum. Einnig er gjarnan til staðar hrörnun á yfirborðsþekju og jafnvel losnar yfirborðsþekjan frá undirliggjandi eiginþynnu slímhúðar. Hins vegar sést ekki þykknun á grunnhimnu slímhúðar undir yfirborðsþekju á sama hátt og í bandvefs-ristilbólgu. Mikilvægasta atriðið við greiningu á eitilfrumuristilbólgu er þó veruleg fjölgun eitilfrumna inni á milli kirtilþekjufrumna, einkum í yfirborðsþekju slímhúðar en einnig þekjufrumna í kirtlum. Miðað er við að fjöldi eitilfrumna inni á milli yfirborðsþekjufrumna sé meiri en 20 eitilfrumur á hverjar 100 þekjufrumur (16, 18-20).
Þessi lýsing hér að ofan rekur þau greiningarskilmerki sem nauðsynlegt er að uppfylla svo unnt sé að gefa afdráttarlausa greiningu á smásærri ristilbólgu. Hins vegar kemur gjarnan fyrir að sýni þau sem tekin eru til mats kveikja grun um smásæja ristilbólgu þó ekki náist að fullnægja þeim ströngu greiningarskilmerkjum sem að ofan er lýst. Í þeim tilvikum er stungið upp á eitilfrumuristilbólgu eða bandvefsristilbólgu þótt afdráttarlaus greining sé ekki gefin.
Yfirleitt eru sýni tekin frá hægri hluta ristils eða þverristli líklegri til að hafa einkennandi skilmerki til greiningar á smásærri ristilbólgu og er því mælt með að gerð sé full ristilspeglun ef grunur leikur á að um slíka ristilbólgu geti verið að ræða. Rétt er einnig að mæla með að tekin séu sýni nokkuð víða úr slímhúð ristilsins því vel er þekkt að ekki er allur ristillinn með sambærilegum smásjárbreytingum og því er vel mögulegt að greining náist ekki ef aðeins fá sýni eru tekin til vefjarannsóknar (13, 17).
Meingerð
Orsakir og meinalífeðlisfræði sjúkdómanna tveggja er ekki vel þekkt en töluverðar rannsóknir eru í gangi og þekking á eðli þeirra fer stigvaxandi. Umdeilt er hve skyldir sjúkdómarnir eru. Þó að vefjameinafræði þeirra sé að miklu leyti lík og einkenni svipuð hafa langtíma rannsóknir ekki sýnt fram á þá tilhneigingu að annar hvor sjúkdómurinn þróist yfir í hinn (3, 6, 21). Ýmsar tilgátur hafa verið settar fram um orsakir. Engin þeirra er þó fullnægjandi þar sem yfirleitt er um að ræða smáar rannsóknir eða veik merki þess eðlis að um orsakasamband sé að ræða.
Athyglisvert er að alvarleiki niðurgangs virðist vera í réttu hlutfalli við bólgubreytingar í eiginþynnu slímhúðar (lamina propria) en þó ekki samhengi við þykkt kollagens í CC (22). Líklega orsakast niðurgangurinn einna helst af minnkuðu frásogi natríumklóríðs auk virkrar klórseytrunar (23). Einnig er um að ræða fækkun á þéttitengjum (tight junctions) í ristlinum sem eykur frekar á niðurgang vegna aukins bakleka (23).
Erfðir
Nokkuð er um rannsóknir sem hafa stutt þátt erfða í smásærri ristilbólgu (24-26). Enn frekar hafa sumar rannsóknir haldið fram tengslum milli MC og annarra bólgusjúkdóma í þörmum (2, 24-25, 27). Óvíst er með þau tengsl þar sem rannsóknir að því lútandi eru frekar smáar og orsakatengslin hafa ekki reynst mjög sterk (28). Nokkuð er um að sumir í sömu fjölskyldu hafi annaðhvort fengið CC eða LC sem styður ættlægni.
Óæskilegir holrúms (luminal) þættir
Því hefur verið haldið fram að óæskilegir holrúmsþættir séu upphafs áhrifaþættir meingerðarinnar (11). Talið er að óæskilegir holrúmsþættir valdi upphaflega slímhúðarskaða sem setji meingerðarferlið í gang og í kjölfarið myndist bólga og einnig kollagen-útfellingar. Þessi kenning hefur verið studd með margvíslegum hætti. Í fyrsta lagi með árangri af hjáveituaðgerðum (29). Sjúkdómseinkenni hafa haft tilhneigingu til að taka sig aftur upp þegar dausgarnarhjáveitu er lokað. Í öðru lagi að elemental-fæði (fæði sem samanstendur af auðmeltanlegum próteinum, kolvetnum og fitum) hefur minnkað niðurganginn til muna hjá sjúklingum með MC (30). Í þriðja lagi með árangri lyfsins cholestýramín. Það lyf bindur bæði niðurbrotsefni baktería og gall.
Bakteríusýkingar
Því hefur verið haldið fram að ýmsar bakteríusýkingar geti orsakað smásæja ristilbólgu. Á meðal þessara baktería er Yersinia enterocolitica sem nefnd hefur verið í tengslum við CC (31). Í einni slíkri rannsókn ræktaðist Yersinia í helmingi sjúklinga með CC og í annarri rannsókn kom í ljós að mótefni gegn Yersinia voru algengari en í viðmiðunarhóp (31-32). Einnig hafa verið sett fram tengsl milli Clostridium difficile og Campylobacter jejuni og CC (33-36). Algengast er þó að hægðaræktanir séu neikvæðar hjá sjúklingum með MC og er því orsakasamhengið við ofannefndar bakteríur óljóst.
Gallsaltavan-frásog
Algengt er að gallsaltavan-frásog sé meðfylgjandi smásærri ristilbólgu og geri einkennin verri fyrir vikið. Gallsaltavan-frásog hefur fundist hjá á milli 27-44% sjúklinga með CC og hjá 9-60% sjúklinga með LC (37-38). Breytingar sjást í lokahluta dausgarnar (ileum) sem geta útskýrt gallsalta-?van-frásogið (38-40). Einnig hafa rannsóknir með svokölluðu SeHCAT prófi sýnt fram á gallsalta-van-frásog (38, 41). Til að styðja þessa kenningu enn frekar hefur meðferð með gallbindandi lyfjum á borð við cholestýramín verið sérstaklega virk fyrir þá sem hafa gallsaltavan-frásog en athyglisvert er að hún hefur einnig gagnast vel fyrir þá sjúklinga sem ekki hafa frásogsvandamálið, sem gæti skýrst af bindingu þess við óæskilega holrúmsþætti, samanber að ofan.
Áhrif lyfja
Talsvert af rannsóknum, sérstaklega tilfellarannsóknum (case studies), hafa sett fram hugmyndir um orsakasamhengi milli ýmissa lyfja og MC. Til að reyna að nálgast viðfangsefnið nánar hafa Beaugerie og Pardi sett fram matskerfi til að meta áhrifin (42). Með aðferð sinni töldu þeir sig komast að því að um 17 lyf hefðu sterk eða meðalsterk tengsl við smásæja ristilbólgu. Þau lyf sem þeir töldu hafa sterk tengsl voru: akarbósi, aspirín, lanzaprazól, bólgueyðandi gigtarlyf, ranitidín, sertralín og ticlídópín. Þau sem höfðu meðalsterk tengsl voru karbamazepín, flútamíl, lísínópríl, levódópa, oxetórón, paroxetín, simvastatín, tardýferón, og vinbúrnín (42).
Sérstaklega hefur verið haldið fram tengslum við bólgueyðandi gigtarlyfjaflokkinn (43-48). Rannsóknir hafa getað sýnt fram á að til muna dragi úr einkennum við það að hætta inntöku lyfjanna og jafnvel hefur verið sýnt fram á að meinafræðibreytingar minnki (43, 49-50). Einnig hafa rannsóknir sýnt fram á versnun einkenna þegar inntaka gigtarlyfjanna er hafin að nýju (51). Ekki hafa þó allar rannsóknir getað sýnt fram á þessi tengsl og í íslenskri rannsókn er bíður birtingar var ekki um bein tengsl á milli gigtarlyfjainntöku og einkenna MC (22, 52). Að vissu leyti gerir það túlkun rannsókna erfiða að sjúklingar með smásæja ristilbólgu hafa gjarnan liðverki af ýmsum orsökum og þurfa því á gigtarlyfjum að halda.
Nitric oxíð (NO)
Nitric oxíð er aukið til muna í ristilslímhúð sjúklinga með smásæja ristilbólgu. Orsakast það af fjölgun á nitrít oxíð synthetasa (iNOS) í ristil-slímhúðinni (53-55). Magn NO í ristlinum hefur reynst í réttu hlutfalli við meinafræðilegar breytingar og alvarleika einkenna (53). Óvíst er þó hvort NO sé skaðvaldur eða endurspegli aðeins sjúkdómsvirknina.
Tengsl við aðra sjúkdóma
Glúteinsjúkdómur
Ýmsir höfundar hafa haldið fram tengslum milli MC og glútein (Celiac) sjúkdóms (56-57). Um 10% sjúklinga með MC hafa glúteinsjúkdóm og um 25% sjúklinga með glúteinsjúkdóm hafa MC. Vegna þessa telja ýmsir að rétt sé að rannsaka alla nýgreinda sjúklinga með MC með tilliti til glúteinóþols. Þessu til stuðning hefur allt að þriðjungur sjúklinga með glúteinóþol meinafræðilegar breytingar sem gætu samrýmst smásærri ristilbólgu (2). Því verður að hafa smásæjar ristilbólgur í huga hjá sjúklingum með glúteinóþol einkum þeim sem ekki svara glúteinsnauðu fæði. Til þess að flækja málið enn frekar mælast ekki antigliadin, antiendomysial og anti-tissue transglutaminase mótefni í marktækt auknum mæli hjá sjúklingum með MC í samanburði við almennt þýði (58-60). Því eru tengsl þessara sjúkdóma nokkuð umdeild.
Sjálfsofnæmissjúkdómur
Þeirri spurningu hefur verið kastað fram hvort smásæ ristilbólga geti verið sjálfsofnæmissjúkdómur þar sem sjúklingarnir hafa sjúkdóma á borð við skjaldkirtilssjúkdóma, glúteinóþol, sykursýki, iktsýki, astma og ofnæmi oftar en búast mætti við (11, 61-63). Þessu til stuðnings hefur verið sýnt fram á að sjálfsmótefni mælast í allt að 40-50% sjúklinga þótt þau séu ósértæk. Gigtarþáttur (rheumatoid factor), antinuclear, antimitochondrial og ANCA mælast öll heldur oftar hjá þessum sjúklingum en samanburðarhópi. Sjálfsmótefni eru þó algengari í CC (53%) en í LC (26%) (63-64). Smásæ ristilbólga er líkt og sjálfsofnæmissjúkdómar yfirleitt algengari í konum. Auk þessa eru frásagnir um hjöðnun sjúkdóms á meðgöngu sem gæti stutt sjálfsofnæmistilgátuna enn frekar.
Hér hafa verið tíundaðar nokkrar kenningar um orsök og meingerð smásærrar ristilbólgu en engin þeirra er að öllu leyti fullnægjandi. Líklegt er að hér sé á ferð samspil margvíslegra þátta, bæði erfða og umhverfis. Þar má hugsa sér að ákveðnir ytri þættir komi sjúkdómsferli í gang hjá viðkvæmum einstaklingum, ekki síst þeim sem hafa erfanlega tilhneigingu til sjálfsofnæmissjúkdóma.
Klínísk einkenni
Einkenni CC og LC eru afar lík og því ómögulegt að aðgreina sjúkdómana á klínískum grunni. Megineinkenni beggja sjúkdómanna er óblóðugur vatnskenndur niðurgangur. Nokkur breytileiki getur verið í magni niðurgangsins. Hann getur verið allt að tveir lítrar hægða á dag (61). Klínískur sjúkdómsgangur er gjarnan lotubundinn en stundum samfelldur. Algengt er að tíðni niðurgangsins sé á milli 4-10 sinnum á dag. Í aftursærri rannsókn frá árinu 1996 á 163 CC sjúklingum kom í ljós að 58% sjúklinga höfðu hæggenga byrjun en 42% bráða (61). Meirihluti sjúklinga hafði hægðir 4-9 sinnum á dag (66%) en um 22% oftar en 10 sinnum á dag. Aðeins 27% höfðu niðurgang að nóttu til. Önnur einkenni voru: þyngdartap (42%), kviðverkir (41%) og þreyta (24%) (61).
Auk niðurgangs er gjarnan um önnur einkenni að ræða frá meltingarvegi. Þau geta verið vægir kviðverkir, ógleði, bráð hægðaþörf og hægðaleki. Einnig þekkjast vel einkenni utan meltingarvegar, svo sem liðverkir, liðbólgur eða æðahjúpsbólga (uveitis). Þó hér sé ekki um sjúkdóm sem styttir líf að ræða geta lífsgæði sjúklinga verið töluvert skert (2).
Vefjasýni við ristilspeglun
Eins og fyrr segir og nafnið reyndar gefur til kynna fæst greining með vefjasýni og yfirleitt er um að ræða eðlilega slímhúð við ristilspeglun. Þó getur sést vægur roði, bjúgur og auðsæranleiki (friability). Útbreiðsla og svæsni breytinganna hefur tilhneigingu til að minnka þegar neðar dregur í ristlinum. Því eru sýni frá hægri hluta ristils talin æskileg. Þetta er þó nokkuð umdeilt meðal meltingarlækna og ber rannsóknum ekki alveg saman. Sumar rannsóknir benda til þess að það dugi að taka sýni við bugaristilsspeglun (sigmoidoscopy) (65) en aðrar rannsóknir mæla gegn því (13). Í aftursærri rannsókn kom í ljós að sjúkdómarnir fundust í 83% tilfella í þverristli, 70% í hægri ristli en 66% í bugðuristli (66). Í annarri rannsókn var munurinn enn meiri milli svæða ristilsins. Þar var sýnt fram á að stök sýnataka frá bugðuristli hefði misst af greiningu í allt að 40% tilfella (67-68). Þessu til stuðnings getur dreifing smásærrar ristilbólgu í ristlinum verið gloppótt, það er með eðlilegri slímhúð inn á milli og helst er það á svæði bugðuristilsins. Því er fullkomin ristilspeglun með töku margra sýna æskileg til að greina smásæja ristilbólgu með vissu og ekki síður til að útiloka aðra sjúkdóma í ristli.
Meðferð
Til að byrja með er mikilvægt að upplýsa sjúklinginn um að þó að sjúkdómurinn geti verið langvinnur og afar hvimleiður er ekkert sem bendi til þess að hann stytti lífslíkur. Gera þarf sjúklingnum grein fyrir því að gjarnan komi góð tímabil á víxl við slæm og niðurgangurinn geti verið daglegur sem og lotubundinn. Vegna ofannefndra tengsla við bólgueyðandi gigtarlyf er mælt með því að stöðva inntöku þeirra (43-44, 69). Sjúklingar með glúteinóþol þurfa að vera á glúteinsnauðu fæði. Einnig er rétt að íhuga takmarkanir á neyslu koffeins, áfengis og mjólkurvöru sem geta gert sjúkdómseinkennin verri (2).
Lyf

Áður en einstakir lyfjahópar eru ræddir er mikilvægt að koma því á framfæri að ekki er við stórar slembirannsóknir að styðjast. Um er að ræða rannsóknir á fáum sjúklingum eða álit sérfræðinga. Í töflu I má sjá yfirlit yfir helstu lyf og skammtastærðir sem notuð eru gegn MC.
Hægðastoppandi lyf
Ýmsir höfundar hafa mælt með lóperamíði (Imodium) sem fyrsta lyfi við vægum sjúkdómi (70). Ekki eru til neinar rannsóknir á hægðastoppandi lyfjum en klínísk reynsla þeirra er ágæt. Lyfin hafa líklega lítil sem engin áhrif á sjúkdómsganginn sem slíkan heldur er eingöngu um einkennastillandi meðferð að ræða. Hægt er að nota hægðastoppandi lyf ein og sér í vægum sjúkdómi en einnig ásamt öðrum lyfjum.
Steralyf
Steralyf eru áhrifaríkustu lyfin við MC. Búdesóníð er mest rannsakaða og best staðfesta meðferðin. Þó að prednisólón sé einnig áhrifaríkt hefur það mun meiri aukaverkanir en búdesóníð (71). Þar sem oft er um langtímameðferð ræða er prednisólon ekki æskilegt lyf. Þrjár framsýnar slembirannsóknir hafa kannað áhrif búdesóníðs (72-74). Þó rannsóknirnar séu ekki stórar bætir búdesóníð (9 mg/dag) marktækt einkenni sjúklinganna í þeim öllum auk þess að bæta lífsgæði þeirra. Í kerfisbundinni greiningu (meta analysis) á þessum þremur rannsóknum reyndist hlutfallslíku-hlutfall (odds ratio) 12,3 (95% CI: 5,5-27,5) og aðeins þurfti að meðhöndla tvo sjúklinga fyrir hvern einn sem fékk sjúkdómshlé (number needed to treat) (75). Allar þessar rannsóknir mældu þó aðeins áhrif búdesóníðs yfir 6-8 vikna meðferðartímabil. Flest allir sjúklingarnir svöruðu meðferðinni á 2-4 vikum og vefjameinafræðileg svörun kom í ljós í öllum þremur rannsóknunum. Þrátt fyrir þessar jákvæðu niðurstöður var bakslagstíðni sjúkdóms há og átti sér stað í um 61-80% meðhöndlaðra sjúklinga og meðaltími að endurkomu einkenna var aðeins tvær vikur eftir að meðferð var stöðvuð (72-74). Í einni víxlrannsókn (crossover study) fengu 61% sjúklinga endurkomu einkenna innan tveggja vikna eftir að þeir fóru á lyfleysu (76). Þess ber þó að geta að sýnt hefur verið fram á árangur af lægri skömmtum af búdesóníð 3-6 mg/dag sem viðhaldsmeðferð (77). Það standa nú yfir rannsóknir sem meta ávinning af langvinnri búdesóníð meðferð.
Salicýlsýra og skyld lyf (5-ASA)
Sulfasalazin og mesalazín hafa nokkuð verið notuð í smásærri ristilbólgu án þess að stórar rannsóknir hafi legið þar að baki. Nokkrar litlar aftursæjar rannsóknir hafa sýnt fram á 21-50% árangur með notkun þessara lyfja. Þau hafa ekki verið borin saman við búdesóníð en eru að öllum líkindum áhrifaminni (61-62, 78).
Kólestýramín
Kólestýramín hefur verið notað með ágætis árangri en ýmsir þola lyfið illa vegna aukaverkana (38, 78). Lyfið hefur lítið verið notað á Íslandi (52).
Bismút (Bismuth subsalicylate)
Bismút hefur gefið ágætis árangur við smásærri ristilbólgu. Ein framsýn rannsókn sýndi fram á sjúkdómshlé í 11 af 13 sjúklingum og meinafræðilegan bata hjá níu þeirra (79). Í frekari slembiraðaðri framsýnni rannsókn kom þessi niðurstaða einnig í ljós (80). Afar fáir sjúklingar hafa verið meðhöndlaðir með þessu lyfi hér á landi enda ekki fáanlegt nema með sérpöntun. Mæla ýmsir höfundar með því áður en gripið er til steralyfja (2).
Skurðaðgerðir
Hjáveituaðgerð kemur til greina gegn erfiðum sjúkdómi sem svarar ekki lyfjameðferð (29). Í rannsókn þar sem gerð var hjáveituaðgerð hjá níu sjúklingum með bandvefsristilbólgu stöðvaðist niðurgangurinn hjá öllum og kollagenþykktin varð eðlileg hjá öllum ef sýni voru tekin eftir hjáveituna (29). Þessar niðurstöður styðja kenninguna um að fráveituaðgerð losi ristilinn við óæskilega holrúmsþætti sem virðast skipta máli, ekki síst í þrálátum sjúkdómi. Vægi skurðaðgerða er þó afar takmarkað í meðferðinni.
Horfur og gangur
Smásæ ristilbólga er ekki lífshættulegur sjúkdómur þó einkennin geti skert lífsgæðin. Náttúrulegur sjúkdómsgangur smásærra ristilbólgna er ekki vel þekktur en í nokkrum rannsóknum hefur sjúklingum verið fylgt eftir í lengri tíma. Í flestum tilfellum virðist sjúkdómsgangurinn vera frekar mildur. Ýmsir höfundar telja sjúkdómsgang LC vera mildari en í CC (20-21). Í rannsókn sem fylgdi 27 LC sjúklingum eftir í að meðaltali 38 mánuði hætti niðurgangurinn í 93% tilfella og meinafræðilegur bati sást í 82% sjúklinga og ekki sást breyting yfir í CC í neinu tilfelli (21). Ekki hefur náðst slíkur árangur í rannsóknum sem hafa fylgt CC sjúklingum eftir (81). Í rannsókn þar sem borinn var saman sjúkdómsgangur 96 sjúklinga með CC við 80 með LC reyndist marktækt betri árangur í LC hópnum en í CC hópnum (20). Í íslensku rannsókninni var ekki marktækur munur á einkennum CC og LC þó að tilhneiging hafi verið yfir í vægari einkenni hjá LC sjúklingum eftir að meðaltali 6,4 ár (52). Öfugt við aðrar ristilbólgur, sérstaklega sáraristilbólgu, hafa smásæjar ristilbólgur ekki verið tengdar við aukna áhættu á ristilkrabbameini (11, 82).
Heimildir
1. Olesen M, Eriksson S, Bohr J, Jarnerot G, Tysk C. Microscopic colitis: a common diarrhoeal disease. An epidemiological study in Orebro, Sweden, 1993-1998. Gut 2004; 53: 346-50.
2. Pardi DS. Microscopic colitis: an update. Inflamm Bowel Dis 2004; 6: 860-70.
3. Lee E, Schiller LR, Vendrell D, et al. Subepithelial collagen table thickness in colon specimens from patients with microscopic colitis and collagenous colitis. Gastroenterology 1992; 103: 1790-6.
4. Bohr J, Tysk C, Eriksson S, et al. Collagenous colitis in Örebro, Sweden an epidemiological study 1984-1993. Gut 1995; 37: 394-7.
5. Mills LR, Schuman BM, Thompson WO. Lymphocytic colitis: A definable clinical and histological diagnosis. Dig Dis Sci 1993; 38: 1147-51.
6. Veress B, Löfberg R, Bergman L. Microscopic colitis syndrome. Gut 1995; 36: 880-6.
7. Jessurun J, Yardley JH, Lee EL, et al. Microscopic and collagenous colitis: Different names for the same condition Gastroenterology 1986; 91: 1583-4.
8. Sylwestrowicz T, Kelly JK, Hwang WS, Shaffer EA. Collagenous colitis and microscopic colitis: the watery diarrhea-colitis syndrome. Am J Gastroenterol 1989; 84: 763-8.
9. Lindström CG. "Collagenous colitis" with watery diarrhoea - a new entity Pathol Eur 1976; 11: 87-9.
10. Lazenby AJ, Yardley JH, Giardiello FM, Jessurun J, Bayless TM. Lymphocytic ("microscopic") colitis: a comparative histopathologic study with particular reference to collagenous colitis. Hum Pathol 1989; 20: 18-28.
11. Nyhlin N, Bohr J, Erkiksson C. Systematic review: microscopic colitis. Alimentary Pharmacology & Therapeutics 2006; 23: 1525-34.
12. Pardi DS, Smyrk TC, Kammer P, et al. The epidemiology of microscopic colitis: a population-based study in Olmsted County, MN. Gut 2007; 4: 504-8.
13. Agnarsdóttir M, Gunnlaugsson O, Örvar KB, et al. Collagenous and lymphocytic colitis in Iceland. Dig Dis Sci 2002; 47: 1122-8.
14. Jackson BK. Are collagenous colitis and lymphocytic colitis distinct syndromes? Dig Dis 1995; 13: 301-11.
15. Gremse DA, Boudreaux CW, Manci EA. Collagenous colitis in children. Gastroenterology 1993; 104: 906-9.
16. Bogomoletz WV. Collagenous, microscopic and lymphocytic colitis. An evolving concept. Virchows Arch 1994; 424: 573-9.
17. Goff JS, Barnett JL, Pelke T, et al. Collagenous colitis: histopathology and clinical course. Am J Gastroenterol 1997; 92: 57-60.
18. Tremaine WJ. Collagenous colitis and lymphocytic colitis. J Clin Gastroenterol 2000; 30: 245-9.
19. Lazenby A, Yardley J, Giardiello FM, Jesserun J, Bayless T. Lymphocytic (microscopic) colitis. A comprehensive histopathologic study, with particular reference to collagenous colitis. Hum Pathol 1989; 20: 18-28.
20. Baert F, Wouters K, D'Haens G, et al. Lymphocytic colitis. A distinct entity - A clinicopathological confrontation of lymphocytic and collagenous colitis. Gut 1999; 45: 375-81.
21. Mullhaupt B, Guller U, Anabitarte M, et al. Lymphocytic colitis. Clinical presentation and long term course. Gut 1998; 43: 629-33.
22. Tremaine WJ. Diagnosing collagenous colitis: Does it make a difference? Eur J Gastroenterol Hepatol 1999; 11: 477-9.
23. Burgel N, Bojarski C, Mankertz J, et al. Mechanisms of diarrhea in collagenous colitis. Gastroenterology 2002; 123: 433-43.
24. Abdo AA, Zetler PJ, Halparin LS. Familial microscopic colitis. Can J Gastroenterol 2001; 15: 341-3.
25. Jarnerot G, Hertervig E, Granno C, et al. Familial occurrence of microscopic colitis: a report on five families. Scand J Gastroenterol 2001; 36: 959-62.
26. van Tilburg AJ, Lam HG, Seldenrijk CA, et al. Familial occurrence of collagenous colitis. A report of two families. J Clin Gastroenterol 1990; 12: 279-85.
27. Kong SC, Keogh S, Carter MJ, et al. Familial occurrence of microscopic colitis. Scand J Gastroenterol 2002; 37: 1344-5.
28. Chutkan R, Sternthal M, Janowitz HD. A family with collagenous colitis, ulcerative colitis, and Crohn's disease. Am J Gastroenterol. 2000; 95: 3638-41.
29. Jarnerot G, Tysk C, Bohr J, et al. Collagenous colitis and fecal stream diversion. Gastroenterology 1995; 109: 449-55.
30. Jensen L, Munck LK. Elementary diet reduces diarrhoea associated with microscopic colitis. Scand J Gastroenterol 2005; 40: 1495-6.
31. Bohr J, Nordfelth R, Jarnerot G, Tysk C. Yersinia species in collagenous colitis: a serologic study. Scand J Gastroenterol 2002; 37: 711-4.
32. Makinen M, Niemela S, Lehtola J, Karttunen TJ. Collagenous colitis and Yersinia enterocolitica infection. Dig Dis Sci 1998; 43: 1341-6.
33. Khan MA, Brunt EM, Longo WE, Presti ME. Persistent Clostridium difficile colitis: a possible etiology for the development of collagenous colitis. Dig Dis Sci 2000; 45: 998-1001.
34. Treanor D, Gibbons D, O' Donoghue DP, Sheahan K. Pseudomembranes on collagenous colitis. Histopathology 2001; 38: 83-4.
35. Vesoulis Z, Lozanski G, Loiudice T. Synchronous occurrence of collagenous colitis and pseudomembranous colitis. Can J Gastroenterol 2000; 14: 353-8.
36. Erim T, Alazmi WM, O'Loughlin CJ, Barkin JS. Collagenous colitis associated with Clostridium difficile: a cause effect. Dig Dis Sci 2003; 48: 1374-5.
37. Fernandez-Banares F, Esteve M, Salas A, et al. Bile acid malabsorption in microscopic colitis and in previously unexplained functional chronic diarrhea. Dig Dis Sci 2001; 46: 2231-8.
38. Ung KA, Kilander A, Willen R, Abrahamsson H. Role of bile acids in lymphocytic colitis. Hepatogastroenterology 2002; 49: 432-7.
39. Padmanabhon V, Callas PW, Li SC, et al. Histopathological features of the terminal ileum in lymphocytic and collagenous colitis: a study of 32 cases and review of the literature. Mod Pathol 2003; 16: 115-9.
40. Sapp H, Ithamukkala S, Brien TP, et al. The terminal ileum is affected in patients with lymphocytic or collagenous colitis. Am J Surg Pathol 2002; 26: 1484-92.
41. Marteau P, Lavergne-Slove A, Lemann M, et al. Primary villous atrophy is often associated with microscopic colitis. Gut 1997; 41: 561-4.
42. Beaugerie L, Pardi DS. Review article: Drug-induced microscopic colitis - proposal for a scoring system and review of the literature. Aliment Pharmacol Ther 2005; 22: 277-84.
43. Giardiello FM, Hansen FC III, Lazenby AJ, et. al. Collagenous colitis in setting of nonsteroidal anti-inflammatory drugs and antibiotics. Dig Dis Sci 1990; 35: 257-60.
44. Riddell RH, Tanaka M, Mazzoleni G. Non-steroidal anti-inflammatory drugs as a possible cause of collagenous colitis: A case-control study. Gut 1992; 33: 683-6.
45. Stampfl ME, Friedman LS. Collagenous colitis. Pathophysiologic considerations. Dig Dis Sci 1991; 36: 705-11.
46. Katanuma A, Kodama T, Tamaki T, et al. Collagenous colitis. Intern Med 1995; 34: 195-8.
47. Bjarnason I, Hayllar J, MacPherson AJ, Russell AS. Side effects of nonsteroidal anti-inflammatory drugs on the small and large intestine in humans. Gastroenterology 1993; 104: 1832-47.
48. Puspok A, Kiener HP, Oberhuber G. Clinical, endoscopic, and histologic spectrum of nonsteroidal anti-inflammatory drug-induced lesions in the colon. Dis Colon Rectum 2000; 43: 685-91.
49. Giardiello FM, Hansen FC, Lazenby AJ, et al. Collagenous colitis in setting of nonsteroidal antiinflammatory drugs and antibiotics. Dig Dis Sci. 1990; 35: 257-60.
50. Yagi K, Nakamura A, Sekine A, et al. NSAID colitis with a histology of collagenous colitis. Endoscopy 2001; 33: 629-32.
51. al Ghamdi MY, Malatjalian DA, Veldhuyzen van Zanten S. Causation: recurrent collagenous colitis following repeated use of NSAIDs. Can J Gastroenterol 2002; 16: 861-2.
52. Sveinsson ÓÁ, Örvar KB, Birgisson S, Agnarsdóttir M, Jónasson JG. Clinical features in microscopic colitis in a nationwide study in Iceland. Scand J Gastroenterol (samþykkt til birtingar).
53. Olesen M, Middelveld R, Bohr J, et al. Luminal nitric oxide and epithelial expression of inducible and endothelial nitric oxide synthase in collagenous and lymphocytic colitis. Scand J Gastroenterol 2003; 38: 66-72.
54. Perner A, Andresen L, Normark M, et al. Expression of nitric oxide synthases and effects of L-arginine and L-NMMA on nitric oxide production and fluid transport in collagenous colitis. Gut 2001; 49: 387-94.
55. Perner A, Nordgaard I, Matzen P, Rask-Madsen J. Colonic production of nitric oxide gas in ulcerative colitis, collagenous colitis and uninflamed bowel. Scand J Gastroenterol 2002; 37: 183-8.
56. Gillett HR, Freeman HJ. Prevalence of celiac disease in collagenous and lymphocytic colitis. Can J Gastroenterol 2000; 14: 919-21.
57. Freeman HJ, Davis JE, Myers DM. Complete histological resolution of collagenous sprue. Can J Gastroenterol 2004; 18: 333-6.
58. Bohr J, Tysk C, Yang P, et al. Autoantibodies and immunoglobulins in collagenous colitis. Gut 1996; 39: 73-76.
59. Fine KD, Do K, Schulte K, et al. High prevalence of celiac sprue-like HLA-DQ genes and enteropathy in patients with the microscopic colitis syndrome. Am J Gastroenterol 2000; 95: 1974-82.
60. Ramzan NN, Shapiro MS, Pasha TM, et al. Is celiac disease associated with microscopic and collagenous colitis [abstract]? Gastroenterology 2001; 120: A684.
61. Bohr J, Tysk C, Eriksson S, Abrahamsson H, Järnerot G. Collagenous colitis: a retrospective study of clinical presentation and treatment in 163 patients. Gut 1996; 39: 846-51.
62. Olesen M, Eriksson S, Bohr J, Jarnerot G, Tysk C. Lymphocytic colitis: a retrospective clinical study of 199 Swedish patients. Gut 2004; 53: 536-41.
63. Koskela RM, Niemela SE, Karttunen TJ, Lehtola JK. Clinical characteristics of collagenous and lymphocytic colitis. Scand J Gastroenterol 2004; 39: 837-45.
64. Kingsmore JGC, Kingsmore DB, Hall BD, et al. Cooccurence of collagenous colitis with seronegative spondyloarthropathy: Report of a case and literature review. J Rheumatol 1993; 20: 2153-7.
65. Fine KD, Seidel RH, Do K. The prevalence, anatomic distribution, and diagnosis of colonic causes of chronic diarrhea. Gastrointest Endosc 2000; 51: 318-28.
66. Surawicz CM. Collating collagenous colitis cases. Am J Gastroenterol 2000; 95: 307-8.
67. Tanaka M, Mazzoleni G, Riddell RH. Distribution of collagenous colitis: Utility of flexible sigmoidoscopy. Gut 1992; 33: 65-70.
68. Carpenter HA, Tremaine WJ, Batts KP, et al. Sequential histologic evaluation in collagenous colitis. Correlation with disease behaviour and sampling strategy. Dig Dis Sci 1992; 37: 1903-9.
69. Katanuma A, Kodama T, Tamaki T, et al. Collagenous colitis. Intern Med 1995; 34: 195-8.
70. Kingham JG. Microscopic colitis. Gut 1991; 32: 234-5.
71. Munck LK, Kjeldsen J, Philipsen E, Fischer Hansen B. Incomplete remission with short-term prednisolone treatment in collagenous colitis: a randomized study. Scand J Gastroenterol 2003; 38: 606-10.
72. Baert F, Schmit A, D?Haens G, et al. Budesonide in collagenous colitis: a double-blind placebo-controlled trial with histologic follow-up. Gastroenterology 2002; 122: 20-5.
73. Miehlke S, Heymer P, Bethke B, et al. Budesonide treatment for collagenous colitis: a randomized, double-blind, placebo-controlled, multicenter trial. Gastroenterology 2002; 123: 978-84.
74. Bonderup OK, Hansen JB, Birket-Smith L, Vestergaard V, Teglbjaerg PS, Fallingborg J. Budesonide treatment of collagenous colitis: a randomised, double blind, placebo controlled trial with morphometric analysis. Gut 2003; 52: 248-51.
75. Feyen B, Wall GC, Finnerty EP, Dewitt JE, Reyes RS. Meta-analysis: budesonide treatment for collagenous colitis. Aliment Pharmacol Ther 2004; 20: 745-9.
76. Miehlke S, Madisch A, Voss C, et al. Long-term follow-up of collagenous colitis after induction of clinical remission with budesonide. Aliment Pharmacol Ther 2005; 22: 1115-9.
77. Bohr J, Olesen M, Tysk C, Järnerot G. Budesonide and bismuth in microscopic colitis. Gut 1999; 45: A202.
78. Pardi DS, Ramnath VR, Loftus EV Jr, Tremaine WJ, Sandborn WJ. Lymphocytic colitis: clinical features, treatment, and outcomes. Am J Gastroenterol 2002; 97: 2829-33.
79. Fine KD, Lee EL. Efficacy of open-label bismuth subsalicylate for the treatment of microscopic colitis. Gastroenterology 1998; 114: 29-36.
80. Fine K, Ogunji F, Lee E, et al. Randomized, double-blind, placebo-controlled trial of bismuth subsalicylate for microscopic colitis (abstract). Gastroenterology 1999; 116: 880.
81. Bonderup OK, Folkersen BH, Gjersoe P, Teglbjaerg PS. Collagenous colitis: A long-term follow-up study. Eur J Gastroenterol Hepatol 1999; 11: 493-5.
82. Chan JL, Tersmette AC, Offerhaus GJ, et al. Cancer risk in collagenous colitis. Inflamm Bowel Dis 1999; 5: 40-3.
