07/08. tbl. 95.árg. 2009
Fræðigrein
Fjölónæmir berklar á Íslandi - tilfellaröð og yfirlit
Multidrug resistant tuberculosis in Iceland - case series and review of the literature
Ágrip
Inngangur: Fjölónæmir berklar eru vaxandi vandamál í heiminum. Árangur meðferðar er verri, sjúkrahúslegur lengri og kostnaður hærri en við lyfnæma berkla. Hér er lýst þremur tilfellum fjölónæmra berkla sem greinst hafa á Íslandi síðastliðin sex ár, 2003-2008.
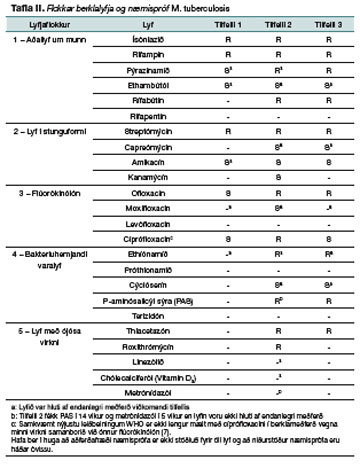
Sjúkratilfelli: Fyrsta tilfellið var 23 ára innflytjandi frá Asíu sem lokið hafði fyrirbyggjandi meðferð vegna jákvæðs berklaprófs. Tveimur árum síðar lagðist hann inn með berkla í kviðarholi sem reyndust vera fjölónæmir. Hann lauk 18 mánaða meðferð og læknaðist. Annað tilfellið var 23 ára maður sem lagðist inn vegna fjölónæmra lungnaberkla. Hann hafði áður fengið meðferð í heimalandi sínu í A-Evrópu en ekki lokið henni. Hann lá inni í sjö mánuði og náði bata en gert var ráð fyrir tveggja ára meðferð. Þriðja tilfellið var 27 ára einkennalaus kona sem greindist með fjölónæma lungnaberkla við rakningu smits vegna fjölónæmra berkla bróður. Fyrirhuguð var 18 mánaða meðferð.
Ályktun: Á síðustu sex árum greindust þrjú tilfelli fjölónæmra berkla hér á landi sem er nálægt 5% allra berklatilfella á tímabilinu. Á 12 árum þar á undan greindist eitt tilfelli og gæti þetta bent til yfirvofandi fjölgunar. Fjölónæmir berklar eru alvarlegir, erfiðir og kostnaðarsamir í meðhöndlun. Mikilvægt er að standa vel að berklavörnum, sérstaklega skimun innflytjenda.
Inngangur
Talið er að þriðjungur jarðarbúa séu smitaðir af berklabakteríunni, Mycobacterium tuberculosis.1, 2 Árið 2006 greindust 9,2 milljónir tilfella berkla í heiminum samkvæmt skráningu Alþjóða heilbrigðismálastofnunarinnar (WHO) og sama ár létust 1,7 milljónir manna af völdum sjúkdómsins. Eru berklar sá smitsjúkdómur sem flesta dregur til dauða á eftir alnæmi.3, 4 Mikill munur er á tíðni berkla milli landsvæða en almennt er talið að um 85% allra tilfella séu í Afríku og Asíu (mynd 1).2-4 Í Afríku hefur nýgengi sjúkdómsins aukist hratt undanfarna tvo áratugi og mest þar sem HIV-smit er útbreiddast, eða allt að 400 tilfelli /100.000 íbúa á ári. Einnig hefur sést aukning í A-Evrópu og Mið-Asíu en almennt hefur nýgengi verið stöðugt eða farið minnkandi annars staðar.3, 4 Nýgengi berkla á Íslandi hefur verið um fjögur tilfelli /100.000 íbúa á ári síðastliðin sex ár sem telst lágt í samanburði við aðrar þjóðir.4-6
Berklar sem eru ónæmir fyrir hefðbundnum berklalyfjum eru vaxandi vandamál. Sé bakterían ónæm samkvæmt næmisprófum fyrir bæði ísóníazíði og rífampíni, sem eru tvö aðallyf berklameðferðar, kallast berklarnir fjölónæmir (multi drug resistant, MDR-TB).7 Sé einnig ónæmi fyrir einhverju flúorókínólóni og að minnsta kosti einu af þremur varalyfjum í stunguformi (amikacíni, kanamýcíni eða capreomycíni) er um að ræða ofurónæma berkla (extensively drug resistant, XDR-TB).7-9 Áætlað er að tæplega 5% allra nýrra berklatilfella séu af völdum fjölónæmra berkla, eða um 500.000 tilfelli á ári í heiminum.4 Flestir greinast í SA-Asíu og leggja Kína og Indland til um helming allra tilfella fjölónæmra berkla.7 Hlutfallslega er tíðnin þó hæst í ríkjum fyrrum Sovétríkjanna í A-Evrópu og Mið-Asíu, þar sem allt að fjórðungur nýrra tilfella eru vegna fjölónæmra stofna (mynd 2).9 Tíðni fjölónæmra berkla eykst einnig hratt í Afríku sunnan Sahara, nátengt alnæmisfaraldrinum í álfunni.4, 9 Ofurónæmum berklum var fyrst lýst árið 200510, 11 en hefur nú verið lýst í 55 löndum.12 Tilfelli ofurónæmra berkla eru enn tiltölulega fá en fjölgar hratt, sérstaklega á svæðum fyrrum Sovétríkjanna þar sem þau eru nú 4-24% af öllum tilfellum fjölónæmra berkla.9, 13 Nýlega hefur verið lýst tilfellum berkla þar sem ónæmi var til staðar gegn öllum þekktum berklalyfjum sem prófað var fyrir.14

Mynd 1. Áætlað nýgengi berkla eftir löndum árið 2006. Nýgengi berkla var hæst í Afríku sunnan Sahara og Mið- og Suðaustur-Asíu. (Birt með leyfi WHO).
Meðferðarárangur við berklum almennt í heiminum öllum var um 85% árið 2005 samkvæmt skýrslum WHO.4 Árangur af meðferð fjölónæmra berkla er mun lakari og meðferðin bæði erfiðari, lengri og kostnaðarsamari. Við góðar aðstæður er árangurinn talinn vera um 75%, en í heiminum öllum líklega um eða innan við 60%.15, 16 Almennt gengur enn verr að meðhöndla ofurónæma berkla.14, 17-21
Undanfarna áratugi hefur nýgengi berkla á Íslandi verið lágt í samanburði við önnur Evrópulönd.5, 6 Læknar og heilbrigðisstarfsfólk eru almennt ekki mjög meðvituð um berkla og fjölónæmir berklar eru flestum okkar framandi. Til að meta vandamálið nánar ákváðu höfundar að taka saman þekkt tilfelli fjölónæmra berkla á Íslandi undanfarin ár.
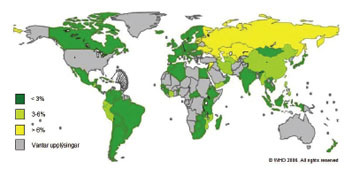
Mynd 2. Hlutfall fjölónæmra berkla (MDR-TB) af nýjum berklatilfellum eftir löndum árin 1994-2007. Tíðni fjölónæmra berkla var hlutfallslega hæst í Austur-Evrópu og Mið-Asíu en eykst nú hratt í Afríku sunnan Sahara. (Birt með leyfi WHO).
Efniviður og aðferðir
Rannsóknaraðilar fundu þau tilfelli fjölónæmra berkla á Íslandi sem þeim var kunnugt um, eitt frá árinu 2003, annað frá 2007 og þriðja frá 2008. Fjölónæmi var skilgreint sem ónæmi fyrir ísóníazíði og rífampíni samkvæmt svipgerðarprófi (phenotypic resistance testing). Árið 2004 var einn sjúklingur að auki greindur með berklasýkingu sem var ónæm fyrir báðum þessum lyfjum samkvæmt arfgerðarrannsókn (genotypic resistance testing), en reyndist hins vegar næm fyrir rífampíni samkvæmt svipgerðarprófi. Bakteríustofninn uppfyllti því ekki skilmerki fyrir fjölónæmi og var sjúkratilfellinu því sleppt. Ekki var að fyrra bragði leitað kerfisbundið, en eftir á var hugað að berklatilfellum með lyfjaónæmi í berklaskrá, sem er hluti smitsjúkdómaskrár sem sóttvarnalæknir heldur lögum samkvæmt yfir tilkynningaskylda sjúkdóma. Þar komu ekki fram önnur tilfelli fjölónæmra berkla á árunum 2003 til 2008. Eitt tilfelli hafði hins vegar greinst árið 1985 og annað 1992. Ekki var sótt um leyfi til Vísindasiðanefndar eða Persónuverndar þar sem um var að ræða röð tilfella sem höfundar höfðu komið að starfa sinna vegna.
Niðurstöður
Sjúkratilfelli 1
23 ára karlmaður leitaði á bráðamóttöku vegna verkja neðan til í kvið sem höfðu farið vaxandi í eitt ár. Á sama tíma hafði hann fundið fyrir slappleika, hitatoppum, breytingum á hægðum og hafði lést um 15 kg. Hann var upprunninn frá Asíu en fluttist til Íslands fjórum árum fyrr. Þá var hann með jákvætt berklapróf (26 mm) og fékk níu mánaða fyrirbyggjandi meðferð með ísóníazíði. Við skoðun var hiti 40,0 °C og þyngd 45 kg. Dreifð eymsli voru í kvið, mest í hægri neðri fjórðungi, og þar þreifaðist fyrirferð. Í blóðprufum voru merki um bólgu og blóðleysi (tafla I). Á tölvusneiðmynd af kvið sást aukin þéttni í hengi (omentum) neðantil hægra megin ásamt fríum kviðarholsvökva og vægum eitlastækkunum. Lungnabreytingar sáust ekki á tölvusneiðmynd. Sjúklingur var lagður inn til kviðarholsspeglunar í greiningarskyni. Í aðgerðinni sást að smágirnislykkjur voru lóðaðar saman, mest í hægri mjaðmargróf (fossa iliaca). Kviðarholið var þakið hvítum skellum og til staðar var gulgrænn kviðarholsvökvi. Útlitið var af skurðlækni talið geta samrýmst útsæði af krabbameini (carcinomatosis) og tekin voru vefjasýni frá skinu (peritoneum). Í vefjaskoðun sáust bólguhnúðar (granuloma) með drepi og sýrufastir stafir. Hann var því greindur með berkla í skinu (tuberculosis peritonei).
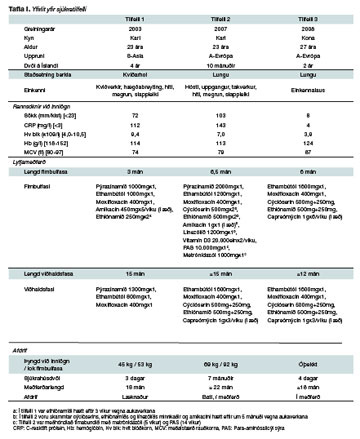
Hafin var fjögurra lyfja meðferð með ísóníazíði, rífampíni, pýrazínamíði og ethambútóli í töflu-formi og útskrifaðist sjúklingurinn á þessum lyfjum þremur dögum síðar. Hann var áfram með viðvarandi hita og slappleika en líðan fór þó heldur batnandi. Átta vikum síðar ræktaðist M. tuberculosis frá vefjabita og var bakterían ónæm fyrir ísóníazíði og rífampíni (tafla II). Þeim lyfjum var því hætt en haldið var áfram með ethambútól og pýrazínamíð og bætt við amikacíni (í æð), moxifloxacíni og ethíónamíði (tafla I). Hætta þurfti síðastnefnda lyfinu eftir þrjár vikur vegna aukaverkana frá meltingarfærum. Amikacín var gefið fyrstu þrjá mánuðina (fimbulfasi) og á því tímabili varð sjúklingurinn einkennalaus og þyngdist úr 45 kg í 53 kg. Meðferð með ethambútóli, pýrazínamíði og moxifloxacíni stóð í samtals 18 mánuði. Að meðferð lokinni var hann við góða heilsu og taldist læknaður.
Sjúkratilfelli 2
23 ára karlmaður, upprunninn frá A-Evrópu, leitaði á bráðamóttöku vegna hita, slappleika, hósta, uppgangs og takverks. Hann lýsti óþægindum vinstra megin í brjóstkassa undanfarna sex mánuði og í þrjá mánuði hafði hann einnig fundið fyrir slappleika ásamt hósta og uppgangi. Hann hafði lést um nærri 10 kg á þeim 10 mánuðum sem hann hafði búið á Íslandi. Við nánari eftirgrennslan og eftir töf vegna tungumálaerfiðleika kom í ljós að hann hafði greinst með berkla í heimalandi sínu tveimur og hálfu ári áður og verið meðhöndlaður í rúmlega eitt ár.
Við skoðun var hann slapplegur og fölur yfirlitum. Hann vóg um 69 kg og hiti var 38,3 °C. Brak heyrðist við hlustun yfir hægra lunga og minnkuð öndunarhljóð og bankdeyfa voru yfir neðri helmingi vinstra lunga. Röntgenmynd sýndi dreifðar hnútóttar þéttingar í báðum lungum ásamt fleiðruvökva vinstra megin (mynd 3a). Á tölvusneiðmynd sást að sumar þéttingarnar innihéldu loft og einnig voru eitlastækkanir í miðmæti (mynd 4a). Í blóði voru merki um verulega bólguvirkni og blóðleysi (tafla I). Í fleiðruvökva sáust merki um vilsu (exudat) og þar voru hvítfrumur 4100 x106 /l (<1000 x106 /l), þar af voru 72% kleyfkjarna frumur. Sýrufastir stafir sáust ekki í smásjárskoðun. Sjúklingurinn var settur í einangrun vegna gruns um berkla.
Daginn eftir sást mikið af sýruföstum stöfum í hrákasýni og þá var hafin fjögurra lyfja berklameðferð með ísóníazíði, rífampíni, pýrazínamíði og ethambútóli. Næstu daga fóru einkenni sjúklings versnandi. Leitað var eftir upplýsingum um fyrri veikindi frá upprunalandi hans og kom þá í ljós að hann hafði verið með fjölónæma berkla en hafði hætt meðferð áður en henni lauk. Bakterían hafði áður verið ónæm fyrir öllum lyfjunum sem sjúklingurinn var nú á og var þeim því hætt nema pýrazínamíði. Hann var í staðinn settur á amikacín í æð, moxifloxacín, cýclóserín, ethíónamíð og línezólíð og byggðist meðferðin á upplýsingum um fyrra næmi. Um tíma fékk hann einnig PAS (Para-amínósalisýl sýru) og metrónídazól. M. tuberculosis óx í ræktunum frá hráka og fleiðruvökva og bárust niðurstöður næmisprófa fjórum vikum eftir innlögn (tafla II). Ethambútól var þá aftur sett inn og einnig D-vítamín í háum skömmtum (tafla I). HIV-próf var neikvætt.
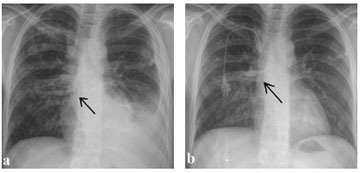
Mynd 3. Röntgenmynd af lungum við a) innlögn og b) útskrift tæpum sjö mánuðum síðar.
a) Dreifðir hnútar með holrýmum sjást, sá stærsti hliðlægt við hægri lungnarót (ör). Auk þess sést þétting í neðra blaði og fleiðruvökvi vinstra megin.
b) Breytingar hafa gengið að miklu leyti til baka, þó sést stærsti hnúturinn enn (ör). Auk þess sést æðaleggur.
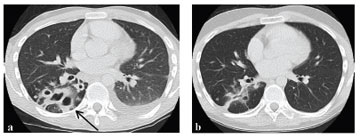
Mynd 4. Tölvusneiðmyndir af lungum við a) innlögn og b) útskrift tæpum sjö mánuðum síðar.
a) Hnútóttar þéttingar sjást í báðum lungum, margar með loftfylltum holrýmum. Stærsta breytingin er ofarlega í neðra blaði hægra lunga (ör).
b) Breytingarnar hafa að miklu leyti rénað og holukerfin smækkað en sjást þó enn greinilega.
Greinileg framför varð á fyrstu vikum meðferðar. Endurteknar myndgreiningar á næstu mánuðum sýndu minnkandi lungnabreytingar (mynd 3b og 4b). Vegna dofa í fótum voru skammtar línezólíðs, ethíónamíðs og cýclóseríns minnkaðir og vegna suðs fyrir eyrum var amikacíni hætt en capreomycín síðar sett inn í staðinn. Sýrufastir stafir sáust í sífellt minna magni í hrákasýnum. Ræktanir urðu neikvæðar um fjórum mánuðum eftir innlögn og smásjárskoðun varð neikvæð einum og hálfum mánuði síðar. Sjúklingurinn útskrifaðist í góðu líkamlegu ástandi tæpum sjö mánuðum eftir innlögn og hafði verið í einangrun allan tímann. Hann hafði þá þyngst um 23 kg frá komu. Við útskrift var pýrazínamíði og línezólíði hætt en haldið áfram með önnur lyf þar á meðal capreomycín í æð þrisvar í viku undir eftirliti heilbrigðisstarfsfólks (tafla I). Áætlaður meðferðartími var alls 22 mánuðir.
Sjúkratilfelli 3
27 ára kona, upprunnin frá A-Evrópu, var kölluð til skoðunar eftir að bróðir hennar hafði greinst með smitandi lungnaberkla (sjá tilfelli 2). Hún hafði engin almenn eða sértæk einkenni um berkla. Húðpróf fyrir berklum var sterkt jákvætt (20 mm). Röntgenmynd af lungum sýndi þéttingar í efra blaði hægra lunga. Smásjárskoðun, PCR og ræktun hrákasýna reyndust neikvæð fyrir berklum. Niðurstöður blóðrannsókna voru ómarkverðar (tafla I). Vegna breytinga á lungnamynd sem líktust berklum var gerð berkjuspeglun. Í smásjárskoðun sýnis úr berkjuskoli sáust ekki sýrufastir stafir en fjölónæmar berklabakteríur uxu í ræktun (tafla II). Hafin var meðferð með ethambútóli, moxifloxacíni, cýclóseríni, ethíónamíði og capreomycíni. Áætlað var að gefa að minnsta kosti 18 mánaða lyfjameðferð, þar af fyrstu 6 mánuðina (fimbulfasi) undir beinu eftirliti (tafla I). 11 mánuðum eftir upphaf meðferðar höfðu lungnabreytingar á röntgenmynd rénað verulega.
Margir einstaklingar sem verið höfðu í nánu samneyti við tilfelli 2 voru kallaðir inn til skoðunar og skimaðir með tilliti til berkla. Í innsta hópi fjölskyldu og vina voru 17 manns prófaðir og auk tilfellis 3 reyndust fjórir fullorðnir ásamt sex ára dóttur konunnar með sterk jákvæð berklapróf. Þau höfðu öll eðlilegar lungnamyndir og enginn var með einkenni um berkla. Vegna fjölónæmis var ákveðið var að gefa hvorki barninu né öðrum fyrirbyggjandi lyfjameðferð heldur fylgjast frekar með þeim með tilliti til einkenna og gert ráð fyrir árlegum myndatökum af lungum. Óstaðfestar upplýsingar eru um að einn þeirra útsettu hafi veikst af lyfþolnum berklum eftir að hafa snúið aftur til heimalandsins. Ekki fundust nýsmitanir meðal vinnufélaga eða heilbrigðisstarfsfólks.
Umræða
Öll þrjú tilfellin sem hér er lýst komu frá löndum með margfalt hærra nýgengi berkla en á Íslandi. Fyrsti sjúklingurinn hafði við komu til landsins greinst með leynda berklasýkingu og lauk níu mánaða fyrirbyggjandi lyfjameðferð með ísóníazíði, sem bakterían reyndist síðar vera ónæm gegn. Annað tilfellið minnir á að lyfþolnir berklar taka sig oft upp að lokinni meðferð og ekki síst hitt að berklasjúklingar geta verið smitberar. Tilfelli 3 sýnir hve mikilvægt það er að rekja smit, sjúkdómurinn fannst á snemmstigi og meðferð varð auðveldari fyrir vikið.
Fljótlega eftir að berklalyf komu á markað um miðja 20. öld fór að bera á ónæmi, en þá var streptómýcín oft notað eitt og sér.22, 23 Margir þættir valda því að berklabakteríur verða ónæmar fyrir sýklalyfjum en orsökin er meðal annars rangt lyfjaval, of lágir lyfjaskammtar, meðferð með einu lyfi og meðferðarvanheldni. Undir slíkum kringumstæðum fer fram val á ónæmum berklabakteríum og verða þær smám saman ríkjandi.1, 24 Vaxandi lyfjaónæmi berkla er því langoftast af mannavöldum og ein meginástæðan fyrir því að mælt er með lyfjainntöku undir beinu eftirliti (directly observed therapy, DOT) sem er mikilvægur þáttur í berklameðferð.7, 25
Hefðbundin meðferð við lyfjanæmum berklum byggir á þremur til fjórum lyfjum í upphafi (fimbulfasi) sem er fækkað niður í tvö í viðhaldsfasa meðferðar. Meðferðin stendur í samtals sex til níu mánuði.25 Mælt er með að meðferð fjölónæmra berkla innihaldi að minnsta kosti fjögur virk lyf samkvæmt næmisprófum, en ákjósanlegt er að virk lyf séu fimm til sex.7 Meðferðarlengdin ætti að vera að minnsta kosti 18 mánuðir eftir að berklaræktun er orðin neikvæð og þar af er gert ráð fyrir stungulyfi fyrstu sex mánuðina.7 Vegna þess hve sjúkdómurinn var langt genginn hjá tilfelli 2 leið langur tími þar til ræktanir urðu neikvæðar og því var fyrirhuguð meðferð með stungulyfi allan tímann í stað sex mánaða (tafla I). Í alvarlegum tilfellum fjölónæmra lungnaberkla getur einnig komið til greina að fjarlægja sýktan lungnavef, annaðhvort með blaðnámi (lobectomy) eða allt lungað.7, 26 Þetta var ekki mögulegt í tilfelli 2 þar sem sjúkdómurinn var ekki staðbundinn (mynd 4).
Flokka berklalyfja má sjá í töflu II7, 25 en af þeim eru stungulyfin og flúorókínólón mikilvægust í meðferð fjölónæmra berkla.7, 9 Næmispróf fyrir lyfjunum eru þó óáreiðanleg sem gerir lyfjaval erfiðara.7 Skilgreining á fjölónæmum berklum byggir á því að ónæmi sé til staðar gegn ísóníazíði og rífampíni, lyfjum sem bæði eru hornsteinar hefðbundinnar meðferðar. Skilgreiningin byggir á svipgerðargreiningu sem er tímafrek. Nýlegri aðferðir, svo sem arfgerðargreining með kjarnsýrumögnun (PCR), eru fljótvirkari og geta greint stökkbreytingar sem tengjast fjöl-ónæmi mun fyrr.27, 28 Sjúklingurinn í tilfelli 1 var í fimbulfasa meðhöndlaður með að minnsta kosti þremur en líklega fimm virkum lyfjum og náði sér (tafla II). Tilfelli 2 og 3 voru með mjög ónæman stofn. Þau voru meðhöndluð með nær öllum flokkum virkra berklalyfja sem þekktir eru og voru virk lyf að minnsta kosti þrjú til fjögur (tafla II). Tilfelli 2 var auk þess meðhöndlað með línezólíði og háskammta D-vítamíni en rannsóknir benda til þess að þessi lyf geti haft þýðingu í meðferð fjölónæmra berkla.29-32 Staða þeirra er enn óljós en mikilvægt er að auka frekar rannsóknir á nýjum lyfjaflokkum gegn berklum.9
Lyf sem notuð eru í meðferð fjölónæmra berkla hafa meiri aukaverkanir en hefðbundin berklalyf og er meðferðin því erfiðari og áhættusamari fyrir sjúklingana.7, 16 Algengar aukaverkanir eru óþægindi frá meltingarvegi, brenglun á lifrarstarfsemi, úttaugakvilli og áhrif á heyrn og jafnvægisskyn.33 Aukaverkanir geta verið alvarlegar og jafnvel lífshættulegar og þær eru enn algengari ef einstaklingur er einnig á meðferð við HIV.7, 34 Í tilfellum 1 og 2 þurfti að breyta um lyf og lyfjaskammta vegna aukaverkana (tafla I) og í öllum tilfellunum var pýridoxín (B6-vítamín) gefið með til að minnka líkur á úttaugaskaða.
Mikilvægt er að berklasjúklingar séu í einangrun á meðan þeir eru smitandi. Forsenda smitsemi er að vessi myndi loftúða með einhverjum hætti, svo sem hósta. Sjúklingur með lungnaberkla telst því smitandi sjáist sýrufastir stafir í hráka.35 Hins vegar er smithætta nánast engin af þvagi og fistilvessum þótt um sýkingu í eitlum eða þvagfærum sé að ræða að því tilskildu að eðlileg smitgát sé viðhöfð. Tilfelli 3 hafði lungnaberkla en þar sem hrákasýni voru neikvæð var ekki þörf á einangrun. Sjúklingurinn í tilfelli 1 var ekki í einangrun þar sem berklar í lokuðum rýmum utan lungna, svo sem í kviðarholi eða heilahimnum, smitast ekki milli manna.
Kostnaður við meðhöndlun fjölónæmra berkla er mikill. Kostnaður við lyfjameðferð tilfellis 2 í sjúkrahúslegunni var um 750.000 kr á mánuði í tæpa sjö mánuði og eftir útskrift um 230.000 á mánuði í 15 mánuði sem gera alls um 9 milljónir fyrir tæplega tveggja ára meðferð (á verðlagi í maí 2008). Ofan á fjárhæðina leggst legudagakostnaður á lyflækningasviði I Landspítala sem á fyrri hluta árs 2008 var um 52.000 kr. á dag, eða tæpar 11 milljónir á sjö mánuðum. Lyfjakostnaður tilfellis 3 var um 300.000 kr. á mánuði, sem gera alls um 5,5 milljónir fyrir 18 mánaða meðferð. Aðrir útgjaldaliðir eru vegna rannsókna, læknisheimsókna og vitjana heimahjúkrunar en þar að auki þarf að huga að framleiðslu- og vinnutapi. Mikilvægustu leiðirnar til að draga úr þessum mikla kostnaði eru skjót greining, rétt meðferð og að koma í veg fyrir að fólk smitist og veikist.
Reynt er að rekja berklasmit þar sem svigrúm er til að bjóða og veita fyrirbyggjandi meðferð.5, 35 Þeir sem hafa verið í nánu samneyti við berklasjúkan einstakling eru rannsakaðir.35 Hér á landi er rakning berklasmits og aðrar aðgerðir til að hefta útbreiðslu berkla í höndum göngudeildar sóttvarna hjá heilsugæslu höfuðborgarsvæðisins. Á þann hátt greindist tilfelli 3 og því var unnt að meðhöndla sjúkdóminn á snemmstigi. Hin fimm sem reyndust með jákvæð berklapróf voru ekki komin með merki um sjúkdóm heldur einungis smit eða leynda berklasýkingu (latent tuberculosis infection). Talið er að um 10% þeirra sem smitast af berklum fái berklaveiki síðar. Gerist það oft á fyrstu tveimur árunum eftir smit. Líkurnar á sjúkdómi eru meðal annars háðar aldri og öðrum þáttum og eru margfalt meiri hjá HIV smituðum.2, 36 Lyfjagjöf í fyrirbyggjandi tilgangi er talin geta minnkað áhættu á sjúkdómi niður í innan við 4% hjá einstaklingum sem ekki hafa HIV.37 Oftast er ísóníazíð gefið í níu mánuði en aðrir möguleikar eru einnig fyrir hendi.25 Þessi meðferð hjálpar hins vegar ekki sé um að ræða fjölónæma berkla eins og sást í tilfelli mannsins með kviðarholsberklana. Rannsóknir á mögulegri gagnsemi lyfjameðferðar við leyndri berklasýkingu með fjölónæmum bakteríum eru fáar og enn skortir úrræði um meðferð slíkra tilfella.38-41 Oft er því talið skást að fylgjast reglulega með einstaklingnum og meðhöndla ef sjúkdómurinn kemur upp eins og ákveðið var að gera hér.
Af 62 berklatilfellum sem greinst hafa á Íslandi 2003-2008 eru þessi þrjú tilfelli fjölónæmra berkla eða 4,8%.5 Á sex árum þar á undan komu engin tilfelli upp og á sex árum þar á undan eitt tilfelli. Þetta er vísbending um að tilfellum fjölónæmra berkla sé að fjölga hér á landi líkt og gerst hefur annars staðar. Öll tilfellin voru innflytjendur. Ferðalög og fólksflutningar stuðla að aukinni útbreiðslu berkla, þar á meðal fjölónæmra berkla, og flyst þá sjúkdómsáhættan eins og hún var í upprunalandinu með til nýja landsins. Reglur um berklavarnir og þar með talið skimun innflytjenda eru mjög mismunandi milli Evrópulanda en áætlanir eru um að samhæfa aðgerðir meira en nú er.42 Ferðamenn geta dvalið hér á landi í allt að þrjá mánuði án afskipta yfirvalda og eru ekki skimaðir fyrir berklum. Hérlendis er berklaskimun í höndum heilsugæslunnar og gerð sem hluti heilbrigðisskoðunar vegna dvalar- og atvinnuleyfisumsókna. Þeir sem koma frá öðrum löndum en löndum Evrópska efnahagssvæðisins (EES), Sviss, Bandaríkjunum, Kanada, Ástralíu og Nýja-Sjálandi, þurfa að undirgangast læknisskoðun. Gert er húðpróf hjá þeim sem eru yngri en 35 ára en röntgenmynd af lungum fengin hjá öllum sem eru 35 ára og eldri eða hafa jákvæð húðpróf.43 Einstaklingurinn í fyrsta tilfellinu var upprunninn í Asíu og hafði verið skimaður fyrir berklum við komuna til landsins og var réttilega greindur en ísóníazíðmeðferð hjálpaði ekki vegna ónæmis. Tilfelli 2 og 3 höfðu ekki verið skoðuð þegar þau fluttust til landsins þar sem ekki er lengur gert ráð fyrir skimun umsækjenda um dvalarleyfi frá löndum A-Evrópu séu þau innan EES, þrátt fyrir hátt nýgengi berkla á svæðinu.4 Vegna frjáls flæðis fólks til dvalar- og atvinnuleyfis innan EES er erfitt um vik að beita komuskimun fyrir sjúkdómum þótt slíkar heimildir séu reyndar í sóttvarnalögum. Spyrja má hvort eðlilegt sé að stjórnmálaleg samskipti milli þjóða komi niður á forvarnarstarfi gegn smitsjúkdómum og hvort ekki væri heppilegra að byggja verklagsreglur um skimun að mestu leyti á tíðni berkla í einstaka löndum frekar en að miða að svo miklu leyti við stjórnmálalega skiptingu landsvæða. Ef það þykir ekki fýsilegt er þó möguleiki að koma eftirlitinu við síðar, til dæmis við nýráðningar hjá fyrirtækjum í landinu. Í ljósi aukinna fólksflutninga og vaxandi lyfjaónæmis í heiminum er líklegt að tilfellum fjölónæmra berkla eigi eftir að fjölga á Íslandi með tilheyrandi sjúkdómsbyrði sjúklinga og kostnaði fyrir heilbrigðiskerfið. Íslenskir læknar þurfa að vera meðvitaðir um berkla og nota greiningartækin eins og við á. Mikilvægt er að standa vörð um og efla skipulag berklavarna hér á landi eins og annars staðar.
Þakkir
Höfundar þakka Einari Jónmundssyni og Adolf Þráinssyni röntgenlæknum fyrir aðstoð við vinnslu röntgenmynda.
Heimildir
1. Fauci AS, NIAID Tuberculosis Working Group. Multidrug-resistant and extensively drug-resistant tuberculosis: the National Institute of Allergy and Infectious Diseases Research agenda and recommendations for priority research. J Infect Dis 2008;197:1493-8.
2. World Health Organisation. Tuberculosis fact sheet. Geneva: World Health Organisation, 2008. Sjá www.who.int/mediacentre/factsheets/fs104/en/index.html.
3. Dye C. Global epidemiology of tuberculosis. Lancet 2006; 367: 938-40.
4. World Health Organisation. Global tuberculosis control - surveillance, planning, financing. WHO Report 2008. WHO/HTM/TB/2008.393. Geneva: World Health Oragnisation, 2008.
5. Landlæknisembættið. Tilkynningaskyldir sjúkdómar. Reykjavík: Landlæknisembættið, 2008. Sjá www.landlaeknir.is/Pages/876
6. World Health Organisation. TB country profile: Iceland. Geneva: World Health Organisation, 2008. Sjá www.who.int/globalatlas/predefinedReports/TB/index.asp?strSelectedCountry=ISL
7. World Health Organisation. Guidelines for the programmatic management of drug-resistant tuberculosis: Emergency update 2008. WHO/HTM/TB/2008.402. Geneva: World Health Organisation, 2008.
8. Centers for Disease Control and Prevention (CDC). Revised definition of extensively drug-resistant tuberculosis. MMWR Morb Mortal Wkly Rep 2006; 55:1176.
9. World Health Organisation. Anti-tuberculosis drug resistance in the world. Fourth global report. WHO/HTM/TB/2008.394. Geneva: World Health Organisation, 2008.
10. Centers for Disease Control and Prevention (CDC). Emergence of Mycobacterium tuberculosis with extensive resistance to second-line drugs--worldwide, 2000-2004. MMWR Morb Mortal Wkly Rep 2006; 55: 301-5.
11. Shah NS, Wright A, Bai GH, et al. Worldwide emergence of extensively drug-resistant tuberculosis. Emerg Infect Dis 2007;13: 380-7.
12. World Health Organisation. Global map and information on XDR-TB. Geneva: World Health Organization, 2009. Sjá www.who.int/tb/challenges/xdr/xdr_map_feb09.pdf
13. Centers for Disease Control and Prevention (CDC). Extensively drug-resistant tuberculosis--United States, 1993-2006. MMWR Morb Mortal Wkly Rep 2007; 56: 250-3.
14. Migliori GB, Ortmann J, Girardi E, et al. Extensively drug-resistant tuberculosis, Italy and Germany. Emerg Infect Dis 2007;13: 780-2.
15. Chan ED, Laurel V, Strand MJ, et al. Treatment and outcome analysis of 205 patients with multidrug-resistant tuberculosis. Am J Respir Crit Care Med 2004; 169: 1103-9.
16. Yew WW, Leung CC. Management of multidrug-resistant tuberculosis: Update 2007. Respirology 2008; 13: 21-46.
17. Kim DH, Kim HJ, Park SK, et al. Treatment Outcomes and Long-term Survival in Patients with Extensively Drug-resistant Tuberculosis. Am J Respir Crit Care Med 2008; 178: 1075-82.
18. Kwon YS, Kim YH, Suh GY, et al. Treatment outcomes for HIV-uninfected patients with multidrug-resistant and extensively drug-resistant tuberculosis. Clin Infect Dis 2008; 47: 496-502.
19. Mitnick CD, Shin SS, Seung KJ, et al. Comprehensive treatment of extensively drug-resistant tuberculosis. N Engl J Med 2008; 359: 563-74.
20. Gandhi NR, Moll A, Sturm AW, et al. Extensively drug-resistant tuberculosis as a cause of death in patients co-infected with tuberculosis and HIV in a rural area of South Africa. Lancet 2006; 368: 1575-80.
21. Keshavjee S, Gelmanova IY, Farmer PE, et al. Treatment of extensively drug-resistant tuberculosis in Tomsk, Russia: a retrospective cohort study. Lancet 2008; 372: 1403-9.
22. Ollé-Goig JE. Editorial: the treatment of multi-drug resistant tuberculosis--a return to the pre-antibiotic era? Trop Med Int Health 2006; 11: 1625-8.
23. Crofton J, Mitchinson DA. Streptomycin resistance in pulmonary tuberculosis. Br Med J 1948; 2: 1009-15.
24. Mitchison DA. How drug resistance emerges as a result of poor compliance during short course chemotherapy for tuberculosis. Int J Tuberc Lung Dis 1998; 2: 10-5.
25. Blumberg HM, Burman WJ, Chaisson RE, et al. American Thoracic Society/Centers for Disease Control and Prevention/Infectious Diseases Society of America: treatment of tuberculosis. Am J Respir Crit Care Med 2003; 167: 603-62.
26. Pomerantz BJ, Cleveland JC, Olson HK, Pomerantz M. Pulmonary resection for multi-drug resistant tuberculosis. J Thorac Cardiovasc Surg 2001; 121: 448-53.
27. Telenti A, Honoré N, Bernasconi C, et al. Genotypic assessment of isoniazid and rifampin resistance in Mycobacterium tuberculosis: a blind study at reference laboratory level. J Clin Microbiol 1997; 35: 719-23.
28. O'Riordan P, Schwab U, Logan S, et al. Rapid molecular detection of rifampicin resistance facilitates early diagnosis and treatment of multi-drug resistant tuberculosis: case control study. PLoS ONE 2008; 3:e3173.
29. Martineau AR, Honecker FU, Wilkinson RJ, Griffiths CJ. Vitamin D in the treatment of pulmonary tuberculosis. J Steroid Biochem Mol Biol 2007; 103: 793-8.
30. Ralph AP, Kelly PM, Anstey NM. Trends Microbiol. L-arginine and vitamin D: novel adjunctive immunotherapies in tuberculosis 2008; 16: 336-44.
31. Ntziora F, Falagas ME. Linezolid for the treatment of patients with [leiðrétt] mycobacterial infections [leiðrétt]: a systematic review. Int J Tuberc Lung Dis 2007; 11: 606-11.
32. Nam HS, Koh WJ, Kwon OJ, Cho SN, Shim TS. Daily half-dose linezolid for the treatment of intractable multidrug-resistant tuberculosis. Int J Antimicrob Agents 2009; 33: 92-3.
33. Nathanson E, Gupta R, Huamani P, et al. Adverse events in the treatment of multidrug-resistant tuberculosis: results from the DOTS-Plus initiative. Int J Tuberc Lung Dis 2004; 8: 1382-4.
34. Breen RA, Miller RF, Gorsuch T, et al. Adverse events and treatment interruption in tuberculosis patients with and without HIV co-infection. Thorax 2006; 61: 791-4.
35. Taylor Z, Nolan CM, Blumberg HM, American Thoracic Society; Centers for Disease Control and Prevention; Infectious Diseases Society of America. Controlling tuberculosis in the United States. Recommendations from the American Thoracic Society, CDC, and the Infectious Diseases Society of America. MMWR Recomm Rep 2005; 54: 1-81.
36. Horsburgh CR. Priorities for the treatment of latent tuberculosis infection in the United States. N Engl J Med 2004; 350: 2060-7.
37. Smieja MJ, Marchetti CA, Cook DJ, Smaill FM. Isoniazid for preventing tuberculosis in non-HIV infected persons. Cochrane Database Syst Rev 2000; 2: CD001363.
38. Fraser A, Paul M, Attamna A, Leibovici L. Treatment of latent tuberculosis in persons at risk for multidrug-resistant tuberculosis: systematic review. Int J Tuberc Lung Dis 2006; 10: 19-23.
39. Fraser A, Paul M, Attamna A, Leibovici L. Drugs for preventing tuberculosis in people at risk of multiple-drug-resistant pulmonary tuberculosis. Cochrane Database Syst Rev 2006; 2: CD005435.
40. Feja K, McNelley E, Tran CS, Burzynski J, Saiman L. Management of pediatric multidrug-resistant tuberculosis and latent tuberculosis infections in New York City from 1995 to 2003. Pediatr Infect Dis J 2008; 27: 907-12.
41. Schaaf HS, Gie RP, Kennedy M, Beyers N, Hesseling PB, Donald PR. Evaluation of young children in contact with adult multidrug-resistant pulmonary tuberculosis: a 30-month follow-up. Pediatrics 2002; 109: 765-71.
42. Coker RJ, Mounier-Jack S, Martin R. Public health law and tuberculosis control in Europe. Public Health 2007; 121: 266-73.
43. Verklagsreglur um læknisrannsókn. Landlæknisembættið, Reykjavík 2007. Sjá www.landlaeknir.is/pages/898
