07/08. tbl. 94.árg. 2008
Fræðigrein
Blóðsýkingar barna með æxli og illkynja sjúkdóma 1991-2000
Bacteremia in children with tumors or malignant diseases 1991-2000
Ágrip
Inngangur: Árlega greinast 10-12 börn með æxli og illkynja sjúkdóma á Íslandi. Meðferð við illkynja sjúkdómum eykur hættu á alvarlegum sýkingum sem mikilvægt er að bregðast rétt við.
Markmið rannsóknarinnar var að meta blóðsýkingar í börnum með æxli og illkynja sjúkdóma, þar með talið einstakar bakteríur og sýklalyfjanæmi þeirra. Áhættuþættir voru einnig kannaðir.
Efniviður og aðferðir: Rannsóknin var aftur-skyggn og var rannsóknarþýðið öll börn á aldrinum 0-15 ára greind með illkynja sjúkdóm eða æxli á árunum 1991-2000 á Barnaspítala Hringsins. Upplýsingum var safnað um greiningu, meðferð, blóðræktanir, blóðgildi og fleira, svo sem sýklalyfjanotkun, aðskotahluti og afdrif.
Niðurstöður: Alls greindust 118 börn með illkynja sjúkdóm eða æxli á tímabilinu. Æxli í miðtaugakerfi (MTK) voru algengust (N=28, 23,7%), þá hvítblæði (N=21, 17,8%) og eitlakrabbamein (N=17, 14%). Meðalaldur barna við greiningu var 5,9 ár.
Upplýsingar úr sjúkraskrám voru fullnægjandi fyrir 99 börn. Af þeim var 51 barn blóðræktað. Fjöldi blóðræktana var 522. Meðalfjöldi blóðræktana var 14,8 hjá börnum með hvítblæði, en 2,6 hjá börnum með föst æxli. Blóðræktanir voru teknar úr holæðalegg eða lyfjabrunni í 63,6%, 5,4% úr útbláæð en 31% tilfella voru ótilgreind. Af 522 ræktunum voru 90 jákvæðar (17,2%). Algengasta bakterían var kóagúlasa-neikvæður stafýlókokkur (KNS) (N=53, 60%), en Staphylococcus aureus næstalgengastur (N=12, 13,3%). Jákvæð ræktun var talin tengjast líklegri eða sannaðri sýkingu í 47 tilfellum (52%), mengun í 17 (18,9%) en óvíst var með 26 ræktanir (27,7%).
Barn hafði daufkyrningafæð (ANC ?1,0 *109/L) við 302 blóðræktanir (61,4%). Meðallengd daufkyrningafæðar var 9,0 dagar. C-reative protein (CRP) var að meðaltali 63,9 mg/L við blóðræktun og meðalhiti var 38,8 °C. Í 183 tilfellum var barn á sýklalyfjum við blóðræktun (35,1%). Rannsóknarniðurstöður barna með jákvæða blóðræktun voru ekki frábrugðnar öðrum.
Ályktanir: Sýkingar af völdum Gram-jákvæðra baktería, sérstaklega KNS, eru nú mun algengari en Gram-neikvæðra baktería. Hluti jákvæðra ræktana getur þó verið mengun. Blóðrannsóknir virðast hafa lítið forspárgildi um niðurstöður blóðræktana.
Ekkert barn lést úr blóðsýkingu af völdum baktería á tímabilinu. Reynslusýklalyfjameðferð hérlendis virðist enn árangursrík.
Inngangur
Krabbamein er algengasta dánarorsök barna af völdum sjúkdóma á Vesturlöndum (1, 2). Langtímahorfur barna sem greinast með krabbamein hafa þó batnað til muna undanfarin ár. Þetta má meðal annars þakka betri og nákvæmari aðferðum við greiningu og flokkun þessara sjúkdóma og bættum meðferðarmöguleikum, þar með talið stuðningsmeðferð (2).
Meðferð krabbameina er aðallega þrenns konar: krabbameinslyf, geislameðferð og skurðlækningar (3). Krabbameinslyf valda meðal annars bælingu á beinmerg (4) og eftir slíka lyfjagjöf tekur það beinmerginn talsverðan tíma að jafna sig og framleiða nýjar frumur (2, 5). Illkynja sjúkdómur getur einnig sjálfur valdið hvítkornafæð (leukopenia) sjúklings og á það aðallega við um illkynja blóðsjúkdóma (3).
Tíðir fylgikvillar krabbameinsmeðferðar eru sýkingar af ýmsum toga, stundum lífshættulegar (6-9). Fari fjöldi daufkyrninga (neutrophila) niður fyrir ákveðin mörk eykst sýkingarhætta verulega (10, 11). Auk þessa geta aðrir þættir, til dæmis lengd og dýpt daufkyrningafæðar haft áhrif (10, 12). Ýmsir aðrir þættir gera sjúklinga enn varnarlausari gegn sýkingum, svo sem slímubólga (mucositis), skurðaðgerðir eða inniliggjandi aðskotahlutir og æðaleggir (11, 13, 14). Gram-jákvæðar bakteríur, sérstaklega kóagúlasa neikvæðir stafýlókokkar, eru nú á dögum aðalmeinvaldur í blóðsýkingum tengdum hita, daufkyrningafæð og inniliggjandi æðaleggjum á Vesturlöndum (10, 15-18).
Klínísk einkenni og niðurstöður rannsókna hafa þó litla fylgni við þróun lífshættulegra veikinda (19). Hjá ónæmisbældum sjúklingum getur ýmis einkenni og merki sýkingar vantað (20). Þessi einkenni hafa því minna gildi hjá sjúklingum í krabbameinsmeðferð og rannsóknaraðilar hafa lengi leitað annarra merkja sem gætu bent til sýkingar. Mest rannsökuð eru CRP, procalcitonin, interleukin-6 og interleukin-8 sem meðal annars kemur fram í yfirlitsgrein (21). Gildi CRP og procalcitonin virðast samsvara best stigi sýkingar og virðist procalcitonin heldur betri mæling (21, 22).
Reynslusýklalyfjameðferð (empiric antibiotic treatment) við hita í krabbameinssjúkum einstaklingum í daufkyrningafæð er afar breytileg á milli landa og stofnana. Á Íslandi hefur samsett reynslumeðferð við hita og daufkyrningafæð í krabbameinsveikum börnum verið breiðvirkt penicillín (píperacillín) og amínóglýkósíð (gentamícín) í samræmi við fyrri ráðleggingar Nordic organisation for paediatric haematology and oncology (NOPHO). Mikilvægt er að velja sýklalyf sem eru breiðvirk og hafa virkni gegn algengustu meinvöldum á hverjum stað og tíma. Algengt er að nota amínóglýkósíð og 3. eða 4. kynslóðar kefalósporin saman en rannsóknir hafa sýnt að 3. eða 4. kynslóðar kefalósporin eitt og sér sé nægjanleg meðferð (11, 23-25). Sumar sjúkrastofnanir nota einnig glýkópepíð (svo sem vankomýcín) sem þriðja lyf í ákveðnum tilfellum, svo sem í krabbameinssjúklingum með inniliggjandi aðskotahluti (11), meðal annars af ótta við alvarlegar sýkingar ónæmra baktería.
Mikil notkun breiðvirkra sýklalyfja getur þó haft ýmis vandamál í för með sér, svo sem aukaverkanir lyfjanna (20) og sýklalyfjaónæmi (26). Af þeim sökum skiptir máli að meðhöndla ekki lengur með breiðvirkum lyfjum en þörf er talin á.
Meðferð krabbameina í börnum hefur tekið miklum framförum, þótt sýkingar séu enn töluvert vandamál. Til að lækka dánartíðni vegna sýkinga er mjög mikilvægt að hefja meðferð snemma og áður en ræktunarniðurstöður eru kunnar (27). Faraldsfræði baktería er þó síbreytileg (21) og því er afar brýnt að afla vitneskju um tíðni algengustu sýkingarvalda og næmi þeirra fyrir sýklalyfjum. Markmið rannsóknarinnar var að varpa ljósi á þessa þætti til að hægt sé að beita bestu sýklalyfjameðferð sem völ er á.
Efniviður og aðferðir
Efniviður og rannsóknaraðferð
Rannsókn þessi var afturskyggn og í hana voru valdir allir sjúklingar á aldrinum 0-15 ára sem greinst höfðu með krabbamein eða önnur æxli á árunum 1991-2000 og voru til meðhöndlunar á Barnaspítala Hringsins. Upplýsingum var safnað úr sjúkraskrám um greiningu, meðferð, blóðræktanir, blóðrannsóknir og aðra þætti, svo sem inniliggjandi aðskotahluti og sýklalyfjanotkun. Fáein börn greindust undir lok tímabilsins en voru enn í meðferð árið 2001, ræktanir sem bárust árið 2001 frá þessum börnum voru teknar með í útreikninga.
Skráningaraðferðir
Skráðar voru sex breytur hjá hverjum þessara sjúklinga. Þær voru: 1) kyn, 2) greining (stuðst var við ICD9 og ICD10 greiningarkerfin og krabbameinsflokkun NOPHO (28)), 3) greiningardagsetning, 4) aldur við greiningu, 5) hvaða meðferð var beitt, þ.e. aðgerð, geislun eða lyfjameðferð og hvaða meðferðaráætlun (NOPHO protocol) var fylgt og 6) hvort blóðræktun hafi verið gerð, bæði á meðan meðferð stóð og á tveggja ára tímabili eftir að meðferð lauk. Ef blóðræktun var gerð voru eftirfarandi breytur skráðar til viðbótar:
Blóðræktun: Eftirfarandi atriði voru skráð: 1) dagsetning ræktunar, 2) hvaðan ræktun var tekin (úr bláæðalegg eða beint úr æð), 3) sýklalyfjanotkun þegar blóðræktun var gerð, 4) sýklalyfjameðferð og 5) niðurstöður ræktunar. Þegar sýklar ræktuðust úr blóði sjúklinga var auk þess skráð: 6) tegund sýkils/sýkla, 7) sýklalyfjanæmi og 8) lagt mat á hvort vöxtur sýkils væri vegna: a) sýkingar, b) líklegrar sýkingar, c) líklegrar mengunar, d) mengunar eða e) óvíst. Við þetta mat var stuðst við líkindi á því að viðkomandi örverutegund tengdist sýkingum eða mengunum, fjölda jákvæðra blóðræktunarsetta, hve fljótt ræktun varð jákvæð og í sumum tilfellum mat sérfræðinga í sýklafræði og/eða smitsjúkdómum (29).
Blóðmynd: Blóðprufuniðurstöður frá sama degi og blóðræktun var fengin voru skoðaðar. Þaðan fengust eftirfarandi breytur: 1) fjöldi hvítra blóðkorna, 2) fjöldi daufkyrninga og 3) CRP gildi. 4) Út frá fjölda daufkyrninga fékkst hvort um daufkyrningafæð væri að ræða þegar blóðræktunin var gerð. Daufkyrningafæð var skilgreind sem heildarfjöldi daufkyrninga <= 1,0 (x109/L) og viðmiðunargildi í samræmi við rannsóknastofu Landspítala (30). 5) Tímalengd daufkyrningafæðar var athuguð.
Líkamshiti: Hæsta hitastig á síðustu 12 klukkustundum fyrir blóðræktun var skráð.
Aðskotahlutir: Skráð var hvort sjúklingar höfðu: 1) inniliggjandi holæðalegg (central venous catheter), 2) lyfjabrunn (Port-A Catheter) eða 3) heilahólfa-kviðarhols ventil/skammhleypu (ventriculo-peritoneal shunt).
Afdrif sjúklinganna voru að lokum athuguð með áherslu á það hvort einhver börn létust úr sýkingu á tímabilinu.
Úrvinnsla og tölfræði: Þeir þættir sem kannaðir voru í sjúkraskrám voru skráðir í FileMaker Pro 5.0v. Eftir gagnasöfnun og úrvinnslu var gerður tölfræðilegur samanburður á börnum með jákvæðar og neikvæðar blóðræktanir og börn sem greindust með hvítblæði voru borin saman við börn sem greindust með föst æxli á tímabilinu.
Allir tölfræðiútreikningar voru gerðir í Excel og GraphPad InStat. Gögnin voru athuguð með ópöruðu t-prófi og Fisher exact prófi og var tölfræðilega marktækur munur talinn sem p-gildi lægra en 0,05.
Leyfi
Sótt var um tilskilin leyfi til Persónuverndar og Siðanefndar Landspítala. Fengið var samþykki fyrir rannsókninni og aðgangi að sjúkraskrám. Allar upplýsingar um sjúklinga voru skráðar undir sérstöku rannsóknarnúmeri og voru ekki persónugreinanlegar.
Niðurstöður
Faraldsfræði æxla og illkynja sjúkdóma
Sjúklingar voru alls 118, 62 drengir og 56 stúlkur. Nítján börnum þurfti að sleppa í athugun á blóðsýnum vegna skorts á gögnum í sjúkraskrám þeirra, einkum gögnum varðandi blóðrannsóknir. Aldur barnanna sem greindust var á bilinu 0 (börn sem höfðu meðfætt krabbamein) til og með 15 ára. Meðalaldur sjúklingahópsins var 5,9 (SD 4,6) ár og miðgildið var 5,0 ár. Ekki var marktækur munur á meðalaldri kynjanna við greiningu. Tíu börn greindust á fyrsta aldursári og þar af höfðu sex börn meðfæddan sjúkdóm. Af 118 börnum sem greindust á tímabilinu eru 15 látin, átta drengir og sjö stúlkur. Ekkert þeirra lést vegna blóðsýkingar af völdum baktería.
Fjöldi greininga æxla og illkynja sjúkdóma
Að meðaltali greindust 11,8 (SD 3,9) börn á ári og var miðgildið 11,5. Flest greindust 1997, alls 19, en fæst 1992 og 1994, sjö hvort ár.
Flokkun æxla og illkynja sjúkdóma og greiningaraldur
Æxli í miðtaugakerfi (MTK) voru 28, hvítblæði greindist hjá 21 barni og eitlakrabbamein í 17. Meðalaldur barna sem greindust með æxli í MTK var 7,2 ± 4,7 ár. Meðalaldur barna sem greindust með hvítblæði var 3,3 ± 1,9 ár. Ekkert barn greindist með hvítblæði eftir 8 ára aldur. Meðalaldur var 5,3 ± 3,9 ár hjá börnum sem greindust með eitlakrabbamein (mynd 1).
Blóðræktanir

Mynd 1. Æxli og illkynja sjúkdómar í 118 börnum, 1991-2000.
Nægar upplýsingar fundust í sjúkraskrám 99 barna af 118 (83,9%) til að hægt væri að hafa þau með í úttekt á blóðsýkingum. Af þessum 99 var 51 barn blóðræktað. Samtals voru gerðar 522 blóðræktanir frá þeim. Af 21 barni með hvítblæði voru átján blóðræktuð, samanlagt 267 sinnum. Af 97 börnum með föst æxli, þar af 81 með fullnægjandi upplýsingar um blóðhag, voru 33 börn blóðræktuð, samanlagt í 255 skipti. Flestar urðu blóðræktanirnar árið 1999, 97 talsins, en fæstar árið 1992, aðeins sjö ræktanir. Að meðaltali var þetta 51 barn blóðræktað 10,2 ± 8,6 sinnum. Miðgildið var 8,0 ræktanir. Flestar blóðræktanirnar urðu 44 hjá einu barni en fimm börn voru aðeins blóðræktuð einu sinni. Ef öll 99 börnin voru tekin með í útreikningana þá var meðaltal blóðræktana á hvert barn 5,3 ± 0,8 og var miðgildið 1,0 ræktun.
Meðalfjöldi blóðræktana á ári var 47,5 ± 28,2 með miðgildi 42,0 ræktanir á ári. Tæpur helmingur blóðræktana, eða 46,9%, voru gerðar hjá börnum með föst æxli en 53,1% ræktana hjá börnum með hvítblæði.
Þrjár blóðræktanir voru teknar úr börnum sem einungis höfðu farið í aðgerð og ein ræktun var dregin úr barni sem aðeins fékk geislameðferð. Hinar 518 ræktanirnar, 99,2%, voru teknar úr börnum sem fengið höfðu krabbameinslyfjameðferð einvörðungu eða sem hluta af sinni meðferð.
Úr holæðarlegg eða lyfjabrunni voru teknar 332 blóðræktanir eða rúmlega 60% ræktana. Í 28 tilfellum voru ræktanir teknar úr útbláæð (peripheral vein). Í 162 blóðræktunum, eða tæplega 30% tilvika, var ekki tilgreint hvaðan ræktunin var tekin.
Niðurstöður ræktana
Bakteríur ræktuðust úr 90 blóðræktunum eða 17,2%. Í fjórum ræktunum uxu tvær gerðir baktería.
Tæp 38% jákvæðra ræktana voru teknar úr börnum með föst æxli en 62,2% úr börnum með hvítblæði.
Þrjátíu og eitt barn hafði einhverja jákvæða ræktun á tímabilinu. Að meðaltali var í þessu 31 barni 2,9 ± 2,1 jákvæðra blóðræktana, en jákvæðu ræktanirnar voru að meðaltali 1,8 ± 2,2 ef öll börnin sem blóðræktuð voru eru tekin með. Flestar urðu jákvæðar ræktanirnar 11 hjá einu barni.
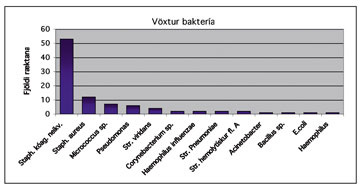
Mynd 2. Bakteríur sem ræktuðust úr blóði barna með æxli og illkynja sjúkdóma, 1991-2001
Algengasta baktería sem ræktaðist var kóagúlasa-neikvæður stafýlókokkur. Hann óx í 53 ræktunum eða í 58,9% jákvæðra ræktana. Næstalgengastur var Staphylococcus aureus, í 12 ræktunum eða 13,3% jákvæðra ræktana (mynd 2).
Skipt niður eftir Grams-litunareiginleikum voru Gram-jákvæðar bakteríur 89,4% en Gram-neikvæðar 10,6%.
Lagt var mat á vöxt þeirra baktería sem ræktuðust, skv. ákveðnum skilgreiningum sem voru hafðar til grundvallar (29). Vöxtur baktería í 26 tilvikum af 94 (27,7%) var talin raunveruleg blóðsýking. Líkleg sýking var metin í 21 tilfelli (22,3%), líkleg mengun í 11 tilvikum (11,7%) og mengun í 6 tilfellum (6,4%). Ekki var hægt að leggja mat á sýkingarlíkur í 26 tilfellum og féllu því 27, 7% sýkla sem ræktuðust í flokkinn óvíst.
Mælingar og aðrir þættir tengdir blóðræktunum
Sýklalyf við blóðræktun
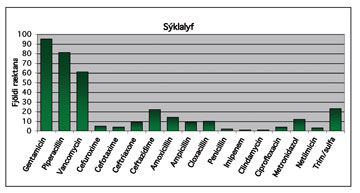
Mynd 3. Sýklalyfjanotkun þegar blóðræktunin var gerð.
Sýklalyfjameðferð var þegar hafin þegar 183 blóðræktanir voru teknar. Af þessum 183 skiptum var gentamícín notað í 51,9% tilfella, píperacillín í 44,3% tilvika og vankomýcín í 33,3% (mynd 3). Gentamícín og píperacillín voru notuð saman þegar 75 blóðræktanir voru teknar, eða í 40,9% tilvika. Vankomýcín var einnig notað með gentamícíni og piperacillini í 25 tilvikum eða 13,7%.
Af þeim blóðræktunum sem teknar voru þegar sýklalyfjameðferð var hafin reyndust 23 jákvæðar frá 13 sjúklingum og ræktuðust KNS í 12 skipti, Staphylococcus aureus í tvö, Pseudomonas í fimm skipti (þar af fjórum sinnum frá sama sjúklingnum) og einu sinni ræktuðust bacillus spp, corynebacterium eða E. coli. Í átta af þessum 23 skiptum var um að ræða varnandi sýklalyfjameðferð eða meðferð einfaldra sýkinga (amoxicillin (með eða án clavulanic sýru), trimetoprim/sulfamethoxazól eða mycostatin) en í 15 tilfellum hafði sterkari sýklalyfjameðferð verið hafin (amínóglýkósíð, 3. eða 4. kynslóðar kefalósporin eða glýkópeptíð).
Sýklalyfjanæmi
Bakteríur voru næmar fyrir gentamícíni, því lyfi sem börnin voru oftast á, í 36 ræktunum af 75, eða í tæplega 50% tilfella. Kóagúlasa-neikvæðir stafýlókokkar voru næmir fyrir gentamícíni í 30,8% tilvika.
Blóðmynd
Skoðaðar voru blóðrannsóknir sem gerðar voru samdægurs blóðræktunum.
Að meðaltali var fjöldi hvítra blóðkorna (leucocyta) 4,2 (x109/L). Miðgildið var 1,8. Ræktanir þar sem fjöldi hvítra blóðkorna samdægurs var <= 0,5 voru 127 eða 25,1% ræktana. Ræktanir þar sem fjöldi hvítra blóðkorna var ? 1,0 voru 185 eða 36,6% (tafla I).
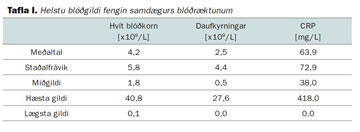
Barn var með daufkyrningafæð (neutropeniu) þegar 302 ræktanir voru gerðar eða í rúmlega 60% tilfella. Daufkyrningafjöldi var að meðaltali 2,5 (x109/L), miðgildi var 0,5. Sum barnanna höfðu hins vegar eðlilegan fjölda daufkyrninga en starfshæfni þeirra var ekki metin. Að meðaltali var daufkyrningafæð 9 daga löng.
Daufkyrningafæð hafði verið til staðar að meðaltali 8,9 ± 10,1 daga þegar blóðræktun var gerð. Miðgildið var 5,0 dagar. Lengsti tími daufkyrningafæðar var 71 dagur. Sjö blóðræktanir voru gerðar á fyrsta degi daufkyrningafæðar, 26 á öðrum degi en alls 46 á þriðja og fjórða degi (mynd 4).
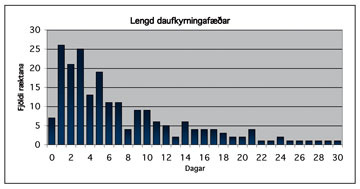
Mynd 4. Tímalengd daufkyrningafæðar þegar blóðræktun var gerð
Líkamshiti
Meðalhiti við blóðræktun reyndist 38,8 ± 0,98 °C og var miðgildið 38,9 °C. Hæsta hitastig var 41,4 °C og lægsti hiti 35,5 °C.
Aðskotahlutir
Skráð var hvort barn hefði einhvern aðskotahlut þegar blóðræktun var gerð. Í 97,3% blóðræktana, það er 508 ræktunum, reyndist barn hafa annað hvort holæðarlegg eða lyfjabrunn og var ekki gerður greinarmunur þar á. Í 14 tilfellum var barn ekki með neinn aðskotahlut þegar blóðræktun var gerð.
Samanburður
Hvítblæði og föst æxli
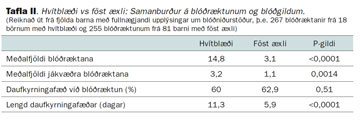
Blóðræktanir og blóðgildi voru borin saman hjá börnum með hvítblæði og föst æxli. Börn með hvítblæði voru 21, fullnægjandi upplýsingar um blóðniðurstöður lágu fyrir hjá öllum og voru blóðræktanir teknar hjá 18. Börn með föst æxli voru 97, fullnægjandi blóðniðurstöður lágu fyrir hjá 81 þeirra og voru blóðræktanir teknar hjá 33. Marktækur munur reyndist vera bæði á fjölda blóðræktana og fjölda jákvæðra ræktana hjá hópunum tveimur (tafla II).
Ekki reyndist marktækur munur á líkum á daufkyrningafæð þegar blóðræktun var gerð, en marktækur munur var á meðallengd daufkyrningafæðar í börnum með hvítblæði og börnum með föst æxli á tímabilinu.
Jákvæðar og neikvæðar blóðræktanir
Bornar voru saman niðurstöður blóðprófa og hiti frá börnum með jákvæðar og neikvæðar blóðræktanir (tafla III). Aldrei var marktækur munur á blóðgildum.
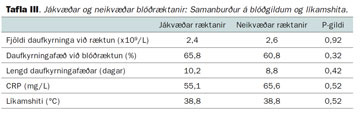
Niðurstöður hjá börnum með jákvæðar og neikvæðar blóðræktanir voru einnig bornar saman með tilliti til hæsta hitastigs síðustu 12 klukkustundir fyrir ræktun. Ekki fannst tölfræðilega marktækur munur á meðalhita og var dreifing hitastigs álíka.
Umræða
Niðurstöður okkar sýna að Gram-jákvæðar bakteríur ræktast nú mun oftar en Gram-neikvæðar bakteríur í börnum í krabbameinsmeðferð, sem ber vel saman við erlendar rannsóknir (8, 11, 25). Reynslusýklalyfjameðferð sem notuð er hérlendis virðist enn sem komið er nægjanleg. Athygli vakti að niðurstöður blóðrannsókna virðast spá illa fyrir um niðurstöður blóðræktana.
Fjöldi blóðræktana var mismunandi eftir árum á tímabilinu. Hér verður þó að hafa í huga að meðferð við krabbameinum tekur oft 2-3 ár (2, 3). Auk þess er breytilegt milli ára hvaða tegundir krabbameina greinast.
Þegar skoðað var hvaða meðferð börn fengu, sem blóðræktuð voru, kom í ljós að rúm 99% blóðræktana, eða 518 ræktanir, voru teknar úr börnum sem fengið höfðu krabbameinslyfjameðferð eingöngu, eða sem hluta af sinni meðferð. Þegar jákvæðar blóðræktanir voru svo skoðaðar reyndust allar þessar ræktanir hafa verið teknar úr börnum sem fengu krabbameinslyf í sinni meðferð.
Niðurstöður jákvæðra blóðræktana sýndu að Gram-jákvæðar bakteríur voru um 90%. Þar af ræktuðust kóagúlasa-neikvæðir stafýlókokkar í 60% tilfella. Á síðustu 20 árum hafa blóðsýkingar krabbameinsveikra barna verið að breytast úr því að vera ráðandi sýkingar Gram-neikvæðra baktería yfir í ráðandi Gram-jákvæðar bakteríusýkingar (8, 11, 25). Þetta má rekja til öflugri krabbameinslyfjameðferða, sem valda djúpri daufkyrningafæð, og aukinni notkun inniliggjandi æðaleggja og lyfjabrunna (8). Í þessari rannsókn voru aðeins rúmlega 10% baktería sem ræktuðust Gram-neikvæðar bakteríur og er þetta hlutfall svipað og fengist hefur í sambærilegum rannsóknum í Bandaríkjunum og Vestur-Evrópu (10, 17, 18).
Lagt var mat á vöxt þeirra baktería sem ræktuðust, þ.e. hvort um sýkingu, líklega sýkingu, líklega mengun eða mengun væri talið að ræða. Í 47 tilfellum eða rúmlega 50% jákvæðra ræktana var vöxtur talinn líkleg eða sönnuð blóðsýking. Erfitt getur verið að meta hvort jákvæð ræktun í ónæmisbældum einstaklingi með inniliggjandi aðskotahlut sé sýking. Í 26 tilfellum var ekki hægt að flokka vöxt sem (líklega) sýkingu eða mengun og því féllu þessi tilfelli í flokkinn óvíst. Hópurinn er því nokkuð misleitur hvað þetta varðar. Einnig má hafa í huga að flestar ræktanirnar voru teknar úr æðaleggjum barna auk þess sem blóðtökustaður var ótilgreindur í nær þriðjungi tilfella.
Athuguð var sýklalyfjanotkun þeirra barna sem blóðræktuð voru. Í alls 183 tilfellum var barn á sýklalyfjum þegar blóðræktun var gerð og voru 23 jákvæðar og var oftast um KNS að ræða. Algengt er að taka blóðræktanir eftir að meðferð er hafin með sýklalyfjum ef bati er hægur og orsök óþekkt. Gentamícín og píperacillín voru langalgengust og voru gefin saman í 40% tilvika. Þessi samsetning er eins og áður sagði reynslusýklalyfjameðferðin við hita og daufkyrningafæð í krabbameinsveikum börnum hér á landi. Sýklalyfjameðferð þarf að taka mið af hvaða bakteríur eru algengar og næmi þeirra fyrir sýklalyfjum. Ekki er hægt að treysta á erlendar rannsóknir í því samhengi heldur er nauðsynlegt að þekkja faraldsfræði baktería og sýklalyfjanæmi þeirra á hverjum stað fyrir sig.
Í þessari rannsókn voru aðeins um 30% af þeim kóagúlasa-neikvæðu stafýlókokkum sem ræktuðust næmir fyrir gentamícíni. Íhuga mætti hvort nauðsynlegt sé að breyta reynslumeðferðinni við daufkyrningafæð og hita í ljósi þessa lága hlutfalls kóagúlasa-neikvæðra stafýlókokka sem næmir voru fyrir gentamícíni. Algengt er að nota amínóglýkósíð og 3. eða 4. kynslóðar kefalósporin saman en rannsóknir hafa sýnt að 3. eða 4. kynslóðar kefalósporin eitt og sér sé í völdum tilfellum nægjanleg meðferð (11, 23-25). Sumar sjúkrastofnanir nota einnig glýkópeptíð (svo sem vankomýcín) sem þriðja lyf í ákveðnum tilfellum, svo sem í krabbameinssjúklingum með inniliggjandi aðskotahluti (11). Ekki hefur þó enn verið sýnt fram á nauðsyn þess að bæta vankomýcíni við reynslusýklalyfjameðferð við hita í sjúklingum með daufkyrningafæð, þó að vísbendingar séu um gagnsemi þess (11, 15, 24, 25). Eru þær niðurstöður einkum byggðar á því að langalgengustu meinvaldar í blóðsýkingum tengdum hita, daufkyrningafæð og inniliggjandi aðskotahlutum eru kóagúlasa-neikvæðir stafýlókokkar (10, 15-18). Alvarleg, bráð blóðsýking af þeirra völdum er afar fátíð og ef um raunverulega sýkingu er að ræða gefst nær alltaf tími til að breyta um sýklalyf við hæfi (11, 15). Sú staðreynd að ekkert þeirra 118 barna sem greindust með krabbamein eða önnur æxli á tímabilinu hefur látist vegna bakteríublóðsýkingar bendir til þess að reynslusýklalyfjameðferð hér á landi sé árangursrík. Af þessum niðurstöðum mætti draga þá ályktun að reynslusýklalyfjameðferð hérlendis skuli vera breiðvirk, ná yfir Gram-jákvæðar og Gram-neikvæðar bakteríur, en að hún þurfi ekki að vera sértæk fyrir óvenjulegar sýkingar af völdum Gram-jákvæðra baktería. Er það samhljóða ályktunum erlendra rannsóknaraðila (11, 15). Ef sjúklingur svarar hins vegar ekki reynslusýklalyfjameðferðinni og niðurstöður ræktunar leiða í ljós Gram-jákvæðar lyfjaónæmar bakteríur þá ætti að skoða aðra möguleika, þar á meðal vankomýcín.
Skoðaðar voru blóðrannsóknir sem gerðar voru samdægurs blóðræktunum. Að meðaltali voru hvít blóðkorn 4,2 (x109/L) þegar blóðræktun var gerð og er það undir eðlilegum fjölda í viðmiðunargildum fyrir börn. Tæpur helmingur barnanna var með hvítkornafæð við blóðræktun. Þetta kemur kannski ekki á óvart ef litið er til þess að langflest barnanna, sem blóðræktuð voru, fengu krabbameinslyf sem hluta af sinni meðferð og ekki óalgengt að blóðgildi slíkra barna séu óeðlileg (4).
Daufkyrningafjöldi var að meðaltali 2,5 (x109/L), en það er innan eðlilegra marka samkvæmt viðmiðunargildum. Þegar miðgildi daufkyrningafjölda var hins vegar skoðað sést að fjöldinn er einungis 0,5, sem er langt undir eðilegum mörkum. Í um 50% blóðræktana voru daufkyrningar færri en 0,5 sem er oft notað sem mörk alvarlegrar daufkyrningafæðar í börnum í krabbameinsmeðferð (10, 12, 31). Sum barnanna höfðu hins vegar eðlilegan fjölda daufkyrninga en starfshæfni þeirra var ekki metin. Að meðaltali var daufkyrningafæð 9 daga löng. Þessar niðurstöður eru líkt og búast mátti við, þar sem það tekur merginn að jafnaði 5-10 daga að jafna sig eftir krabbameinslyfjameðferð (11).
CRP var að meðaltali 63,9 (mg/L) þegar börn voru blóðræktuð. CRP er einna best þekkta bólgumerki í krabbameinssjúklingum (32) og hafa rannsóknir sýnt að sé CRP gildi hærra en 90 er líklegt að sýking af völdum baktería sé til staðar (12). Í þessari rannsókn reyndist CRP vera yfir 90 í rúmlega 20% blóðræktana. Þetta passar vel við fjölda jákvæðra blóðræktana en er þó eilítið hærra. Ýmsar ástæður geta verið fyrir því, meðal annars getur CRP verið hækkað vegna annarra sýkinga eða vegna virkni undirliggjandi illkynja sjúkdóms (32). Ljóst er einnig í rannsókn okkar að CRP greinir ekki milli einstaklinga sem reyndust með jákvæðar eða neikvæðar blóðræktanir. Því má ekki styðjast eingöngu við þessar mælingar, heldur ættu þær frekar að vera hluti af heildarmati á ástandi sjúklings (21).
Meðalhiti við blóðræktun reyndist 38,8°C og var tæpur helmingur blóðræktana tekinn þegar hitinn var á bilinu 38,5-39°C. Athyglisvert er því að alls 62 blóðræktanir, eða 13% ræktana, voru gerðar þegar hiti barns var lægri en 38°C. Hér ber þó að minnast að ýmis önnur einkenni geta bent til sýkingar, svo sem verkir, hósti og roði á húð (21) og því eru blóðræktanir oft gerðar þótt barn hafi ekki háan hita.
Borin voru saman börn sem höfðu föst æxli og börn sem höfðu hvítblæði á tímabilinu. Í ljós kom að tölfræðilega marktækur munur var á meðalfjölda blóðræktana, fjölda jákvæðra ræktana og á því hversu lengi sjúklingar voru í daufkyrningafæð. Sjúklingar með illkynja blóðsjúkdóma virðast því móttækilegri fyrir blóðsýkingum en sjúklingar með föst æxli, og eru þessar niðurstöður sambærilegar niðurstöðum annarra rannsókna (18). Ástæður þessa geta annaðhvort verið vegna sjúkdómsins sjálfs, svo sem beinmergsbæling af völdum hvítblæðis, eða vegna meðferðarinnar, en sjúklingar með hvítblæði þurfa jafnan að gangast undir erfiðari og lengri krabbameinslyfjameðferð og vegna þess lengri hvítkorna- og daufkyrningafæð en sjúklingar með föst æxli (8, 11, 31, 33).
Þegar bornar voru saman tölur frá börnum með jákvæðar og neikvæðar blóðræktanir kom í ljós að aldrei var marktækur munur á blóðgildum. Blóðrannsóknir virðast því hafa lítið forspárgildi á niðurstöður blóðræktana. Hér verður þó að athuga að fjöldi hvítra blóðkorna og daufkyrninga getur í mörgum tilfellum verið óeðlilega lágur vegna illkynja sjúkdómsins sjálfs og oft verður ekki hvítkornafjölgun hjá þessum börnum (20). CRP hækkar þar að auki ekki marktækt fyrr en 24-48 klukkustundum eftir upphaf bólguviðbragða, auk þess sem samband er á milli styrks þess í blóði og vefjaskemmda eða virkni undirliggjandi illkynja sjúkdóms (32). Einnig getur CRP hækkað við aðrar sýkingar, svo sem veirusýkingar í blóði (32). Að auki ber að geta þess að næmi blóðræktana er ótryggt þegar aðeins ein blóðræktun er tekin.
Börn með jákvæðar og neikvæðar blóðræktanir voru einnig borin saman með tilliti til hæsta hitastigs síðustu 12 klukkustundir fyrir ræktun. Ekki fannst tölfræðilega marktækur munur á meðalhita og var dreifing hitastigs álíka þegar um jákvæðar og neikvæðar ræktanir var ræða. Þessar niðurstöður benda til þess að líkamshiti við blóðræktun segi ekki vel fyrir um hvort ræktun muni verða jákvæð eða neikvæð. En líklegt verður þó að teljast að einhverjar þessara jákvæðu ræktana séu mengun.
Dánartíðni af völdum blóðsýkinga í krabbameinsveikum börnum hefur farið sífellt lækkandi á síðustu árum, þrátt fyrir aukna krabbameinslyfjameðferð. Þetta má meðal annars þakka bættri stuðningsmeðferð fyrir krabbameinsveik börn, svo sem tíðari gjöfum vaxtarþátta sem örva myndun blóðfrumna í merg, sem og árangursríkri reynslusýklalyfjameðferð við grunuðum sýkingum. Stöðug endurskoðun á reynslusýklalyfjameðferð við hita og daufkyrningafæð er þó ákaflega mikilvæg. Til að svo megi verða er nauðsynlegt að afla nýjustu þekkingar á tíðni algengustu sýkingarvalda og næmi þeirra fyrir sýklalyfjum.
Þessi rannsókn svarar brýnum spurningum og bætir við þekkingu manna á blóðsýkingum barna hérlendis. Staðfestir hún einnig mikilvægi eftirlits með börnum sem gangast þurfa undir erfiða krabbameinsmeðferð og verða móttækilegri fyrir hvers kyns sýkingum. Ennfremur gefur hún ekki að svo stöddu tilefni til breyttrar reynslusýklalyfjameðferðar hjá börnum með daufkyrningafæð og hita á Barnaspítala Hringsins þó vissulega beri að hafa í huga umtalsverðan fjölda af kóagúlasa neikvæðum stafýlókokkum.
Niðurstöðurnar renna styrkum stoðum undir kenningar erlendra rannsóknaraðila en gefa einnig tilefni til frekari rannsókna. Athyglisvert væri að gera áframhaldandi rannsókn, sem næði yfir lengra tímabil og hefði þar af leiðandi stærri sjúklingahóp. Þá væri einnig forvitnilegt að skoða aðrar sýkingar í þessum hópi barna, svo sem staðbundnar sýkingar eða blóðsýkingar af völdum sveppa eða veira. Vonandi gefst tækifæri til þess síðar meir.
Þakkir
Starfsfólk skjalasafns Landspítala í Vesturhlíð, sem og ritarar á Barnaspítala Hringsins, fá kærar þakkir. Einnig viljum við þakka rannsóknarhópnum á Barnaspítala Hringsins og kvennadeild Landspítala.
Heimildir
1. Longo DL. Approach to the patient with cancer. In: Kasper DL, Braunwald E, Fauci AS, Hauser SL, Longo DL, Jameson JL, editors. Harrison´s Principles of Internal Medicine. 16th ed. New York: he McGraw-Hill Companies, Inc; 2005. p. 435-41.
2. Nachman JB, Abelson HT. Oncology. In: Behrman E, Kliegman R, editors. Nelson Essentials of Pediatrics. 4th ed. Philadelphia: W.B.Saunders Company; 2002: 645-69.
3. Sausville EA, Longo DL. Principles of cancer treatment: surgery, chemotherapy and biologic therapy. In: Kasper DL, Braunwald E, Fauci AS, Hauser SL, Longo DL, Jameson JL, editors. Harrison´s Principles of Internal Medicine. 16th ed. New York: The McGraw-Hill Companies, Inc.; 2005: 464-89.
4. Allison AC. Immunosuppressive drugs: the first 50 years and a glance forward. Immunopharmacology 2000; 47: 63-83.
5. Kristinsson VH, Kristinsson JR, Jónmundsson GK, Jónsson OG, Thorsson AV, Haraldsson Á. Immunoglobulin Class and Subclass Concentrations After Treatment of Childhood Leukemia. Pediatric Hemato Oncol 2001; 18: 167-72.
6. Shaw PJ. Suspected infection in children with cancer. J Antimicrobial Chemotherapy 2002; 49 Suppl 1: 63-7.
7. Finberg R. Infections in Patiens with Cancer. In: Kasper DL, Braunwald E, Fauci AS, Hauser SL, Longo DL, Jameson JL, editors. Harrison´s Principles of Internal Medicine. 16th ed. New York: The McGraw-Hill Companies, Inc.; 2005: 489-97.
8. Auletta JJ, O?Riordan MA, Nieder ML. Infections in children with cancer: a continued need for the comprehensive physical examination. J Pediatric Hemato Oncol 1999; 21: 501-8.
9. Urrea M, Rives S, Ofelia C, Navarro A, García JJ, Estella J. Nosocomial infections among pediatric hematology/oncology patients: results of a prospective incidence study. Am J Infection Control 2004; 34: 205-8.
10. Pizzo PA. Fever in Immunocompromised Patients. Current Concepts 1999; 341: 893-9.
11. Blijlevens NMA, Donnelly JP, de Pauw BE. Empirical therapy of febrile neutropenic patients with mucositis: challenge of risk-based therapy. Clin Microbiol Infection 2001; 7: 47-53.
12. Santolaya ME, Alvarez AM, Becker A, et al. Prospective, multicenter evaluation of risk factors associated with invasive bacterial infection in children with cancer, neutropenia, and fever. J Clin Oncol 2001; 19: 3415-21.
13. Dourd MC, Arlet G, Leverger G, et al. Quantitative blood cultures for diagnosis and management of catheter-related sepsis in pediatric hematology and oncology patients. Intensive Care Med 1991; 17: 30-5.
14. Pizzo PA. Management of Fever in Patients with Cancer and Treatment-Induced Neutropenia. N Engl J Med 1993; 328: 1323-32.
15. Langley J, Gold R. Sepsis in febrile neutropenic children with cancer. Pediatr Infect Dis J 1988; 7: 34-7.
16. Rosato AE, Tallent SM, Edmond MB, Bearman GML. Susceptibility of coagulase-negative staphylococcal nosocomial boodstream isolates to the chlorhexidine/silver sulfadiazine-impregnated central venous catheter. Am J Infect Control 2004; 32 :486-8.
17. Philpott DC, Georg RH. Central venous catheter-related septicaemia in peadiatric cancer patients. J Hosp Infection 1997; 36: 67-76.
18. Hengartner H, Berger C, Nadal D, Niggli FK, Grotzer MA. Port-A-Cath infections in children with cancer. Eur J Cancer 2004; 40 (2452-8).
19. West DC, Marcin JP, Mawis R, He J, Nagle A, Dimand R. Children with cancer, fever, and treatment-induced neutropenia: risk factors associated with illness raquiring the administration of critical care therapies. Pediatr Emerg Care 2004; 20: 79-84.
20. Klastersky J. Empirical treatment of sepsis in neutropenic patients. Int J Antimicrobial Ag 2000; 16: 131-3.
21. Cohen J, Brubn-Buisson C, Torres A, Jorgensen J. Diagnosis of infection in sepsis: An evidence-based review. Crit Care Med 2004; 32(11 (Suppl.)): 466-94.
22. Luzzani A, Polati E, Dorizzi R, Rungatscher A, Pavan R, Merlini A. Comparison of procalcitonin and C-reactive protein as markers of sepsis. Crit Care Med 2003; 31: 1737-41.
23. Chuang YY, Hung IJ, Yang CP, Jaing TH, Lin TY, Huang YC. Cefepime versus ceftazidime as empiric monotherapy for fever and neutropenia in children with cancer. Pediatr Infect Dis J 2002; 21: 203-9.
24. Kline RM, Baorto EP. Treatment of Pediatric Febrile Neutropenia in the Era of Vancomycin-Resistant Microbes. Pediatr Blood Cancer 2005; 44: 207-14.
25. Haslam DB. Managing the child with fever and neutropenia in an era of increasing microbial resistance. J Pediatr 2002; 140: 5-7.
26. Ammann RA, Hirt A, Luthy AR, Aebi C. Identification of Children Presenting With Fever in Chemotherapy-Induced Neutropenia at Low Risk for Severe Bacterial Infection. Med Pediatr Oncol 2003; 41: 436-43.
27. Rúnarsson G, Önundarson PT, Kristinsson KG, Jóhannsson GM, Björnsdóttir J, Magnússon S. Sýkingar sjúklinga með brátt hvítblæði og neutropeniu á Landspítalanum 1981-1991. Læknablaðið 1992; 78(Fylgirit 21).
28. Gustafsson G, Langmark F, Wesenberg F, Lannering B, Heyman M, de Verdier B. Childhood Cancer in the Nordic Countries: Report on Epidemiologic and Therapeutic Results From Registries and Working Groups. NOPHO Annual Meeting; 2005; Lillehammer; 2005.
29. Árnason S, Thors VS, Guðnason Þ, Kristinsson KG, Haraldsson Á. Blóðsýkingar barna á Íslandi 1994-2005. Læknablaðið 2008; 94: 525-9.
30. Blóðmeinafræði - Klínísk efnafræði - Handbók B. Available from: URL: www4landspitaliis/lsh_ytrinsf/pages/rabokbhtm. Maí 2005.
31. Pastura PSVC, Land MGP, Santoro-Lopes G. Predictive Model for the Length of Hospital Stay of Children With Hematologic Malignancies, Neutropenia, and Presumed Infection. J Pediatr Hematol Oncol 2004; 26: 813-6.
32. Fleischhack G, Kambeck I, Cipic D, Hasan C, Bode U. Procalcitonin in paediatric cancer patients: its diagnostic relevance is superior to that of C-reactive protein, interleukin 6, interleukin 8, soluble interleukin 2 receptor and soluble tumor necrosis factor receptor II. Brit J Haematol 2000; 111: 1093-102.
33. Abbas AAH, Fryer CJH, Paltiel C, et al. Factors Influencing Central Line Infections in Children With Acute Lymphoblastic Leukemia: Results of a Single Institutional Study. Pediatr Blood Cancer 2003; 42: 325-31.
