10. tbl 93. árg. 2007
Fræðigrein
Fósturköfnun og heilakvilli - áhættuþættir og afleiðingar fyrir nýbura
Birth asphyxia, neonatal risk factors for hypoxic ischemic encephalopathy
Ágrip
Tilgangur: Þeirri spurningu er enn ósvarað hvers vegna sum börn sem verða fyrir fósturköfnun (asphyxia perinatalis) við fæðingu fá í kjölfarið heilakvilla af völdum súrefnisþurrðar (hypoxic ischemic encephalopathy, HIE) á meðan önnur ná fullum bata. Tilgangur rannsóknarinnar var að kanna tíðni fósturköfnunar HIE í kjölfar á Landspítala á árunum 1997-2001 auk þess að leita að forspárþáttum hjá barninu sem auka líkurnar á fósturköfnun og HIE í kjölfarið.
Efniviður og aðferðir: Sjúklingahópurinn samanstóð af þeim börnum sem fengu greininguna fósturköfnun, voru fullburða, fædd á Kvennasviði Landspítala 1997-2001 að báðum árum meðtöldum, með Apgar stig <6 við fimm mínútna aldur. Upplýsingum var safnað á afturskyggnan hátt úr sjúkraskrám barnanna og mæðra þeirra. Apgar stig voru skráð við einnar, fimm og tíu mínútna aldur. Jafnframt sýrustig blóðs, blóðgös, fjöldi kjarnaðra rauðra blóðkorna og magn blóðrauða úr fyrsta blóðsýni. Einnig voru lengd og þyngd barnanna við fæðingu skráð.
Niðurstöður: Nýgengi HIE meðal fullburða barna var 1,4/1000 á rannsóknartímabilinu. Börn sem fengu HIE reyndust hafa marktækt meiri blóðsýringu eftir fæðingu ásamt því sem basaskortur (base deficit) var marktækt og bíkarbónat var marktækt lægra hjá þeim börnum sem fengu HIE en þeim sem einungis fengu fósturköfnun. Gildi blóðrauða reyndist marktækt lægra hjá þeim sem fengu HIE en þeim sem ekki fengu HIE. Apgarstig voru einnig marktækt lægri hjá börnum sem fengu HIE.
Ályktanir: Tíðni HIE í þessari rannsókn var lág miðað við samanburðarrannsóknir. Lág Apgar stigun, mikil blóðsýring og lægri fæðingarþyngd við fæðingu hafa forspárgildi um hvaða börn fá HIE eftir fósturköfnun. Öfug fylgni er á milli magns blóðrauða barns við fæðingu og hættu á HIE í kjölfar fósturköfnunar.
Inngangur
Ferðin gegnum fæðingarveginn er ekki hættulaus. Allt sem hefur áhrif á súrefnisflutning frá móður til fósturs getur stefnt fóstrinu í hættu. Þó er því eðlislægt að lifa af í súrefnisskertu umhverfi, þar sem hlutþrýstingur súrefnis í fósturblóðrásinni er ekki nema 20-25 mmHg en 85-100 mmHg eftir fæðinguna (1). Lækkun á hlutþrýstingi súrefnis verður í öllum fæðingum en stefnir fóstrinu ekki í hættu nema í fáum tilvikum. Fari súrefnisþurrðin niður fyrir þolmörk fósturs leiðir það til breytinga á efnaskiptum þess. Frumur fósturs skipta þá yfir í loftfirrtan bruna á glúkósa og þannig eykst þéttni mjólkursýru og sýrustig í vefjum og blóði þess lækkar. Þessi súrefnisþurrð við burðarmál hefur verið nefnd ,,asphyxia perinatalis" og á íslensku fósturköfnun. Alvarleg fósturköfnun getur valdið óafturkræfum líffæraskemmdum og jafnvel fósturdauða.
Erlendar rannsóknir sýna breytilegar tíðnitölur fyrir fósturköfnun frá tveimur til níu /1000 lifandi fæddra barna (2-4). Endurspegla þessar breytilegu tölur vel hvernig skilgreining fósturköfnunar hefur verið á reiki. Lengst af hefur verið stuðst við tvo þætti til greiningar í því sambandi, annars vegar Apgar stigun og hins vegar sýrustigsmælingar í blóði barns eftir fæðingu (5). Miðað hefur verið við að Apgar stig séu færri en sjö við fimm mínútna aldur og að sýrustig í nýfæddu barni með fósturköfnun sé <7,20 í blóði frá naflastrengsslagæð. Basaskortur (base deficit) þarf að vera meira en 6 mmól/L og lækkun á sýrustigi á að vera vegna aukins magns mjólkursýru en ekki vegna aukins koltvísýrings í blóði barnsins (6, 7).
Börn sem verða fyrir fósturköfnun eru í aukinni hættu á að fá heilakvilla af völdum súrefnisþurrðar (hypoxic ischemic encephalopathy, HIE) (8). Tíðni þessa heilkennis er samkvæmt erlendum rannsóknum á bilinu tvö til sjö/1000 fullburða börn (2, 9, 10). HIE kemur fram á fyrstu dögum eftir fæðingu og einkennist af auðertanleika, öndunarslævingu, minnkaðri vöðvaspennu, minnkuðum sogkrafti, skertri meðvitund og í alvarlegri tilfellum krömpum eða algjöru meðvitundarleysi (8). Einkenni heilakvilla af völdum súrefnisþurrðar hafa þótt spá betur fyrir um afdrif barna í kjölfar fósturköfnunar heldur en Apgar stigun eða sýrustigsmælingar (8, 11, 12).
Engar fyrri rannsóknir á fósturköfnun og HIE í íslensku þýði hafa verið birtar. Tilgangur rannsóknarinnar var jafnframt að leita að áhættuþáttum nýbura fyrir alvarlegri fósturköfnun og HIE í kjölfarið. Einnig að kanna hvort greiningaraðferðin á fósturköfnun og HIE sem notuð hefur verið á Landspítala sé byggð á réttum forsendum.

Mynd 1. Rannsóknarhópurinn.
Efniviður og aðferðir
Um var að ræða afturskyggna hóprannsókn á börnum sem urðu fyrir fósturköfnun og fæddust á Kvennadeild Landspítala á árunum 1997-2001 að báðum árum meðtöldum. Innan hóprannsóknarinnar var gerður samanburður á börnum sem fengu HIE og hinum sem ekki fengu merki um HIE.
Skilyrði fyrir þátttöku í rannsókninni
Barnið þurfti að hafa fengið ICD-10 greininguna fósturköfnun með greiningarnúmerum P21.0, P21.1 eða P21.9. Barnið þurfti að hafa fengið minna en sjö í Apgar stigun fimm mínútum eftir fæðingu og vera fætt eftir fulla meðgöngulengd (> 37 vikur samkvæmt ómskoðun á 19. viku).
Klínískar upplýsingar
Skráð var þyngd, lengd og höfuðummál barnanna. Apgar stigun sem barnið fékk við eina, fimm og tíu mínútur, einnig hvernig öndunaraðstoð barnið þurfti á að halda. Skráð var hvaða börn fengu HIE, sem var nánar greint niður í þrjá flokka samkvæmt skilgreiningu Sarnat og Sarnat. Fyrsta stig einkennist af ofurertanleika, líflegum taugaviðbrögðum, auknum einkennum frá semjuhluta sjálfvirka taugakerfisins og einkenni vara skemur en 24 klukkustundir. Annað stig einkennist af hypótóníu, kreppum í fjarlægari liðamótum og flogum sem eiga upptök á fleiri en einum stað í heila. Þriðja stig einkennist af meðvitundarleysi og viðbragðaleysi hjá nýburanum (8). Bæði var stuðst við upplýsingar úr sjúkraskrá um greininguna auk þess sem slík greining var alltaf borin undir greinarhöfunda (AD og ÞÞ) til staðfestingar. Sýrustig, þéttni bíkarbónats, basaskortur (base deficit), hlutþrýstingur koltvísýrings og þéttni mjólkursýru úr fyrsta blóðgasasýni frá barni var skráð sem og tíminn sem leið frá fæðingu þar til sýnið var tekið. Við samanburð á blóðgasamælingum milli HIE hóps annars vegar og þeirra sem ekki fengu HIE hins vegar voru eingöngu tekin með þau sýni sem voru tekin innan við klukkustund frá fæðingu. Einnig voru blóðhagur og fjöldi kjarnaðra rauðra blóðkorna í fyrsta blóðsýni skráð. Við samanburð á blóðrauðagildum milli hópanna tveggja var aðeins reiknað með þeim sýnum sem voru tekin innan við tveimur klukkustundum frá fæðingu.
Tölfræði og úrvinnsla
Við úrvinnslu niðurstaðna var notað eftir því sem við átti, Mann-Whitney próf, t-próf, kí-kvaðrats-próf og Anova próf í tölfræðiforritinu SPSS. Viðeigandi leyfi fyrir rannsókninni voru fengin frá Persónuvernd og Siðanefnd Landspítala. Leyfi til athugana á sjúkraskrám voru fengin hjá vörslumönnum sjúkraskráa á Kvennasviði Landspítala og Barnaspítala Hringsins.
Niðurstöður
Á rannsóknartímabilinu var heildarfjöldi fæddra barna á Kvennadeild Landspítala 14.217 þar af 13.495 fullburða (>37 vikna meðganga). Á sama tímabili fengu 248 börn ICD-10 greiningarnúmerin sem stuðst var við. Samræmdust 132 þeirra inntökuskilyrðum í rannsóknina. Af þeim fengust ófullnægjandi upplýsingar fyrir fimm börn og því voru 127 börn í rannsóknarhópnum. Hin 116 voru ýmist fyrirburar, fædd á öðrum sjúkrahúsum eða höfðu fengið meira en sex í Apgar við fimm mínútna aldur. Nýgengi fósturköfnunar á rannsóknartímabilinu var því 9,4/1000 lifandi fullburða börn (13).
Í fósturköfnunarhópnum (n=127) sýndu 19 merki um HIE eða 15% hópsins, þar af voru fimm sem fengu alvarlegasta form HIE. Nýgengi HIE meðal fullburða barna á rannsóknartímabilinu var því 1,4 barn af hverjum 1000 fullburða fæddum. Af þeim fimm börnum sem fengu alvarlegasta form HIE dóu fjögur börn á fyrstu dögum eftir fæðinguna. Dánartíðni vegna HIE meðal fullburða barna var 0,3/1000 á rannsóknartímabilinu. Dánartíðni (case fatality) af völdum fósturköfnunar var 3,15%. Fimmta barnið sem fékk merki um alvarlega HIE hlaut varanlegar heilaskemmdir og er fjölfatlað og þroskaheft.
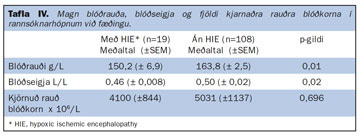
Í töflum I-IV sést nánari samanburður milli barna sem sýndu merki um HIE (n=19) og þeirra barna sem ekki sýndu merki um HIE (n=108). Í ljós kom að þau börn sem fengu HIE voru marktækt léttari (p=0,03) og styttri (p=0,04) en þau sem ekki fengu HIE (tafla I). Meðaltal Apgar stiga hjá börnunum í HIE hópnum reyndust marktækt lægri við 1, 5 og 10 mínútna aldur (tafla II). Við samanburð blóðgasamælinga eftir fæðingu kom í ljós að þau börn sem fengu HIE voru marktækt súrari, með meiri basaskort og lægra bíkarbónat en þau sem ekki fengu merki um HIE (tafla III). Þá reyndist gildi blóðrauða marktækt lægri hjá börnunum sem fengu HIE heldur en hjá hinum sem ekki fengu HIE, (tafla IV). Ekki var tölfræðilega marktækur munur á fjölda kjarnaðra rauðra blóðkorna (normoblasta) í blóði barnanna í hópunum tveimur.



Umræður
Dánartíðni eftir fósturköfnun og nýgengi HIE í þessari rannsókn var lægri en í sambærilegum erlendum rannsóknum (4, 10, 14). Ef til vill er verið að ofgreina fósturköfnun hérlendis og benda niðurstöður rannsóknarinnar til að hverfa ætti frá þeirri greiningu nema að barnið fái HIE. Áður var talið að orsaka heilalömunar (cerebral palsy) væri oftast að leita í fæðingu og að heilalömun kæmi í kjölfar súrefnisþurrðar. Nú benda flestar rannsóknir til þess að aðeins megi rekja lítinn hluta af alvarlegri tilfellum heilalömunar til súrefnisþurrðar í fæðingu (15-17). Í flestum tilvikum þar sem börn eru með alvarlegan heilaskaða er ástæðan óþekkt og tímasetning heilaskaðans einnig óþekkt. Í rannsókninni kom fram að afdrif barna sem fá alvarlegasta form HIE í kjölfar fósturköfnunar eru slæm. Há dánartíðni var í þeim hópi og eina barnið sem lifði af er varanlega þroskaskert og hreyfihamlað.
Marktækur munur á Apgar stigun barna sem fengu HIE og hinna sem ekki fengu HIE styður forspárgildi Apgar stigunar. Miðgildi Apgar stiga við eina, fimm og tíu mínútur reyndist einnig lægra hjá HIE hópnum samanborið við hinn. Það styrkir enn frekar gildi Apgar stigunar við mat á alvarleika fósturköfnunar við burðarmál. Munurinn var mestur við tíu mínútna aldur sem er í samræmi við það sem áður var bent á að forspárgildi Agpar stigunar sé best eftir að barnið hefur náð fimm mínútna aldri (18).
Okkar niðurstöður sýna að lágt sýrustig í blóði barns eftir fæðingu er marktækur forspárþáttur fyrir HIE í kjölfar fósturköfnunar. Sömuleiðis gefa niðurstöðurnar til kynna áreiðanleika sýrustigsmælinga og basaskortsmælinga til að staðfesta greiningu marktækrar fósturköfnunar. Börn sem fengu HIE í kjölfar fósturköfnunar reyndust að meðaltali með sýrustig 6,95 við fæðingu, basaskort rúmlega 20 mmól/L og bíkarbónat í kringum 13 mmól/L. Þetta gefur sterklega til kynna að þegar ofangreindar breytingar á efnaskiptum eru til staðar má rekja truflanir á starfsemi heila (HIE) til afleiðinga súrefnisþurrðar í heila.
Nokkuð kom á óvart að gildi blóðrauða við fæðingu reyndist marktækt lægri í blóði barna sem fengu HIE í kjölfar fósturköfnunar heldur en hinna sem ekki fengu HIE. Þessu sambandi hefur ekki verið lýst áður. Hins vegar hefur verið lýst sambandi milli hárra gilda blóðrauða og hærri Apgar stigunar hjá börnum sem eru fædd lítil miðað við meðgöngulengd (19). Það samband er talið skýrast af örvun á nýmyndun rauðra blókorna vegna hlutfallslegs súrefnisskorts. Rökrétt er að áætla að hærra gildi blóðrauða í blóði barna sem verða fyrir súrefnisþurrð í fæðingu geti verndað þau fyrir afleiðingum súrefnisþurrðar og minnkað þannig líkur á HIE. Þetta samband þarfnast frekari athugunar í framtíðinni.
Rannsóknir sýna öfugt samband milli annars vegar Apgar stiga og sýrustigs í blóði og hins vegar fjölda kjarnaðra rauðra blóðkorna (20). Í þessari rannsókn var fjöldi kjarnaðra rauðra blóðkorna mikill hjá báðum hópum. Fjöldinn var um fjórðung meiri í börnum sem ekki fengu HIE heldur en hinum, þó svo sá munur hafi ekki náð tölfræðilegri marktækni. Leiða má líkur að því að börn sem hafa fleiri kjörnuð rauð blóðkorn séu betur í stakk búin að þola álag erfiðrar fæðingar þar sem fleiri kjörnuð rauð blóðkorn mynda hærra gildi blóðrauða.
Af ofangreindu er ljóst að meingerð HIE er flókin og greining fósturköfnunar erfið. Greiningartæknin sem notuð er í fæðingum er hvorki sérlega næm eða sértæk til greiningar á yfirvofandi fósturköfnun. Seint verður þó lögð of mikil áhersla á mikilvægi þess að bera kennsl á fósturstreitu tímanlega til að koma megi í veg fyrir þjáningar barna og foreldranna sem í hlut eiga. Þörf er á nýrri tækni sem er sértækari og næmari á yfirvofandi alvarlega fósturköfnun og eins er frekari rannsókna þörf á þeim þáttum fóstursins sem gera það veikara fyrir. Niðurstöður rannsóknarinnar benda til þess að greiningarskilmerki á alvarlegri fósturköfnun megi byggja á Apgar stigun og klínískum einkennum nýburans í samhengi við blóðgasagildi.
Þakkir
Anna Björg Jónsdóttir ritari á Kvennasviði og starfsfólk skjalasafna Landspítala.
Heimildir
1. Ross MG. EM, Novak D. Placental and Fetal Physiology. In: Gabbe SG. NJ, Simpson JL., ed. Obstetrics Normal and Problem Pregnancies: Churchill Livingstone, 2002: 37-62.
2. Thornberg E, Thiringer K, Odeback A, Milsom I. Birth asphyxia: incidence, clinical course and outcome in a Swedish population. Acta Paediatr 1995; 84: 927-32.
3. Vannucci RC, Perlman JM. Interventions for perinatal hypoxic-ischemic encephalopathy. Pediatrics 1997; 100: 1004-14.
4. Wu YW, Backstrand KH, Zhao S, Fullerton HJ, Johnston SC. Declining diagnosis of birth asphyxia in California: 1991-2000. Pediatrics 2004; 114: 1584-90.
5. Sutton L, Sayer GP, Bajuk B, Richardson V, Berry G, Henderson-Smart DJ. Do very sick neonates born at term have antenatal risks? 1. Infants ventilated primarily for problems of adaptation to extra-uterine life. Acta Obstet Gynecol Scand 2001; 80: 905-16.
6. Sykes GS, Molloy PM, Johnson P, Gu W, Ashworth F, Stirrat GM, et al. Do Apgar scores indicate asphyxia? Lancet 1982; 1: 494-6.
7. Boylan PC, Parisi, V. Fetal acid base balance. In: Creasy RK, Resnik, R., ed. Maternal-fetal medicine. Third ed: W. B Saunders company, 1994: 349-58.
8. Sarnat HB, Sarnat MS. Neonatal encephalopathy following fetal distress. A clinical and electroencephalographic study. Arch Neurol 1976; 33: 696-705.
9. Hull J, Dodd KL. Falling incidence of hypoxic-ischaemic encephalopathy in term infants. Br J Obstet Gynaecol 1992; 99: 386-91.
10. Badawi N, Kurinczuk JJ, Keogh JM, Alessandri LM, O?Sullivan F, Burton PR, et al. Intrapartum risk factors for newborn encephalopathy: the Western Australian case-control study. BMJ 1998; 317: 1554-8.
11. Levene MI, Sands C, Grindulis H, Moore JR. Comparison of two methods of predicting outcome in perinatal asphyxia. Lancet 1986; 1: 67-9.
12. Robertson C, Finer N. Term infants with hypoxic-ischemic encephalopathy: outcome at 3.5 years. Dev Med Child Neurol 1985; 27: 473-84.
13. Pálsdóttir K, Dagbjartsson A, Þórkelsson Þ, Harðardóttir H. Fósturköfnun og heilakvilli af völdum súrefnisþurrðar - tíðni og áhættuþættir á meðgöngu og í fæðingu. Læknablaðið 2007; 93: 595-601.
14. Milsom I, Ladfors L, Thiringer K, Niklasson A, Odeback A, Thornberg E. Influence of maternal, obstetric and fetal risk factors on the prevalence of birth asphyxia at term in a Swedish urban population. Acta Obstet Gynecol Scand 2002; 81: 909-17.
15. Nelson KB, Leviton A. How much of neonatal encephalopathy is due to birth asphyxia? Am J Dis Child 1991; 145: 1325-31.
16. Nelson KB, Ellenberg JH. Antecedents of cerebral palsy. Multivariate analysis of risk. N Engl J Med 1986; 315: 81-6.
17. Blair E, Stanley FJ. Intrapartum asphyxia: a rare cause of cerebral palsy. J Pediatr 1988; 112: 515-9.
18. Casey BM. MD, Leveno KJ. The continuing value of the Apgar score for the assessment of newborn infants. N Engl J Med 2001; 344: 467-71.
19. De Grauw TJ, Budde H, Samsom JF, Hopkins MB. Hematocrit in relation to Apgar scores in SGA infants. J Perinat Med 1991; 19: 305-11.
20. Hanlon-Lundberg KM, Kirby RS. Nucleated red blood cells as a marker of acidemia in term neonates. Am J Obstet Gynecol 1999; 181: 196-201.
