07/08. tbl 93. árg. 2007
Fræðigrein
Beina- og kalkbúskapur sjúklinga með herslismein
Bone mineral density and bone turnover in Systemic Sclerosis
Úrdráttur
Bakgrunnur: Herslismein (Systemic Sclerosis) er sjaldgæfur fjölkerfasjúkdómur. Fjölmargir þættir í sjúkdómsbirtingu og meðferð sjúkdómsins geta valdið ótímabærri beinþynningu. Markmið þessarar rannsóknar var að kanna beinhag sjúklinga með herslismein á Íslandi og meta hvort sérstakra ráðstafana sé þörf hvað varðar beinvernd.
Efniviður og aðferðir: Allir einstaklingar sem greindir hafa verið með herslismein á Íslandi voru boðaðir til þátttöku, sem fólst í stöðluðu viðtali og líkamsskoðun með tilliti til beinþynningar og sjúkdómsvirkni, ítarlegri blóð- og þvagrannsókn. Beinþéttnimæling var framkvæmd af mjóhrygg og mjöðm (QDR 4500 Elite).
Niðurstöður: Þekktir voru 29 einstaklingar með herslismein þegar rannsóknin fór fram, en 24 sjúklingar mættu til þátttöku (83%); 20 konur og fjórir karlar. Meðalaldur þátttakenda var 60 ± 15 ár. 17 konur voru komnar í tíðahvörf. Tólf sjúklingar höfðu beinbrotnað, samtals 18 sinnum. Fjórir einstaklingar voru á bisfósfónatmeðferð. Kalsíumútskilnaður reyndist undir viðmiðunarmörkum, en beinvísar voru eðlilegir. DEXA mælingar sýndu að átta sjúklingar höfðu beinrýrnun (T-gildi -1,0 - -2,5), en þrír höfðu beinþynningu (T-gildi < -2.5). Samanborið við einstaklinga á sama aldri voru sex einstaklingar með beinþéttni einu staðalfráviki neðan aldursviðmiða.
Ályktun: Meirihluti íslenskra sjúklinga með herslismein hafa eðlilega beinumsetningu og beinþéttni, þó hafa einstaka sjúklingar truflun á kalk- og beinumsetningu sem endurspeglast í marktækum kalksparnaði í þvagútskilnaði, sem ef til vill endurspeglar skerta frásogsgetu í görn. Rannsóknin gefur ekki tækifæri til að meta áhrif meðferðar á beinþéttni þessa sjúklingahóps. Rannsóknin sýnir að nauðsynlegt er að kanna beinþéttni sjúklinga með herslismein og í völdum tilfellum íhuga sérhæfða beinverndandi meðferð.
Inngangur
Herslismein (systemic sclerosis eða scleroderma) er sjaldgæfur fjölkerfasjúkdómur af ónæmisfræðilegum toga með algengi um sjö tilfelli á hverja 100.000 íbúa hérlendis (1). Sjúkdómurinn einkennist af smáæðaþrengingu vegna þykknunar í æðaþelslagi (intima) smárra og meðalstórra slagæða, sem leiðir af sér blóðrásartruflanir og bandvefsaukningu í húð og innri líffærum og vísar nafn sjúkdómsins, það er herslismein, til þessarar bandvefsaukningar í húð (2). Óþekkt er hvað leysir sjúkdóminn úr læðingi.
Útbreiðsla herslismeins í húð er mismikil, en er mest áberandi á höndum og í andliti (1,2). Bandvefsaukningar verður einnig vart í innri líffærum, svo sem í meltingarfærum, stoðkerfi, lungum, nýrum og hjarta. Því er birtingarmynd sjúkdómsins breytileg frá einum sjúklingi til annars (3). Margt í meingerð herslismeins, sem og í meðferð, til dæmis sykursterar og ónæmisbælandi meðferð, getur haft áhrif á kalk- og beinabúskap sjúklinga með herslismein. Fyrri rannsóknir á þessu sviði hafa sýnt misvísandi niðurstöður (4-10).
Beinþynning einkennist af minnkun á beinþéttni, það er steinefnamagni í beinvef, og breytingu á innri uppbyggingu beinvefsins, sem leiðir til aukinnar áhættu á beinbrotum. Beinþéttni er mæld sem steinefnainnihald í beinum á flatarmálseiningu (Bone Mineral Density (BMD)), en niðurstöðurnar eru gefnar upp annarsvegar í T-gildum, sem er fjöldi staðalfrávika frá hámarksbeinþéttni ungra einstaklinga af sama kyni, og í Z-gildi hinsvegar, sem er frávikið í fjölda staðalfrávika frá aldurs- og kynbundinni meðaltalsbeinþéttni. Samkvæmt Alþjóðaheilbrigðisstofnuninni (WHO) er um beingisnun (osteopenia) að ræða þegar T-gildið er -1,0 til -2,5, en beinþynning (osteoporosis) þegar beinþéttnigildið (T-gildi) er lægra en -2,5(10). Vel þekkt er að langvinnir bólgusjúkdómar, til dæmis rauðir úlfar (SLE) og iktsýki (RA), valda svokallaðri fylgibeinþynningu (secondary osteoporosis). Hinsvegar er óljóst hver áhrif herslismeins eru á beinbúskapinn.
Stirðleiki og hreyfihömlun meðal sjúklinga með herslismein er algeng, meðal annars vegna bandvefsauka í húð ásamt lið- og vöðvaverkjum, sem hvoru tveggja hefur áhrif á vöðva og bein. Enn fremur getur fjölvöðvabólga (polymyositis) verið fylgikvilli við herslismein, sem ásamt bólguvirkni í innri líffærum kallar á sykurstera og/eða aðra ónæmisbælandi meðferð, sem hvort tveggja er vel þekktur orsakavaldur beinþynningar (12-13). Þá sýna röngtenrannsóknir oft á tíðum breytingar í stoðkerfi sjúklinga með herslismein, ekki eingöngu mjúkvefjakalkanir, heldur einnig beineyðingu í fjærkjúkum fingra og beinþynningu aðlægt liðum (periarticular osteoporosis) (14), en allt þetta beinir athyglinni að því að sjúklingar með herslismein geta verið í aukinni áhættu á ótímabærri beinþynningu.
Auk ofannefndra stoðkerfisvandamála, geta ýmsir aðrir þættir haft áhrif á beinumsetningu þessa sjúklingahóps. Fyrst er að nefna að herslis-mein er bólgusjúkdómur og geta frumuboðefni, t.d. TNF-alfa og IL-6 haft neikvæð áhrif á beinumsetningu (15). Meltingarfæratruflanir geta verið hluti af birtingarmynd sjúkdómsins og getur leitt til frásogstruflana og þannig haft neikvæð áhrif á kalk- og D-vítamínfrásog frá görn (16). Einnig hafa rannsóknir sýnt fram á að konur með herslismein fá oft snemmkomin tíðahvörf sem einnig hefur neikvæð áhrif á beinhag (7,9). Truflun á blóðrásarstjórnun er talin geta verið orsök örmyndunar í innri líffærum herslimeinssjúklinga, en óvíst er hvort þetta geti haft neikvæð áhrif á bein. Þá eru sjúklingar með fjölkerfasjúkdóma oft meðhöndlaðir með lyfjum sem hafa neikvæð áhrif á beinaumsetningu eins og fyrr greinir frá.
Dual X-ray absorptiometry (DEXA) mæling er „gullstandard“ í beinþéttnimælingum í dag, en þrjár af sjö fyrri rannsóknum á beinþéttni sjúklinga með herslimein notuðu eldri mælingaaðferðir (5-7). Ein þeirra studdist við Single Photon Absorptiometry (SPA) og tvær Dual Photon Absorptiometry (DPA). Tvær þessara rannsókna (5-6) sýndu fram á lægri beinþéttni sjúklinga með herslismein, en sú þriðja sýndi ekki marktækan mun á beinþéttni sjúklinga með herslismein og viðmiða. Hinsvegar framkvæmdu Di Munno og félagar DPA mælingu á framhandlegg og höfðu til samanburðar DEXA mælingu hjá 43 konum með herslismein, jafnframt sem þeir könnuðu kalsíumbúskap þeirra (8). Niðurstöður þeirra sýndu að sjúklingar með herslismein höfðu marktækt lægri beinþéttni og tengdist beinþéttnin alvarleika herslismeinsins. Mjúkpartakölkun hafði hinsvegar ekki áhrif á beinþéttni og reyndist kalkbúskapur vera eðlilegur. Önnur rannsókn sem einnig notaðist við DEXA aðferð hjá 47 konum með herslismein (9), sýndi að sjúklingarnir höfðu lægri beinþéttni samanborið við heilbrigð viðmið. Beinþéttnigildin virtust einnig tengjast alvarleika sjúkdómsins. Rannsókn Carbone og félaga á 15 konum (10), styður einnig tengsl á milli herslismeins og beinþynningar. Rannsókn Neuman og félaga (4) sýndi hinsvegar aðrar niðurstöður en fyrrnefndar tvær rannsóknir. Þeir rannsökuðu 30 konur og reyndist eingöngu ein þeirra hafa beinþynningu, en 11 beingisnun og þeir fundu ekki tengsl á milli alvarleika sjúkdómsins og beinþéttni.
Í samantekt sýna tvær eða jafnvel þrjár rannsóknir að konur með herslismein geta haft lægri beinþéttni en heilbrigðar jafnöldrur. Hinsvegar er þýði allra rannsóknanna sérvalið og býður því upp á bjögun. Engin rannsóknanna kannaði beinumsetningu með beinvísum. Því er áhugavert að kanna kalk- og beinabúskap íslenska sjúklingaþýðisins með herslismein.
Efni og aðferðir
Sjúklingar með herslismein voru fundnir í skrám gigtardeildar Landspítala háskólasjúkrahúss (LSH) og einnig var leitað kerfisbundið í sjúkdómaskrám LSH samkvæmt IDC kóðum. Kynningarbréf var sent til allra sjúklinga sem fundust í fyrrnefndum gagnagrunnum og voru lifandi 31/12 2003. Í kjölfarið var haft símasamband við allan hópinn og þeir sem samþykktu þátttöku voru boðaðir til viðtals og beinþéttnimælingar (sjá nánar að neðan).
Viðtal og skoðun
Við komu á beinþéttnimóttöku LSH var framkvæmt staðlað viðtal sem tók til áhættuþátta fyrir beinþynningu, ættarsögu og einnig var spurt um neysluvenjur með tilliti til kalks og D-vítamín inntöku. Einnig var spurt um líkamshreyfingu og íþróttaiðkun þátttakenda. Þá var framkvæmd líkamsskoðun með tilliti til útbreiðslu herslisbreytinga í húð, þar sem yfirborði húðarinnar var skipt í 24 svæði og gefin stig frá núll upp í þrjá, allt eftir alvarleika herslimeinsbreytinganna. Möguleg húðstigaeinkunn var því frá 0 upp í 72 stig. Í kjölfarið voru þátttakendur flokkaðir í tvo hópa eftir alþjóðlegri flokkun eftir því hvort þeir væru með takmarkað eða dreift herslismein í húð (17).
Meðferð lífsýna og mæling lífefna
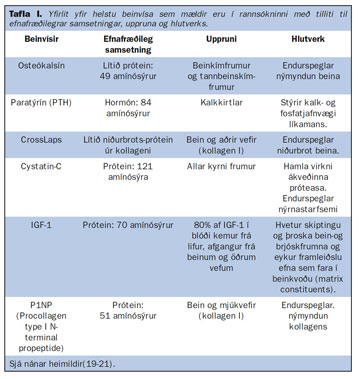
Öll lífsýnataka og meðferð sýna fylgdi stöðluðum verkferlum. Morgunþvagsýni og fastandi blóðsýni voru tekin fyrir kl 10:00 að morgni vegna dægursveiflu margra lífefna sem mæld voru. Blóðhagur var mældur með Cell Dyn 3200, en blóðsölt, kreatínín, heildarmagn alkalísks fosfatasa, albúmín og kolsýra í blóði var mælt jafnóðum með Vitros 950 tæki (Vitros) og hvarfefnum frá Ortho Clinical Diagnostics (Rochester, Bandaríkjunum). Einnig var mælt jóniserað kalsíum með jónasértækum rafskautum (ion-selective electrodes) með Radiometer 720 tæki (Kaupmannahöfn, Danmörku). Þá var mælt osteókalsín, paratýrín, CrossLaps, PINP, týrótrópín (TSH), östradíól, testósterón, frítt T4 og frítt T3 í blóði með hjálp mótefna og rafefnaljómunar (electrochemiluminscence immunoassay) með Elecsys tæki frá Roche Diagnostics GmbH (Mannheim, Þýskalandi). Styrkur 25-OH vítamíns D var mældur með hjálp mótefna og geislavirks joðs (DiaSorin,Stillwater, Bandaríkjunum). Insulin-like Growth Factor-1 (IGF-1) var mældur með mótefnum og geislavirku joði (radioimmunoassay) og komu hvarfefnin frá Diagnostic System Laboratories (Webster, Bandaríkjunum). Cystatin-C var mælt með gruggmælingu og hjálp mótefna frá DAKO (Glostup, Danmörku) á Vitros 30 tæki. Tafla I gefur yfirlit um uppruna og hlutverk helstu beinvísa sem mældir eru í þessari rannsókn.
Sjúklingarnir voru beðnir að kasta af sér þvagi heima snemma morguns, þ.e. áður en þeir komu til rannsóknar og skrá tímann hjá sér. Þegar þeir komu til rannsóknar var tekið þvagsýni. Magn og tíminn frá því þeir höfðu þvaglát um morguninn var skráð og 10 ml sendir til rannsóknarstofu. Í þessu sýni var mældur styrkur kalíum, kalsíum og kreatíníns. Reiknaður var útskilnaður þessara efna á sólarhring sem og kreatínín úthreinsun (creatinine clearance), ásamt hlutfalls kalsíums og kreatíníns í þvagi.
Beinþéttnimælingar
Beinþéttni þátttakenda var mæld með QDR 4500 Elite beinþéttnimæli. Tækið mælir magn steinefna í beinum (bone mineral content (BMC)) og gefur það upp sem steinefnainnihald á flatarmálseiningu (bone mineral density (BMD)). Sú niðurstaða er síðan umreiknuð í T-gildi (18) og eru þær tölur notaðar til kynningar á niðurstöðum. Mæld var beinþéttni í lendarliðum (L1-L4), lærleggsháls, mjöðm ásamt líkamanum í heild.
Tveir þátttakendur áttu ekki möguleika að koma til Reykjavíkur til beinþéttnimælingar. Þeir voru mældir með Hologic 2000 DEXA-mæli sem staðsettur er á Fjórðungssjúkrahúsinu Akureyri. Þátttaka þessara tveggja sjúklinga var að öðru leyti ekki frábrugðin.

Gagnasöfnun, tölfræði og leyfisveitingar
Öllum gögnum var safnað í gagnagrunn í Excel-skjal. Lýsandi tölfræði var notuð til að lýsa rannsóknarniðurstöðum. Leyfi frá siðanefnd LSH (20/2004) og Persónuvernd (S1859/2004 og 2004020124) var fengið fyrir rannsókninni. Þá var fengið leyfi Geislavarna ríkisins vegna beinþéttni-mælinganna (8/30/2004). Allir þátttakendur skrifuðu undir upplýst samþykki.

Niðurstöður
Tuttugu og níu einstaklingar voru greindir með herslismein hér á landi við upphaf rannsóknar. Tveir einstaklingar afþökkuðu þátttöku í rannsókninni, tveir einstaklingar bjuggu erlendis og fimmta sjúklinginn tókst ekki að hafa samband við, því tóku 24 einstaklingar með herslismein þátt í rannsókninni eða 83% af heildarsjúklingaþýðinu hér á landi. Konur voru 74% þátttakenda og meðalaldur hópsins var 60 ± 15 ár. Að meðaltali höfðu þátttakendur verið veikir í 15 ± 10 ár (1-33). Sjá nánar upplýsingar um þátttakendur í töflu II.
Þrír þátttakendur höfðu að sögn ættarsögu um beinþynningu (13%), átta voru með hreyfihömlun (35%) og fimm voru með sjúkdóm í meltingarfærum (22%). Fimm af sextán konum sem komnar voru í tíðahvörf (31%) höfðu snemmkomin tíðahvörf (tíðahvörf fyrir 42 ára aldur). Fjórtán af 24 sjúklingum voru á sykursterameðferð (61%) og fimm voru á methotrexati (22%).
Tólf einstaklingar höfðu brotnað samtals 18 sinnum. Einn hafði brotnað fjórum sinnum (á báðum framhandleggjum, öxl og upphandlegg), einn hafði brotnað þrisvar sinnum (rifbein og viðbein) og einn hafði brotnað tvívegis (framhandlegg og hrygg). Samtals voru átta framhandleggsbrot (33%), tvö brot í upphandlegg (8%) og tvö rifbeinsbrot (8%), þar að auki voru eitt eftirtalinna brotafótbrot, samfallsbrot í hrygg, handleggsbrot, brot um olnboga og viðbeinsbrot. Fjórar konur voru á beinverndandi meðferð með bisfósfónati (17%).
Neysluvenjur og hreyfing
Neysla mjólkurvara var ígildi tveggja mjólkurglasa og fjögurra ostsneiða á dag að meðaltali. Átta einstaklingar tóku auk þess kalktöflur reglulega og 20 tóku daglega lýsi eða fjölvítamín. Fimmtán einstaklingar stunduðu reglulega líkamsæfingar eða aðrar íþróttir að meðaltali fimm sinnum í viku.
Blóð- og þvagrannsóknir
Blóðrauði (Hb = 139 g/L), fjöldi hvítra blóðkorna (6,3 x 109/L) og blóðflögur (258 x 109/L) voru innan eðlilegra marka.
Meðaltalsstyrkur þvag- og blóðgilda hvað varðar kalsíumbúskap var innan eðlilegra marka að frátöldu kalsíum í þvagi sem var að meðaltali 2,4 mmól/24 klst og helmingur sjúklinga (56%) reyndust með umreiknað sólarhringsgildi undir viðmiðunarmörkum (2,5 - 7,5 mmól/24 klst). Þegar kalsíumútskilnaður var metinn miðað við kreatínínúthreinsun (þ-kalsíum/þ-kreatínín), reyndist eingöngu einn sjúklingur hafa hækkað kalsíum/kreatínín hlutfall í þvagi (< 0,59 mmol/mmol) og hafði sá einnig beinþynningu samkvæmt DEXA-mælingu. Þessi einstaklingur hafði einnig hækkað s-jónaserað kalsíum 1,44 (viðmiðunargildi: 1,13 - 1,33 mmol/L), en önnur gildi voru innan eðlilegra marka. Nánari upplýsingar er að finna í töflu III.
Beinumsetningarvísar
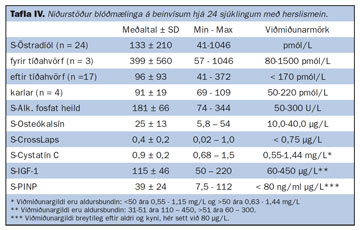
Öll meðalgildi beinumsetningarvísa voru innan viðmiðunargilda (tafla IV). Tveir sjúklingar höfðu þó lækkuð osteókalsínigildi og hafði hvorugur þeirra beinrýrnun eða beinþynningu við beinþéttnimælingu. Þrír sjúklingar höfðu hækkað osteókalsíngildi og tveir af þeim voru með beinrýrnun í lærleggshálsi. Tveir þátttakendur höfðu hækkað Crosslaps og reyndust báðir hafa beinrýrnun. Einn sjúklingur reyndist hafa hækkað Cystatin-C, sá hafði einnig væga nýrnabilun (S-kreatínín 156 µmól/L).
Tveir sjúklingar höfðu hækkað PTH, annar þeirra hafði kalsíum í blóði við lægri viðmiðunarmörkin eða 2,17 mmol/L (viðmiðunarmörk: 2,15-2,60) og hafði sá framhandleggsbrotnað. Hinn sjúklingurinn hafði lækkað D-vítamín gildi í blóði (30,4 nmol/L) og var hann einnig á prednisólonmeðferð og með lág beinrýrnunargildi í hrygg (T-gildi = ?2,2) og hafði hann ökklabrotnað. Jóniserað kalsíum var hinsvegar eðlilegt hjá þeim báðum. Sjö einstaklingar höfðu D-vítamíngildi undir 45 nmól/L. Enginn hafði þó beinþynningargildi samkvæmt DEXA-mælingu. Einn einstaklingur hafði hækkað D-vítamín í blóði og hafði hann einnig lágan kalkútskilnað í þvagi.
Ekki reyndist marktækur munur á meðaltalsgildum beinumsetningavísa með tilliti til þess hvort sjúklingarnir voru meðhöndlaðir með bisfósfónötum eða ekki. Hinsvegar reyndust sjúklingar á sykursterameðferð hafa marktækt lægristyrk á s-Alk. fosfatasa í heild (167 vs 199 U/L; p =0,03), s-osteókalsín (16,0 vs 27,9 ng/ml; p = 0,03) og s-CrossLaps (0,3 vs 0,5 µg/L; p = 0,03), miðað við þá sjúklinga sem ekki voru sykursterameðferð. Þeir höfðu einni lægri styrk á s-P1NP, en það náði ekki marktækum mun (25,0 vs 45,5; p = 0,058).
Beinþéttnimælingar
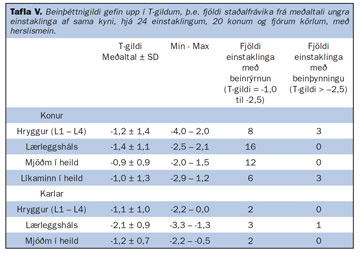
Í töflu V er meðaltal T-gilda gefið upp fyrir allan hópinn, en þar kemur fram að hvorki meðaltöl kvenna né karla náðu beinþynningargildum (T-gildi < -2,5) í hrygg eða mjöðm. Hinsvegar reyndist hópurinn uppfylla skilyrði á öllum mælingarstöðum fyrir beinrýrnun, þ.e. T-gildi á bilinu -1,0 til -2,5.
Þrjár konur höfðu beinþynningargildi (T < -2,5) í hrygg (15%) og fimm konur til viðbótar voru með beinrýrnun í hrygg (25%) ásamt tveim körlum (50%) (T-gildi -1,0 - -2,5). Einn karl hafði beinþynningu í lærleggshálsi (25%) og tveir höfðu beinrýrnun í lærlegg (50%). Hinsvegar hafði engin kona beinþynningargildi í lærlegghálsi né í mjöðm, þó höfðu 16 konur mælingargildi beinrýrnunar í lærleggshálsi (80%).
Þegar beinþéttnigildi sjúklinganna voru borin saman við kyn- og aldurstöðluð viðmið voru fjórar konur (20%) og tveir karlar (50%) með lækkuð beinþéttnigildi í hrygg og þrjár konur (15%) ásamt tveim körlum (50%) með lækkuð gildi í lærleggshálsi þegar miðað var við frávik sem var meira en einu staðalfráviki neðan aldursmeðaltalsins.
Tengslagreining
Marktæka fylgni milli beinþéttni og áhættuþátta eða sjúkdómsbirtingar herslismeinsins var ekki unnt að staðfesta. Hinsvegar reyndust sjúklingar með sögu um barksterameðferð hafa fimm prósent lægri beinþéttni, en þeir sem ekki höfðu fengið barkstera ef miðað var við aldurstöðluð viðmið (p < 0,55) og þeir sjúklingar sem höfðu sjúkdómseinkenni frá meltingarfærum höfðu tvö prósent lægri beinþéttni miðað við þá sem ekki höfðu meltingafæraeinkenni (p < 0,77). Þá höfðu konur með sögu um snemmkomin tíðahvörf (fyrir 42 ára aldur) 12% lægri beinþéttni miðað við hinar konurnar (p < 0,23). Á hinn bóginn voru sjúklingar sem stunduðu leikfimi eða fóru reglulega í sjúkraþjálfun með 10% hærri beinþéttni, en þeir sem gerðu hvorugt (p < 0,18). Ekki mældist lægri beinþéttni hjá einstaklingum sem höfðu sögu um beinbrot, þeim sem voru á ónæmisbælandi lyfjameðferð, né þeim sem höfðu mikla bólguvirkni í upphafi veikinda sinna. Ekki var hærri beinþéttni meðal þeirra sem neyttu ígildi tveggja mjólkurglasa á dag miðað við þá sem neyttu minna af mjólkurafurðum.
Umræða
Rannsókn okkar bendir til þess að íslenskir sjúklingar með herslismein séu í aukinni hættu á beinrýrnun eða beinþynningu miðað við jafnaldra þeirra. Engin ein orsök virðist vera undirliggjandi í þáttagreiningu, en væg tengsl fundust þó við barksteranotkun, meltingarfærafylgikvilla við herslismeinið og snemmkomin tíðahvörf hjá konum með herslismein. Ennfremur virtist helmingur sjúklinga hafa truflun í kalkbúskap, sem birtist meðal annars í lækkuðum kalkútskilnaði í þvagi, sem gæti verið varnarviðbragð líkamans.
Rannsóknarþýðið er allur íslenski sjúklingahópurinn sem nær til rúmlega 80% þeirra sem eru með herslismein hér á landi. Hlutfall kvenna í rannsókninni er hærra en í öðrum sambærilegum rannsóknum (22), eða 83% miðað við 75%, og einnig er meðalaldur íslenska hópsins um sex árum hærri en í fyrrnefndum rannsóknum. Sjúklingar voru ekki útilokaðir frá þátttöku sem áður höfðu þurft barkstera gegn sjúkdómi sínum, né einstaklingar sem höfðu byrjað sérhæfða beinverndandi lyfjameðferð eins og gert hefur verið í flestum öðrum rannsóknum (6,9-11). Þá höfðu fleiri sjúklingar í okkar þýði dreift herslismein (diffuse systemic sclerosis), miðað við þá sem höfðu takmarkaða birtingu sjúkdómsins (limited systemic sclerosis). Konur í okkar rannsókn höfðu tíðahvörf við 45 ára aldur að meðaltali, sem er mun fyrr en meðaltal íslenska kvenna, sem er við 49 ára aldur (23). Þetta samrýmist þó vel öðrum rannsóknum um herslismein (7,9). Þó að rannsóknarhópur okkar sé lítill, samrýmist hann fjölda í þeim rannsóknum sem hafa notast við DEXA-mælingar hjá þessum sjúklingahópi. Rannsókn okkar er þó víðtækari vegna ítarlega blóðrannsókna með tilliti til beinumsetningar. Því eru ályktunarmöguleikar okkar ekki síðri en fyrri rannsókna.
Helmingur sjúklinganna með herslismein reyndist hafa lágan kalkútskilnað í þvagi. Þetta endurspeglast þó ekki í meðaltalsgildum kalks í blóði, né hækkuðu PTH og önnur mæligildi voru innan viðmiðunarmarka hvað kalkbúskap varðar. Ennfremur var styrkur D-vítamíns innan viðmiðunarmarka í hópnum. Hafa ber í huga að stuðst var við svokallaða takmarkaða þvagsöfnun, þar sem tekin var þvagprufa eftir morgunþvag og sólarhringsútskilnaður umreiknaður. Ef lækkaður kalkútskilnaður hjá sjúklingahópnum endurspeglar skekkjumörk í aðferðafræðinni, það er að tíma- eða magnskekkja sé fyrir hendi, ætti það einnig að hafa áhrif á kalíum- og kreatíníngildin, en svo er ekki. Þegar kalsíumútskilnaðurinn var metinn með hlutfallsstyrk kalsíums og kreatíníns í þvagi sýndu niðurstöður einnig marktækt minnkaðan kalsíumútskilnað. Þetta rennir því stoðum undir að þessar niðurstöður endurspegli raunverulegan kalksparnað og er það í samræmi við fyrri rannsóknir (5). Megin orsök þessa gæti verið sú að herslismeinið trufli frásogshæfni þarma á kalki (16).
Styrkur hinna ýmsu beinumsetningavísa gaf ekki til kynna að sjúklingahópurinn væri með aukna beinumsetningu með auknu beinniðurbroti eða beinuppbyggingu. Hinsvegar höfðu nokkrir einstaklingar styrk einstakra beinumsetningarvísa utan viðmiðunargilda. Þetta endurspeglaðist í flestum tilfellum ekki í beinþéttnigildum. Því má álykta að mæling beinumsetningavísa hjá sjúklingum með herslismein nýtist ekki í daglegri klínískri ákvarðanatöku hvað varðar beinþynningu hjá sjúklingum með herslismein. Nýta mætti þó suma þessara beinvísa sem mælikvarða á meðferðarsvari við notkun bisfósfónata í völdum tilfellum, en við fundum þó ekki mun á styrk þessara efnavísa með tilliti til meðferðar. Niðurstöðurnar sýndu að einn sjúklingur var með óeðlilega lágt D-vítamín í blóði, minnkaðan útskilnað af kalsíum í þvagi og einnig lág beinþéttnigildi (tveimur staðalfrávikum neðan aldursviðmiða). Hann var reyndar meðhöndlaður með barksterum. Hvort þessi einstaklingur hafi steraorsakaða beinþynningu eða beinmeiru (oteomalasia) er útilokað að staðfesta út frá þessum niðurstöðum. Til þess þyrfti vefjasýni úr beini svo unnt væri að skera út um þessar tvær mismunagreiningar.
Beinþéttnimælingar sýndu að hópurinn var með byrjandi beinþynningu, eða svokallaða beinrýrnun, fjórðungur kvennanna og tveir af fjórum körlum mældist þó með beinþéttni samsvarandi beinþynningu eða T-gildi lægri en -2,5. Miðað við jafnaldra var fimmtungur kvennanna og tveir karlar með marktækt lægri beinþéttni en jafnaldrar (meira en eitt staðalfrávik frá aldursviðmiðum). Álykta má því frá okkar rannsókn og fyrri sambærilegum rannsóknum að sjúklingar með herslismein hafi aukna tilhneigingu til beintaps og beinþynningar.
Athyglisvert er að þrátt fyrir að hópurinn í heild sé ekki með beinþynningu samkvæmt beinþéttni-mælingum, hafði meira en helmingur þátttakenda beinbrotnað og margir oftar en einu sinni. Þetta er líklega hærri brotatíðni en meðal jafnaldra Íslendinga, en staðlaðar brotatölur eru þó ekki fyrirliggjandi hér á landi. Orsök þessara beinbrota er því ekki unnt að skýra út frá beinþéttnigildum né auknu beinumbroti. Hinsvegar mætti leiða að því rök að sjúkdómurinn og barksterameðferðin hafi neikvæð áhrif á uppbyggingu beinsins, það er beingæðin, og sé meginástæða þessara beinbrota. Frekari rannsóknir á þessu sviði eru nauðsynlegar, en til þess að skoða innri uppbyggingu beinsins þarf annarsvegar að taka vefjasýni frá beini eða framkvæma háupplausnar tölvusneiðmyndatöku.
Rannsókn okkar er á tvennan hátt ólík fyrri rannsóknum. Í fyrsta lagi er allt íslenska sjúklingaþýðið boðað til þátttöku án sérhæfra útilokunarskilyrða. Í annan stað eru bæði karlar og konur í okkar rannsókn, en eingöngu konur í fyrri rannsóknum. Þetta er mikilvægt í ljósi þess að helmingur karlanna í rannsókninni hafði merki um beinþynningu. Þá framkvæmdum við ítarlegt viðtal með tilliti til áhættuþátta og mældum fjölmarga beinumsetningarvísa sem endurspeglar uppbyggingu og niðurbrot beina. Takmarkanir okkar rannsóknar er annarsvegar lítill sjúklingahópur og hópurinn er margbreytilegur með tilliti til meðferðar og sjúkdómseinkenna hinsvegar, því er erfitt að fá marktækar niðurstöður, en fyrri rannsóknir á þessu sviði eru sömuleiðis fámennar.
Meginniðurstöður eru að kanna verður beinþéttni allra sjúklinga með herslimein, óháð öðrum áhættuþáttum. Þar sem orsakir beinþynningar hjá þessum sjúklingahópi geta verið margslungnar verður að kanna með frekari rannsóknum undirliggjandi ástæður og leiðrétta ef kostur er. Þá er nauðsynlegt að tryggja fullnægjandi beinvernd þessara sjúklinga, hvort sem um er að ræða fyrsta eða annars stigs forvörn, sem og meðferð við einkennagefandi beinþynningu, það er þeirra sem eru með beinþynningu og sögu um beinbrot.
Heimildir
1. Geirsson ÁG, Steinsson K, Guðmundsson S, Sigurðsson V. Fjölkerfa-herslismein á Íslandi. Læknablaðið 1992; 78: 287-91.
2. Mitchell R, Kumar V. Diseases of immunity: Basic Pathology. 7 ed. Stanley Robbins, 2003, Philadelphia: Independence Square West, p.141-143.
3. Generini S, Fiori G, Moggi Pignone A, Matucci Cerinic M, Cagnoni M. Systemic sclerosis. A clinical overview. Adv Exp Med Biol 1999; 455: 73-83.
4. Neumann K, Wallace DJ, Metzger AL. Osteoporosis--less than expected in patients with scleroderma? J Rheumatol 2000; 27: 1822-3.
5. Serup J, Hagdrup H, Tvedegaard E. Bone mineral content in systemic sclerosis measured by photonabsorptiometry. Acta Derm Venereol 1983; 93: 235-7.
6. La Montagna G, Vatti M, Valentini G, Tirri G. Osteopenia in systemic sclerosis. Evidence of a participating role of earlier menopause. Clin Rheumatol 1991; 10: 18-22.
7. da Silva HC, Szejnfeld VL, Assis LS, Sato EI. Study of bone density in systemic scleroderma. Rev Assoc Med Bras 1997; 43: 40-6.
8. Di Munno O, Mazzantini M, Massei P et al. Reduced bone mass and normal calcium metabolism in systemic sclerosis with and without calcinosis. Clin Rheumatol 1995; 14: 407-12.
9. Frediani B, Baldi F, Falsetti P et al. Bone mineral density in patients with systemic sclerosis. Ann Rheum Dis 2004; 63: 326-7.
10. Carbone L, Tylavsky F, Wan J, McKown K, Cheng S. Bone mineral density in scleroderma. Rheumatology 1999; 38: 371-2.
11. Consensus Development Conference. Diagnosis, prophylaxis, and treatment of osteoporosis. Am J Med 1992; 6: 852-7.
12. Gudbjornsson B, Júlíusson UI, Gudjónsson FV. The prevalence of long term steroid therapy and the frequency of decision making to prevent steroid-induced osteoporosis in daily clinical praxis. Ann Rheum Dis 2002; 61: 32-6.
13. Mazanec DJ, Grisanti JM Drug-induced osteporosis. Cleve Clin J Med 1989; 56: 297-303.
14. La Montagna G, Sodano A, Capurro V, Malesci D, Valentini G. The arthropathy of systemic sclerosis: a 12 month prospective clinical and imaging study. Skeletal Radiol. 2005; 34: 35-41.
15. Roodman GD. Role of cytokines in the regulation of bone resorption. Calcif Tissue Int. 1993; 53 (Suppl 1): S94-8.
16. Lundberg AC, Akesson A, Akesson B. Dietary intake and nutritional status in patients with systemic sclerosis. Ann Rheum Dis 1992; 51: 1143-8.
17. Clements PJ, Lachenbruch P, Seibold J, et al. Inter and intraobserver variability of total skin thickness score (modified Rodnan TSS) in systemic sclerosis. J Rheumatol 1995; 22: 1281.
18. Ellis KJ. Human Body Composition: in Vivo Methods. Physiol Rev 2000; 80: 649-80.
19. Ólafsdóttir E. Handbók rannsóknardeildar Landspítalans. Vol. 4. 1996, Reykjavík: Landspítalinn.
20. Graham Russell, Introduction: bone metabolism and its regulation (p.1-26); Caren M Gundberg, Osteocalcin (p. 65-72): Bone Markers, Richard Eastell, M.B., Nicholas R. Hoyle, Lothar Wieczorek. 2001, London: Martin Dunitz.
21. Stephen G. Chaney. Principles of nutrition II: Micronutrients: Textbook of Biochemistry with clinical correlations. 5 ed. Devlin T.M., 2002, New York: Wiley-Liss, p. 1137-1168.
22. Geirsson AJ, Wollheim FA, Åkesson A. Disease severity of 100 patients with systemic sclerosis over a period of 14 years: using a modified Medsger scale. Annals of the Rheumatic Diseases 2001; 60: 1117-20.
23. Krabbameinaskrá 1986-1989. Persónulegar upplýsingar frá Laufeyju Tryggvadóttur og Elínborgu Ólafsdóttur.
